ARTÍCULO ORIGINAL
Detección por inmunohistoquímica de Leishmania infantum en hámster infectado experimentalmente
Detection of Leishmania infantum in an experimentally-infected hamster using immunohistochemistry
]]>
MSc. Lisset Fonseca Géigel, Dra.Virginia Capó de Paz, Lic. María Caridad López, Lic. Alfredo Gutiérrez
Instituto de Medicina Tropical "Pedro Kourí". La Habana, Cuba.
Introducción: la leishmaniasis visceral se considera la forma más severa de las leishmaniasis y puede llegar a ser fatal en ausencia de tratamiento oportuno. En América Latina la infección es causada por Leishmania infantum (syn. Leishmania chagasi). El diagnóstico inequívoco y la selección de un adecuado modelo experimental son una necesidad para emprender estudios con este agente biológico.
Objetivo: determinar la utilidad de la técnica de inmunohistoquímica en la identificación de Leishmania.
Métodos: los animales se inocularon con promastigotes de Leishmania infantum. Se monitoreó el peso corporal de cada animal y se determinó el peso relativo de bazos e hígados. Para la identificación de amastigotes se prepararon improntas coloreadas con Giemsa y se desarrolló un protocolo de inmunohistoquímica en tejido incluido en parafina.
Resultados: se reprodujo la infección en el modelo experimental. La técnica de inmunohistoquímica fue positiva en los cortes de los animales infectados y no reactiva para el grupo control. Al comparar con la tinción mediante Giemsa, esta metodología facilitó la identificación, particularmente en órganos con escasos parásitos.
Conclusiones: la inmunohistoquímica es una herramienta específica para la detección de Leishmania, facilita la observación y evita confusiones en la identificación del parásito, lo que mejora la calidad del diagnóstico.
Palabras clave: Leishmania infantum, leishmaniasis visceral, hámster, immunohistoquímica.
Introduction: visceral leishmaniasis is considered the most severe form of this disease and can be fatal if not properly treated. In Latin America, the infection is caused by Leishmania infantum (syn. Leishmania chagasi). The unequivocal diagnosis and the selection of a suitable experimental model are required to undertake studies on this biologic agent.
Objective: to determine the advantages of immunohistochemistry in identifying Leishmania.
Methods: hamsters were inoculated with Leishmania infantum promastigotes. The body weights of every animal were monitored, and the relative weights of their spleens and livers were estimated. For identification of amastigotes, Giemsa-stained imprints and an immunohistochemistry protocol in paraffin-embedded tissues were developed.
Results: the infection was reproduced in the experimental model. The immunohistochemistry was positive in infected animal sections and non-reactive for the control group. When compared with the Giemsa staining, this methodology facilitated the identification, particularly in organs infected with few parasites.
Conclusions: immunohistochemistry is a specific tool for detection of Leishmania since it facilitates observation and eliminates any confusion in the identification of the parasite, thus improving the quality of diagnosis.
Keywords: Leishmania infantum, visceral leishmaniasis, hamster, immunohistochemistry.
INTRODUCCIÓN
La leishmaniasis constituye un espectro de enfermedades causada por protozoos del género Leishmania. Afecta a diferentes países de variados contextos geográficos y corresponde a una infección antropozoonótica que llega al hombre por la picadura de insectos infectados.1
La manifestación clínica con comprometimiento de las vísceras es conocida como leishmaniasis visceral (LV), que es endémica en 62 países y coloca en riesgo a 200 millones de personas, estimándose 500 000 nuevos casos por año.2 Se considera una enfermedad emergente en franca expansión en áreas tropicales y subtropicales, es la forma más severa de las leishmaniasis, con 98 % de mortalidad en ausencia de tratamiento oportuno.3 La enfermedad es extremadamente polimórfica y la observación del parásito en los tejidos es necesaria para confirmar el diagnóstico. Los amastigotes pueden ser identificados por tinción con Wright, Giemsa o Leishman en preparaciones como frotis o secciones de tejidos obtenidos de lesiones en la piel, bazo, hígado, médula ósea y aspirados de nódulos linfáticos. Este procedimiento puede llevar a resultados falsos negativos por el bajo número de parásitos en las muestras clínicas o por dificultades en la identificación morfológica.4 Otros métodos convencionales, para el diagnóstico parasitológico, incluyen al cultivo in vitro de fragmentos o de aspirado de tejido y la inoculación en animales de laboratorio. La baja sensibilidad de estos procedimientos hace que los resultados sean frecuentemente inconclusos, requieren de repetidas tomas de muestra así como de personal adiestrado.5 El análisis histopatológico de órganos infectados como el bazo, hígado, nódulos linfáticos y médula ósea, es otro de los métodos para la detección de parásitos intracelulares; aunque los amastigotes, con frecuencia, no son fácilmente reconocidos y la observación de las láminas teñidas con hematoxilina-eosina, en ocasiones, no aportan resultados concluyentes.6 La inmunohistoquímica (IHQ), por medio de anticuerpos específicos, permite la identificación del parásito y ha sido descrita como técnica de alta sensibilidad. Este procedimiento puede utilizarse como herramienta complementaria para confirmar el diagnóstico sospechado en secciones teñidas con hematoxilina-eosina, particularmente en órganos que no tienen alta carga parasitaria.7
El objetivo del presente trabajo fue implementar, en el laboratorio del Instituto de Medicina Tropical "Pedro Kourí" (IPK), un protocolo de IHQ para detectar Leishmania, en muestras incluidas en parafina, según técnica de rutina para histopatología, como metodología alternativa al ensayo directo de tinción con Giemsa. ]]>
MÉTODOS
Parásitos
Se utilizó la cepa de Leishmania infantum (L. infantum) MHOM/BR2000/MERIVALDO, gentilmente cedida por el Dr. Pontes de Carvalho del Centro de Investigaciones Gonçalo Moniz-FIOCRUZ, Salvador, Bahía, Brasil. Los parásitos fueron cultivados como promastigotes a 26 °C en medio RPMI (Sigma Chemical, St Louis, USA), suplementado con 10 % de suero fetal bovino, 100 U/mL de penicilina y 100 µg/mL de sulfato de estreptomicina (Sigma Chemical, St Louis, USA). Se realizaron subcultivos y se utilizaron los parásitos en la fase estacionaria de crecimiento. Los promastigotes se lavaron con solución salina estéril por centrifugación a 1 500 x g durante 10 min y ajustada la concentración a 107 parásitos.
]]>
Animales
Como animal de experimentación se utilizó el hámster Mesocricetus auratus, cepa AURA. Animales machos jóvenes, de aproximadamente 30 d de edad y peso entre 80 y 90 g se obtuvieron del Centro Nacional de Producción de Animales de Laboratorio (CENPALAB, La Habana-Cuba) y mantenidos en el Bioterio del IPK. Los animales se colocaron en jaulas de policarbonato de 180 cm2, con acceso libre a alimento y agua. Los experimentos se realizaron siguiendo las guías institucionales sobre el manejo y cuidado de animales de laboratorio, establecidas internacionalmente.
Infección experimental
Se anestesiaron 20 hámsters por inhalación con éter y se inocularon por vía intraperitoneal.8 Se inocularon 10 animales con 107 promastigotes metacíclicos de L. infantum y se utilizó como vehículo 200 µL de salina estéril. Otros 10 animales se utilizaron como controles negativos, por lo que solo recibieron el vehículo. Los animales inoculados con promastigotes se dividieron en 2 grupos: 4 hámsters fueron sacrificados a la semana 14 posinoculación (p.i.), y 6, así como los controles, a la semana 35 p.i. El peso de cada animal se monitoreó antes y p.i., semanalmente, hasta el momento del sacrificio. Después de la eutanasia, por asfixia en atmósfera de éter, el bazo e hígado de cada animal se extrajeron de manera aséptica y se pesaron en balanza analítica (Denver Instrument). El peso relativo de los órganos se determinó teniendo en cuenta la relación: peso individual de cada órgano/peso del animal respectivo.
Análisis de los tejidos
]]>
Fragmentos de bazo e hígado se colectaron para la búsqueda de amastigotes. Se prepararon improntas9 y las láminas se fijaron con metanol por 3 min, se tiñeron con Giemsa (Quimefa) por 10 min y se lavaron con agua corriente. Este material se observó al microscopio óptico con objetivo de inmersión (100 x) y ocular de 10 x. Paralelamente, secciones del bazo se incluyeron en parafina y se cortaron en fragmentos de 5 µm para realizar la detección del parásito mediante IHQ.10
Inmunohistoquímica
Se utilizó como anticuerpo primario, un suero anti-Leishmania, obtenido en conejo producido en el Laboratorio de Inmunología Molecular y Celular, FIOCRUZ, Salvador, Brasil; cortesía del doctor WLC dos Santos. El protocolo de trabajo fue el siguiente:
Desparafinado: se logró mediante el pase de los cortes por xileno (10 min), y graduaciones decrecientes de alcohol etílico (100º 10 min; 90º 10 min; 50º 5 min y 30º 5 min).
Rehidratación: los cortes se lavaron consecutivamente con agua corriente, agua destilada y solución tampón fosfato salino (PBS) 0,1M pH 7,2.
Tratamiento con tripsina: los cortes fueron sometidos a digestión enzimática con 0,1 % de tripsina y cloruro de calcio. Se incubó a 37 °C durante 30 min y se realizaron 3 lavados con PBS.
Bloqueo: la actividad endógena de la fosfatasa se inhibió por incubación de los cortes en solución de tetramisol 1 mM durante 20 min a temperatura ambiente. Se lavó 3 veces con PBS por 5 min. Las reacciones inespecíficas se bloquearon con suero bovino (SB) a 20 % en PBS y se incubó por 20 min a temperatura ambiente. ]]>
Anticuerpo: La experiencia se repetió con las diluciones del anticuerpo policlonal siguientes: 1/500, 1/1 000 y 1/2 000, en PBS que contenía SB a 0,5 %, durante toda la noche a 4 ºC, en cámara húmeda. Como controles negativos, de la técnica, se reemplazó el anticuerpo primario por suero no inmune de conejo, de hámster y PBS. La especificidad del anticuerpo primario también se analizó sobre cortes de tejidos de hámsters parasitológicamente negativos a Leishmania (animales controles).Revelado de la reacción: los cortes se incubaron con un anticuerpo marcado con biotina y con el complejo estreptavidina-fosfatasa. Ambas incubaciones fueron de 15 min con un lavado intermedio, con PBS, de 5 min. El revelado se realizó siguiendo las instrucciones del juego comercial Dako New Fuchsin, con fuchina y fosfato de naftol como cromógeno. La reacción fue monitoreada por observación en microscopio óptico Olympus, con lente de 10 x y 20 x, y se detuvo por inmersión de las láminas en agua destilada. Las preparaciones se observaron con objetivo 40 x y las fotografías se tomaron con una cámara digital acoplada al microscopio.
Análisis estadístico
Se utilizó el método Kolmogorov Smirnov y se aplicó la prueba t de Student de comparación de medias para analizar la diferencia de peso de los órganos entre los grupos inoculados y los controles.
RESULTADOS
]]>
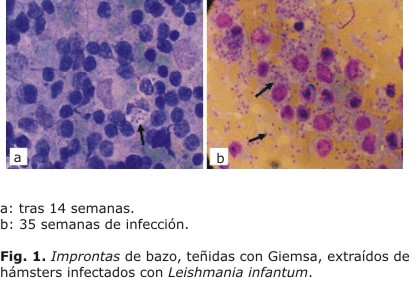
La evaluación parasitológica indicó el comprometimiento visceral en todos los animales inoculados con L. infantum. El examen de los tejidos mediante el estudio de improntas coloreadas con Giemsa mostró estructuras, caracterizadas como amastigotes, en las 14 y 35 semanas p.i. (Fig. 1a y 1b, respectivamente). La observación de las láminas correspondientes a las 14 semanas p.i., por el escaso número de parásitos, demandó tiempo y esfuerzo, para lograr un resultado diagnóstico preciso. Sin embargo, en las láminas correspondientes a las 35 semanas p.i., por la alta infección, resultó muy evidente la identificación de los parásitos. Los amastigotes se observaron en el citosol de macrófagos, así como extracelulares.Se observó inmunodetección positiva en los cortes de bazo de hámster infectados experimentalmente con L. infantum. La positividad estuvo dada por una coloración de rosado a fucsia intensa, que se observó a los 30 min de exposición del sustrato (Fig. 2 a). No se observó reacción en los cortes de tejido de los animales del grupo control ni en los controles internos de la coloración de IHQ (Fig. 2 b). El bloqueo con SB fue eficiente una vez que no se visualizaron reacciones inespecíficas. Los experimentos realizados con el anticuerpo primario permitieron escoger a 1:1 000 como dilución óptima.
El comprometimiento visceral, característica clínica de la LV, se aprecia en las figuras 3 y 4. En los animales inoculados se observaron órganos aumentados de tamaño, hecho no asociado a pérdidas ni a incrementos apreciables en el peso. Las diferencias resultaron altamente significativas para el peso relativo de los hígados (Fig. 3) y de los bazos (Fig. 4) de los animales inoculados y sus controles, para cada grupo, con valores de p= 0,009 y p= 0,00009, respectivamente.
DISCUSIÓN ]]>
Diferentes han sido los métodos descritos para el diagnóstico de la LV.11,12 Sin embargo, en la leishmaniasis, como para otras enfermedades infecciosas, la identificación del agente etiológico continua siendo el diagnóstico de referencia.13 En este trabajo se demostró por IHQ la presencia de amastigotes de L. infantum, en tejido de hámster, mediante la observación microscópica de inmunoprecipitados citoplasmáticos de color fucsia intenso. Se obtuvo un buen contraste entre el tejido de fondo y las células con marcaje de antígenos, lo cual demostró que los parámetros seleccionados para la digestión enzimática, bloqueo contra reacciones inespecíficas, dilución del anticuerpo, así como los tiempos de incubación, resultaron eficientes. La tripsinización también resultó eficiente. La tripsina, al igual que otras enzimas proteolíticas, puede utilizarse para potenciar la reacción porque desenmascara o recupera los antígenos e incrementa la positividad y el contraste entre la reacción específica y la coloración inespecífica de fondo.14 Se observó nitidez de las láminas, un resultado positivo bien definido y un contraste evidente entre los tejidos positivos y los controles. Por otra parte, se comprobó la especificidad del método por la ausencia de reacción al aplicar el suero no inmune de conejo, de hámster o PBS en sustitución del anticuerpo anti-Leishmania. La especificidad del anticuerpo primario también fue definida porque no hubo inmunodetección al utilizarlo en los cortes de tejido de los animales del grupo control. Al combinar elementos inmunológicos, histológicos y bioquímicos, la IHQ permite localizar un antígeno mediante el uso de anticuerpos específicos. Es un procedimiento relativamente sencillo de alta sensibilidad y especificidad que ha sido útil para el diagnóstico de diversas enfermedades así como en estudios de biología celular.15 La literatura apoya el desarrollo de esta técnica para la identificación de Leishmania,16 como alternativa a las dificultades encontradas en el diagnóstico parasitológico. La caracterización morfológica de amastigotes en cortes de tejidos, convencionalmente realizada por tinción con Giemsa en frotis o secciones histopatológicas teñidas con hematoxilina-eosina, requiere un análisis cuidadoso y prolongado, sobre todo cuando los parásitos son escasos.17 Estas dificultades se evidenciaron en el presente trabajo al analizar las preparaciones teñidas con Giemsa, obtenidas a las 14 semanas p.i. Con la experiencia del microscopista no quedó excluida la necesidad de revisar las láminas en más de una ocasión, lo que demandó esfuerzo y prolongó el resultado diagnóstico. Al evaluar las láminas obtenidas a las 35 semanas p.i., la visualización de los parásitos fue inmediata, se consideró como consecuencia de la profusión de la infección. En nuestra experiencia, la IHQ demostró ser útil como herramienta complementaria para confirmar el diagnóstico de la infección visceral, particularmente en órganos con pocos amastigotes (semana 14), que facilita el resultado diagnóstico.
Los resultados comprobaron que se reprodujo experimentalmente y de forma progresiva, la manifestación visceral de la leishmaniasis en el modelo animal seleccionado. El aumento de las dimensiones y del peso de los órganos, en el grupo inoculado, demostró tropismo de la infección hacia el bazo. Las diferencias significativas para el peso relativo de hígados y bazos con sus respectivos controles apoyan la observación de una marcada esplenomegalia y una hepatomegalia menos intensa. Aunque la patogenia de la LV no está totalmente dilucidada, se sabe que los macrófagos parasitados diseminan la infección a todas las partes del organismo con tropismo definido a médula ósea, hígado y bazo.18 También se describe que en animales infectados la pérdida de peso es un indicador de infección severa.19 Los resultados del presente trabajo no coinciden con lo anterior, una vez que se observaron estadios con alta producción de amastigotes (semana 35) no asociados a pérdidas apreciables en el peso corporal. Desde el punto de vista práctico esto se consideró un resultado positivo, que puede facilitar la realización de experimentos a largo plazo sin la depauperación de los animales.
En la actualidad, los modelos seleccionados para la LV experimental son el ratón y el hámster. Los mejores resultados, con el modelo murino, se han relacionado con la infección subclínica. En el hámster dorado, Mesocricetus auratus, es donde se reproducen los hallazgos clínico patológicos observados en la enfermedad humana.20 Esta condición lo convierte en el modelo mejor definido de la LV, a pesar de la escasa disponibilidad de reactivos para los estudios inmunológicos y moleculares.21 Por nuestros resultados se sugiere la utilidad del hámster en el diseño de ensayos prolongados, los que en ocasiones son una necesidad en los estudios de la LV experimental. A su vez, se aportan evidencias de la utilidad de la IHQ en la identificación de Leishmania, con alto grado de contraste entre el parásito y la célula hospedera, aun cuando los amastigotes en el tejido no eran abundantes. Esta es una técnica específica y respecto a la tinción con Giemsa, hace más evidente la observación del antígeno y evita las confusiones en la identificación del parásito, lo cual mejora la calidad del diagnóstico. Se concluye que la IHQ es una herramienta útil en el diagnóstico de la leishmaniasis, que podría ser utilizada con éxito en la investigación y aun facilitar el diagnóstico retrospectivo. Futuros estudios son necesarios referente a la sensibilidad de la IHQ y su relación con otras herramientas diagnósticas.
AGRADECIMIENTOS
Al doctor W. L. C. dos Santos del Centro Gonçalo Moniz-FIOCRUZ, Salvador Bahía, por donar el suero hiperinmune anti-Leishmania. Al laboratorio de IMC, de la entidad mencionada antes, por brindarnos la cepa de L. infantum y al doctor Jorge Cantillo del Bioterio del IPK, por las indicaciones para el manejo de los animales utilizados en este estudio.
]]>
REFERENCIAS BIBLIOGRÁFICAS
1. Desjeux P. Leishmaniasis: current situation and new perspectives. Comp Immunol Microbiol Infect Dis. 2004;27:305-18.
2. Chappuis F, Sundar S, Hailu A, Ghalib H, Rijal S, Peeling R, et al. Visceral leishmaniasis: what are the needs for diagnosis, treatment and control? Nature Reviews. 2007;5:873-82.
3. Romero GAS, Boelaert M. Control of Visceral Leishmaniasis in Latin America A Systematic Review. PLoS Negl Trop Dis. 2010;4:584. doi:10.1371/ journal.pntd.0000584. ]]>
4. Herwaldt B. Leishmaniasis. Lancet. 1999;354:1191-9.
5. Sundar S, Rai M. Laboratory Diagnosis of Visceral Leishmaniasis. Minireview. Clin Diag Lab Immunol. 2002;9:951-8.
6. Tafuri WL, de Oliveira MR, Meloc MN, Tafuri WL. Canine visceral leishmaniosis: a remarkable histopathological picture of one case reported from Brazil. Vet Parasitol. 2001;96:203-12.
7. Hofman V, Brousset P, Mougneau E, Marty P, Lamant L, Antoine JC, et al. Immunostaining of visceral leishmaniasis caused by Leishmania infantum using monoclonal antibody (1011) to the Leishmania homologue of receptors for activated C-kinase. Am J Clin Pathol. 2003;120:567-74.
8. Lindoso JA, Cotrim PC, Goto H. Apoptosis of Leishmania chagasi amastigotes in hamsters infected with visceral leishmaniasis. Int J Parasitol. 2004;34:1-4. ]]>
9. Sacks DL, Melby PC. Animal Models for Infectious Diseases. Current Protocols Immunol. 1998;19(2):1-20.
10. Bourdoiseau G, Marchal T, Magnol JP. Immunohistochemical detection of Leishmania infantum in formalin-fixed, paraffin-embedded sections of canine skin and lymph nodes. J Vet Diagn Invest. 1997;9:439-40.
11. Pedras MJ, de Gouvea Viana L, de Oliveira EJ, Rabello A. Comparative evaluation of direct agglutination test, rK39 and soluble antigen ELISA and IFAT for the diagnosis of visceral leishmaniasis. Trans R Soc Trop Med Hyg. 2008;102:172-8.
12. Chappuis F, Rijal S, Soto A, Menten J, Boelaert M. A meta-analysis of the diagnostic performance of the direct agglutination test and rK39 dipstick for visceral leishmaniasis. BMJ. 2006;333:723.
13. Pattabhi S, Whittle J, Mohamath R, El-Safi S, Moulton GG, Guderian JA, et al. Design, development and evaluation of rK28-based point-of-care tests for improving rapid diagnosis of visceral leishmaniasis. PLoS Negl Trop Dis. 2010;4: 822. doi:10.1371/journal.pntd.0000822. ]]>
14. Nadji M, Morales AR. Immunoperoxidase techniques: a practical approach to tumor diagnosis. Chicago: American Society of Clinical Pathologist P; 1986. p. 1-10.
15. Spraker TR, O'Rourke KI, Balachandran A, Zink RR, Cumings BA, Miller MW, et al. Validation of monoclonal antibody F99/97.6.1 for immunohistochemical staining of brain and tonsil in mule deer (Odocoileus hemionus) whith chronic wasting disease. J Vet Diagn Invest. 2002;14:3-7.
16. Tafuri WL, Lima-Santos R, Estévez RM, Gonçalves R, Norma de Melo M, Márques MS. An alternative immunochemistry methods for detecting Leishmania amastigotes in paraffin-embedded canine tissues. J Immunol Methods. 2004;292:7-23.
17. Gomes YM, Paiva Cavalcanti M, Lira RA, Abath FGC, Alves LC. Diagnosis of canine visceral leishmaniasis: Biotechnological advances. Veterinary J. 2008;175:45-52.
18. Reis AB, Martins-Filho OA, Teixeira-Carvalho A, Carvalho MG, Mayrink W, França-Silva JC, et al. Parasite density and impaired biochemical/ hematological status are associated with severe clinical aspects of canine visceral leishmaniasis. Res Vet Sci. 2006;81:68-75. ]]>
19. Soliman MFM. The persistence, dissemination, and visceralization tendency of Leishmania major in Syrian hamsters. Acta Trop. 2006;97:146-50.
20. Garg R, Dube A. Animal models for vaccine studies for visceral leishmaniasis. Indian J Med Res. 2006;123:439-54.
21. Melby PC. Recent developments in leishmaniasis. Curr Opin Infect Dis. 2002;15:485-90.
Recibido: 2 de noviembre de 2010. ]]> Aprobado: 12 de abril de 2011.
Lisset Fonseca Géigel. Instituto de Medicina Tropical "Pedro Kourí". Autopista Novia del Mediodía km 6 ½, entre Autopista Nacional y Carretera Central. Lisa, La Habana Cuba. AP 601, CP 11300. La Habana, Cuba. Teléf.: 53-7 2020650 Fax: 53-7 2043317. Correo electrónico: lfgeigel@ipk.sld.cu ]]>