Hospital Clinicoquirúrgico Docente Hermanos Ameijeiras
Dra. Geldris P. Hernández Galano, Dr. Raúl de Castro Arenas, Dr. Calixto Hernández Cruz, Dra. Dayana Pérez Valiente, Dr. José Carnot Uría, Dr. Jorge Muñío Perurena, Dr. Carlos A. Martínez Fernández y Dr. Guillermo Pérez Román
La púrpura trombocitopénica idiopática es una enfermedad hemorrágica autoinmune relativamente frecuente. Se realizó un estudio retrospectivo en 141 pacientes atendidos entre los años 1983 y 2003, con el objetivo de evaluar los resultados terapéuticos obtenidos en esta enfermedad. Del total evaluado, el 98,6 % necesitó tratamiento con diferentes esquemas terapéuticos y el 1,4 % restante mostró remisiones espontáneas. La modalidad de primera línea (tratamiento esteroideo) fue aplicada al 97,1 % de los pacientes al momento del diagnóstico inicial; la mayoría respondió favorablemente (65,7 %). La esplenectomía fue la segunda modalidad terapéutica, realizada al 54,6 % de los enfermos, que resultó en largos períodos de remisión (62 %, 59,7 % y 54,5 % de respuesta completa sostenida a los 3, 6 y 12 meses posesplenectomía). El tratamiento de tercera línea fue empleado en el 29,1 % de los casos refractarios a las terapias escogidas, con un índice de respuesta del 61,0 %. La prednisona sola o combinada fue el agente terapéutico más utilizado después del fracaso con los esteroides y/o esplenectomía. Los inmunosupresores y los alcaloides de la vinca fueron los más efectivos en estos casos, con 60 % y 71,4 % de respondedores. Se encontró significación estadística al evaluar la respuesta obtenida por línea de tratamiento al mes y a los 6 meses, y al comparar la respuesta inicial según la edad.
Palabras clave: púrpura trombocitopénica idiopática, tratamiento esteroideo, esplenectomía, inmunosupresores.
La púrpura trombocitopénica idiopática (PTI) es una enfermedad hemorrágica autoinmune caracterizada por el desarrollo de autoanticuerpos dirigidos contra antígenos de algunos de los complejos mayores de glicoproteínas plaquetarias (GpIIb/IIIa, GpIb/IX/V o GpIa/IIa, GpIV), las cuales son destruidas por fagocitosis en el bazo y con menor frecuencia en el hígado. El síndrome clínico de la PTI está caracterizado por sangramientos cutáneo mucosos con diferencias establecidas entre la infancia y la etapa adulta. La PTI infantil es casi siempre aguda, posterior a una infección viral, en la mayoría de los casos es autolimitada y resuelve espontáneamente, en su mayoría, en menos de 6 meses, sin requerir tratamiento. En el adulto generalmente el inicio es más gradual y fluctuante, sin ninguna enfermedad precedente, con un curso crónico mayor de 6 meses (en un pequeño porcentaje de los adultos la enfermedad puede ser aguda), y la gran mayoría de los pacientes requieren tratamiento para normalizar las plaquetas.1
La PTI es la causa más frecuente de trombocitopenia en el adulto, la mayoría de los enfermos son menores de 45 años y la relación masculino-femenina es de 3/4:1. Esta entidad cursa con trombocitopenia periférica y un número normal o aumentado de megacariocitos en la médula ósea, consecuencia del aclaramiento acelerado de plaquetas sensibilizadas (por anticuerpos). La severidad de la enfermedad refleja el balance entre la producción de plaquetas por los megacariocitos y la destrucción prematura de estas, preferentemente al nivel esplénico. El diagnóstico de la PTI es primariamente por exclusión, descartando otras entidades que cursan con trombocitopenia autoinmune (infecciones, colagenosis, síndromes linfoproliferativos, reacciones a drogas, hiperesplenismo, etc.).2
Existen varios pilares terapéuticos para esta enfermedad. El tratamiento inicial se basa en la utilización de corticoides, preferentemente de acción intermedia (prednisona, prednisolona, metilprednisolona). La esplenectomía es generalmente un tratamiento de segunda línea, basado en la extirpación del sitio principal de destrucción plaquetaria y una importante fuente de síntesis de anticuerpos antiplaquetarios.
Una de las características más relevantes de esta enfermedad es su variabilidad en relación con la respuesta al tratamiento. La PTI crónica continúa siendo un trastorno de difícil manejo, particularmente en pacientes resistentes al uso de corticoesteroides y esplenectomía. El tratamiento de tercera línea requiere la utilización racional e individualizada de ciertos fármacos como danazol, gammaglobulina (IgIV) a altas dosis, inmunosupresores, alcaloides de la vinca, interferón a, colchicina, etc. Esta terapéutica generalmente se inicia cuando hay fracaso en los tratamientos de primera y segunda líneas, aunque en algunas circunstancias y grupos de pacientes se han utilizado antes de la esplenectomía.3,4
Teniendo en cuenta todo lo expuesto anteriormente se realiza el siguiente estudio, con el fin de evaluar los resultados obtenidos según las diferentes modalidades de tratamiento utilizados, en los pacientes diagnosticados como PTI crónica, en el Servicio de Hematología del Hospital Docente Clinicoquirúrgico Hermanos Ameijeiras, con el fin de conocer la efectividad de la estrategia terapéutica planteada para los pacientes con esta enfermedad.
El diagnóstico de la PTI crónica se hizo por exclusión, considerando como tal aquellos casos con trombocitopenia en sangre periférica, con sistema megacariopoyético íntegro o hiperplástico en médula ósea y ausencia de otras causas de trombocitopenia inducida por drogas, colagenopatías, infecciones, neoplasias, púrpura postransfusional, hiperesplenismo, hemangioma gigante, etc.
Para realizar el estudio los pacientes se separaron en 2 subgrupos, según las terapéuticas empleadas y la edad.
• De acuerdo con la terapéutica:
-Primera línea.
-Segunda línea.
-Tercera línea.
• De acuerdo con la edad:
]]> -Menores de 45 años.
-Mayores de 45 años.
La estrategia terapéutica se estableció de la siguiente forma:
Primera línea (corticoesteroides):
El glucocorticoide empleado fue la prednisona. Con dosis inicial de 1mg/kg/día repartidos en 3 ó 4 tomas durante 4-6 semanas, disminuyendo progresivamente la dosis en los pacientes que alcanzaron recuentos plaquetarios normales, hasta su suspensión total, o manteniendo una dosis equivalente (5-10 mg/día) de prednisona, para estabilizar el recuento plaquetario en cifras de 50x109 /L. En los casos en que ocurrió recaída después de una respuesta inicial se administró otra forma de terapia. Los pacientes con contraindicaciones para el uso de esteroides (hipertensión arterial grave, ulcus péptico activo, diabetes mellitus insulino dependiente e insuficiencia cardíaca congestiva), fueron candidatos al esquema de segunda línea.
Segunda línea (esplenectomía):
Este tratamiento estuvo indicado en:
Tercera línea:
Los esquemas de tercera línea se agruparon en :
a) Dosis bajas de esteroides posesplenectomía a razón de 10 -15 mg/día.
b) Danazol: 200 mg 3 ó 4 veces/día durante 10 meses a 1 año.
]]> c) Gammaglobulina intravenosa a altas dosis (IgIV): 400 mg/kg/día durante 5 días consecutivos administrados por infusión intravenosa en 4-6 horas.d) Inmunosupresores:
e) Alcaloides de la Vinca:
f) Interferón a : dosis de 3 millones por vía subcutánea 3 días en la semana y con una duración de 4 semanas.
Los pacientes elegidos para iniciar esta línea de tratamiento fueron aquellos con refractariedad, recidivas o contraindicaciones para el uso de las terapéuticas anteriores, y los que rechazaron la esplenectomía como opción terapéutica.
La evaluación de la respuesta clínica a los diferentes esquemas terapéuticos se hizo según los criterios siguientes:
• Respuesta completa (RC): conteo de plaquetas a más de 150x109 /L por 4 semanas o más.
• Remisión parcial (RP): conteo de plaquetas a más de 50x109 /L hasta 150x109 /L por 4 semanas o más.
• Respuesta transitoria (RT): reaparición de la trombocitopenia antes del mes de suspendido el tratamiento.
• Respuesta completa sostenida (RCS): mantenimiento del conteo de plaquetas en 150x109 /L o más, 6 meses después de suspendido el tratamiento
]]> • Respondedores (R): todos los pacientes con respuestas completa y parcial.• No respondedores (NR): aquellos pacientes que después del tratamiento no alcanzaron cifras de plaquetas superiores a 50x109 /L, o aquellos con reaparición de la trombocitopenia (menos de 50x109 /L) antes del mes de suspendido el tratamiento.
• Recaída: cuando después de haber alcanzado cifras de plaquetas superiores a 50x109 /L por al menos 1 mes, reaparece la trombocitopenia al disminuir o suspender el tratamiento.
El dato primario se obtuvo de la revisión detallada de historias clínicas generales y hematológicas de los pacientes. Los resultados obtenidos se expresaron con medidas de estadística descriptiva y para analizar la muestra se empleó el test de proporción y el de significación estadística.
La muestra estuvo constituida por 141 adultos con diagnóstico inicial de PTI crónica. De estos pacientes, 56 (39,7 %) eran hombres y 85 (60,3 %) mujeres. Los pacientes menores de 45 años fueron más numerosos que los que superaban esta edad, con cifras de 94 (67 %) y 47 (33 %), respectivamente.
Un total de 139 pacientes (98,6 %) recibieron tratamiento con los diferentes esquemas terapéuticos y 2 pacientes (1,4 %) mostraron remisión espontánea temprana en un período aproximado de 21-28 días, por lo que no recibieron terapia alguna.
Fueron tratados con corticoesteroides al momento del diagnóstico inicial 137 pacientes que representan el 97,1 %; solo 2 enfermos (1,4 %) no recibieron este tipo de terapia por presentar contraindicaciones específicas para su uso.
La segunda línea de tratamiento (esplenectomía), incluyó 77 pacientes (54,6 %): 1 paciente con hipertensión arterial severa que contraindicaba el uso de corticoides, 33 pacientes que no respondieron al tratamiento esteroideo inicial y 43 pacientes con recaída poscorticoterapia.
Las combinaciones terapéuticas de tercera línea fueron utilizadas en 41 pacientes (29,1 %): 1 paciente con contraindicaciones para los tratamientos de primera y segunda líneas, 2 pacientes que rechazaron el proceder operatorio, 3 pacientes con riesgo quirúrgico, 10 pacientes refractarios a la esplenectomía, 20 pacientes que no respondieron a esta última, y 5 pacientes que recibieron esta forma de tratamiento como segunda línea.
Como puede observarse en la tabla 1, de 137 pacientes tratados con corticoesteroides, el 65,7 % respondió inicialmente, alcanzando la remisión el 50,4 % de forma completa y el 15,3 % parcialmente. Aproximadamente el 29,9 % mantuvo remisiones completas sostenidas 6 meses después de suspendido el tratamiento; alrededor del 34,3 % no respondió adecuadamente a este (10,2 % de RT y 24,1 % de NR). A los 6 meses, el 39,4 % se hallaba en recaída.
]]> Tabla 1. Respuesta postratamiento esteroideo| Respuesta | 1 mes | Total | 6 meses | Total | ||||
| No. | % | No. | % | ]]> No. | % | No. | % | |
| RC | 69 | 50,4 | 90 | 65,7 | 41 | ]]> 29,9 | 50 | 36,5 |
| RP | 21 | 15,3 | 9 | 6,6 | ]]> | |||
| RT | 14 | 10,2 | 47 | 34,3 | NA | - | - | - |
| ]]> NR | 33 | 24,1 | 33 | 24,1 | 33 | 24,1 | ||
| Recaída | ]]> NA | - | - | - | 54 | 39,4 | 54 | 39,4 |
NA: no aplicable; RC: remisión completa; RP: remisión parcial; RT: remisión transitoria; NR: no respondedor.
En la tabla 2 se muestra la respuesta a la esplenectomía. De 77 pacientes sometidos a este proceder, el 71,4 % respondió a la misma, 49 pacientes lo hicieron con respuestas completas (63,6 %) y 6 pacientes con respuestas parciales (7,8 %). Solo en 2 pacientes (2,6 %) se registró una respuesta transitoria, con conteo de plaquetas que retornaron a cifras inferiores a 50x109 /L al mes de realizada la cirugía. En contraste, 20 pacientes no respondieron (26 %). A los 3, 6 y 12 meses, el status de respuesta completa fue de 62 %, 59,7 %, y 54,5 %, respectivamente. A los 6 meses de la cirugía, cerca del 7,8 % de los respondedores se encontraban en recaída, valor que aumentó un año después, alcanzando cifras del 13 %. Solo 2 pacientes presentaron recaída después de los 2 años.
Tabla 2. Respuesta posesplenectomía
| Respuesta | 1 mes | ]]> 3 meses | 6 meses | ³ 12 meses | ||||
| No. | % | No. | % | No. | % | No. | ]]> % | |
| RC | 49 | 63,6 | 48 | 62,3 | 46 | 59,7 | 42 | 54,5 |
| ]]> RP | 6 | 7,8 | 5 | 6,5 | 5 | 6,5 | 5 | 6,5 |
| RT | ]]> 2 | 2,6 | NA | - | NA | - | NA | - |
| NR | 20 | ]]> 26 | 20 | 26 | 20 | 26 | 20 | 26 |
| Recaída | NA | - | ]]> 4 | 5,2 | 6 | 7,8 | 10 | 13 |
NA: no aplicable; RC: remisión completa; RP: remisión parcial; RT: remisión transitoria; NR: no respondedor.
La terapéutica de tercera línea fue empleada en 41 pacientes (29,1 %) refractarios a los tratamientos de primera y segunda líneas (tabla 3 ). Luego de una respuesta inicial de hasta el 61,0 % (RC 39,1 % y RP 21,9 %), solo el 19,5 % mantuvo la respuesta por más de 6 meses, el 39,0 % no respondió y el 53,6 % mostró desaparición de la respuesta al suspender el tratamiento.
Tabla 3. Respuesta con esquemas de tercera línea
| Respuesta | ]]> 1 - 3 meses | ³ 6 meses | ||
| No. | % | No. | % | |
| RC | 16 | 39,1 | 8 | ]]> 19,5 |
| RP | 9 | 21,9 | 2 | 4,9 |
| RT | 7 | 17,1 | NA | ]]> - |
| NR | 9 | 21,9 | 9 | 21,9 |
| Recaídas | NA | - | 22 | ]]> 53,7 |
NA: no aplicable; RC: remisión completa; RP: remisión parcial; RT: remisión transitoria; NR: no respondedor.
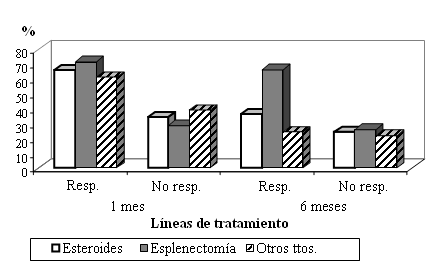
En cuanto a la respuesta obtenida a las diferentes modalidades terapéuticas empleadas (fig. 1, tabla 4), observamos que la esplenectomía mostró mejores resultados iniciales (71,4 %) que los esquemas de primera (65,7 %) y tercera líneas (61,0 %), con el 66,2 % de respuestas (59,7 % de remisiones completas y 6,5 % de remisiones parciales) a los 6 meses de realizado el proceder quirúrgico (p<0,005).
Fig. 1. Respuesta por línea de tratamiento al mes y a los 6 meses.
Tabla 4. Respuesta al mes y a los 6 meses por línea de tratamiento
| Líneas de tratamiento | 1 mes | 6 meses | ||
| Respuesta | ]]> No respuesta | Respuesta | No respuesta | |
| Esteroides | 90 (65,7) | 47 (34,3) | 50 (36,5)* | 33 (24,1) |
| Esplenectomía | 55 (71,4) | 22 (28,6) | ]]> 51 (66,2)* | 20 (26,0) |
| Otros | 25 (61,0) | 16 (39,0) | 10 (24,4) | 9 (21,9) |
*p<0,005.
De los 41 pacientes enfermos con recaída (tabla 5), 10 recibieron prednisona sola, de ellos 7 mostraron una respuesta completa o parcial (70 %), y los 3 restantes se comportaron como no respondedores (30 %). De los respondedores, 3 pacientes (30 %) tuvieron una respuesta completa estable después de suspendido el tratamiento, y otros 3 pacientes (los de respuesta parcial) fueron corticodependientes, por lo que fue necesario extender el tratamiento por un período de 3-6 meses, y administrar otro tipo de terapia.
Nueve casos fueron tratados con Danazol solo o combinado con prednisona: 4 mostraron respuesta completa (44,4 %), y 2 respuesta parcial (22,2 %); es decir, el 66,6 % de pacientes respondedores, y 3 no respondieron a este derivado semisintético de la etiniltestosterona (33,4 %). No obstante, excepto para los 2 pacientes con RP, 4 pacientes obtuvieron respuesta sostenida después de interrumpido el tratamiento de 10 meses de duración; dichos pacientes fueron mujeres mayores de 55 años.
]]> En el presente estudio, la ciclofosfamida fue utilizada para tratamiento en 5 pacientes; 2 mostraron una respuesta completa (40 %), la cual fue sostenida en uno de ellos; 1 paciente mostró una respuesta parcial insostenida (20 %), mientras que 2 pacientes no respondieron al tratamiento con este inmunosupresor (40 %). Para lograr un ascenso en el conteo de plaquetas, se requirió la administración prolongada de esta droga por varias semanas (10 semanas).Cinco pacientes fueron tratados con azatioprina, con o sin prednisona; 3 mostraron ausencia de respuesta (60 %), 2 respuestas adecuadas (40 %), la cual no fue sostenida en ninguno de los respondedores. Fue necesario el tratamiento al menos por 4 meses, antes de considerar al paciente no respondedor.
Siete pacientes recibieron alcaloides, de forma aislada o combinada con otras drogas de tercera línea: 5 mostraron incremento del conteo de plaquetas (71,4 %) en 1-3 semanas de iniciado el tratamiento, de los cuales el 14,6 % fue continuada (requiriendo no suspender el tratamiento por al menos 3 meses), mientras que 2 no respondieron (28,6 %).
Cinco pacientes recibieron IGIV: 1 caso mostró respuesta completa (20 %), otro respuesta parcial (20 %), y 3 respuesta transitoria (60 %). Solamente uno de ellos alcanzó respuesta completa continuada, y coincidió con la administración conjunta de prednisona.
Como puede observarse en el figura 2, en los adultos menores de 45 años con PTI crónica clásica, el esquema de primera línea resultó ser el más empleado (65,7 %), mostrándose una buena respuesta inicial (51,1 %) significativa, con un valor de p < 0,005 al tratamiento esteroideo estándar. De 47 pacientes sometidos a esplenectomía (61,0 %), 40 respondieron adecuadamente (51,9 %) y un porcentaje muy bajo no respondió (9,1 %). La terapéutica de tercera línea se empleó en un pequeño número de enfermos (34,1 %) con escasa respuesta (19,5 %). En los adultos mayores de 45 años, el tratamiento inicial con esteroides se aplicó en 47 pacientes (34,3 %), de los cuales 20 respondieron adecuadamente (14,6 %), y un mayor porcentaje de pacientes no respondió (19,7 %). La esplenectomía se realizó en 30 pacientes (39 %), y se acompañó de escasa respuesta (19,5 %); en tanto, la terapia de tercera línea fue empleada en 27 pacientes (65,9 %) con una respuesta excelente (46,4 %), siendo estadísticamente significativo (p < 0,005).
Fig. 2. Respuesta clínica inicial por línea de tratamiento según edad.
La PTI continúa siendo una entidad que entraña un reto terapéutico indiscutible, a pesar de los avances en las últimas décadas, principalmente en los pacientes adultos, en los cuales, según diversos estudios retrospectivos sobre PTI crónica, 3-5 la remisión espontánea es muy poco frecuente, con una ocurrencia estimada inferior al 5 %.
La pregunta de cuándo se debe iniciar la corticoterapia es aún controversial; algunos recomiendan comenzar cuando las cifras de plaquetas son inferiores a 30x109/L o 50x109/L en pacientes sintomáticos.6 Los pacientes que generalmente fallan con la terapia esteroidea después de 6 semanas, deben ser considerados tributarios para esplenectomía, así como aquellos que tienen recaída después de suspender los esteroides.1,2,7
El 65,7 % de los pacientes, de los 137 tratados al debut con esteroides, obtuvieron una respuesta inicial, con el 29,9 % de respuestas completas sostenidas 6 meses después de suspendido el tratamiento. Estos resultados son comparables con otros estudios sobre PTI crónica, con respuestas iniciales al tratamiento esteroideo entre el 50 y 80 %, algunos indican hasta el 90 %.2,4,8-10 La respuesta ocurre dentro de las primeras 3-4 semanas postratamiento. El rango de incidencia de la remisión continuada es variable, desde menos del 5 % hasta cifras superiores al 30 %.4,10 Kumar y colaboradores reportaron en su estudio sobre PTI entre el 15 y 40 % de respuesta sostenida.1
]]> La PTI continúa siendo una de las indicaciones más comunes para la esplenectomía, esta es el tratamiento definitivo para muchos casos de PTI crónica, que consigue largos períodos de remisión. El rango de remisión con la esplenectomía observado (71,4 % de respuesta al inicio y 54,5 % de respuesta completa sostenida a los 12 meses), es similar al de algunos investigadores, con el 70-80 % de respuesta, 1,2,4,11-13 y entre el 50-80 % de respuesta completa sostenida. Blanchette y colaboradores, en su revisión sobre PTI, señalan que del 30 al 40 % de los pacientes no responden o recaen después de este proceder.2 Otros autores también coinciden con dicho resultado,6,7 entre ellos, Srinivasan y colaboradores,14 que obtuvieron 72 % de respuesta completa, 7 % de respuesta parcial y 21 % no respondió. Muchos de los estudios revisados muestran entre el 10 y 16 % de recaída tras la respuesta inicial, la mayoría en el primer año que sigue a la operación, y son más raras las recaídas tardías en los 5 años posesplenectomía. Muchas de las recaídas ocurrían dentro de los primeros 2 años. (Mochamuk RS. Immune thrombocytopenic: Current understanting and future research. Highlights of the 8 th congress of the European Hematology 2003 Association).1,12-17En el presente estudio, el 29,1 % de los casos ameritó un tratamiento de tercera línea, con respuestas iniciales del 61,0 %. Similares resultados sobre PTI refractaria fueron registrados por Nomura, 15 con el 25 al 30 % de casos refractarios a los esteroides y a la esplenectomía, con respuestas iniciales de hasta 50 al 70 %, que fueron prolongadas en un 20-25 %, y en los que fue necesario continuar el tratamiento de forma indefinida para mantener la respuesta obtenida. Un escaso número de pacientes mantiene períodos largos de remisión una vez suspendida esta medicación.1, 4,18
Analizando la respuesta a las distintas variantes de tratamiento empleadas en el actual estudio, se observó que la esplenectomía mostró los mejores resultados iniciales (71,4 %). Aunque los esteroides están definidos actualmente como el tratamiento inicial en la PTI crónica, la esplenectomía continúa siendo el más efectivo: es un proceder curativo con morbimortalidad mínima que ofrece largos períodos de remisión en los casos que fallan a la respuesta esteroidea convencional, recaen o experimentan complicaciones secundarias al tratamiento inicial con corticoides. (Mochamuk RS, citado anteriormente). En un estudio realizado desde 1983 hasta 1996, en 71 pacientes esplenectomizados con PTI crónica, se registraron respuestas completas de hasta el 82 %, con el 42 % de respuestas mantenidas 60 meses después de la operación, lo que señala el verdadero rol de la esplenectomía en esta enfermedad.14
Varios agentes se han utilizado en pacientes refractarios, incluyendo esteroides en bajas dosis, danazol, inmunosupresores, alcaloides de la vinca, IGIV en dosis altas, inmunoglobulina anti-D, interferón alfa, pulsos de dexametasona o metilprednisolona, entre otros.4,8,11 Como se observa en la tabla 5, las terapias adicionales con múltiples drogas fueron utilizadas también en la muestra estudiada, donde la prednisona sola o combinada, resultó ser el agente terapéutico más usado. El probable efecto beneficioso que este esteroide pudiera añadir al emplearse junto con otras drogas en pacientes refractarios, no fue posible evaluarlo, por la escasa cantidad de casos incluidos en cada combinación.
Tabla 5. Respuesta clínica según esquemas de tercera línea
| Tipo de tratamiento | Tratados | Respondedores | No respondedores | RCS | ||
| RC | RP | ]]> RC | RP | > 6 meses | ||
| Prednisona (dosis bajas) | 10 | 4 | 3 | 1 | 2 | 3 |
| ]]> Danazol con o sin prednisona | 9 | 4 | 2 | - | 3 | 4 |
| Ciclofosfamida | 5 | 2 | 1 | ]]> - | 2 | 1 |
| Azatioprina con o sin prednisona | 5 | 1 | 1 | 3 | - | - |
| Vincristina | ]]> 3 | 1 | - | - | 2 | - |
| Vincristina | 2 | 1 | ]]> 1 | - | - | 1 |
| Vincristina | 1 | 1 | - | ]]> - | - | - |
| Vinblastina | 1 | 1 | - | - | ]]> - | - |
| Inmunoglobulina IV | 4 | - | 1 | 3 | - | - |
| Inmunoglobulina IV Prednisona | ]]> 1 | 1 | - | - | - | 1 |
| Total | 41 | 16 | 9 | ]]> 7 | 9 | 10 |
RC: remisión completa; RP: remisión parcial; RCS: respuesta completa sostenida.
Los resultados obtenidos en el uso de la prednisona sola en los casos refractarios (con el 70 % de respuesta inicial) ya han sido descritos con anterioridad, 7 con un rango de respuesta a la prednisona entre el 70 y 80 %, y una muy escasa respuesta sostenida.1 Sin embargo, algunos refieren que la esplenectomía puede mejorar la respuesta a los esteroides, y pacientes que necesitaban dosis elevadas de prednisona para alcanzar una respuesta previa a este proceder quirúrgico, pueden ser mantenidos con bajas dosis de esteroides posteriores al mismo.6,19
Con respecto al empleo del danazol (con el 44,4 % de respuestas completas en la presente evaluación), y según algunos estudios, 1,20,21 el índice de respuesta al mismo oscila entre el 10 y 80 %, con muy pocas respuestas sostenidas. El número de respondedores aumenta con la edad, sobre todo en mujeres, alcanzándose hasta el 80 % en las mayores de 65 años. En pacientes mayores de 45 años, puede constituir el fármaco de elección cuando fracasa el tratamiento esteroideo, independientemente de que haya sido o no esplenectomizado, especialmente en mujeres de edad avanzada, donde incluso se puede usar como tratamiento inicial.20,22,23
Algunos estudios sugieren que la terapia inmunosupresora puede ser más efectiva en pacientes esplenectomizados. La razón para esta observación no ha sido evaluada completamente y la efectividad global de estas potentes drogas es variable, con remisiones muy cortas.1,4 Sin embargo, es meritorio mencionar los resultados favorables obtenidos en pacientes que no han respondido a la esplenectomía o a los esteroides.4 El tratamiento inmunosupresor debe ser reservado para casos refractarios, sobre todo para pacientes mayores de 45 años, cuando fallan otras alternativas de terapias menos tóxicas.1,16,23
En relación con el empleo de la ciclofosfamida, el 40 % de respuestas completas de acuerdo con la experiencia aquí analizada, coincide con lo ya comunicado.24
En los casos en que se aplicó la azatioprina, los resultados fueron desalentadores (ninguna respuesta sostenida). No obstante, se ha planteado que el tratamiento con azatioprina produce normalización del conteo de plaquetas en el 45 % de los pacientes con PTI crónica, incluyendo aquellos que no responden a la esplenectomía; en algunos podría ser sostenida por varios meses o años sin tratamiento adicional. Sin embargo, el 50 % de los pacientes requiere tratamiento continuo con dicho fármaco para mantener las cifras de plaquetas.6, 25,26
Los alcaloides de la vinca: vincristina y vinblastina, han sido usados para el tratamiento de esta entidad por más de 2 décadas, con algunos beneficios reportados,24,27,28 y son tan efectivos como la ciclofosfamida, pero tienen acción más rápida, con frecuencia en más o menos 7 días.2,26,9,30 El empleo de este tipo de medicación en el actual estudio mostró resultados positivos (en 71,4 % de los pacientes se registró incremento del número de plaquetas). Se debe señalar que muchos de estos pacientes recibieron tratamiento combinado con corticoides, azatioprina y danazol, lo cual dificultó la verdadera apreciación de la eficacia de los alcaloides en el tratamiento de la PTI crónica.
]]> En relación con la IGIV, se ha señalado que se obtienen generalmente buenas respuestas, pero con duración limitada, e incluso un pequeño porcentaje, próximo al 10 %, permanece en remisión.4,31 Por el contrario, un tercio de los enfermos llegan a ser totalmente refractarios,2,4,6, 31-34 todo lo cual coincide con lo observado en esta serie.Los resultados del presente estudio mostraron conclusiones muy similares a los de la literatura revisada 4,35-37 al analizar la respuesta clínica inicial según la línea de tratamiento y la edad, donde se identificaron 2 subgrupos de pacientes dentro de la PTI crónica con respuestas diferentes a las distintas terapias disponibles. Los adultos menores de 45 años mostraron buena respuesta al tratamiento inicial con corticoides, los pacientes refractarios a estos últimos respondieron bien a la esplenectomía como segunda línea de tratamiento, con el 50 al 80 % de respuesta. Los adultos mayores de 45 años respondieron en menor medida al tratamiento inicial con esteroides, pero la esplenectomía se intentó retrasar en los casos refractarios, ya que se acompañó de poca respuesta (20-30 %) y mayor morbimortalidad; en tales casos se ensayaron otras terapias primeramente, como el danazol y los inmunosupresores.6,16,38,39
Como ha quedado evidenciado en el actual trabajo, los esteroides mantienen su vigencia como tratamiento de primera línea para adultos con PTI crónica; en tanto la esplenectomía tiene el potencial de proporcionar un largo período de control de la enfermedad en los adultos con PTI crónica, que muestran fallo al tratamiento esteroideo o son esteroideo dependientes, y cerca del 70 % de los sometidos a esta cirugía, muestran un incremento de las plaquetas, con una duración de meses o años. Por último, los inmunosupresores, alcaloides de la vinca y el danazol, pueden ser agentes beneficiosos en el tratamiento de la PTI refractaria.
Diopathic thrombocytopenic purpura is a relatively common autoimmune hemorrhagic disease. A retrospective study was conducted among 141 patients that received attention from 1983 to 2003 aimed at evaluating the therapeutic results obtained in this disease. Of the total of evaluated patients, 98.6 % needed treatment with different therapeutic schemes and the other 1.4 % showed spontaneoous remissions. The first-line modality (treatment with steroids) was applied to 97.1 % of the patients at the moment of the initial diagnosis. Most of them had a favorable response (65.7 %). Splenectomy was the second therapeutic modality and it was performed in 54.6 % of the sick. It had long periods of remission (62 %, 59.7 % and 54.5 % of sustained complete response at 3, 6 and 12 months postsplenectomy). The third-line treatment was used in 29.1 % of the cases refractory to the therapies selected, with an index of response of 61.0 %. Prednisone alone or combined was the most used therapeutic agent after the failure with steroids and/or splenectomy. The immunosuppressors and alkaloids from Vinca were the most efficient in these cases, with 60 % and 71.4 % of responders. Statistical significance was found on evaluating the response attained by the treatment line at one month and at six months, and on comparing the initial response according to age.
Key words: Idiopathic thrombocytopenic purpura, steroid treament, splenectomy, immunosuppressors.
1. Kumar S, Dieh M, Gertz A, Tefferi A. Splenectomy for immune thrombocytopenic purpura: Long-term results and treatment of postsplenectomy relapses. Div Hematol Intern Med 2002;1:312-7.
2. Cines BD, Blanchette VS. Immune thrombocytopenic purpura. N Engl J 2002;346:995-1008.
3. Stasi R, Stipa E, Masi M. Long-term observation of 208 adults with chronic idiopathic thrombocytopenic purpura. Ann J Med 1995;98:436-42.
4. Parker SL. Thrombocytopenia caused by Inmunologic Platelet Destruction: Idiopathic autoimmune thrombocytopenic purpura. En: Lee R, Foerster J, Lukens J, eds. Wintrobe´s Clinical Hematology. Pennsylvania : Lippincott William and Wilkins; 2002. p. 1592-1600.
]]> 5. Dameshek W, Rubio F, Mahoney JP, Reeves WH, Burgin L. Treatment of idiopathic thrombocytopenic purpura (ITP) vvith Prednisone. JAMA 1958;166:1805-15.6. The American Society of Hematology ITP Practice Guideline Panel. Diagnosis and treatment of idiopathic thrombocytopenic purpura: recommendations of the American Society of Hematology. Ann Intern Med 1997;26:319-26.
7. Neylon AJ, Sunders PW, Howard MR, Proctor SJ, Taylor PR. Clinically significant newly presenting autoimmune thrombocytopenic purpura in adults. A prospective study of a population-based cohort of 245 patients. Br J Hematol 2003;122:966-74.
8. George JN. Idiopathic thrombocytopenic purpura current issues for pathogenesis, diagnosis and management in children and adults. Hematology Oncology Section. Curr Hematol Rep 2003;2:381-7.
9. Sandler GS, Kosty MP. Immune thrombocytopenic purpura. Med J 2001;2:11-7.
10. George JN, Woolf SH, Raskob GE. Idiopathic thrombocytopenic purpura a practice guideline develop by explicit methods for the American Society of Hematology. Blood 1996;88:3-40.
11. Wong GC, Lee LH. A study of thrombocytopenic purpura (ITP) patients over a ten year period. Ann Acad Med Singap 1998;27:789-93.
12. Cheng Y, Wong RSM, Soo YOY, Chui CH, Lau FY, Chan NPH, et al. Initial treatment of immune thrombocytopenia purpura with high-dose Dexamethasona. N Engl J Med 2003;349:831-836.
13. Silverman MA, Michelson AE. Idiopathic thrombocytopenic purpura. J Med 2001;2:1-10.
14. Bourgeois E, Caulier M, Delarozee C, Brouillard M, Bauters F, Fenaux P. Long-term follow-up of chronic autoimmune thrombocytopenic purpura refractory to splenectomy: A prospective analysis. Br J Hematol 2003;120(6):1079-88.
]]> 15. Nomura S. Idiopathic thrombocytopenic purpura. Intern Med 2003;61(4):552-7.16. Srinivasan S, Sabapathy K, Bharadwaj T, Sethuraman S. Role of splenectomy in chronic idiopathic thrombocytopenic purpura. J Assoc Physicians India 2003;51:159-62.
17. Mazzuconi MG, Arista MC, Peraino M, Chistolini A, Felici C, Francavilla V, et al. Long-term follow up of autoimmune thrombocytopenic purpura (ATP) patients submitted to splenectomy. Eur J Hematol 1999;62:219-22.
18. Glomsaker T, Faerden AE, Reierten O, Edwin B, Rosseland A. Laparoscopic splenectomy. Tidsskr Nor Laegeforen 1999;119:1268-71.
19. Vianelly N, Valdre L, Fiacchini M, de Vivo A, Gugliotta L, Catani L, et al. Long-term follow-up of idiopathic thrombocytopenic purpura in 310 patients. Hematologic 2001;86:504-9.
20. Gillis S, Eldor A. Immune thrombocytopenic purpura in adults clinical aspects. Baillieres Clin Hematol 1998;11:361-72.
21. Agganwal A. Reprint address about Rituximab and others agents in patients with refractory ITP. South Med J 2002;95:1209-12.
22. Kolodny L, Lawrence LH, Bernard-Uwe S, Harvey B, Yeon SA. Danazol relieves refractory pruritus associated with myeloproliferative disorders and others diseases. Am J Hematol 1996;51:112-6.
23. Fenaux P, Quiquandon I, Huart J, Caulier M, Bauters F. The role of Danazol in the treatment of refractory idiopathic thrombocytopenic purpura (ITP). A report of 22 cases. Nouv Rev Fr Hematol 1990;32:259-64.
24. Keiner A, Gernsheimer S, Slichter SJ. Pulse cyclophosphamide therapy for refractory autoimmune thrombocytopenic purpura. Blood 1995;85:351-8.
]]> 25. Harold Kl, Schlinkert Rt, Mann DK, Reeder CB, Noel CB, Fitch TD, et al. Long-term results of laparoscopic splenectomy for immune thrombociytopenic purpura. Mayo Clin Protc 1999;11:361-72.26. Quiquandon J, Fenaux P, Caulier MT, Pagniez D, Huart JJ, Bauters F. Re-evaluation of the role of Azatioprine in the tretament of adults with chronic idiopathic thrombocytopenic purpura: A report on 53 cases. Br J Hematol 1990; 74:223-8.
27. Huhn RD, Fogarty PF, Nakamura R. High-dose Cyclophosphamide with autologus lymphocyte-depleted peripheral blood stem cell support for treatment of refractory chronic autoimmune thrombocytopenia. Blood 2003;101:71-7.
28. Godeau B, Zini JM, Schaeffer A, Bierling P. High-dose methylprednisolone is an alternative treatment for adults with autoimmune thrombocytopenic purpura refractory to intravenous inmunoglobulins and oral corticosteroids. Ann J Hematol 1995;48:282-4.
29. Facon T, Caulier MT, Wattel E. A randomized trial comparing vinblastine in slow infusion and by i.v. injection in idiopathic thrombocytopenic: A report in 42 patients. Br J Hematol 1994;86:678-80.
30. Ahn YS, Harrintong WJ, Seelman RC, Eytel CS. Vincristine therapy of idiopathic and secondary thrombocytopenias. N Engl J Med 1974;291:376-80.
31. Manoharan A. Slow infusion of vincristine in the treatment of idiopathic of immune thrombocytopenia. Aust NZ J Med 1991;21:405-7.
32. Bussel JB. Fc receptor blockade and immune thrombocytopenic purpura. Sem Hematol 2000;37:261-6.
33. McMillan, R. Long-term outcomes after treatment for refractory immune thrombocytopenic purpura. N Engl J Med 2001;344:1402-3.
34. Ruiz GJ, Lopez B, Flores J, Ruiz A, Romano B. An affordable Fc receptor blockade method to treat patients with chronic refractory immune thrombocytopenic purpura. Hematologica 2001;86:552-3.
]]> 35. Bocher A, Hagman F, Kreiter. Chronic idiopathic thrombocytopenic purpura. Current therapy concept and introduction to phatophysiologic, clinical, diagnosis aspects and treatment. Med Clin 1998;93:707-18.36. Kuwana M. Advances in inmunological aspects of idiopathic thrombocytopenic purpura. Nippon Rinsho 2003;61:670-5.
37. Pizzuto CJ, Gutiérrez EG. Plaquetas y púrpuras trombocitopénicas. En: Pizzuto CJ. Fundamentos de Hematología. 2 ed. México: Médica Panamericana; 1998. p. 289-311.
38. Tarantino MD, Goldsmith G. Treatment of acute immune thrombocytopenic purpura. Sem Hematol 1998;35:28-35.
39. Gigot JF, De Ville J, van Bevers BE, Reding R, Etienne J, Jadoul P, et al. Laparoscopic splenectomy in adults and children: Experience with 31 patients. Surg 1996;119:384-9.Recibido: 20 de agosto de 2006. Aprobado: 13 de septiembre de 2006.
Dra. Geldris P. Hernández Galano. Instituto de Hematología e Inmunología. Apartado Postal 8070, Ciudad de La Habana, CP 10800, Cuba. Tel (537) 6438268, 6438695, 6434214, Fax (537) 442334. e -mail: ihidir@hemato.sld.cu