ARTÍCULO ORIGINAL
Relación entre hemólisis con la presencia y cuantificación de inmunoglobulinas en hematíes, en la anemia hemolítica autoinmune
Relation between hemolysis with presence and quantification of immunoglobulin in red blood cells in cases of autoimmune hemolytic anemia
DrC. Antonio A. Bencomo-Hernández; Dra. María E. Alfonso-Valdés; Dr. Onel M. Ávila-Cabrera; Dr. Edgardo Espinosa-Martínez; Dr. Juan C. Jaime-Fagundo; Prof. DrC. Porfirio Hernández-Ramírez
Instituto de Hematología e Inmunología. Ciudad de La Habana, Cuba. ]]>
RESUMEN
Se realizó estudio en 135 pacientes: 111 adultos y 24 niños con anemia hemolítica autoinmune caliente (AHAIC). La caracterización de los autoanticuerpos eritrocitarios y el número de moléculas de inmunoglobulinas por hematíe se determinó en un ELISA. En 51 pacientes se investigó, además, el patrón de subclases de IgG. La intensidad de la hemólisis se clasificó por la concentración de hemoglobina, el conteo de reticulocitos y las cifras de haptoglobina plasmática. En los pacientes con hemólisis de alto grado se detectaron autoanticuerpos IgM en combinación con los isotipos IgG, IgA. En los casos con presencia únicamente de IgG, el número de moléculas de autoanticuerpos por hematíe fue el factor determinante en la hemólisis. No se observaron diferencias en relación con el patrón de subclases. La severidad de la hemólisis en la AHAIC está en relación con la coexistencia de múltiples inmunoglobulinas en los hematíes y en especial de la IgM.
Palabras clave: anemia hemolítica autoinmune, autoanticuerpos, subclases de IgG, cuantificación, ELISA.
ABSTRACT ]]>
A group of 135 patients was studied: 111 adults and 24 children presenting hot autoimmune hemolytic anemia (HAIHA) The erythrocyte characterization and the number of immunoglobulin molecules by red blood cells was determined by ELISA. In 51 patients the pattern of IgG subclasses was investigated. The hemolysis intensity was classified by the hemoglobin concentration, the reticulocytes count and the figures of plasma haptoglobin. In patients presenting with high degree hemolysis IgM autoantibodies were detected in combination with IgG, IgA isotypes. In cases only with the presence of IgG, the number of molecules of autoantibodies by red blood cells was the determinant factor in hemolysis. There were not differences in relation to subclasses pattern. The severity of hemolysis in HAIHA is related to the coexistence of multiple immunoglobulins in red blood cells and especially of the IgM.Key words: Autoimmune hemolytic anemia, autoantibodies, IgG subclasses, quantification, ELISA.
INTRODUCCIÓN
La prueba de antiglobulina (Coombs) directa es el método más empleado para el diagnóstico inmunohematológico de las anemias hemolíticas autoinmunes. La mayoría de los casos se clasifican como anemia hemolítica autoinmune caliente (AHAIC) por la presencia de autoanticuerpos IgG reactivos a 37 oC y en menor frecuencia, de los isotipos IgA e IgM.1
La repercusión clínica del resultado de la prueba de antiglobulina directa (PAD) todavía es un tema de estudio, debido al hallazgo de casos con PAD intensamente positiva con hemólisis ligera y de otros con PAD débil positiva, incluso negativa, con anemia grave.2 Múltiples factores se invocan en relación con la intensidad de la hemólisis como: la detección de autoanticuerpos de varios isotipos, las subclases de IgG presentes y la función del sistema mononuclear fagocítico de los pacientes, entre otros.3
Los estudios relacionan los autoanticuerpos de la subclase IgG3, con una hemólisis severa,4 aunque otros autores han demostrado autoanticuerpos de esta subclase en los hematíes de pacientes sin evidencias clínicas de hemólisis.5 La hemólisis autoinmune mediada por autoanticuerpos de la subclase IgG2 es muy poco frecuente y los anticuerpos de la subclase IgG4 no median la destrucción inmune de los hematíes. Al parecer, la destrucción de los hematíes por la IgG1 depende de la concentración de los autoanticuerpos que recubren a los hematíes in vivo.3
No obstante, el valor de la cuantificación de autoanticuerpos en relación con el grado de hemólisis es un aspecto controvertido. Van der Meulen y otros, fueron los primeros en encontrar que la intensidad de la hemólisis depende de la concentración de autoanticuerpos;6 sin embargo, estudios posteriores concluyeron que aunque existe una relación cuantitativa, este parámetro, por sí solo, no es aplicable en todos los casos.7
La sensibilidad de los métodos de detección y de cuantificación empleados es otro de los factores que pueden influir en la variabilidad de los resultados. Es conocido que la PAD tiene limitaciones, ya que en ocasiones no detecta los autoanticuerpos IgA e IgM, aún con el uso de reactivos antiglobulínicos monoespecíficos. Por otra parte, no permite la cuantificación de las inmunoglobulinas en los hematíes.8 ]]>
Nuestras investigaciones previas demostraron que el ELISA es un método más sensible que la PAD para la detección de autoanticuerpos IgG, IgA e IgM en el eluato de hematíes de lo pacientes con AHAIC, además de permitir la determinación de su concentración expresada en número de moléculas de anticuerpos por hematíe.9 En este estudio se identifica la asociación entre la intensidad de la hemólisis con la presencia y concentración de autoanticuerpos de los isotipos IgG, IgA e IgM detectados a través del ELISA, así como su relación con la detección de autoanticuerpos de las diferentes subclases de IgG en los hematíes de los pacientes con AHAIC.
MÉTODOS
El diagnóstico de AHAIC se realizó por una disminución de la hemoglobina inferior a 120g/L, un incremento de los reticulocitos superior al 2 % y de la bilirrubina no conjugada a valores superiores a 13,7 µmol/L. En todos los casos, la PAD fue positiva con suero de antiglobulina humana poliespecífico con actividad anti-IgG y anti-C3dg y se confirmó la ausencia de autoanticuerpos fríos de importancia clínica. El hemograma se realizó por las técnicas convencionales y sus resultados se obtuvieron de la historia clínica. Todos los casos fueron investigados en el Departamento de Inmunohematología del Instituto de Hematología e Inmunología.
El estudio se realizó en una muestra de 135 pacientes: 111 adultos (76 femeninos y 35 masculinos) y 24 niños (13 femeninos y 11 masculinos) al diagnóstico de la AHAIC, cuando aún no habían recibido tratamiento para esta enfermedad. El rango de edad de los adultos fue de 20 a 88 años y de 1 a 16 años para los niños. En 70 casos (51,8 %) la AHAIC se consideró idiopática (8 con síndrome de Evans-Fisher); en el resto estuvo asociada con otras enfermedades como: 20 pacientes con hemopatías malignas, 5 con tumores sólidos, 6 con otras enfermedades autoinmunes, 27 con infecciones virales, 4 secundarios al tratamiento con alfa metildopa y en 3, asociado con otras enfermedades.
El patrón de inmunoproteínas presentes en los eritrocitos y el número de moléculas de inmnunoglobulinas (Igs) por hematíe se determinó en un ensayo inmunoenzimático (ELISA) para la cuantificación de IgG, IgA e IgM en el eluato, obtenido por el método del éter,10 a partir de 1 mL de hematíes.
El ELISA se realizó en placas de poliestireno de 96 pocillos de fondo plano (Nunc, Immunoplates) que se recubrieron con 100 µL en el pocillo correspondiente, de la fracción IgG de anticuerpos de carnero anti- IgG(g), anti-IgA(a) o anti-IgM(µ) humano (Sigma), a una concentración de 5 µg/mL en solución balanceada de carbonato bicarbonato 0,05M a pH 9,6. Las placas se incubaron a 4 oC durante 16-18 horas y fueron posteriormente lavadas 4 veces con solución salina balanceada con fosfato 0,15 mol/L pH 7,2 con tween 20 al 0,2 % (SSBF-Tw). Los eluatos de los hematíes de los pacientes y la curva patrón de IgG, IgA e IgM diluidos en SSBF-Tw 0,05 % con albúmina bovina al 0,4 % (SSBF-Tw-A) se añadieron a razón de 100 µL por pocillo y se incubaron a 37 oC durante 1 hora. Las curvas de cuantificación se prepararon a partir del suero de referencia Nor-Partigen, Behring en concentraciones desde 0,0025 a 0,07 µg/mL de IgG e IgM; y de 0,0025 µg a 0,06 µg/mL de IgA. Los 4 lavados posteriores se realizaron con SSBF-Tw 0,05 % y se añadieron a los pocillos apropiados 100 µL de la fracción IgG de carnero conjugado con peroxidasa (Sigma) anti-Fc de la IgG e IgM humana diluidos 1: 5000, o anti-Fc de la IgA humana diluido 1:1000 en SSBF-Tw 0,05 %. Las placas se incubaron con los conjugados durante 1 hora a 37 oC y fueron posteriormente lavadas 4 veces con SSBF-Tw 0,05 %. La reacción se reveló con la adición de 100 µL por pocillo de ortofenilendiamina (Merck) en una concentración de 0,24 mg/mL en solución balanceada de ácido cítrico pH 5,0 que contenía peróxido de hidrógeno al 0,024 %. La reacción se detuvo a los 15 min con la adición de 100 mL por pocillo, de ácido sulfúrico 3M; las densidades ópticas de cada muestra en duplicado se leyeron a 492 nm en un lector de microelisa (Titertek Multiscan). Las concentraciones de Igs en los eluatos fueron calculadas a partir de la curva patrón por medio de un ensayo de regresión lineal. El resultado se expresó como un aproximado del número de moléculas de Igs por hematíe con el uso del número de Avogadro y del peso molecular de la IgG o IgA (160,000 daltons) y de la IgM (970,000 daltons). De acuerdo con el número de Avogadro 1 µg contiene 370 X 1010 moléculas de IgG o IgA y 62 X 1010 moléculas de IgM. El número de moléculas de Igs por hematíe es igual a la concentración de Igs en µg/ mL del eluato multiplicado por el número de moléculas de Igs en 1µg y dividido entre el número de hematíes en 1 mL (1,1 x 1010 hematíes).9 Se consideró como valor positivo en el ELISA un número de moléculas por hematíe de IgG³163, de IgA³90 y de IgM³20 moléculas, que corresponde con la media más 3 desviaciones estándar de los valores obtenidos en los individuos normales .
En 51 pacientes con autoanticuerpos de la clase IgG se investigaron además las subclases presentes en los eluatos en la técnica de microplacas descrita previamente y que se resume a continuación:11
Se sensibilizó una mezcla de hematíes de donantes de sangre de grupo "O" con cada uno de los eluatos de los hematíes de los pacientes y se incubaron a 37 ºC durante 1 hora. Posteriormente, los hematíes se lavaron 3 veces con solución salina al 0,9 % y se resuspendieron al 0,5 % en solución salina. En microplacas fondo en V (Greiner) se mezclaron, en el pocillo correspondiente, 25µL de la suspensión de los hematíes sensibilizados con 25µL de la dilución 1:20 en solución salina balanceada de fosfato 0,15 mol/L de pH 7,2 (SSBF) que contenía suero fetal bovino al 1 %, de los reactivos anti-IgG1, -IgG2, -IgG3 y anti-IgG4 (CLB, Amsterdam). Como controles positivos se utilizaron hematíes sensibilizados con anticuerpos monoclonales anti-D (IgG) de las 4 subclases y como control negativo, hematíes del grupo "O" no sensibilizados. La placa se incubó 12 horas a 4 °C y la lectura se realizó después de inclinarla en un ángulo de 45 o durante 10 min. Se consideró un resultado positivo la presencia de un botón de hematíes en el fondo del pocillo y como negativo, el corrimiento de los hematíes hasta sus bordes externos.
A todos los pacientes se les determinaron los valores de haptoglobina plasmática estimada por su capacidad de unión con la hemoglobina y su posterior separación por filtración en gel (Sephadex G-100, Pharmacia). Los valores normales de haptoglobina plasmática de referencia oscilan entre 0,4 y 2,4 g/L. ]]>
La intensidad de la hemólisis se clasificó según la concentración de hemoglobina (Hb), el conteo de reticulocitos y las cifras de haptoglobina plasmática. Se consideró en el grupo con hemólisis de alto grado a aquellos casos que presentaron cifras de Hb menores de 90 g/L, conteo de reticulocitos superiores al 5 % y valores de haptoglobina menores de 0,4g/L; y en el grupo con hemólisis de bajo grado, aquellos casos que presentaron cifras de Hb mayores o iguales a 90 g/L, conteo de reticulocitos entre el 3 y el 5 % y valores normales de haptoglobina plasmática.Se utilizó la prueba de Chi-cuadrado (X2) para el análisis de la distribución de los patrones de Igs y de las subclases de IgG en los hematíes de los pacientes de los grupos con hemólisis de alto y bajo grado. La prueba U de Mann-Whitney se empleó para la comparación entre el número de moléculas de Igs/hematíes de acuerdo con la intensidad de la hemólisis. Para ambos ensayos se consideró significativo un valor de p<0,05.
RESULTADOS
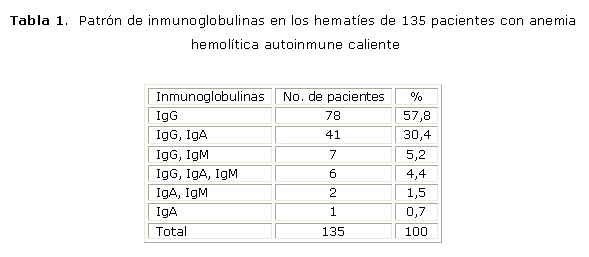
En el 97,8 % de los pacientes se detectó IgG en los hematíes. Los autoanticuerpos de la clase IgA se evidenciaron en el 36,3 % y los de la clase IgM en el 11,1 %. En un paciente se identificaron solo autoanticuerpos IgA (tabla 1).
Los autoanticuerpos de la subclase IgG1 fueron los más frecuentes y se hallaron combinaciones de subclases en 26 pacientes (51,0 %) la combinación de IgG1+ IgG3 fue la más observada (23,6 %). En 2 casos, la subclase IgG2 fue la única identificada en los hematíes (tabla 2).

Los autoanticuerpos IgM en combinación con los de los isotipos IgG, IgA o con ambos, se detectaron solamente en los pacientes con hemólisis de alto grado. El número de moléculas de IgM por hematíe no fue objeto de análisis debido a que todos los casos con autoanticuerpos IgM pertenecían a este grupo. La presencia en los eritrocitos de IgG e IgA fue más frecuente también en el grupo con hemólisis de alto grado (tabla 3). El número de moléculas de IgG e IgA por hematíe no mostró diferencias significativas entre los grupos estudiados en los pacientes con este patrón de Igs en los eritrocitos (tabla 4).
La mayoría de los casos en los que se detectó IgG como única inmunoproteína en los hematíes fueron clasificados dentro del grupo con hemólisis de bajo grado (tabla 3). Sin embargo, el número de moléculas de IgG por hematíe fue significativamente superior (p=0,003) en los pacientes del grupo con hemólisis de alto grado (tabla 5). No fue posible definir un valor de corte en el número de moléculas de IgG que permita diferenciar a los pacientes por la severidad de la hemólisis debido a la gran superposición de los resultados (figura). No se observaron diferencias significativas entre la presencia de IgG3, IgG1 o de 2 o más subclases en los eritrocitos de los pacientes estudiados (tablas 6-7).
]]>
DISCUSIÓN
En la AHAI, los anticuerpos causantes de la hemólisis son predominantemente de la clase IgG y con menor frecuencia de las clases IgA e IgM.12 Los resultados de este estudio apoyan estas afirmaciones y coinciden con los comunicados por otros autores para las frecuencias de autoanticuerpos de las clases IgG e IgM, no así en lo que respecta a la IgA.3,13,14
La presencia de IgA en los hematíes se ha demostrado entre el 6 y el 14 % de los pacientes con AHAI.15,16 La frecuencia de autoanticuerpos IgA en el grupo de pacientes que fueron analizados es superior a lo comunicado previamente, debido a que en el estudio se empleó un ensayo inmunoenzimático para la cuantificación de Igs en los hematíes, que es un método más sensible que las técnicas de aglutinación. La AHAI mediada únicamente por autoanticuerpos de la clase IgA es poco frecuente y se ha identificado en el 0,2 % del total de pacientes, lo que es similar a lo encontrado en nuestra serie.17
La distribución de las subclases de IgG de los autoanticuerpos y sus combinaciones se asemejan a las comunicadas en otros estudios.3 La presencia de únicamente autoanticuerpos IgG2 en los hematíes se identificó en el 3,9 % de los pacientes, lo que coincide con lo demostrado por otros autores,5 pero difiere de otras investigaciones en las que se encontró en menos del 1 % de los casos.18 Estas diferencias podrían atribuirse al número de pacientes estudiados y al método de detección de las subclases empleado en los diferentes estudios.
Muy pocas investigaciones han abordado la relación entre la coexistencia de múltiples inmunoglobulinas en los hematíes con la hemólisis mediada por autoanticuerpos, debido probablemente a que con los procedimientos convencionales se detecta este patrón en el 15 % de los casos.3 Sin embargo, con la introducción de técnicas más sensibles, se demuestra en el 37 % de los pacientes con AHAI.18
El único estudio realizado con el empleo de un ELISA directo cualitativo concluye que la identificación de autoanticuerpos IgG acompañados de autoanticuerpos IgA, IgM o de ambas Igs, es la causa principal de la hemólisis autoinmune.18 Esta investigación relacionó la presencia de 2 o más Igs con la severidad de la hemólisis, pero no clasificó a los pacientes de acuerdo con el patrón específico de las Igs detectadas en sus eritrocitos.
Nuestro estudio sugiere que la presencia en los hematíes de autoanticuerpos IgM, en combinación con autoanticuerpos de los isotipos IgG, IgA o con ambos, es un factor fundamental en la severidad de la hemólisis en los pacientes con AHAI. Estos hallazgos difieren de los anteriores y lo atribuimos a la IgM, cuando está presente, el papel primordial como mediador de la hemólisis, al encontrarse que todos los pacientes con autoanticuerpos de este isotipo fueron clasificados dentro del grupo con hemólisis de alto grado. Las discrepancias entre nuestros resultados con los comunicados previamente pueden deberse a las diferencias en las metodologías empleadas para la clasificación de los pacientes de acuerdo con los isotipos de los autoanticuerpos detectados.
Los hematíes sensibilizados con autoanticuerpos IgM, IgG e IgA son atrapados eficientemente por lo macrófagos del bazo y del hígado a través de los receptores para el fragmento Fc de la IgG (RFcg) y de la IgA (RFca) y por los receptores RC1 y RC3 para los fragmentos C3b y C3bi del complemento. La presencia de estos últimos es mediada fundamentalmente por los anticuerpos IgM.19
Los autoanticuerpos calientes IgM generalmente son monómeros y no provocan la lisis directa de los hematíes mediada por complemento, debido a la acción de las proteínas inhibidoras del complemento presente en la membrana de dichas células. Dentro de estas se encuentran el factor acelerador de la degradación o DAF (CD55), que impide el ensamblaje de la C3 convertasa; la proteína de unión al C8 que interfiere en la interacción C8-C9 y en la polimerización de este último; y el CD59 o inhibidor de la lisis reactiva (MIRL) que evita la incorporación del C9 en el complejo C5b-9. Por lo tanto, la activación del complemento culmina con la deposición en los hematíes del C3b que es reconocido por sus receptores en los macrófagos y se produce la fagocitosis o la lisis citotóxica de estas células.3,20 ]]>
No obstante, es difícil evaluar la patogenicidad de los autoanticuerpos IgM cuando estos concomitan con autoanticuerpos IgG e IgA. En el reducido número de casos en los que se han identificado únicamente autoanticuerpos IgM, hay evidencias de hemólisis intravascular con una mortalidad significativa, lo que confirma su importancia clínica.21,22La mayoría de los pacientes con IgG e IgA en los hematíes fueron clasificados con hemólisis de alto grado. Los eritrocitos recubiertos con anticuerpos IgA son destruidos por un mecanismo similar al de la IgG, aunque en ocasiones pueden activar el complemento por la vía alternativa, probablemente vía lectina, y provocar hemólisis intravascular.23,24
Se ha demostrado que existe un efecto sinérgico de los autoanticuerpos IgA con los IgG, especialmente con los IgG1, en la aparición de hemólisis severa.15 No obstante, el 34 % de los pacientes estudiados con autoanticuerpos de estos isotipos fueron clasificados con hemólisis de bajo grado, por lo que otros factores pueden influir en la destrucción de los eritrocitos por los autoanticuerpos. Dentro de estos se señala la actividad del sistema mononuclear fagocítico de los pacientes y el balance de citocinas que regulan la expresión de los receptores Fc presentes en los macrófagos, y de esta forma, modulan la destrucción inmune de los hematíes.25
Janvier y otros, comunicaron un caso de AHAI severa mediada por autoanticuerpos IgA que reconocen a antígenos localizados en el tercer lazo de la banda 3 eritrocitaria.26 Otros autores han encontrado que estos autoanticuerpos tienen especificidad para los antígenos del sistema Rh y en un caso no se realizó su identificación,27,28 por lo que la especificidad de los autoanticuerpos IgA no ha sido apropiadamente evaluada como un factor que pudiera influir en su patogenicidad.
Generalmente la destrucción de los hematíes es proporcional a la cantidad de anticuerpos unidos con estas células.25 Sin embargo, no se encontraron diferencias entre el número de moléculas de IgG e IgA por hematíe en los pacientes de los grupos con hemólisis de alto y bajo grado. Hasta donde conocemos, no se han realizado estudios previos de cuantificación de autoanticuerpos IgA y su relación con la intensidad de la hemólisis que permitan comparar estos resultados. Al parecer, la coexistencia de autoanticuerpos IgG e IgA por sí misma predispone a una mayor severidad de la hemólisis no influenciada por el número de moléculas de estas Igs que recubren a los eritrocitos in vivo.
En el estudio se demostró, además, un aumento significativo en el número de moléculas de IgG por hematíe en los pacientes con este patrón serológico pertenecientes al grupo con hemólisis de alto grado en comparación con los del grupo con hemólisis de bajo grado.
Otros autores han obtenido evidencias a favor de que la cantidad de IgG unida con los eritrocitos pueda predecir la gravedad de la hemólisis en los pacientes con AHAI.6,29 En contraste, Garratty y Nance no pudieron confirmar este hallazgo en un estudio posterior.7 Las divergencias entre estos resultados pudieran estar relacionadas con diferencias en los reactivos antiglobulínicos utilizados, la selección de los pacientes estudiados y los criterios usados para la clasificación de la hemólisis.
Nuestros resultados, sin embargo, coinciden con los de estos autores7 en cuanto a que no es posible determinar un umbral que pueda predecir la ocurrencia o no de hemólisis, ya que se demuestra un gran solapamiento de los valores de cuantificación de IgG por hematíe entre pacientes con diferentes grados de hemólisis. Como se expuso anteriormente, otros factores modulan la destrucción inmune de los hematíes que pueden influir en los resultados.
La presencia de IgG3 y de múltiples subclases de autoanticuerpos se asocia con signos de hemólisis manifiesta.13,18 La IgG3 es más eficiente que la IgG1 en su interacción con los macrófagos, debido a su gran afinidad por los receptores Fc presentes en estas células.4,5.
En nuestro estudio no se obtuvieron diferencias significativas en la distribución de los autoanticuerpos IgG3 e IgG1 entre los pacientes de los grupos con hemólisis de alto y bajo grado. Otros autores encontraron resultados similares y han demostrado la presencia de estas subclases en los eritrocitos de donantes con prueba de antiglobulina positiva sin manifestaciones de anemia.5,30 ]]>
Por otra parte, aunque la presencia de múltiples subclases en los hematíes fue más frecuente en los pacientes con hemólisis de alto grado, no se obtuvieron diferencias significativas en la distribución de este patrón entre los grupos estudiados. Es conocido que el patrón de subclases depende de factores como la presentación antigénica, el microambiente de citocinas y de factores genéticos; no obstante, consideramos que las diferencias con otros estudios pudieran atribuirse también a que la caracterización de las subclases de los autoanticuerpos se realizó en una muestra reducida de los casos.Los hallazgos de este estudio permiten plantear que la severidad de la hemólisis en los pacientes con AHAIC se relaciona con la coexistencia de múltiples inmunoglobulinas en los hematíes, y en especial, de la IgM. En los pacientes con presencia únicamente de IgG, el número de moléculas de autoanticuerpos por hematíe es un factor determinante en la hemólisis, aunque este parámetro por sí solo no pueda explicar las discrepancias observadas en muchos casos.
Más allá de estas consideraciones, la cuantificación de autoanticuerpos en los hematíes es una herramienta que podría emplearse para la evaluación del tratamiento inmunosupresor y en la decisión de la conducta terapéutica en estos pacientes. Con este ensayo es posible determinar la concentración de autoanticuerpos en los hematíes en estudios longitudinales en relación con el tratamiento y de esta forma, podría evaluarse en cada paciente la respuesta al fármaco administrado.
REFERENCIAS BIBLIOGRÁFICAS
1. Packman CH. Hemolytic anemia due to warm autoantibodies. Blood Rev 2008;22:17-31.
2. Garraty G. The James Blundell Award Lecture 2007: Do we really understand immune red cell destruction? Transf Med 2008;18:321-34.
3. Petz LD, Garraty G. Immune hemolytic anemias. 2 ed. Philadelphia: Churchill Livingstone; 2004.
4. Das SS, Nityanand S, Chaudhary R. Clinical and serological characterization of autoimmune hemolytic anemia in a tertiary care hospital in North India. Ann Hematol 2009;88:727-32.
5. Garratty G. Factor affecting the pathogenicity of red cell auto and alloantibodies. En: Nance S, ed. Immune destruction of red cell. Arlington, VA: American Association of Blood Banks; 1989. pp. 109-69.
6. Van der Meulen FW, de Bruin HG, Goosen PCM. Quantitative aspects of the destruction of red cells sensitized with IgG1 autoantibodies: An application of flow cytofluorometry. Br J Haematol 1980;46:47-56.
7. Garratty G, Nance SJ. Correlation between in vivo hemolysis and the amount of red cell-bound IgG measured by flow cytometry. Transfusion 1990;30:617-21.
8. Petz LD. Diagnostic complexities in autoimmune hemolytic anemias. Transfusion 2009;49:202-3.
9. Bencomo AA, Díaz M, Alfonso Y, Valdés O, Alfonso ME. Quantitation of red cell-bound IgG, IgA, and IgM in patients with autoimmune hemolytic anemia and blood donors by enzyme-linked immunosorbent assay. Immunohematology 2003;19:47-53.
10. Brecher ME, ed. AABB Technical manual. 14 ed. Bethesda, MD: American Association of Blood Banks; 2002.
11. Alfonso Y, Bencomo AA, Díaz M, Alfonso ME. Micrométodo para la detección de clases y subclases de inmunoglobulinas en el eluido de eritrocitos de pacientes con AHAI. Rev Cubana Hematol Inmunol Hemoter 2002;18:20-6.
12. Khan S. Clinical utility of the Coombs test. Can Med Assoc J 2006;175:919.
13. Gehrs BC, Friedberg RC. Autoimmune hemolytic anemia. Am J Hematol 2002;69:258-71.
14. Genty I, Michel M, Hermine O, Schaeffer A, Godeau B, Rochant H. Characteristics of autoimmune hemolytic anemia in adults: Retrospective analysis of 83 cases. Rev Med Intern 2002;23:901-9.
15. Sokol RJ, Booker DJ, Stamps R, Booth JR, Hook V. IgA red cell autoantibodies and autoimmune hemolysis. Transfusion 1997;37:175-81.
16. Vaglio S, Arista MC, Perrone MP, Tomei G, Testi AM, Coluzzi S, et al. Autoimmune hemolytic anemia in childhood: serologic features in 100 cases. Transfusion 2007;47:50-54.
17. Sokol RJ, Booker DJ, Stamps R, Booth JR. Autoimmune hemolytic anemia due to IgA class autoantibodies. Immunohematology 1996;12:14-9.
18. Sokol RJ, Hewitt S, Booker DJ, Bailey A. Erythrocyte autoantibodies, subclasses of IgG and autoimmune haemolysis. Autoimmunity 1990;6:99-104.
19. Yazkanbakhsh K. Controlling the complement system for prevention of red cell destruction. Curr Opin Hematol 2005;12:117-22.
20. Daniels G. Functions of red cell surface proteins. Vox Sang 2007;93:331-40.
21. Nowak-Wegrzyn A, King KE, Shirey RS, Chen AR, McDonough C, Lederman HM. Fatal warm autoimmune hemolytic anemia resulting from IgM autoagglutininis in an infant with severe combined immunodeficiency. Am J Pediatr Hematol Oncol 2001;23:250-2.
22. Arndt PA, Leger RM, Garratty G. Serologic findings in autoimmune hemolytic anemia associated with immunoglobulin M warm autoantibodies. Transfusion 2009;49:235-42.
23. Becker EA, van Guldener C, Overbeeke MA, van Rhenen DJ. Intravascular hemolysis by IgA red cell autoantibodies. Neth J Med 2001;58:204-7.
24. Suankratay C, Zhang Y, Jones D, Lint TF, Gewurz H. Enhancement of lectin pathway haemolysis by immunoglobulins. Clin Exp Immunol 1999;117:435-41.
25. Domen RE. Warm red blood cell autoantibodies and the direct antiglobulin test revisited. Am J Clin Pathol 2004;122:673-4.
26. Janvier D, Sellami F, Missud F, Fenneteau O, Vilmer E, Cartron J, et al. Severe autoimmune hemolytic anemia caused by a warm IgA autoantibody directed against the third loop of band 3 (rbc anion-exchange protein 1). Transfusion 2002;42:1547-52.
27. Sokol RJ, Booker DJ, Stamps R, Murphy F, Booth JR. Severe autoimmune haemolytic anaemia due to strong IgA class autoantibodies showing Rh especificity. Transfus Med 1994;4(suppl 1):47.
28. Bardill B, Mengis C, Tschopp M, Wuillemin WA. Severe IgA-mediated auto-immune haemolytic anaemia in a 48-yr-old woman. Eur J Haematol 2003;70:1-4.
29. Lin JS, Hao TC, Lyou JY, Chen YJ, Liu HM, Tzeng CH, et al. Clinical application of a flow cytometric direct antiglobulin test. Transfusion 2009;49:1335-46.
30. Bellia M, Georgopoulos J, Tsevrenis V, Nomikou E, Vgontza N, Kontopoulou-Griva I. The investigation of the significance of a positive direct antiglobulin test in blood donors. Immunohematology 2002;18:78-81.
]]>
Recibido: 1 de junio del 2010.
DrC. Antonio A. Bencomo-Hernández. Instituto de Hematología e Inmunología. Apartado 8070, CP 10800. Ciudad de La Habana, Cuba. Tel (537) 643 8695, 8268. Fax (537) 644 2334. E-mail: ihidir@hemato.sld.cu
]]>