Caracterización fenotípica de células madre mesenquimales humanas de médula ósea y tejido adiposo. Resultados preliminares
Phenotypic characterization of mesenchymal human stem cell from bone marrow and adipose tissue.preliminary results
]]>
DraC. Consuelo Macías-AbrahamI, Lic. Lázaro O del Valle-PérezI, DrC. José Armando Galván CabreraI, Lic.Karelys de la Cuétara BernalII, Lic. Berta B Socarrás FerrerI, Prof, DrC. Porfirio Hernández RamírezI, Prof. DrC. José M Ballester SantoveniaI
I Instituto de Hematología e Inmunología, La Habana, Cuba.
II Centro Internacional de Restauración Neurológica, La Habana, Cuba.
]]>
Introducción: las células madre mesenquimales (CMM) poseen características fenotípicas y funcionalesque les confieren un amplio potencial terapéutico por su posible uso en la terapia celular regenerativa, en el rechazo del trasplante alogénico y en enfermedades inflamatorias crónicas.
Objetivo: evaluar la expresión de moléculas de membrana que permiten identificar la expresión de patrones moleculares característicos de CMM humanas mantenidas en cultivo.
Métodos: se estudió la expresión fenotípica de células mononucleares procedentes de médula ósea obtenidas mediante aspiración medular, separadas por gradiente de Ficoll y cultivadas ex vivo entre los pases o subcultivos 3 y 16; y adipocitos cultivados procedentes de la extracción enzimática de tejido adiposo de donantes sanos. Se realizó doble marcaje para las moléculas CD34/CD45, CD34/CD90, CD34/CD117, y CD34/CD44.
Resultados: en los resultados preliminares obtenidos se observó que las células cultivadas procedentes de médula ósea, entre los pases 4 y 8 de cultivo expresaron 45,13 % de células CD34-/CD45- (doblemente negativas), lo que correspondió con el 25,24 % de células CD34-/CD90+ y el 96,90 % de CD34-/CD117-. En las células procedentes de cultivo de adipocitos se observó el52,3 % de CD34-/CD45- (doblemente negativas),12,31 % de CD34-/CD90+,43,31 % de CD34-/CD117- y 64,68 % de CD34-/CD44+.Estos resultados sugieren que ambos cultivos se diferenciaron a CMM. Las CMM procedentes de adipocitos mostraron el 64,68 % de células con expresión de la molécula de adhesión CD44 a la que se atribuyen propiedades funcionalescomo el asentamiento tisular.
Conclusiones: estos resultados preliminares permiten corroborar que ambos métodos experimentales de cultivo son efectivos para la obtención de CMM con fines terapéuticos.
Palabras clave: células madres mesenquimales humanas, caracterización fenotípica, medicina regenerativa.
ABSTRACT ]]>
Introduction: mesenchymal stem cells (MSCs) have phenotypic and functional characteristics whichgives them a broad therapeutic potential for possible use in regenerative cell therapy, allogeneic transplant rejection and chronic inflammatory diseases.Keywords: human mesenchymal stem cells, phenotypic characterization, regenerative medicine.
INTRODUCCIÓN ]]>
La adherencia y la capacidad multipotencial de las células mononucleares (CMN) de la médula ósea de diferenciarse y proliferar a células del tejido al que son trasplantadas, se encuentran directamente relacionadas con la expresión de determinadas moléculas en su membrana o fenotipo de diferenciación y con la interacción de las moléculas de adhesión con sus ligandos a nivel del tejido receptor. La caracterización de las células empleadas en la terapia celular es de gran importancia para el perfeccionamiento de este proceder terapéutico.1Las células madre mesenquimales (CMM) son clasificadas como células madre adultas ya que tienen la capacidad de diferenciarse a células neuronales, pulmonares, islotes de células beta pancreáticas, células epiteliales corneales y cardiomiocitosex vivo e in vivo, por lo que pueden usarse para el tratamiento de numerosos tejidos dañados y desórdenes degenerativos.2-7 Las CMM residentes en la medula ósea son designadas también como células estromales y su progenie bien diferenciada localizada en los nichos perivasculares tienen la capacidad de regenerar estroma medular, osteocitos, condrocitos, adipocitos vasos sanguíneos y miocitosin vivo e in vitro, por lo que se le ha adjudicado a este tipo celular un amplio potencial en la práctica clínica.2-7
Las CMM poseen propiedades que permiten una obtención y manipulación favorables para su manejo en el laboratorio, como son los altos índices de proliferación en expansiones ex vivo y la capacidad de diferenciación a diferentes líneas celulares.4 Estas células pueden obtenerse a partir de la médula ósea y se identifican por sus marcadores específicos como CD29, CD44, CD71, CD90, CD13, CD105, SH-3 y STRO-1, así como también del tejido adiposo (células madre derivadas de tejido adiposo) mediante extracción enzimática con lo que se obtiene hasta 40 veces más CMM que de médula ósea.4,8Aunque presentan características fenotípicas muy similares, las CMM derivadas del tejido adiposo expresan marcadores de adhesión específicos como son CD49d (VLA-4), CD106 (VCAM-1) e CD54 (ICAM-1) conocidas por su amplia participación en la interconectividad celular y la respuesta inflamatoria. Sin embargo, no se han descrito diferencias funcionales en la adherencia, crecimiento y diferenciación a otros tipos celulares entre ambas.8-11
La Sociedad Internacional de Terapia Celular (ISCT, del inglés: International Society of CellularTherapy) propuso tres criterios para definir las CMM:deben ser adherentes en cultivo; expresar los antígenos CD73, CD90 y CD105 en ausencia de antígenos hematopoyéticos como CD34 y CD45, marcadores de monocitos, macrófagos y linfocitos B; y diferenciarse in vitro en osteoblastos, adipocitos y condrocitos, bajo condiciones estándares de cultivo.10,12 Dos aspectos adicionales para clasificarlas como células madre son: 1)las CMM realizan procesos de autorrenovación; y 2)son capaces de desarrollar «plasticidad clonogénica» o diferenciación hacia tejidos de diferentes capas embrionarias como ectodermo y endodermo.6
Se ha demostrado que las CMM humanas inducen inmunosupresión 12-16 y pueden ser utilizadas como matriz para la expansión de poblaciones enriquecidas de células CD34+por su potencial terapéutico en la enfermedad de injerto contra huésped.17,18 También se les atribuyen potencialidades terapéuticas para las enfermedades autoinmunes, el rechazo de trasplante de órganos y el control de procesos inflamatorios.
Tres mecanismos fundamentales contribuyen al efecto supresor sobre la reacción alogénica:12-14 1) son hipoinmunogénicas, pues no expresan antígenos de clase II y otras moléculas coestimulatorias; 2) previenen la respuesta de las células T indirectamente a través de la modulación de las células dendríticas, durante su maduración pueden inhibir la expresión de moléculas involucradas en la presentación de antígenos como CD1a, CD40, CD80, CD86 y HLA-DR 19 y actúan directamente inhibiendo la función de las células asesinas naturales (inhibiendo la proliferación y producción de IFN) y las células T CD4+, e inducen un fenotipo regulador CD4+/CD25alto, CD4+/CTLA-4+, CD4+/CD25+/CTLA-4+;20 y 3)inducen un microambiente supresor local a través de la producción de prostaglandinas e interleucina-10.13Esta acción inmunorreguladora es comparable con la referida en la tolerancia materno-fetal y similar a la descrita en los mecanismos de evasión o escape del tumor a la respuesta inmunológica norma.9
Por su importancia para la introducción en la práctica clínica, se evaluó la expresión fenotípica de moléculas de membrana que permitieran identificar y confirmar la expresión de patrones moleculares característicos de CMM humanas en células procedentes de CMN de médula ósea y de tejido adiposo mantenidas en cultivo, en ambos casos a partir de donantes sanos, obtenidas por primera vez en Cuba.
]]>
MÉTODOSCaracterísticas de la muestra
CMM procedentes de cultivo ex vivo de CMN humanas de médula ósea obtenidas mediante aspiración medular y CMM procedente de tejido adiposo de un donante adulto sano para cada caso, respectivamente.
Métodos de obtención celular
Las CMN de médula ósea procedentes de extracción medular mediante biopsia se aislaron por el método manual de Boyüm modificado.1Se cultivaron en medio áMEM (del inglés, minimalessentialmedium á modificación, Sigma Aldrich) suplementadocon 10 % de suero fetal bovino (SFB) (Gibco) y 2 mM de L-glutamina (Sigma) a 37°C y atmósfera húmeda con CO2 al 5 %, con cambios de medio de cultivo cada 3 días. Cuando las células cubrieron completamente la superficie de cultivo (confluencia del cultivo), se desprendieron mediante tratamiento enzimático con tripsina (Sigma Aldrich)al 0,25 % y nuevamente se cultivaron,lo que constituyó el pase o subcultivo inicial. Para los estudios propuestos, las células se procesaron de esta forma hasta 16 subcultivos y los tiempos de cultivo entre cada subcultivo oscilaron entre 2 y 17 días en dependencia de la confluencia celular.
El tejido adiposo fue obtenido de una donante sana de 24 años sometida a abdominoplastia estética bajo anestesia general, luego de suscribir su consentimiento informado. La separación de adipocitos se realizó mediante el método descrito por Bunnell y col. con algunas modificaciones.21 Se extrajeron 50 mL de tejido que fueron lavados con una solución buffer fosfato salino (PBS pH 7.2) y finamente cortado hasta obtener fragmentos de aproximadamente 2 mm. Para llevar a cabo la digestión enzimática se resuspendió el tejido en igual volumen de PBS que contenía 0,25 % de colagenasa III (Sigma Aldrich); se incubó la mezcla durante 1 h a 37ºC y posteriormente se filtró la solución mediante una membrana de nylon de 100ìm (Falcon) y se centrifugó a 1200 g durante 10 min para obtener el botón celular. El sobrenadante se descartó y al botón se le realizaron dos lavados en PBS con penicilina estreptomicina al 1 %, ambos seguidos de centrifugaciones a 1200 g durante 10 min. El botón obtenido se sembró en frascos de cultivo a una densidad de 2x104cm2, con medio de proliferación formado por DMEM suplementado con 20 % de SFB (Gibco) y 1 % de solución de antibióticos (100 U/mL de penicilina y 100 ìg/mL de estreptomicina). Se incubaron a 37°C en una atmósfera húmeda con 5 % de CO2durante 24 h; después se realizó el primer cambio de medio para eliminar los eritrocitos residuales. Posteriormente, el medio fue cambiado cada 3 días hasta alcanzar una confluencia de más del 70 % del cual se obtuvo la muestra para su caracterización inmunológica.
Citometría de flujo
La caracterización de las CMM se realizó mediante citometría de flujo utilizando anticuerpos monoclonales (AcMo) específicos para diferentes moléculas específicas de la membrana celular mediante doble marcaje: CD34/CD45, CD34/CD90, CD34/CD117, y CD34/CD44. ]]>
Se tomaron 100 µL de cada suspensión celular con una concentración de 1x106 células/mL y se incubaron con 10 µL de cada AcMo conjugado con isotiocianato de fluoresceína (FITC) o ficoeritrina (PE) (DAKO) durante 30 min a 4oC, al mismo tiempo que se realizaba el doble marcaje. Las células se lavaron dos veces con solución balanceada de fosfato (PBS pH 7.2) y se centrifugaron a 1 500 rpm; el botón celular obtenido se resuspendió en 500 µL del mismo PBS y la lectura se realizó en un citómetro de flujo Gallios (BeckmanCoulter) mediante la obtención de 50 000 células en cada caso.
RESULTADOS
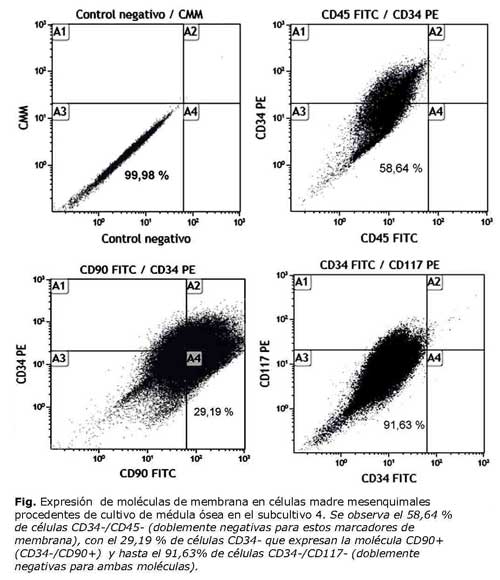
Las CMM cultivadasprocedentes de médula ósea en el subcultivo 4, expresaron: 59,19 % de células CD34-/CD45- (doblemente negativas para estos marcadores de membrana), con 30.26 % de células CD34- que expresan la molécula CD90+ (CD34-/CD90+) y hasta el 91,83 % de células CD34-/CD117- (doblemente negativas para ambas moléculas) y en el subcultivo 8 expresaron 45,13 % de células CD34-/CD45- (doblemente negativas para estos marcadores de membrana), el 21,24 % de células CD34- que expresan la molécula CD90+ (CD34-/CD90+) y el 96,90 % de células CD34-/CD117- (doblemente negativas para ambas moléculas) (tabla1 y figura).
En las células procedentes de cultivo de adipocitos se observó el 52,3 % de células CD34-/CD45-(doblemente negativas para ambas moléculas), el 12,31 % de células CD34-, que expresaron la molécula de membrana CD90+, hasta el 43,31 % de CD34-/CD117- (doblemente negativas) y una frecuencia de expresión del 64,68 % de células que no expresaban CD34 y expresaron en su membrana la moléculaCD44 (CD34-/CD44+) (tabla 2).
]]>
DISCUSIÓNLas CMM procedentes de médula ósea mostraron que en los pases 4 y 8 existe una adecuada expresión del patrón de moléculas de membrana específicas de este tipo celular, lo que corresponde con el fenotipo descrito por otros autores.7, 21-26
En el pase 16 se observó el aumento del porcentaje de células que expresan las moléculas CD45/CD34,lo que sugiere la diferenc.ción espontánea a células neuronales según lo descrito por otros autores.27, 28Estos resultados corresponden con una diferenciación espontánea a célula madre neural en estudios inmunohistoquímicos mediante la presencia de nestina y beta tubulina +++.1* Las CMM procedentes de la expansión del cultivo celular hasta el pase o subcultivo 8 constituyen un potencial terapéutico para la terapia celular regenerativa de diferentes enfermedades crónicas, enfermedades inflamatorias y el trasplante alogénico. Sin embargo, las CMM obtenidas a partir del pase 16 sugieren una diferenciación neural espontánea que de ser comprobado, permitirían su uso en el tratamiento de enfermedades degenerativas y lesiones del sistema nervioso.
Las CMM procedentes de adipocitos mostraron un patrón de expresión de marcadores celulares específicos consistentes con este tipo celular y una frecuencia de expresión del 64,68 % de la molécula de adhesión CD44 (molécula de adhesión que se expresa en las CMM), lo que contribuye al asentamiento de estas en diferentes tejidos y su diferenciación celular especializada.
Estos resultados permiten corroborar de manera preliminar, que los métodos experimentales de cultivo utilizados en ambos casos son efectivos para la obtención y desarrollo de un banco de CMM con fines terapéuticos.
En la actualidad, es de gran interés ampliar la posible aplicación de la terapia celular como alternativa terapéutica de enfermedades crónicas no transmisibles y asociadas al trasplante y sus complicaciones.
REFERENCIAS BIBLIOGRÁFICAS
1. Macías-Abraham C, del Valle-Pérez LO, Baganet-Cobas A, Dorticós-Balea E, Jaime-Fagundo JC, Lam-Díaz RM, et al. Caracterización fenotípica de las células madre de médula ósea utilizadas en la terapia celular regenerativa. Rev. Cub. HematolInmunolHemoter 2011;27(2):233-43. ]]>
2. Hernández Ramírez P. Medicina regenerativa y células madre. Mecanismos de acción de las células madre adultas. Rev Cubana HematolInmunolHemoter [revista en Internet]. 2009[Acceso: 14 de enero de 2013]; 25(1): Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0864-02892009000100002&lng=es.
3. Dahlgren LA. Review of treatment options for equine tendon and ligament injuries: what's new and how do they work? En: 51st Annual Convention American Association Equine Practitioners. Seattle, Washington, USA. 2005Dic. 3-7.
4. Strem B, Hicok K, Zhu M, Wulur I, Alfonso Z, Schreiber R, et al. Multipotential Differentiation of Adipose Tissue - Derived Stem. Keio J Med 2005;54:132-41.
5. Zuk P, Zhu M, Ashjian P, De Ugarte DA, Huang JI, Mizuno H, et al.Human adipose tissue is a source of multipotent stem cells. MolBiol Cell. 2002; 13:4279-95.
6. Dominici M, Le Blanc K, Mueller I, StaperCortenbach I, Marini F, Krause D et al. Minimal criteria for defining multipotentmesenchymal stromal cells. The International Society for Cellular Therapy position statement. Cytotherapy 2006; 8:315-17. ]]>
7. Macías-Abraham C, del Valle-Pérez LO, Hernández-Ramírez P, Ballester-Santovenia JM. Características fenotípicas y funcionales de las células madre mesenquimales y endoteliales. Rev Cubana HematolInmunolHemoter. 2010;26(4):256-75.
8. De Ugarte DA, Alfonso Z, Zuk PA, Elbarbary A, Zhu M, Ashjian P, et al. Differential expression of stem cell mobilization-associated molecules on multi-lineage cells from adipose tissue and bone marrow. ImmunolLetter 2003;89(2-3):267-70.
9. Beyer N, Da Silva L. Mesenchymal Stem Cells: Isolation in vitro. Expansion and characterization. HandbExpPharmacol. 2006;174:249-82.
10. Lakshmipathy U, Verfaille C. Stem Cell Plasticity. Blood Rev 2005; 19:29-38.
11. Rodriguez V. Células Madre: Conceptos Generales y Perspectivas de Investigación. UniversitasScientiarum 2005;10:5-14. ]]>
12. Ryan JM, Barry FP, Murphy JM, Mahon BP. Mesenchymal stem cells avoid allogeneic rejection. J Inflamm 2005;2: 8.
13. Ryan JM, Barry F, Murphy JM, Mahon BP. Interferon-gamma does not break, but promotes the immunosuppressive capacity of adult human mesenchymal stem cells. ClinExpImmunol 2007;149:353-63.
14. Tse WT, Pendleton D, Beyer W, D`Andrea A, Guinan EC. Bone marrow derived mesenchymal stem cells (MSC) suppress T-cell activation without inducing anergy. Cytotherapy 2001;3:417a.
15. Holyoake TL, Alcorn MJ, Richmond L, Farrell E, Pearson C, Green R, et al. CD34 positive PBPC expanded ex vivo may not provide durable engraftment following myeloablativechemoradiotherapy regimens. BM Transplant 1997;19:1095-101.
16. Tse WT, Pendleton JD, Beyer WM, Egalka MC, Guinan EC. Suppresion of allogenic T-cell proliferation by human marrow stromal cells: implications in transplantation. Transplant 2003;75:389-97. ]]>
17. Le Blanc K, Tammik L, Sundberg B, Haynesworth SE, Ringden O. Mesenchymal stem cells inhibit and stimulate mixed lymphocyte cultures and mitogenic responses independently of the major histocompatibility complex. Scand J Immunol 2003;57:11-20.
18. Aggarwal S, Pittenger MF. Human mesenchymal stem cells modulate allogenic immune cell responses. Blood 2005;105:1815-22.
19. Zhang W, Ge W, Li C, You S, Liao L, Han Q, et al. Effects of mesenchymal stem cells on differentiation, maduration, and function of human monocyte-derived dendritic cells. Stem Cells Dev 2004;13:263-71.
20. Maccario R, Podesta M, Moretta A, Cometa A, Comoli P, Montagna D, et al. Interaction of human mesenchymal stem cells with cells involved in alloantigen _specific immune response favors the differentiation of CD4+ T-cell subsets expressing a regulatory / suppressive phenotype. Haematologica 2005;90:516-25.
21. Bunnell BA, Flaat M, Gagliardi C, Patel B, Ripoll C. Adipose-derived stem cells: isolation, expansion and differentiation. Methods 2008 Jun; 45(2):115-20. doi: 10.1016/j.ymeth.2008.03.006. ]]>
22. D`Ippolito G, Diabira S, Howard GA, Menei P, Roos BA, Schiller PC. Marrow _isolated adult multilineage inducible (MIAMI) cells, a unique population of postnatal young and old human cells with extensive expansion and differentiated potential. J Cell Science 2004;117:2971-81.
23. Zuba-Surma EK, Kucia M, Ratajczak J, Ratajczak MZ. Small stem cells in adult tissues: Very small embryonic-like stem cells stand up! Cytometry Part A 2009;75A: 4-13.
24. Reyes M, Lund T, Lenvik T, Aguiar D, Koodie L, Verfaillie CM. Purification and ex vivo expansion of postnatal human marrow mesodermal progenitor cells. Blood 2001;98:2615-25.
25. Clarke E, Wognum AW, Marciniak R, Eaves AC. Mesenchymal cell precursors from human bone marrow have a phenotype that is distinct from cultured mesenchymal cells and are exclusively present in a small subset of CD45low, SH2+cells. Blood 2001;98:355a.
26. Jones EA, Kinsey SE, English A, Jones RA, Straszynski L, Meredety DM, et al. Isolation and Characterization of bone marrow multipotentialmesenchymal progenitors cell. Arthritis and Rheumatism 2002;46:3349-60. ]]>
27. Foudah D, Redondo J, Caldara C, Carini F, Tredici G, Miloso M. Expression of Neural Markers by Undifferentiated Rat Mesenchymal Stem Cells. J Biomed Biotechnol. Published on Line 2012 Oct. doi: 10.1155/2012/820821.
28. Foudah D, Redondo J, Caldara C, Carini F, Tredici G, Miloso M. Human mesenchymal stem cells express neuronal markers after osteogenic and adipogenic differentiation. CellBiol Mol Lett 2013; Jun;18 (2):163-66.
Recibido: Julio 22, 2013.
Aceptado: Octubre 19, 2013.
]]>
CORRESPONDENCIA A:
DraCM. Consuelo Macías Abraham. INSTITUTO DE HEMATOLOGÍA E INMUNOLOGÍA. Apartado 8070, La Habana, CP 10800, CUBA.
Tel (537) 643 8695, 8268. Fax (537) 644 2334. Email: rchematologia@infomed.sld.cu
]]>