Función del sistema NADPH oxidasa en la formación de trampas extracelulares de los neutrófilos (NETs)
Role of nadph oxidase system in the neutrophil extracelular Traps (NETs) formation
Gabriel Jaime Vélez Tobón, Yermis Carolina Rocha Arrieta, Andrés Augusto Arias Sierra, Juan Álvaro López Quintero
Grupo de Inmunodeficiencias Primarias. Universidad de Antioquia. Medellín, Colombia.
]]>
RESUMEN
Las trampas extracelulares de los neutrófilos son estructuras fundamentalmente compuestas de cromatina y proteínas granulares, que una vez liberadas constituyen un mecanismo de defensa que tiene la capacidad de atrapar y destruir microorganismos patógenos. El proceso que libera estas estructuras es conocido como NETosis y en el caso que provoque muerte celular, esta es diferente a la apoptosis y a la necrosis. Si bien no se conocen todos los eventos moleculares involucrados en la formación de las NETs, se sabe que dependiendo del estímulo, las especies reactivas del oxígeno son esenciales para que ocurra la descondensación de la cromatina y se lleve a cabo el proceso de NETosis.
Palabras clave: trampas extracelulares de neutrófilos, NETs, enfermedad granulomatosa crónica, EGC.
ABSTRACT
Neutrophil extracellular traps (NETs) are structures mainly composed of chromatin and granule proteins that once released constitute a defense mechanism due to their ability to trap and destroy pathogen microorganisms. The process by which these structures are released is known as NETosis and in case this may lead to cell death is different to apoptosis and necrosis. Although all the molecular events involved in the formation of NETs are poorly understood, it is known that depending on the stimulus, reactive oxygen species (ROS) are essential to the chromatin decondensation and subsequent NETs formation.
Keywords: neutrophil extracellular traps, NETs, chronic granulomatous disease, CGD.
INTRODUCCIÓN
]]> Los polimorfonucleares neutrófilos (PMNs) son células que actúan como mediadores primarios ante una respuesta inflamatoria y realizan una función esencial en la defensa innata del hospedero frente a agentes patógenos. Uno de los principales mecanismos de destrucción de estas células es la fagocitosis de microorganismos y partículas extrañas que logran atravesar las barreras primarias de defensa, como piel y mucosas.1,2 Una vez que el microorganismo es fagocitado y se encuentra dentro del fagolisosoma, se inicia su destrucción mediante sustancias proteolíticas contenidas en los gránulos citoplasmáticos y por la producción de especies reactivas del oxígeno (ROS). Estas últimas se generan a través de un proceso conocido como “explosión respiratoria”, llevado a cabo por el complejo multienzimático NADPH oxidasa (del inglés, nicotinamide adenine dinucleotide phosphate).3El sistema NADPH oxidasa está localizado en la membrana celular y de los gránulos secundarios de los fagocitos y se compone de proteínas de membrana y citosólicas codificadas por genes independientes (tabla).4 El componente de membrana está conformado por las proteínas gp91phox (“phox” del inglés phagocyte oxidase) y p22phox, las cuales conforman el centro catalizador de la oxidasa conocido como flavohemocitocromo b558. En el citosol se encuentran las subunidades p47 phox, p67phox, p40phox y las proteínas reguladoras Rac1 y Rac2.3
La gp91phox (conocida también como NOX2) es una glicoproteína de 91 kDa responsable de unir NADPH, FAD y grupos hemo, importantes para la transferencia de electrones hacia el oxígeno molecular que se encuentra en la vacuola fagocítica y la inducción de la producción de anión superóxido (O2-). La proteína p22phox (22 kDa), posee una región rica en prolina (PRR) que interactúa con un dominio de homología de las Src (SH3) que se encuentra en p47phox;5 esta proteína es la que permite que la gp91phox se acople con las subunidades citosólicas y se inicie la producción de ROS.6
La p47phox (47 kDa) interactúa con los demás componentes citosólicos del sistema oxidasa a través de dos dominios SH3, un PRR y un dominio PX, este último importante para su interacción con la membrana celular.7
Otro de los componentes citosólicos, la proteína p67phox(67kDa), posee un dominio de activación esencial para la transferencia de electrones a través del centro reductor del flavohemocitocromo b558. 8 Igualmente, la p67phox posee dos dominios SH3 importantes para la interacción con p47phox, un dominio de repeticiones tetratricopetídicas (TPR) que facilita la interacción con la proteína Rac,9 y un dominio PB1 (Px-phox y Bem1) importante para la interacción entre p67phox y p40phox.10
Finalmente, se encuentra la proteína p40phox (40 kDa), en la que se han identificado tres dominios: PX, SH3 y PB1. La función de esta proteína en humanos es mantener acoplado el sistema oxidasa durante la activación y la producción de anión superóxido (O 2-).11
Como componentes reguladores de este complejo enzimático se encuentran las proteínas Rac1 y Rac2, las cuales, para estimular la producción de ROS, pasan de una forma inactiva unida a GDP a la forma activa unida a GTP.12,13
ACTIVACIÓN DEL SISTEMA NADPH OXIDASA
Durante la fagocitosis o por la acción de agentes microbianos, citocinas o quimiocinas, se induce la activación del sistema NADPH oxidasa y la posterior producción de ROS. Este mecanismo comienza con la migración de las proteínas citosólicas (p47phox, p67phox y p40phox) hacia la membrana citoplasmática o la membrana del fagolisosoma para unirse con el flavohemocitocromo b558. Durante esta activación, p47phox es fosforilada mediante la acción de fosfatidilInositol 3 quinasa (PI3K) y la proteína quinasa C (PKC). En este evento la participación de Rac es fundamental para la formación de un complejo enzimáticamente activo.4,14
Una vez activo el sistema NADPH oxidasa, el flavohemocitocromo b558 transfiere electrones al oxígeno molecular (O2) a partir de la molécula NADPH y gener el O2- (figura 1). Esta molécula puede transformarse por dismutación espontánea para generar peróxido de hidrógeno (H2O2); o bien, esta reacción puede ser catalizada por la enzima superóxido dismutasa. Cuando reacciona el H2O2 con el O2- se da la formación de oxígeno “singlete” y radicales hidroxilo (HO); asimismo, el H2O2 le sirve de sustrato a la enzima mieloperoxidasa (MPO) para la formación, en presencia de cloro (Cl–), de ácido hipocloroso (HClO).15,16 En consecuencia, debido a la formación de todos estos compuestos (conocidos como ROS), en el interior del fagolisosoma se crea un ambiente altamente tóxico para los microorganismos, lo que ocasiona su destrucción.16
]]> ENFERMEDAD GRANULOMATOSA CRÓNICA (EGC)Cuando se presentan mutaciones en uno de los genes que codifican para las proteínas del sistema NADPH oxidasa, se produce la enfermedad granulomatosa crónica (EGC). Esta inmunodeficiencia primaria se caracteriza por la incapacidad que tienen los fagocitos como los PMNs, de producir ROS que conlleve a la eliminación de algunos microorganismos dentro del fagolisosoma.17 La EGC se presenta aproximadamente en 1 de cada 200 000 a 250 000 nacidos vivos18 y se caracteriza porque los pacientes presentan infecciones recurrentes causadas por S aureus, Nocardiasp, A fumigatus, C albicans, C glabrata y P boydii, que ocasionan úlceras crónicas, linfadenitis y neumonía; además se pueden afectar otros órganos como hígado, huesos, riñones, bazo y cerebro.17,19,20
El patrón de herencia de la EGC puede estar ligado al cromosoma X (EGC-X) cuando se presentan mutaciones en el gen CYBB que codifica para gp91 phox; cuando los defectos están en los genes que codifican para los demás componentes del sistema oxidasa, el patrón de herencia es autosómico recesivo4,18,21(tabla). Aproximadamente el 70 % de los casos de EGC son por mutaciones en el gen CYBB, que pueden ser causadas por deleciones (35,6 %), mutaciones con cambio de sentido (21,3 %), mutaciones sin sentido (14,1 %), mutaciones en los sitios de corte y empalme a nivel intrónico (17,6 %), inserciones (7,9 %), inserción/deleción (2,8 %) y mutaciones en las regiones promotoras (0,7 %).22
Por otra parte, el 30 % corresponde a mutaciones autosómicas recesivas, de las cuales el 20 % se presentan en el gen NCF1, el 5 % por mutaciones en el gen CYBA y el otro 5 % es por alteraciones en el gen NCF2.18,23-25 Con respecto al gen NCF4, solo se han reportado defectos en un paciente que presentaba colitis granulomatosa y tenía defectos exclusivamente en la producción de O2 - en el interior del fagosoma.12
El tratamiento de la EGC se basa en una terapia profiláctica con antibióticos y antimicóticos. Al combinar los anteriores tratamientos con el inmunomodulador interferón gamma (IFNg) recombinante, el riesgo de infecciones graves puede reducirse hasta en el 70 %.26,27 El mecanismo de acción del IFNg en estos pacientes aún no se conoce completamente; sin embargo, su administración se basa en el efecto que esta citocina tiene sobre las células fagocíticas, donde induce una mayor actividad del sistema NADPH oxidasa, debido posiblemente a un aumento de la generación de transcriptos del gen CYBB.28, 29 No obstante, a pesar de la terapia antimicrobiana y el uso del IFNg, los pacientes con EGC continúan presentando altas tasas de morbi-mortalidad, por lo que la única terapia curativa es el trasplante de células madre hematopoyéticas.17,30 Aunque se ha propuesto la terapia génica como una opción curativa para la EGC, esta ha tenido pobres resultados porque la recuperación en la producción de ROS por las células fagocíticas ha sido transitoria; además de la problemática en el desarrollo de un vector seguro que no genere efectos adversos como síndromes mielodisplásicos o cáncer.31,32
TRAMPAS EXTRACELULARES DE NEUTRÓFILOS
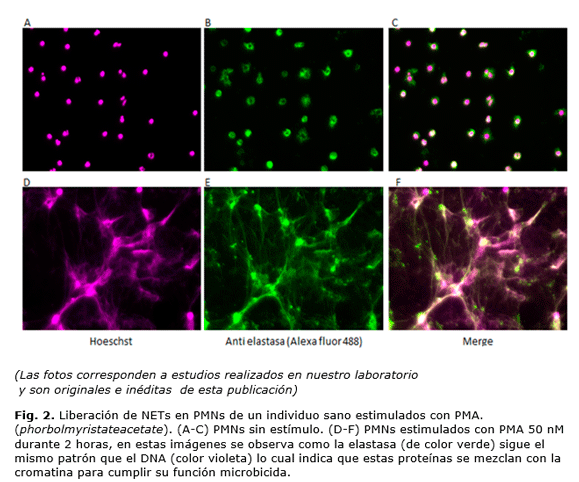
En el 2004 fue descrito un nuevo mecanismo microbicida de los neutrófilos llamado trampas extracelulares de neutrófilos (NETs), en el cual se induce la liberación de redes de cromatina en asociación con histonas, proteínas citoplasmáticas, del citoesqueleto o proteínas granulares hacia el medio extracelular para atrapar y destruir microorganismos patógenos.33 Estructuralmente, las NETs se componen principalmente de una matriz de DNA con una longitud de 15 a 17 nm, sobre la cual se ubican dominios globulares con un diámetro de 25 nm. Se determinó que los principales componentes microbicidas son las histonas nucleares (H1, H2A, H2B, H3, H4) y proteínas granulares como elastasa (figura 2), MPO, catepsina G, lactoferrina, proteínas bactericidas de aumento de la permeabilidad (BPI), gelatinasa, defensina, catelicidina, pentraxina 3, lisozima C.34 También se ha descrito la presencia de proteínas del citoesqueleto (a-actina, miosina 9, plastina, citoqueratina 10), del citoplasma (calprotectina, calgrulina), enzimas del peroxisoma (catalasa) y glicolíticas (a-enolasa,
transcetolasa).34-38
El proceso de liberación de NETs se describe como un proceso que induce la muerte del neutrófilo o no la provoca, y se clasifica en NETosis lítica y NETosis vital.39 La NETosis lítica es aquella donde se libera el ADN mezclado con las diferentes proteínas al medio extracelular a través de la ruptura de la membrana plasmática del neutrófilo. Dentro de la NETosis vital se han descrito dos mecanismos: el primero, descrito en el 2009 por Yousefi y col, plantea que la estimulación con factor estimulante de colonia de granulocitos-macrófagos (GM-CSF) y ligandos de TLR-4 o C5a, inducen la liberación NETs por neutrófilos viables; estas NETs están compuestas de ADN mitocondrial y no nuclear 40. Sin embargo, la gran mayoría de artículos de NETs reportan la presencia de ADN nuclear e histonas y contradicen los resultados de este artículo, por la poca cantidad de mitocondrias en los PMNs, por el pequeño tamaño del genoma mitocondrial y por la ausencia de histonas antimicrobianas en estas NETs.41 El segundo mecanismo fue descrito con S aureus, donde los neutrófilos forman y liberan al medio extracelular vesículas que contienen ADN; en ese medio se explotan y liberan su contenido en forma de red que atrapa y elimina las bacterias.42
]]> Cuando la NETosis ocasiona la muerte del neutrófilo, esta es diferente, tanto de la apoptosis como de la necrosis y presenta las siguientes características:- La formación de NETs se da 10 minutos después de la activación, un tiempo más corto que la presentación de la apoptosis;
- durante la NETosis no se ha descrito la activación o participación de caspasas;
- no hay fragmentación del ADN, ni exposición de fosfatidilserina; y
- en el proceso de producción de NETs hay pérdida de la integridad de la membrana nuclear mientras que en la necrosis no la hay.38
Se conoce que el mecanismo molecular que induce la NETosis es mediado por el tipo de estímulo y la activación de receptores específicos de los neutrófilos que desencadena una cascada de señalización mediada por la PKC, la vía Raf– MEK–ERK, la activación del sistema NADPH oxidasa y la formación de ROS. Este último paso es indispensable para la liberación de NETs inducida por ciertos estímulos.43
ALTERACIONES EN LA PRODUCCION DE NETs
En los PMNs de neonatos prematuros hay una inmunodeficiencia fisiológica en la que se presenta un deterioro de la fagocitosis, alteraciones en la destrucción de bacterias intracelulares y una disminución en la producción de ROS. Como consecuencia de lo anterior y en relación con el defecto en la producción de ROS, las células de estos individuos son incapaces de producir NETs, comparados con los PMNs de neonatos a término o adultos sanos.44 También se han reportado defecto en la producción de NETs, en el otro extremo de la vida, los ancianos.
En el 2014, Hazeldine y col realizaron un estudio con PMNs de individuos jóvenes (media de edad 25 años) e individuos ancianos (media de edad 70 años), y demostraron que la producción de NETs en individuos ancianos era menor en comparación con la de los individuos jóvenes, luego de que los PMNs fueran preactivados con factor de necrosis tumoral alfa (TNF-a) y posteriormente estimulados con lipopolisacárido (LPS) o interleucina 8 (IL-8). Igualmente, evidenciaron que los PMNs de los ancianos producían menos cantidad de ROS comparado con los individuos jóvenes y que, por tanto, este podía ser un mecanismo que explicara la reducción de las NETs en esta población.45
Otra de las alteraciones que conduce a un defecto en la producción de NETs es la deficiencia de la MPO. Como se ha mencionado, esta enzima participa en la descondensación de la cromatina y en la formación de ROS, gracias a que cataliza la producción de HClO a partir del H2O 2 y Cl–. En individuos con deficiencia absoluta de MPO no hay producción de NETs debido a que no se logra la formación del HClO; este radical oxidante está involucrado en la cloración de las histonas y la posterior descondensación de la cromatina, como también en la ruptura de la membrana nuclear, lo que permite la salida del ADN hacia el citoplasma, donde se mezcla con los gránulos citoplasmáticos para la formación de las NETs.16,46
]]> Finalmente, se conoce que las alteraciones en la explosión respiratoria de pacientes con EGC conducen a un bloqueo en la producción de NETs, como se explicará en el siguiente apartado.33,47NETs, SISTEMA NADPH OXIDASA Y ENFERMEDAD GRANULOMATOSA CRÓNICA
La función de los ROS en la inducción de NETs ha sido motivo de controversia en los últimos años. Por un lado, varios estudios han demostrado que los neutrófilos obtenidos de pacientes con EGC no tienen la capacidad de liberar NETs; un ejemplo de esto es el estudio de Fuchs y col, donde se demostró que al estimular con ésteres de forbol (PMA, phorbolmyristateacetate) neutrófilos de individuos con EGC, no se producía NETosis. Además, en el mismo estudio se observó que dicho efecto se podía revertir al adicionar glucosa oxidasa (GO) como fuente productora de H2O2 exógeno.38 Igualmente, Brinkmann observó este mismo fenómeno en sus estudios iniciales.33 Asimismo, Bianchi y col observaron cómo un paciente con EGC-X sometido a terapia génica recuperó la actividad del sistema NADPH oxidasa y parcialmente la producción de NETs. La actividad microbicida contra A nidulans y Candida spp mejoró notoriamente, dado que las NETs inhibieron en el 80 % la germinación de las conidias, y en el 40 %, el crecimiento de las hifas; estos resultados son contundentes en cuanto a la función vital que cumplen las ROS y las NETs en la inmunidad innata.47
Se conoce que al tratar con IFNg a los PMNs humanos se induce un aumento en la producción de ROS, un perfil génico diferencial; es decir, se expresan genes que responden al estímulo con IFNg. Martinelli y col determinaron la función del IFNg para la activación de los neutrófilos. Utilizando un ensayo con micromatrices se demostró cómo los PMNs maduros, a diferencia de aquellos en los estadios más inmaduros, expresaban una mayor cantidad de genes de respuesta al estímulo con IFNg. Igualmente, describió cómo los interferones tipo 1 y 2 preactivaban los PMNs maduros y de esta manera, al ser estimulados con el factor del complemento C5a, producían NETs.48
La actividad del IFNg es mediada por una cascada de señalización donde la JAK1-2 y STAT1-a (cuyas funciones están relacionadas con la regulación de la expresión génica) intervienen en la regulación de la transcripción del gen CYBB y posterior exportación de transcriptos desde el núcleo hacia el citoplasma.49 También se ha demostrado que el IFNg puede intervenir en la modulación del splicing alternativo, lo cual corrige de manera parcial la actividad oxidativa de PMNs de individuos con EGC.50 Se ha observado que estimula células progenitoras, lo que favorece la aparición de una población de fagocitos con un incremento en su función oxidativa hasta 28 días después del estímulo inicial con esta citosina.51 En otro estudio realizado en ratones, se muestra la importancia del IFNg para combatir las infecciones por S pneumoniae, al activar la NETosis. En cepas IFNg−/−hay una disminución significativa en la producción de NETs; este mismo fenómeno fue observado en un modelo de ratones de EGC que carecían de gp91phox.52
Por otra parte, Remijsen y col demostraron cómo la inducción de NETosis mediante la utilización de PMA se relacionaba con la producción de ROS y con la autofagia, y afirmaron que ningún mecanismo era capaz de inducir NETosis de forma aislada. Así, la inhibición de la autofagia impide la descondensación de la cromatina e inhibe la de la NETosis, a pesar de que la producción de O2- no se ve afectada, lo cual quiere decir que la actividad del sistema NADPH oxidasa es necesaria pero no suficiente para la inducción de la NETosis. Igualmente, demostraron que al inducir autofagia en los PMNs de individuos con alteraciones en la producción de ROS, no se presentaba descondensación de la cromatina, típica de la NETosis.53
En resumen, se han reportado cuatro líneas de evidencia que soportan el papel de las ROS en este mecanismo.
1. Se conoce que el H2O2 es un potente inductor de NETs en concentraciones fisiológicas y a diferencia del O2 -, es permeable a la membrana celular y tiene una vida media más prolongada, lo que sugiere que el H2O2 exógeno también podría estar involucrado en la generación de NETs.
2. La inhibición farmacológica del sistema NADPH oxidasa con difenilyodonio (DPI) bloquea la formación de NETs; sin embargo, esta acción se puede revertir al inducir la generación de H2O2 exógeno por medio de GO adicionada a los PMNs.
3. El efecto inductor de NETs por medio de H2O2 se puede regular negativamente al adicionar catalasa al sistema; este efecto puede ser restablecido al adicionar un inhibidor de la catalasa (3-amino-1, 2,4-triazol), lo cual permite que los PMNs recuperen su capacidad de formar NETs.
]]> 4. Se ha demostrado que neutrófilos de individuos con EGC no producen NETs.38,42La función de otras ROS en la formación de NETs también se ha demostrado; se ha encontrado que la ausencia de cloro (Cl-) extracelular disminuye la producción de NETs, mientras que con la adición de HClO se recupera la capacidad de inducir NETosis.16
En el año 2010, Pilsczek y col describieron cómo la citolisina panton valentine leucocidina (PVL) de Staphylococcus aureus indujo la liberación de NETs en un mecanismo independiente de producción de ROS; en este caso se demostró que la liberación del DNA se produjo de una forma no lítica a través de vesículas, como anteriormente se mencionó.42 En este mismo año, Marcos V y col demostraron que la estimulación de PMNs con ligandos de CXCR2 induce la formación de NETs, un proceso que involucra quinasas de la familia Src pero que es independiente del sistema NADPH oxidasa.54
En el 2012, Parker y col demostraron que la ionomicina, un ionóforo de calcio, induce NETs independiente del sistema NADPH oxidasa. También demostraron que los PMNs obtenidos de un paciente con deficiencia de MPO produjeron NETs cuando se estimularon con PMA y P aeruginosa. Con PMA se produjo menos NETS en los PMNs del paciente, en comparación con un individuo sano, pero no hubo diferencias en la formación de NETs entre las células del individuo sano y las del paciente cuando se estimulaba con P aeruginosa; por tanto, concluyeron que las NETs pueden ser inducidas por diferentes estímulos pero no por un mecanismo común.55
La producción de NETs a través de mecanismos independientes del oxígeno también fue reportada en 2013 por Byrd y col en un modelo de C albicans. En este estudio se demostró cómo el reconocimiento del β-glucano a través del receptor CR3 conduce a una rápida liberación de NETs (antes de 30 minutos), siempre y cuando los neutrófilos estén en contacto con el β-glucano y componentes de la matriz extracelular.56
En el 2014, Arai y col investigaron el efecto del ácido úrico en la formación de NETs. Ellos encontraron que bajas concentraciones de ROS inhiben la formación de NETs dependiente de Nox; sin embargo, altas concentraciones de ácido úrico, más que inhibir las NETs inducen su formación de una manera independiente de Nox. Este hallazgo fue confirmado cuando se realizaron los experimentos con PMNs de pacientes con EGC. 57
A partir del descubrimiento de la producción de NETs, estas estructuras han sido ampliamente estudiadas en diferentes modelos y se ha logrado establecer como un mecanismo de muerte celular independiente de la apoptosis y la necrosis. A pesar de que aún no se conocen todos los eventos moleculares que permiten que se lleve a cabo la NETosis, se sabe que tanto la autofagia, la producción de ROS, como la descondensación de la cromatina, permiten la liberación de las NETs. La actividad microbicida de los componentes de las NETs ha sido bien caracterizada, pues se sabe que las proteínas nucleares como histonas o enzimas como la elastasa y la MPO, tienen alto poder microbicida, lo que contribuye a la eliminación de agentes patógenos. La estructura de la NET también es importante, ya que funciona como una red que atrapa el microorganismo e impide su diseminación.
A pesar del desarrollo en la investigación de los mecanismos de destrucción que utilizan los PMNs en la respuesta inmune, aún se debe ampliar el estudio de los mecanismos de destrucción de estas células y su comportamiento en ciertas enfermedades. En el caso de la EGC, el sistema NADPH oxidasa y sus defectos genéticos han sido ampliamente estudiados, sin llegar a conocerse todos los aspectos moleculares que rodean esta inmunodeficiencia. Si bien se han logrado importantes avances en las alternativas terapéuticas, el mecanismo del IFNg todavía no está claro.
Actualmente no hay reportes que relacionen directamente el efecto del IFNg en PMNs de pacientes con EGC en los que se esperaría ver una recuperación parcial en la capacidad de producir NETs. Asimismo, el descubrimiento de la NETosis genera un campo de acción en el que se podrían estudiar mecanismos inmunorreguladores que potencien la actividad de las células fagocíticas frente a microorganismos patógenos o que regulen su producción con el fin de evitar efectos adversos de la NETosis. Aunque la EGC es una enfermedad de baja incidencia, se debe profundizar en la investigación de los factores asociados con la explosión respiratoria y la NETosis, lo cual contribuiría a dilucidar aspectos relacionados con mejores alternativas terapéuticas y consejería genética.
CONFLICTO DE INTERESES
]]> Los autores declaran no tener conflictos de interés en la publicación de este artículo.FINANCIACIÓN
Este artículo fue posible gracias a la financiación del Departamento Administrativo de Ciencia Tecnología e Innovación COLCIENCIAS al proyecto 111554531412.
REFERENCIAS BIBLIOGRÁFICAS
1. Borregaard N. Neutrophils, from marrow to microbes. Immunity. 2010;33(5):657-70.
2. Kolaczkowska E, Kubes P. Neutrophil recruitment and function in health and inflammation. Nat Rev Immunol. 2013;13(3):159-75.
3. de Oliveira-Junior EB, Bustamante J, Newburger PE, Condino-Neto A. The human NADPH oxidase: primary and secondary defects impairing the respiratory burst function and the microbicidal ability of phagocytes. Scand J Immunol. 2011;73(5):420-7.
4. Arango JC, Gámez LY, López JÁ. Sistema NADPH oxidasa: nuevos retos y perspectivas. Iatreia. 2010;23(4):362-72.
5. Ueyama T, Tatsuno T, Kawasaki T, Tsujibe S, Shirai Y, Sumimoto H, et al. A regulated adaptor function of p40phox: distinct p67phox membrane targeting by p40phox and by p47phox. Mol Biol Cell. 2007;18(2):441-54.
6. Tahara T, Shibata T, Wang F, Nakamura M, Sakata M, Nakano H, et al. A genetic variant of the p22PHOX component of NADPH oxidase C242T is associated with reduced risk of functional dyspepsia in Helicobacter pylori-infected Japanese individuals. Eur J Gastroenterol Hepatol. 2009;21(12):1363-8.
7. Xu W, Ma L, Li W, Brunson TA, Tian X, Richards J, et al. Functional pseudogenes inhibit the superoxide production. Precis Med.[En línea] 2015 [citado el 02 de mayo de 2015];1(1). Disponible en: http://www.smartscitech.com/index.php/pm/article/view/745/pdf_7
8. Streeter J, Schickling BM, Jiang S, Stanic B, Thiel WH, Gakhar L, et al. Phosphorylation of Nox1 regulates association with NoxA1 activation domain. Circ Res. 2014;115(11):911-8.
]]>9. Brennan AM, Suh SW, Won SJ, Narasimhan P, Kauppinen TM, Lee H, et al. NADPH oxidase is the primary source of superoxide induced by NMDA receptor activation. Nat Neurosci. 2009;12(7):857-63.
10.Roesler J, Segerer F, Morbach H, Kleinert S, Thieme S, Rösen-Wolff A, et al. P67-phox (NCF2) lacking exons 11 and 12 is functionally active and leads to an extremely late diagnosis of chronic granulomatous disease (CGD). PLoS One. [En línea] 2012 [Citado el 12 de enero de 2015];7(4). Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3326000/pdf/pone.0034296.pdf
11.Matute JD, Arias AA, Dinauer MC, Patiño PJ. p40phox: the last NADPH oxidase subunit. Blood Cells Mol Dis. 2005;35(2):291-302.
12.Matute JD, Arias AA, Wright NA, Wrobel I, Waterhouse CC, Li XJ, et al. A new genetic subgroup of chronic granulomatous disease with autosomal recessive mutations in p40 phox and selective defects in neutrophil NADPH oxidase activity. Blood. 2009;114(15):3309-15.
13.Miyano K, Sumimoto H. Role of the small GTPase Rac in p22phox-dependent NADPH oxidases. Biochimie. 2007;89(9):1133-44.
14.Brandes RP, Weissmann N, Schröder K. Nox family NADPH oxidases: Molecular mechanisms of activation. Free Radic Biol Med. 2014;76:208-26.
15.Lambeth JD. NOX enzymes and the biology of reactive oxygen. Nat Rev Immunol. 2004;4(3):181-9.
16.Akong-Moore K, Chow OA, von Köckritz-Blickwede M, Nizet V. Influences of chloride and hypochlorite on neutrophil extracellular trap formation. PLoS One. [En línea] 2012 [Citado el 18 de febrero de 2015] ;7(8). Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3418225/pdf/pone.0042984.pdf
17.Holland SM. Chronic granulomatous disease. Hematol Oncol Clin North Am. 2013;27(1):89-99.
18.Roos D, de Boer M. Molecular diagnosis of chronic granulomatous disease. Clin Exp Immunol. 2014;175(2):139-49.
19.Blumental S, Mouy R, Mahlaoui N, Bougnoux ME, Debré M, Beauté J, et al. Invasive mold infections in chronic granulomatous disease: a 25-year retrospective survey. Clin Infect Dis. 2011;53(12):159-69.
]]>20.Song E, Jaishankar GB, Saleh H, Jithpratuck W, Sahni R, Krishnaswamy G. Chronic granulomatous disease: a review of the infectious and inflammatory complications. Clin Mol Allergy. [En línea] 2011 [Citado el 04 de marzo de 2015];9(1):10. Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3128843/pdf/1476-7961-9-10.pdf
21.Battersby AC, Cale AM, Goldblatt D, Gennery AR. Clinical manifestations of disease in X-linked carriers of chronic granulomatous disease. J Clin Immunol. 2013;33(8):1276-84.
22.Roos D, Kuhns DB, Maddalena A, Roesler J, Lopez JA, Ariga T, et al. Hematologically important mutations: X-linked chronic granulomatous disease (third update). Blood Cells Mol Dis. 2010;45(3):246-65.
23.Jakobsen MA, Katzenstein TL, Valerius NH, Roos D, Fisker N, Mogensen TH, et al. Genetical analysis of all Danish patients diagnosed with chronic granulomatous disease. Scand J Immunol. 2012;76(5):505-11.
24.Martel C, Mollin M, Beaumel S, Brion JP, Coutton C, Satre V, et al. Clinical, Functional and Genetic Analysis of Twenty-Four Patients with Chronic Granulomatous Disease - Identification of Eight Novel Mutations in CYBB and NCF2 Genes. J Clin Immunol. 2012;32(5):942-58.
25.Ramírez-Vargas NG, Berrón-Ruiz LR, Berrón-Pérez R, Blancas-Galicia L. [Chronic granulomatous disease diagnosis: Patients and carriers]. Rev Alerg Mex. 2011;58(2):120-5.
]]>26.Errante PR, Frazão JB, Condino-Neto A. The use of interferon-gamma therapy in chronic granulomatous disease. Recent Pat Antiinfect Drug Discov. 2008;3(3):225-30.
27.Smith NL, Denning DW. Clinical implications of interferon-γ genetic and epigenetic variants. Immunology. 2014;143(4):499-511.
28.Filiz S, Uygun DF, Köksoy S, Şahin E, Yeğin O. In vitro interferon γ improves the oxidative burst activity of neutrophils in patients with chronic granulomatous disease with a subtype of gp91phox deficiency. Cent Eur J Immunol. 2015;40(1):54-60.
29.Condino-Neto A, Newburger PE. Interferon-gamma improves splicing efficiency of CYBB gene transcripts in an interferon-responsive variant of chronic granulomatous disease due to a splice site consensus region mutation. Blood. 2000;95(11):3548-54.
30.Kang EM, Marciano BE, DeRavin S, Zarember KA, Holland SM, Malech HL. Chronic granulomatous disease: overview and hematopoietic stem cell transplantation. J Allergy Clin Immunol. 2011;127(6):1319-26.
31.Seger RA. Chronic granulomatous disease: recent advances in pathophysiology and treatment. Neth J Med. 2010;68(11):334-40.
32.Segal BH, Veys P, Malech H, Cowan MJ. Chronic granulomatous disease: lessons from a rare disorder. Biol Blood Marrow Transplant. 2011;17(1 Suppl):S123-31.
33. Brinkmann V, Reichard U, Goosmann C, Fauler B, Uhlemann Y, Weiss DS, et al. Neutrophil extracellular traps kill bacteria. Science. 2004;303(5663):1532-5.
34. Urban CF, Ermert D, Schmid M, Abu-Abed U, Goosmann C, Nacken W, et al. Neutrophil extracellular traps contain calprotectin, a cytosolic protein complex involved in host defense against Candida albicans. PLoS Pathog. [En línea] 2009 [Citado el 13 de marzo de 2015];5(10). Disponible en: http://www.sciencedirect.com/science/article/pii/S1083879110003885
35. Guimarães-Costa AB, Nascimento MT, Wardini AB, Pinto-da-Silva LH, Saraiva EM. ETosis: A Microbicidal Mechanism beyond Cell Death. J Parasitol Res.[En línea] 2012[Citado el 06 de marzo de 2015];2012. Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3321301/pdf/JPR2012-929743.pdf
36.Medina E. Neutrophil extracellular traps: a strategic tactic to defeat pathogens with potential consequences for the host. J Innate Immun. 2009;1(3):176-80.
37.Brinkmann V, Zychlinsky A. Neutrophil extracellular traps: is immunity the second function of chromatin? J Cell Biol. 2012;198(5):773-83.
38.Fuchs TA, Abed U, Goosmann C, Hurwitz R, Schulze I, Wahn V, et al. Novel cell death program leads to neutrophil extracellular traps. J Cell Biol. 2007;176(2):231-41.
39. Yipp BG, Kubes P. NETosis: how vital is it? Blood. 2013;122(16):2784-94.
40.Yousefi S, Mihalache C, Kozlowski E, Schmid I, Simon HU. Viable neutrophils release mitochondrial DNA to form neutrophil extracellular traps. Cell Death Differ. 2009;16(11):1438-44.
41. Remijsen Q, Kuijpers TW, Wirawan E, Lippens S, Vandenabeele P, Vanden Berghe T. Dying for a cause: NETosis, mechanisms behind an antimicrobial cell death modality. Cell Death Differ. 2011;18(4):581-8.
42. Pilsczek FH, Salina D, Poon KK, Fahey C, Yipp BG, Sibley CD, et al. A novel mechanism of rapid nuclear neutrophil extracellular trap formation in response to Staphylococcus aureus. J Immunol. 2010;185(12):7413-25.
43. Brinkmann V, Zychlinsky A. Beneficial suicide: why neutrophils die to make NETs. Nat Rev Microbiol. 2007;5(8):577-82.
44. Yost CC, Cody MJ, Harris ES, Thornton NL, McInturff AM, Martinez ML, et al. Impaired neutrophil extracellular trap (NET) formation: a novel innate immune deficiency of human neonates. Blood. 2009;113(25):6419-27.
45. Hazeldine J, Harris P, Chapple IL, Grant M, Greenwood H, Livesey A, et al. Impaired neutrophil extracellular trap formation: a novel defect in the innate immune system of aged individuals. Aging Cell. 2014;13(4):690-8.
46. Metzler KD, Fuchs TA, Nauseef WM, Reumaux D, Roesler J, Schulze I, et al. Myeloperoxidase is required for neutrophil extracellular trap formation: implications for innate immunity. Blood. 2011;117(3):953-9.
47. Bianchi M, Niemiec MJ, Siler U, Urban CF, Reichenbach J. Restoration of anti-Aspergillus defense by neutrophil extracellular traps in human chronic granulomatous disease after gene therapy is calprotectin-dependent. J Allergy Clin Immunol. [En línea] 2011 [Citado el 08 de marzo de 2015];127(5). Disponible en: http://www.sciencedirect.com/science/article/pii/S0091674911000662
48. Martinelli S, Urosevic M, Daryadel A, Oberholzer PA, Baumann C, Fey MF, et al. Induction of genes mediating interferon-dependent extracellular trap formation during neutrophil differentiation. J Biol Chem. 2004;279(42):44123-32.
49. Contursi C, Wang IM, Gabriele L, Gadina M, O'Shea J, Morse HC, et al. IFN consensus sequence binding protein potentiates STAT1-dependent activation of IFNgamma-responsive promoters in macrophages. Proc Natl Acad Sci U S A. 2000;97(1):91-6.
50. Newburger PE, Ezekowitz RA, Whitney C, Wright J, Orkin SH. Induction of phagocyte cytochrome b heavy chain gene expression by interferon gamma. Proc Natl Acad Sci U S A. 1988;85(14):5215-9.
51. Ezekowitz RA, Sieff CA, Dinauer MC, Nathan DG, Orkin SH, Newburger PE. Restoration of phagocyte function by interferon-gamma in X-linked chronic granulomatous disease occurs at the level of a progenitor cell. Blood. 1990;76(12):2443-8.
52. Yamada M, Gomez JC, Chugh PE, Lowell CA, Dinauer MC, Dittmer DP, et al. Interferon-γ production by neutrophils during bacterial pneumonia in mice. Am J Respir Crit Care Med. 2011;183(10):1391-401.
]]>53. Remijsen Q, Vanden Berghe T, Wirawan E, Asselbergh B, Parthoens E, De Rycke R, et al. Neutrophil extracellular trap cell death requires both autophagy and superoxide generation. Cell Res. 2011;21(2):290-304.
54. Marcos V, Zhou Z, Yildirim AO, Bohla A, Hector A, Vitkov L, et al. CXCR2 mediates NADPH oxidase-independent neutrophil extracellular trap formation in cystic fibrosis airway inflammation. Nat Med. 2010;16(9):1018-23.
55. Parker H, Dragunow M, Hampton MB, Kettle AJ, Winterbourn CC. Requirements for NADPH oxidase and myeloperoxidase in neutrophil extracellular trap formation differ depending on the stimulus. J Leukoc Biol. 2012;92(4):841-9.
56. Byrd AS, O'Brien XM, Johnson CM, Lavigne LM, Reichner JS. An extracellular matrix-based mechanism of rapid neutrophil extracellular trap formation in response to Candida albicans. J Immunol. 2013;190(8):4136-48.
57. Arai Y, Nishinaka Y, Arai T, Morita M, Mizugishi K, Adachi S, et al. Uric acid induces NADPH oxidase-independent neutrophil extracellular trap formation. Biochem Biophys Res Commun. 2014;443(2):556-61.
]]>
Recibido: mayo 07, 2015.
Aceptado: septiembre 10, 2015.
Gabriel Jaime Vélez Tobón . Grupo Inmunodeficiencias Primarias – IDP. Centro Jeffrey Modell para Diagnóstico e Investigación JMCN. Calle 62 # 52-59 Sede de investigación Universitaria SIU. Medellín - Colombia. Teléfono: 57-4-219647
Email: gjvelez@gmail.com