COMUNICACIÓN BREVE
Anticuerpos anticitomegalovirus y antivirus de Epstein Barr en pacientes cubanos en espera de trasplante hematopoyético
Anti-citomegalovirus and anti-Epstein Barr virus seroprevalence in cuban patients waiting for hematopoietic stem cell transplant
Delfina Costales ElizaldeI, Luz M Morera Barrios I, Nadezhda González GarcíaII, Arturo Chang MonteagudoI, Lelyem Marcell Rodríguez I, Catalino R Ustariz GarcíaI, Antonio Bencomo HernándezI
]]> I Instituto de Hematología e Inmunología, La Habana, CubaII Hospital Clínico Quirúrgico Hermanos Ameijeiras, La Habana, Cuba
RESUMEN
Las complicaciones secundarias a las infecciones por citomegalovirus (CMV) y virus de Epstein Barr (EBV) constituyen las principales causas de morbilidad y mortalidad por infecciones en los pacientes que reciben injertos de células progenitoras hematopoyéticas (CPH). La detección de anticuerpos específicos contra cada uno de estos virus en el periodo pretrasplante permite prevenir la primoinfección durante la inmunosupresión terapéutica.La investigación tuvo como objetivo determinar la seroprevalencia de anticuerpos anti-CMV y anti-EBV e identificar aquellos pacientes con riesgo de adquirir una infección primaria postrasplante.Se realizó la detección de anticuerpos IgM e IgG anti-CMV y anti-EBV por ELISA, a 110 pacientescon indicación de pruebas de histocompatibilidad para trasplante de CPH, entre enero del 2013 y enero del 2016, en el Departamento de Histocompatibilidad del Instituto de Hematología e Inmunología de La Habana.La seroprevalencia de anticuerpos anti-CMV en la población estudiada fue del 84,5 % y anti-EBV, del 90,9 %. Los menores de 9 años presentaron un porcentaje de positivad del 70,6 y 64,7 % para IgG anti-CMV y EBV respectivamente, encontrándose un incremento de la seroprevalencia con la edad.La seroprevalenciade anticuerpos anti-CMV y anti-EBV en los pacientes en espera de trasplante de CPH en Cuba es semejante a otras poblaciones; lo que sugiere la necesidad evitar el contagio por transmisión a los casos seronegativos.
Palabras clave: anticuerpos, anti-CMV, anti-EBV, antígenos leucocitarios humanos, complejo principal de histocompatibilidad, trasplante de progenitores hematopoyéticos.
ABSTRACT
Secondary complications due to infections caused by Cytomegalovirus (CMV) and Epstein Barr virus (EBV) are the major infectious causes of morbidity and mortality in recipients of hematopoietic stem cell (HSC) grafts. Detection of specific antibodies against each of those viruses in the pre-transplant period allows the prevention of the primary infection during the immune suppressive therapy.The aim of the investigation was to determine seroprevalence of antibodies against CMV and EBV and also to identify the patients in risk of a primary infection in the post-transplant period.The investigation was conducted between January 2013 and January 2016 by the Histocompatibility Department of Instiute of Hematology and Immunology. Antibodies IgM and IgG against CMV and EBV were tested by ELISA in 110 patients with the indication for histocompatibility testing for a HSC graft.Seroprevalence of antibodies against CMV in this population was 84.5% and seroprevalence of antibodies against EBV was 90.9%. The 70.6% of children less than 9 years old had positive IgG CMV antibodies and the 64.7% of them had positive IgG EBV antibodies. An increase of seroprevalence with age was found.
The seroprevalence of antibodies against CMV and EBV in patients waiting for a HSC transplant in Cuba is similar to the populations in other countries. This result suggests the need of avoiding the transmissiontoseronegative recipients.
]]> Keywords: antibody, anti-CMV, anti-EBV, human leukocyte antigens, major histocompatibility complex, hematopoietic stem cell transplantation.
INTRODUCCIÓN
Las complicaciones secundarias a las infecciones por citomegalovirus (CMV) y virus de Epstein Barr (EBV) posteriores al trasplante constituyen las principales causas de morbilidad y mortalidad por infecciones de los pacientes que reciben injertos de células progenitoras hematopoyéticas (CPH)1-3.
En estos casos estas infecciones pueden adquirirse de forma exógena por exposición en la comunidad, mediante la transfusión de hemocomponentes y a través del propio injerto; o por vía endógena, debido a la reactivación de agentes infecciosos que se encuentran de manera latente en el organismo4.
En los receptores de trasplante de CPH las complicaciones por estos herpesvirus pueden deberse a una infección primaria, reactivación o reinfección. La infección primaria ocurre cuando se adquiere el virus por primera vez, generalmente a partir de transfusiones sanguíneas o en los casos en que el donante es seropositivo y el receptor es seronegativo (D+/R-)5, 6.
La reactivación ocurre cuando el virus entra a un estado latente episomal en el receptor, y se vuelve activo luego de la supresión de las defensas7; y la reinfección se manifiesta en aquellos pacientes que han estado en contacto con una cepa y se infectan con otra que sea suficientemente diferente a la inicial5.
Cuando las defensas del hospedero están disminuidas puede ocurrir la enfermedad debido a la reactivación o la reinfección por el virus en el 10 - 20 % de los receptores. Generalmente, los síntomas son moderados o leves en comparación con aquellos que desarrollan enfermedad por infección primaria. Cuando los pacientes son seropositivosal igual que el donante(D+/R+), la reactivación y la reinfección son fenómenos comunes luego del trasplante 8.
A pesar de que la detección de IgM e IgG específicas para estos virus no es un método útil para el diagnóstico postrasplante, debido a la depresión de la inmunidad humoral;estas pruebas se recomiendan en el periodo pretrasplante, lo cual es de importancia para aquellos receptores negativos cuyos donantes sean positivos (D+/R-); lo que justificaría el empleo de profilaxis antiviral postrasplante8.
]]> El 90 % de los adultos a nivel mundial tiene anticuerpos del tipo IgG específicos contra el CMV por haber presentado primoinfección. De igual forma, del 40 al 80 % es positivo paraIgG anti-EBV1. Sin embargo, aunque en Cuba se han conducido investigaciones sobre el estatus serológico frente a estos herpes virus en algunos grupos especiales 9-14, hasta la fecha no se ha determinado en pacientes en espera de trasplante de CPH.Teniendo en cuenta la importancia de los mencionados estudios, se realizó la detección de anticuerpos anti-CMV y anti-EBV a todos los pacientes con enfermedades hematológicas e indicación de pruebas de histocompatibilidadpara posible trasplante de CPH, con el objetivo de determinar la seroprevalencia de infección por CMV y EBV e identificar aquellos pacientes con riesgo de adquirir una infección primaria postrasplante.
MÉTODOS
La detección de anticuerpos IgM e IgG anti-CMV y anti-EBV se realizó, en el Departamento de Histocompatibilidad del Instituto de Hematología e Inmunología de La Habana, entre enero del 2013 y enero del 2016, a todos los pacientes con enfermedades hematológicas del país con indicación de pruebas de histocompatibilidadpara trasplante de CPH.
Se estudió un total de 110 pacientes con edades entre 3 y 67 años; 45 del sexo femenino y 65 del sexo masculino; con diagnóstico de leucemias mieloblásticas (34 agudas y 13 crónicas), leucemias linfoblásticas (29 agudas y 2 crónicas), aplasias medulares (15), linfomas (11) y otras enfermedades (6).
Las determinaciones se realizaron por el método de ELISA, mediante inmunoensayos indirectos cuantitativosde detección de anticuerpos. Se utilizaron los estuches comercialesCytomegalovirusIgG ELISA, CytomegalovirusIgM ELISA, Epstein-Barr virus VCA IgG y Epstein-Barr virus VCA IgM(IBL International, Alemania), siguiendo las instrucciones del fabricante. Todas las técnicas se realizaron de forma automatizada mediante un analizador CHEMWELL® 2910 (AwarenessTechnology, EEUU).
Se respetaron los principios éticos relacionados con las investigaciones médicas15.
RESULTADOS
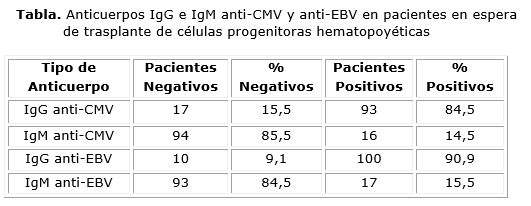
]]> La seroprevalencia de anticuerpos IgG anti-CMV en la población estudiada fue del 84,5 %. De los 110 pacientes estudiados, 17 tuvieronniveles indetectables de anticuerpos IgG anti-CMV (tabla).En 16 pacientes se encontraron anticuerpos IgM anti-CMV (tabla), de ellos, 15 también fueron positivos a IgG, lo que indicó que la infección no era reciente. Solo en un caso, un niño de 8 años, la IgG anti-CMV fue indetectable lo que, unido con el cuadro clínico, permitió orientar al equipo médico sobre la posibilidad de que estuviera cursando la primoinfección por CMV.
La seroprevalenciade los anticuerpos anti-EBV fue del 90,9 %. Un total de 10 pacientes presentaron niveles indetectables de anticuerpos IgG anti-EBV, los cuales constituyeron el grupo al que se le aplicó especial atención desde el punto de vista médico (tabla).
En la muestra estudiada, 17 pacientes presentaron anticuerpos IgM anti-EBV positivos (tabla); sin embargo, todos ellos también tuvieron niveles detectables de IgG anti-EBV; indicativo de que en estos casos la primoinfección no era reciente.
Los menores de 9 años presentaron un porcentaje de positivad del 70,6 y 64,7 % para CMV y EBV, respectivamente. Estas seroprevalencias fueron en aumento con la edad, hasta que a partir de los 50 años alcanzaron el 100 % para ambos herpesvirus (figura).
DISCUSIÓN
La seroprevalencia de anticuerpos anti-CMV en la muestra estudiada concuerda con lo referido en la literatura para la población general, aunque por debajo del 100 % encontrado por Loutfy y colaboradores en un estudio similar en 68 niños con leucemia linfoblástica aguda en Egipto16-18.
El hallazgo de anticuerpos del tipo IgG contra el CMV en una población es un hecho común dado por la fácil diseminación, las múltiples vías de transmisión y las características propias del virus, que incluyen la latencia, la reactivación y la excreción asintomática4.
]]> La seroprevalencia de anticuerpos específicos contra el CMV varía según el país y la presencia de algunos factores de riesgo como la etnia y las condiciones socieconómicas de vida19, pero en el presente estudio no se realizaron dichos análisis, con excepción de la estratificación por edades debido a la homogeneidad de la población estudiada.Algunas investigaciones previas han reportado que no existen diferencias significativas en la seroprevalencia entre hombres y mujeres 17,20,21, aunque autores como Hassan en Irlanda y Korndewal en Holanda encontraron lo contrario. 22, 23.Teniendo en cuenta la desproporción numérica entre hombres y mujeres y el tamaño de muestra del presente estudio no se realizó análisis por sexos.
Los pacientes con niveles indetectables de anticuerpos IgG anti-CMV, aunque estuvieron en minoría en comparación con los que resultaron positivos, constituyeron un hallazgo de suma importancia desde el punto de vista clínico, por cuanto fue el grupo con mayor riesgo de complicaciones postrasplante y que requirió una conducta médica diferenciada.
El CMV tiene un efecto inmunosupresor sobre el sistema inmune, al provocar la disminución de la expresión de las moléculas HLA clase I y II en las células T y en las células presentadoras de antígenos. Por otra parte, como parte de su mecanismo de escape, la infección induce la producción de moléculas HLA clase I solubles que bloquean el reconocimiento por células NK y T. Al mismo tiempo, la reactivación y reinfección es favorecida por el tratamiento de inmunosupresión administrado a los pacientes que requieren trasplante7, 24.
El incremento de la seroprevalencia para CMV con la edad fue reportado por Voigt y colaboradores, aunque los porcentajes que determinaron estos investigadores fueron mucho menores que los del presente estudio, oscilando entre el 21,5 y 32,0 % para 1 y 17 años, respectivamente20.
La seroprevalencia de los anticuerpos anti-EBV coincide con lo reportado internacionalmente4, 25. Para el caso de receptores renales seronegativos a EBV Babel y colaboradores propusieron inducir la primoinfección en el pre trasplante mediante transfusiones sanguíneas, para evitar el riesgo de la enfermedad linfoproliferativa 26.
La positividad a anticuerpos IgG anti-EBV en la población en espera de trasplante de CPH de Cuba también concuerda con el metanálisis de seroprevalencia para EBV realizado por Dowd y colaboradores en población norteamericana entre los 6 y 19 años de edad, aunque por el diseño de dicha investigación no pudieron realizarse comparaciones a partir de los 20 años27.
Al ser la primoinfección de estos herpes virus causante de disminución de la sobrevida en los receptores de un injerto de CPH 28, la detección serológica de anticuerpos anti-CMV y anti-EBV mediante un ELISA en la etapa pre trasplante es un método sencillo y económico que permite tomar medidas tempranas para disminuir la morbimortalidad.
Los resultados del presente estudio demostraron que la seroprevalencia de CMV y EBV en los pacientes en espera de trasplante de CPH en Cuba es semejante a la de otras poblaciones; lo que sugiere la necesidad de tomar medidas para evitar el contagio por transmisión sanguínea a los casos seronegativos.
1. Kourí V, Correa C, Martínez PA, Sanchez L, Alvarez A, González G, et al. Prospective, comprehensive, and effective viral monitoring in Cuban children undergoing solid organ transplantation. Springerplus. 2014; 3: 247. doi: 10.1186/2193-1801-3-247.
2. Jaskula E, Dlubek D, Sedzimirska M, Duda D, Tarnowska A, Lange A. Reactivations of cytomegalovirus, human herpes virus 6, and Epstein-Barr virus differ with respect to risk factors and clinical outcome after hematopoietic stem cell transplantation. Transplant Proc. 2010 Oct;42(8):3273-6. doi: 10.1016/j.transproceed.2010.07.027.
3. Caston JJ, Cisneros JM, Torre-Cisneros J. Effects of viral infection on transplant recipients. Enferm Infecc Microbiol Clin. 2007;25(8):535-48.
4. Reddehase MJ, Lemmermann N. Cytomegaloviruses: Molecular Biology and Immunology. Norfolk: Caister Academic Press; 2006.
5. de la Torre-Cisneros J, Farinas MC, Caston JJ, Aguado JM, Cantisan S, Carratala J, et al. GESITRA-SEIMC/REIPI recommendations for the management of cytomegalovirus infection in solid-organ transplant patients. Enferm Infecc Microbiol Clin. 2011;29(10):735-58.
6. De Paschale M, Clerici P. Serological diagnosis of Epstein-Barr virus infection: Problems and solutions. World J Virol. 2012;1(1):31-43.
7. Hussein AA, Al-Antary ET, Najjar R, Al-Hamdan DS, Al-Zaben A, Frangoul H. Incidence and risk factors for cytomegalovirus (CMV) reactivation following autologous hematopoietic stem cell transplantation in children. Pediatr Blood Cancer. 2015;62(6):1099-101.
8. Britt W. Primate models: Pros and cons. In: Reddehase MJ, ed. Cytomegaloviruses: from molecular pathogenesis to intervention. Norfolk: Caister Academic Press; 2006.
9. Resik S, Enamorado A, Tallo Y, Suárez C, Kourí V, Acosta B, et al. Prevalencia de anticuerpos contra virus herpes simple, virus Epstein-Barr y Citomegalovirus en un grupo de pacientes con hemodiálisis realizada. Rev cubana medtrop. 1999;51(3):172-6.
10. Alfonso Valdés ME, Macias Abraham C, Lorigados L, Fonte L, Orbeal L, Basanta P, et al. Presencia de anticuerpos contra CMV en pacientes politransfundidos. III Congreso Nacional de Microbiología y Parasitología. La Habana;1986. p. 440.
11. Lorigados L, Aranda RE, Rivero R, Salas M, Rojas A, Ballester JM. Detección de anticuerpos contra el citomegalovirus en donantes de sangre. Rev Cubana Hematol Inmunol Hemoter 1987;3(1):105-12.
12. Rivero RA, Lorigados LC, Macías C, Machado H, Álvarez PL, Hernández A, Ballester JM. Anticuerpos anticitomegalovirus humano (CMV) en embarazadas a término y en recién nacidos vivos de Ciudad de La Habana. Rev Cubana Hematol Inmunol Hemoter 1988;4(1):117-24.
13. Silva E, Navea L, Suárez O, Rivero R. Seropositividad al citomegalovirus (CMV) en receptores de transplante renal. Rev Cubana Hematol Inmunol Hemoter. 1990;6(1):75-83.
14. Marcell Rodríguez L, Morera Barrios LM, Costales Elizalde DT, Chang Monteagudo A, Ustariz García C, Bencomo Hernández A. Anticuerpos anticitomegalovirus y antivirus de Epstein Barr pretrasplante renal en Cuba. Rev Cubana Hematol Inmunol Hemoter [revista en Internet]. 2016 [citado 2017 Feb 17];32(4):[aprox. 0 p.]. Disponible en: http://www.revhematologia.sld.cu/index.php/hih/article/view/463
15. Declaración de Helsinki de la AMM - Principios éticos para las investigaciones médicas en seres humanos. 2013.[citado 19 Abr 2015].Disponible en: http://www.wma.net/es/30publications/10policies/b3/ .
]]>16. Freeman RB, Jr. The 'indirect' effects of cytomegalovirus infection. Am J Transplant. 2009;9(11):2453-8.
17. Shaiegan M, Rasouli M, Zadsar M, Zolfaghari S. Meta-analysis of cytomegalovirus seroprevalence in volunteer blood donors and healthy subjects in Iran from 1992 to 2013. Iran J Basic Med Sci. 2015;18(7):627-34.
18. Loutfy SA, Alam El-Din HM, Ibrahim MF, Hafez MM. Seroprevalence of herpes simplex virus types 1 and 2, Epstein-Barr virus, and cytomegalovirus in children with acute lymphoblastic leukemia in Egypt. Saudi Med J. 2006;27(8):1139-45.
19. Jansen MA, van den Heuvel D, Bouthoorn SH, Jaddoe VW, Hooijkaas H, Raat H, et al. Determinants of Ethnic Differences in Cytomegalovirus, Epstein-Barr Virus, and Herpes Simplex Virus Type 1 Seroprevalence in Childhood. J Pediatr. 2016;170:126-34 e6.
20. Voigt S, Schaffrath Rosario A, Mankertz A. Cytomegalovirus Seroprevalence Among Children and Adolescents in Germany: Data From the German Health Interview and Examination Survey for Children and Adolescents (KiGGS), 2003-2006. Open Forum Infect Dis. 2015 Dec 9;3(1):ofv193. doi: 10.1093/ofid/ofv193.
]]>21. Mahmoud RA, El-Mazary AA, Khodeary A. Seroprevalence of Hepatitis C, Hepatitis B, Cytomegalovirus, and Human Immunodeficiency Viruses in Multitransfused Thalassemic Children in Upper Egypt. Adv Hematol. 2016;2016:9032627.
22. Hassan J, O'Neill D, Honari B, De Gascun C, Connell J, Keogan M, et al. Cytomegalovirus Infection in Ireland: Seroprevalence, HLA Class I Alleles, and Implications. Medicine. 2016;95(6):e2735.
23. Korndewal MJ, Mollema L, Tcherniaeva I, van der Klis F, Kroes AC, Oudesluys-Murphy AM, et al. Cytomegalovirus infection in the Netherlands: seroprevalence, risk factors, and implications. J ClinVirol. 2015;63:53-8.
24. Eid AJ, Brown RA, Hogan WJ, Lahr BD, Eckel-Passow JE, Litzow MR, et al. Kinetics of interferon-gamma producing cytomegalovirus (CMV)-specific CD4+ and CD8+ T lymphocytes and the risk of subsequent CMV viremia after allogeneic hematopoietic stem cell transplantation. Transpl Infect Dis. 2009;11(6):519-28.
25. Levine H, Balicer RD, Rozhavski V, Halperin T, Shreberk M, Davidovitch N, et al. Seroepidemiology of Epstein-Barr virus and cytomegalovirus among Israeli male young adults. Ann Epidemiol. 2012;22(11):783-8.
]]>26. Babel N, Gabdrakhmanova L, Hammer M, Rosenberger C, Oppert M, Volk HD, et al. Induction of pre-transplant Epstein-Barr virus (EBV) infection by donor blood transfusion in EBV-seronegative recipients may reduce risk of post-transplant lymphoproliferative disease in adolescent renal transplant patients: report of two cases. Transpl Infect Dis. 2005;7(3-4):133-6.
27. Dowd JB, Palermo T, Brite J, McDade TW, Aiello A. Seroprevalence of Epstein-Barr virus infection in U.S. children ages 6-19, 2003-2010. PLoS One. 2013;8(5):e64921.
28. Xuan L, Huang F, Fan Z, Zhou H, Zhang X, Yu G, et al. Effects of intensified conditioning on Epstein-Barr virus and cytomegalovirus infections in allogeneic hematopoietic stem cell transplantation for hematological malignancies. J Hematol Oncol. 2012;5:46.
Recibido: diciembre 08, 2016.
Aceptado: enero 31, 2017.
Lic. Delfina Costales Elizalde. Instituto de Hematología e Inmunología. Apartado 8070, La Habana, CP 10800, CUBA.
Email: rchematologia@infomed.sld.cu