Descriptores DeCS: VACUNAS CONTRA HEPATITIS B/inmunología; ASMA/sangre; ANTIGENOS DE SUPERFICIE DE LA HEPATITIS B/análisis; CAMPAÑAS DE VACUNACIÓN; PROGRAMAS DE INMUNIZACIÓN; CUBA.
La hepatitis viral B constituye un problema mundial de salud; en el mundo existen más de 300 000 000 de portadores crónicos del virus que la produce, el virus de la hepatitis B (VHB) que es el responsable a su vez, de más de 80 % de los casos de cáncer primario del hígado, y resulta uno de los escasos virus cuya relación con la aparición del cáncer en el hombre está demostrada.1,2
La característica epidemiológica más importante de la enfermedad, que afecta su endemicidad y debe ser reconocida a la hora de desarrollar estrategias de prevención, es en primer lugar, el carácter asintomático de muchos de los infectados por el virus, así como la edad en la que se produce la infección, que a su vez se relaciona primariamente con la vía de trasmisión del virus. La probabilidad de desarrollar las formas crónicas de la enfermedad es muy alta (70-90 %) si la infección se produce en edades tempranas de la vida, lo que a su vez incrementa la mortalidad.3 Es así que los esfuerzos para prevenir la hepatitis B deben estar dirigidos en gran medida a la población mundial más joven.4
La herramienta más simple e importante para prevenir y controlar esta enfermedad es la vacuna contra su agente etiológico. Su uso en cantidades suficientes y con estrategias apropiadas, permitirá a corto plazo una reducción de los niveles de infección por el VHB y, a largo plazo, podría permitir la eliminación de la hepatitis como enfermedad para el hombre.3,5
Cuba posee una prevalencia de portadores crónicos del VHB entre baja e intermedia con variaciones regionales (0,8-1 %) (Ministerio de Salud Pública de Cuba. Dirección Nacional de Epidemiología. La hepatitis B en Cuba. [Informe anual]. La Habana, 1998) y desde hace 5 años inmuniza a todos sus recién nacidos con la vacuna antihepatitis B de subunidades, obtenida por la tecnología del ADN recombinante producida en el Centro de Ingeniería Genética y Biotecnología (Heberbiovac-HB), que ha demostrado ser segura e inmunogénica. El éxito de la vacunación en lo que respecta a protección, radica en que la respuesta sea intensa y duradera, y se acepta como protectora una concentración de anticuerpos contra el antígeno de superficie (anti-AgsHB) de al menos 10 UI/L.6 Uno de los retos impuestos a los programas de vacunación en los países donde la vacuna antihepatitis B forma parte del Programa Ampliado de Inmunización, consiste en evaluar si se reproducen los resultados obtenidos en los estudios controlados cuando se sobreim-ponen las condiciones de trabajo en el terreno; y si los niveles de anticuerpos persisten por largos períodos después de culminado un esquema completo de 3 dosis. Mediante este trabajo se quiso conocer si la vacunación con la vacuna Heberbiovac-HB aplicada a niños cubanos como parte del Programa Nacional de Inmunización antihepatitis B lograba niveles de protección adecuados y persistencia de los anticuerpos al menos 3 años después de terminado el esquema. Asimismo se evaluó si algunos factores conocidos como modificadores de la respuesta inmune podrían influenciar en la respuesta en los niños estudiados.
Por tratarse de un estudio en que se evaluó el impacto del programa en el terreno, no se establecieron criterios de exclusión de la muestra, sino que se recogieron en entrevista natural las informaciones ofrecidas por las madres con respecto a historia de infecciones a repetición, empleo de esteroides y enfermedades conocidas como generadoras de disreacción (asma bronquial y otras formas de atopia, neoplasias, etc.). En la entrevista se interrogó a las madres acerca de si sus niños habían sido vacunados con un esquema completo, con vistas a evaluar la cobertura del programa.
Las muestras se distribuyeron en 3 grupos de acuerdo con rangos de edades de la manera siguiente: Un primer grupo desde 7 a 11 meses y 29 d, un segundo grupo desde 12 a 23 meses y 29 d y un tercero desde 24 a 36 meses. El primer grupo estuvo formado por 580 niños, el segundo por 430 y el tercero por 270 para un total de 1 280. La estratificación por rangos de edades y no por años tuvo como propósito incrementar el número de niños en cada grupo. En la muestra se incluyeron niños de ambos sexos, sin considerarlos dentro de grupos diferentes, porque esta variable comienza a ser relevante en la respuesta inmune sólo cuando se ha llegado a la pubertad.
Vacuna, dosis y esquema de inmunización: Se empleó la vacuna cubana de subunidades (AgsHB) obtenida mediante la tecnología del ADN recombinante de la firma Heber Biotec (Heberbiovac-HB, CIGB). La dosis empleada fue de 10 µg por inóculo con un esquema de 3 dosis, administradas al nacimiento, al mes y a los 6 meses de nacidos.
Obtención de las muestras: Se obtuvo la sangre por punción yugular en los niños más pequeños y por punción venosa en la región antecubital en los mayores. Después de retraer el coágulo, se extrajeron los sueros, y se conservaron a -20 oC hasta que se realizó el ensayo de detección y cuantificación del AgsHB y anti-AgsHB de manera concurrente y por un mismo técnico. ]]>
Métodos: Se estudiaron los marcadores del sistema de superficie del VHB mediante 2 métodos inmunoenzimométricos tipo sandwich, producidos y validados en el Laboratorio de Inmunología del Instituto de Ciencias Básicas y Preclínicas (ICBP) "Victoria de Girón". Para la detección del AgsHB se empleó un ELISA tipo sandwich de doble anticuerpo con una sensibilidad entre 0,5 y 1 ng/mL, y en el caso del anti-AgsHB, el ELISA fue de doble antígeno con una sensibilidad de 7 UI/L; para el recubrimiento y el conjugado se empleó el antígeno recombinante con que se fabricó la vacuna.La concentración del anti-AgsHB en cada grupo se estimó mediante el cálculo de la media geométrica (raíz n del producto de los valores individuales detectados). Para ello se obtuvo la sumatoria de la transformación logarítmica de las concentraciones de anti-AgsHB iguales o superiores a 1 UI/L, y se tomó finalmente el antilogaritmo del valor medio de los datos transformados.
Se consideraron los porcentajes de seroprotección e hiperrespuesta en cada grupo, se incluyeron en la seroprotección aquéllos cuyas concentraciones de anti-AgsHB fueron superiores a 10 UI/L, y con hiperrespuesta a los que presentaron cifras iguales o mayores que 100 UI/L.
Se compararon mediante la prueba de chi cuadrado los valores obtenidos para la seroprotección e hiperrespuesta intergrupos, y las medias geométricas transformadas se compararon mediante un test de Mann Whitney (para muestras independientes en ausencia de normalidad de la población). En el muestreo se incluyeron los niños de acuerdo con el orden en que acudieron a los servicios de atención primaria y secundaria donde se realizó la investigación, y por la disposición de las madres para participar en el estudio, manifestada mediante la firma del consentimiento informado. Los niveles de anti-AgsHB se determinaron en los ensayos inmunoenzimáticos sin que los operadores conociesen las edades o las enfermedades que padecían los niños.
En los 3 grupos de niños vacunados los porcentajes de seroprotección fueron superiores a 95 %. Los porcentajes de hiperrespuesta más elevados se encontraron en el grupo de niños menores de 1 año (tabla 1).
TABLA 1. Porcentajes de seroprotección e hiperrespuesta en niños vacunados con la vacuna cubana antihepatitis B (Heberbiovac HB)
| Grupos | | | ||
| ]]> No. | | | | |
| 7 meses - 1 año | | | | |
| | | ]]> 390/430 | | |
| 2 años - 3 años | | | | |
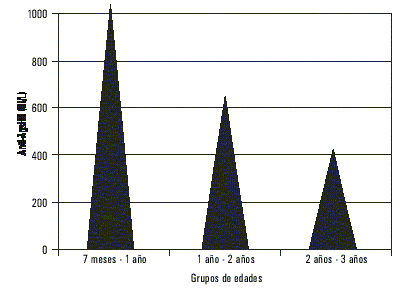
Al comparar la variable seroprotección entre grupos no se encontró significación, pero sí para la variable hiperrespuesta a favor del grupo de los niños entre 12 y 23 meses con respecto a los mayores de 24 meses, y del grupo de 7 a 11 meses también con respecto a los mayores de 24 meses. Los valores de las medias geométricas de anti-AgsHB para los diferentes grupos fueron de 1 056, 699 y 483 UI/L (fig. 1), esto representa una disminución de 1,5 veces entre los 6 y los 18 meses después de terminado un esquema completo de vacunación y de 2 veces cuando habían transcurrido entre 19 y 30 meses.
De todas las posibles enfermedades que se registraron en la entrevista natural, sólo el asma bronquial tuvo suficiente representatividad dentro de la muestra para permitir comparaciones entre afectados y no afectados, el total de niños asmáticos fue de 600, para 46,8 %. La distribución dentro de cada grupo de edades se muestra en la tabla 2, así como los porcentajes de seroprotección e hiperrespuesta. Para la variable seroprotección no se encontró significación al comparar dentro de cada grupo los valores obtenidos para asmáticos y no asmáticos, pero sí fueron significativas las diferencias entre éstos en los grupos de niños con edades comprendidas entre 7 y 11 meses y en los de 24 y 36 meses para la variable hiperrespuesta.
TABLA 2. Porcentaje de seroprotección e hiperrespuesta en niños asmáticos y no asmáticos vacunados con la vacuna cubana antihepatitis B (Heberbiovac HB)
| ]]> Grupos Seroprotección | | ||||
| | | | | ||
| 7 meses | |||||
| Asmáticos | | | | | ]]> * p < 0,05 |
| No asmáticos | | | | | |
| 1 año - 2 años | |||||
| Asmáticos | | | | | |
| No asmáticos | | ]]> 100 | | | |
| 2 años - 3 años | |||||
| Asmáticos | | | | | |
| No asmáticos | | | ]]> 0/180 | | |
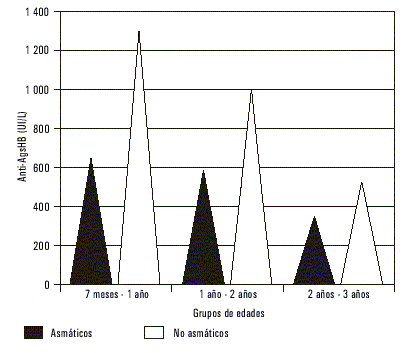
Los valores de las medias geométricas en los niños asmáticos fueron de 687, 620 y 402 UI/L para cada uno de los 3 grupos y resultaron significativamente menores que las obtenidas para los que no exhibieron ese marcador genético, que fueron de 1 341, 1 047 y 528 UI/L respectivamente (fig. 2). Estas diferencias se hicieron menos evidentes en el grupo de niños mayores de 24 meses. La caída de las concentraciones de anticuerpos entre los niños asmáticos no siguió el mismo patrón que el encontrado para el total de la muestra, pues cuando habían transcurrido entre 6 y 18 meses de terminado el esquema, sólo habían disminuido 1,1 veces y 1,53 al pasar entre 19 y 30 meses. En el caso de los niños no asmáticos la disminución fue de 1,28 veces y de 1,98 veces, respectivamente.

Del mismo modo, la estimación de la inmunogenicidad de una vacuna en una población abierta después que ha sido estudiada en grupos controlados, contribuye a evaluar el producto, pues se administra a personas que pueden tener comprometida la respuesta inmune, permite medir la efectividad del programa que está en ejecución, así como conocer el grado de protección alcanzado en la población vacunada. Es de destacar que con excepción del grupo de niños menores de 1 año, pueden considerarse protegidos todos los inmunizados con esta vacuna. El valor de seroprotección encontrado en ese grupo lo determinó la ausencia de anti-AgsHB en niños no infectados con el virus, y en los cuales no se reportaron en la entrevista natural, enfermedades o ingestión de medicamentos conocidos como comprometedores de la respuesta inmune. Estos resultados coinciden con trabajos realizados con vacunas similares, por lo que se pueden clasificar como no respondedores a la vacuna, de acuerdo con lo reportado.7-10 ]]>
Teniendo en cuenta que la clasificación de hiperrespuesta se basa en la presencia de concentraciones de anticuerpos superiores o iguales a 100 UI/L, es de esperar que transcurrido 1 año o más del final de una serie de vacunas que integran el esquema, los niveles hayan descendido; pues se ha demostrado que ellos caen más de 6 veces entre los 9 y los 18 meses luego de terminada la vacunación, y declinan después más gradualmente.11,12 Sin embargo, la relación de disminución de esas cifras en este estudio fue de 1,5 veces entre cada uno de los grupos y de 2 veces entre el primero y el tercero; lo que podría hacer pensar que influyeron factores como son la forma transversal en que se realizó el muestreo y la estimación de las medias por grupos de edades, a diferencia de los estudios longitudinales que reportan caídas más bruscas. No obstante, el hecho de que otros investigadores que han usado la vacuna cubana (Juliao O. Estudio longitudinal de inmunogenicidad con la vacuna Heberbiovac-HB después de la segunda y la tercera dosis, al segundo y cuarto año posesquema 0-1-2 meses en niños de 1 a 10 años. En: Profilaxis y control de la hepatitis B en niños y jóvenes. Editado por el Hospital Pediátrico Docente "Juan Manuel Márquez". La Habana. Cuba, febrero 1997:21-7) reportaron en un estudio longitudinal controlado, que la media geométrica de anti-AgsHB a los 2 años fue 1,9 veces inferior a la obtenida al finalizar el esquema, hizo pensar que estas diferencias podrían atribuirse al hecho de que las vacunas utilizadas no fueron las mismas en los estudios que describieron pérdidas mayores de anticuerpos. Otro elemento a considerar es el origen étnico de las poblaciones vacunadas, muy similar entre los grupos evaluados con la utilización de la vacuna Heberbiovac-HB, y diferente a la de los estudios con caucásicos, por el papel que desempeña el componente genético en la generación y mantenimiento de la respuesta inmune. La disminución en general siguió un patrón similar a lo reportado en otros trabajos,11,12 más agudo en los primeros meses, con una declinación menor en los últimos y con cifras elevadas aun después de transcurridos los 36 meses de culminado el esquema.No obstante existir la opinión de que es importante evaluar la persistencia de los anticuerpos frente a la proteína de superficie del VHB, de acuerdo con el criterio de que el nivel mínimo requerido para ofrecer protección es de 10 UI/L,6 a la cual los autores de este trabajo se han adscrito, recientemente se discute el verdadero papel de la respuesta humoral en la protección frente a la infección luego de la administración de un esquema completo de vacuna Ello se sustenta en los reportes de homosexuales promiscuos que no tuvieron seroconversión al ser vacunados, y que no sólo no se infectaron en el transcurso de los 10 años que duró el estudio, sino que en ellos se encontraron anticuerpos contra el antígeno core (anti-AgcHB); indicadores de puesta en contacto con viriones completos, y esto podría sugerir que la protección dependió de otro tipo de respuesta.13 Este hecho pondría en tela de juicio la interpretación de forma absoluta de que sólo la presencia de anticuerpos es indicadora de protección, o al menos, el de considerar a los no respondedores como no protegidos contra la infección por este virus. Sería quizás recomendable realizar evaluación de respuesta celular en los individuos que no desarrollen anticuerpos, antes de considerar de manera categórica que no tuvieron ningún tipo de respuesta a la vacunación.
El porcentaje de niños asmáticos en este estudio es muy superior al reportado nacionalmente, que puede llegar hasta 12 en la población infantil (Ministerio de Salud Pública de Cuba. Dirección Nacional de Epidemiología. Reporte de Enfermedades crónicas no trasmisibles [asma bronquial]. Informe anual. La Habana, Cuba. 1998). Ello se debe al sesgo de la muestra, pues una de las causas más frecuentes de concurrencia a los servicios médicos de atención primaria en Cuba es el asma bronquial o el denominado "síndrome de atrapamiento agudo de aire".
La significación encontrada al comparar los porcentajes de hiperrespuesta de niños asmáticos y no asmáticos, podría atribuirse a la influencia del marcador genético de atopia en la desviación de la respuesta inmune hacia un patrón fundamentalmente humoral o celular. Se conoce que la selección de una población de linfocitos T apropiada frente a un reto antigénico ocurre durante estadios tempranos de la respuesta en un huésped virgen y en ella intervienen múltiples factores, entre los que se encuentran el tipo de antígeno, las células que lo presentan y los mediadores producidos en ese evento. Si la selección favorece la proliferación de células T cooperadoras del tipo 1 (Th 1) que secretan interleucina 2 (IL 2) e interferón gamma (IFN g) entre otros, se producirá una respuesta a expensas de inmunoglobulinas de clase G (IgG) y de clase A (IgA) de bajo nivel, no patogénica. Sin embargo, la emergencia de células cooperadoras del tipo 2 (Th 2) secretoras de interleucinas 4 y 5 (IL 4 e IL 5), podría originar la producción de inmunoglobulinas de clase E (IgE), eosinofilia y enfermedades atópicas.4 Por lo tanto, la aparición de IgE en los individuos atópicos en respuesta a diferentes estímulos se explica por la activación selectiva de células Th 2 en respuesta a los alergenos comunes ambientales y están involucradas en la patogénesis de la respuesta alérgica mediada por IgE.15
La demostración de que los atópicos pueden tener también incrementos temporales de la IgE en respuesta a los neoantígenos16 sugiere la existencia en ellos de una tendencia general a la producción de ese isotipo de inmunoglobulina. Otra evidencia de que este patrón de respuesta es frecuente en pacientes alérgicos al enfrentarse a antígenos no alergénicos, son los resultados obtenidos cuando se evaluó la respuesta a la tuberculina en niños atópicos inmunizados con BCG. En ellos se demostró una fuerte asociación inversa entre los niveles de IgE séricos y el diámetro de lectura de la prueba de hipersensibilidad retardada, así como entre esta última y la gravedad de los síntomas alérgicos a cualquier edad; además de la conversión de respondedores a la tuberculina hacia no respondedores y viceversa, de acuerdo con la mejoría o el empeoramiento de los síntomas.16 Podría pensarse entonces que en los niños asmáticos incluidos en la muestra se produjo una respuesta de anti-AgsHB a predominio de IgE, anticuerpos que no pudieron detectarse, bien porque por su citofilia salieron de la circulación para unirse a los mastocitos o bien por ser de menor afinidad y por tanto no detectados en métodos inmunoenzimáticos que requieren de uniones fuertes en los inmunocomplejos. Estos resultados obligan a realizar estudios controlados en poblaciones de asmáticos, bien sea en niños ya vacunados con un diagnóstico de certeza de asma bronquial, o en adultos sin marcadores de infección viral (susceptibles); en los cuales pueda evaluarse la respuesta a la inmunización de manera prospectiva en relación con la gravedad de las manifestaciones alérgicas y con los fármacos que se emplean para el tratamiento de estas enfermedades.
En lo que respecta a la caída del anti-AgsHB, si bien en los asmáticos se encontraron valores inferiores al estimar la razón entre las medias geométricas de los diferentes grupos, no podemos aseverar que la cinética de desaparición de los anticuerpos sea en ellos más lenta, por la ausencia de significación al comparar los valores encontrados en los asmáticos y los no asmáticos. Tal vez la realización de un estudio longitudinal logre un mejor ajuste en los resultados y permita aclarar este aspecto.
De acuerdo con la persistencia de anti-AgsHB 30 meses después de terminado el esquema de vacunación, se puede inferir que no se requiere dosis de refuerzo en ese momento, y posiblemente tampoco a los 5 años como se ha sugerido en ocasiones; si tenemos en cuenta las elevadas concentraciones detectadas y la tendencia más lenta a su disminución en esta fase, resultados que coinciden con los hallazgos de otros investigadores17 para 4 años después de terminado el esquema de 3 dosis. Se ha reportado que en un estudio de persistencia de anti-AgsHB en niños de madres infectadas por VHB, 11 % no tenía anticuerpos detectables en el suero a los 5 años de seguimiento pos-vacunal, pero ninguno infectó y además, después de ponerles un refuerzo vacunal tuvieron una respuesta elevada de anti-AgsHB. Esto evidenció que la memoria inmunológica había persistido después de la desaparición de los anticuerpos en el suero.18 Por lo tanto, la ausencia de anticuerpos después de montada una buena respuesta no indica ausencia de protección ante una posible infección por el VHB, ni impide que durante el período de incubación de ésta se pueda organizar una fuerte respuesta de memoria.13
Los resultados de este estudio en una población abierta en lo que se refiere a inmunogenicidad y efectividad de la vacuna son similares a los reportados en trabajos previos, realizados en Cuba y en otros países donde se comercializa este producto vacunal.19-23 Esto avala su calidad y permite predecir que en la medida en que se amplíe el programa de inmunización a otras edades y grupos de riesgo,24 se darán pasos importantes en el control de la enfermedad.
Se concluye que los porcentajes de seroprotección e hiperrespuesta obtenidos permiten afirmar que la inmunogenicidad de la vacuna Heberbiovac-HB evaluada en un estudio abierto es similar a la obtenida en los estudios controlados. Las concentraciones de anti-AgsHB encontradas en los niños después de transcurridos 30 meses de terminado un esquema completo de inmunización son indicadoras de protección prospectiva al menos para 4 ó 5 años, sin que se requieran dosis de refuerzo.
Las medias geométricas de anticuerpos en los niños asmáticos fueron significativamente inferiores a las de los no asmáticos, esto podría evidenciar una desviación de la respuesta inmune hacia un patrón Th 2 frente a este antígeno vacunal, con el requerimiento de estudios controlados de vacunación en poblaciones de asmáticos, para corroborar estos resultados y poderlos explicar.