
Dr. José E. Oliva Linares, Dra. Celia Bosch Salado, Dra. Rosario Carballo Martínez y Dr. José E. Fernández-Britto Rodríguez
Se hizo un breve repaso conceptual de la ética y la bioética médica para encausar un tema de singular importancia: el consentimiento informado ¿Por qué es importante su concepto y su aplicación? En Cuba en esta última década se han incrementado los estudios científicos médicos e investigativos para mejorar la salud de la población y la obtención de nuevos medicamentos. Los ensayos clínicos con pacientes siempre deberán cumplir un basamento ético que permita el respeto a la vida humana, en esta revisión se detalla conceptualmente el ensayo clínico, la hoja de información al paciente y su contenido, el consentimiento informado, sus principios y elementos. La mezcla de todos hará más humano el trabajo científico.
DeCS: ETICA MEDICA; ENSAYOS CLINICOS; INVESTIGACION; BIOETICA; PRINCIPIOS MORALES; CONSENTIMIENTO CONSCIENTE; CONFIDENCIALIDAD.
Aspectos preliminares En las últimas décadas de este siglo que concluyó, la investigación con seres humanos, los trasplantes de corazón, la manipulación del código genético, fecundación in vitro, etc., han suscitado problemas desconocidos hasta ahora.1 La necesidad de dar explicación adecuada y resolverlos de forma lúcida ha hecho aparecer una nueva disciplina, la Bioética, cuyo concepto se establece como: "El estudio sistemático de la conducta humana en el área de las ciencias de la vida y de la salud, examinada a la luz de los principios y valores morales".2 Términos como confidencialidad, el secreto médico, la solicitud del consentimiento del paciente para la participación en ensayos clínicos se entremezclan en esta disciplina que unida a la ética médica, hoy día humanizan aún más el desarrollo de la ciencia.
El basamento legal y ético internacional para la realización de los ensayos clínicos, tiene sus inicios en el juramento hipocrático que en la actualidad ha generado una serie de regulaciones y normas que deben ser cumplidas por todos los técnicos y profesionales de la salud.
Principios de la Bioética
La regulación ética y legal del consentimiento informado en los ensayos clínicos presenta una indudable importancia.3 El desarrollo a la autonomía del paciente debe ser respetado ante todo. Resulta imprescindible que el sujeto otorgue con libertad su consentimiento informado siempre antes de que pueda ser incluido en algún estudio o ensayo clínico. De acuerdo con la bibliografía consultada se debe expresar que el ensayo clínico consultado (ECC)4-6 continúa siendo la mejor herramienta para evaluar la eficacia y seguridad de un nuevo tratamiento. Mucho se ha trabajado en analizar detenidamente los defectos de los primeros diseños, encaminados a ir mejorándolos y en la actualidad el ECC puede ser considerado como el estándar de oro en la investigación clínica. De forma paulatina con la profusión de diferentes temas en el campo investigativo de la Ciencia se han ido desarrollando métodos de evaluación más objetivos, en los cuales se emplea de forma generalizada. Estos son la aleatorización, el enmascaramiento y el correcto análisis estadístico; lo antes citado se considera como los pilares sobre los que descansa la calidad de un ensayo clínico (EC) y los que garantizan la fiabilidad de los resultados obtenidos.7,8
Para la evaluación de los ensayos clínicos (en especial para los que se publican en la actualidad, se recomienda internacionalmente por algunas revistas médicas contar con métodos que ayuden a evaluar de forma rápida y sistemática su calidad, mediante el análisis de los requisitos metodológicos y éticos, necesarios para que puedan ser aceptadas sus conclusiones. De ahí la aparición de los check-list con los diferentes aspectos que debe tener un ensayo clínico para que pueda ser aceptada su publicación. Sin profundizar sobre este tema, pero sin dejar pasarlo por alto, se debe apuntar que en estos últimos años han surgido distintos cuestionarios o check-list4 (anexos 1 y 2).



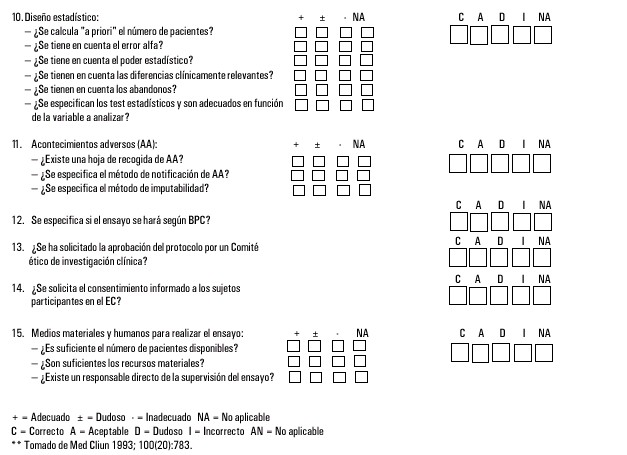
El objetivo fundamental de estos cuestionarios es el de valorar si los métodos utilizados y los resultados obtenidos en la investigación son adecuados para producir información útil, por otra parte los chek-list cumplen una importante labor informativa, aportan información, métodos e hipótesis nuevas y fomentan el sentido crítico con los estudios realizados o los que puedan realizarse en el futuro. Para más detalle se propone la consulta de la bibliografía,9 y en algunos países como España, en estos momentos se hacen estudios en la profundización del análisis detallado de la legibilidad de la información escrita que se le proporciona a los pacientes reclutados para ensayo clínico. Debe aclararse que para la iniciación del ensayo clínico es necesario confeccionar una hoja de información al paciente (HIP), que en el caso de España es la que recoge y contiene todos los aspectos fundamentales del ensayo clínico o investigativo a realizar.10
]]> Características de la hoja de información al pacienteContenido de las hojas de información al paciente
Consentimiento informado
]]> Descripción y aspectos fundamentalesSegún la presente revisión se plantea que en la edición de 1984 del Manual de Ética del Colegio de Médicos americanos11 se definía:
"El consentimiento informado consiste en la explicación, a un paciente atento y mentalmente competente, de la naturaleza de su enfermedad, así como del balance entre los efectos de la misma y los riesgos y beneficios de los procedimientos terapéuticos recomendados para a continuación solicitarle su aprobación para ser sometido a esos procedimientos. La presentación debe ser comprensible y no sesgada; la colaboración del paciente ser conseguida sin coerción; el médico o especialista no debe sacar partido de su potencial dominancia psicológica sobre el paciente".
Se debe aclarar ante todo que la única forma válida de obtener el consentimiento es mediante una conversación,3 indudablemente es un acto de habla, un acontecimiento de comunicación; el profesional que simplemente crea que por haber obtenido la firma de su paciente en un papel ha cumplido con los requisitos del consentimiento informado, está equivocado.
El formulario impreso ha de ser tenido, por cuanto constituye un magnífico medio de apoyo para la trasmisión de información. En EE.UU. algunos médicos emplean en lugar de formularios, la toma de notas en la misma hoja clínica, otros utilizan grabaciones de las conversaciones mantenidas con sus pacientes acerca de los procedimientos a que van a ser sometidos y en la actualidad se está generalizando el uso de videos para transmitir la información sencilla, clara y estandarizada y a continuación obtener la firma del formulario correspondiente.12
Todo formulario debe constar de 2 partes, una parte de información donde se implicarían los principios de cantidad y calidad de información y una segunda parte de declaraciones y firmas donde deberían reflejarse los principios de voluntariedad y competencia. No se recomienda que por un lado existan hojas informativas equivalentes a la parte de información y otros formularios de consentimiento que consignen tan solo declaraciones y firmas. Es recomendado un único documento, una unidad conceptual, el consentimiento informado. Tan importante es asegurar que el paciente reciba al menos un mínimo de información justa o ampliada si él lo desea, como preocuparse de que emita el consentimiento y firme un papel.
A manera de resumen es necesario dejar claro que el consentimiento informado debe sentar su base sobre el principio de voluntariedad del paciente y siempre tener en cuenta los elementos siguientes:
Red de ensayos clínicos en Cuba
A partir de los años 80 en Cuba se produce una revolución en la generación de medicamentos y productos biotecnológicos entre el interferón, PPG, la vacuna antimeningocóccica y otros.14
Cuba, dentro de su estrategia tuvo que crear y desarrollar a un alto nivel en la industria médico-farmacéutica y biotecnológica y se fue encaminando en todo sentido a mejorar la calidad de estos productos, que posibilitaron alcanzar niveles superiores en el estado de salud de la población y por otra parte todo este trabajo se ha ido convirtiendo en una fuente de ingreso, al comercializarse algunos de los productos antes citados en el nivel internacional. Es justo en ensayos clínicos con estudios multicéntricos que agrupan a gran cantidad de pacientes donde se han llegado a validar estos productos para su comercialización.
En Cuba, a la altura de estos años, el comportamiento de los pacientes paso a paso se va acercando a las tendencias del comportamiento del paciente en un país desarrollado, con respecto a su participación en ensayos clínicos; con la particularidad de que se mantiene la confianza y la seguridad en su médico.
Los comités de revisión y ética de Cuba son multiinstitucionales.15 Esto corresponde con la necesidad de valorar con alta frecuencia ensayos clínicos multicéntricos y con la conveniencia de buscar expertos en determinadas especialidades y aclarar que cada institución mediante su comité de ética institucional puede aprobar la participación o no en el ensayo clínico, independiente de que exista un comité de revisión y ética que lo haya evaluado.16
Hasta aquí todo lo relacionado con el consentimiento informado para la realización de ensayos clínicos. Queda claro que Cuba marchará parejo a todo este trabajo investigativo que en el ámbito internacional cada día trata de perfeccionarse en pos de la contribución de la ciencia cubana e internacional y de la salud del ser humano.
A brief conceptual review of the medical ethics and bioethics was made to deal with a topic of particular importance: the informed consent. Why is its concept and application important? The scientific medical and research studies have increased in Cuba during the last decade in order to improve the health of the population and the obtention of new drugs. The clinical trials with patients should always have an ethical foundation that allows the respect to human life. The clinical trial, the sheet of information given to the patient and its content, the informed consent, its principles and elements are conceptually detailed in this review. The combination of all of them will make scientific work more human.
Subject headings: ETHICS, MEDICAL; CLINICAL TRIALS; RESEARCH; BIOETHICS; MORALS; INFORMED CONSENT; CONFIDENTIALITY.
Recibido: 20 de abril del 2000. Aprobado: 31 de mayo del 2000.
Dr. José E. Oliva Linares. Centro de Investigación y Referencia de Aterosclerosis. Apartado 6493. La Habana, CP 10600, Cuba.