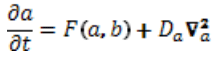
Implantes Scaffolds para regeneración ósea. Materiales, técnicas y modelado mediante sistemas de reacción-difusión
Scaffolds implants for the bone regeneration. Materials, techniques and modeling by means of reaction-diffusion systems
]]>
Marco Antonio Velasco PeñaI; Diego Alexander Garzón AlvaradoII
IMáster en Ciencias. Ingeniero Mecánico, Profesor. Universidad Santo Tomás, Bogotá, Colombia.
IIDoctor en Ciencias (PhD), Máster en Ciencias, Ingeniero Mecánico. Profesor Adjunto. Facultad de ingeniería. Universidad Nacional de Colombia, Bogotá.
RESUMEN
El presente trabajo hace una revisión de los biomateriales usados en implantes óseos y sus aplicaciones clínicas y propone la hipótesis que un sistema reacción-difusión puede ser usado para regular el porcentaje de porosidad, el tamaño de poro y la interconectividad de los mismos en cementos óseos inyectables. En la primera parte se describen los biomateriales en la ingeniería de tejidos óseos, en la segunda se detallan las propiedades mecánicas y geométricas necesarias para el proceso de regeneración ósea, en la tercera se explican los métodos de conformación y aplicación de implantes, en la cuarta se hace una revisión de las técnicas de modelado computacional aplicadas a los procesos de manufactura de implantes y al proceso de regeneración ósea y por último se propone la idea de que un sistema reacción-difusión puede servir para modular la porosidad de un cemento óseo inyectable.
]]>
Palabras clave: scaffold, hueso, cemento óseo, sistemas reacción-difusión.
ABSTRACT
The aim of present paper is to review of biomaterial used in bone implants and its clinical applications and also to propose the hypothesis that a reaction-diffusion system may be used to regulate the porosity percentage, the pore size and their interconnection in injectable bone cement. In the first part are described the biomaterial in the bone tissue engineering, in the second one, are detailed the mechanical and geometric properties needed for the bone regeneration process, in the third one are explained the implant conformation and application methods, in the fourth one we made a review of computation modeling techniques applied to implant manufacture process and the bone regeneration process and finally, we propose the notion that a reaction-diffusion system may to serve to modulate the porosity of a injectable bone cement.
Key words: Scaffold, bone, bone cement, reaction-diffusion system.
INTRODUCCIÓN ]]>
La ingeniería de tejidos usa los principios y métodos de la ingeniería, la biología y la bioquímica para la comprensión de la estructura y la función de los tejidos normales y patológicos de los mamíferos y el consecuente desarrollo de sustitutos biológicos para restaurar, mantener o mejorar su función.1 Los sustitutos hacen uso de tres metodologías que pueden actuar solas o combinadas para recuperar la biofuncionalidad: biomateriales, factores de crecimiento y cultivos celulares. En el campo de los sustitutos óseos es de especial importancia el primer factor, pues los huesos son los elementos estructurales del cuerpo humano y su función se determina principalmente por las propiedades mecánicas del material del que se componen.En Estados Unidos se llevaron a cabo cerca de 500 000 procedimientos con implantes óseos en el año 2000, mientras que la empresa consultora de mercados Kalorama estima que el mercado de implantes óseos en el 2010 será de $ 3 500 millones USD.2 Es evidente que el desarrollo de implantes óseos cerámicos, poliméricos o compuestos en forma de estructuras sólidas porosas (scaffolds, matrices o andamios) o como cementos óseos inyectables es importante.
Los métodos de fabricación de scaffolds buscan controlar la arquitectura de los mismos a diferentes niveles pues tanto la forma externa como la estructura interna son parámetros de diseño de ingeniería necesarios para lograr la regeneración de tejido. Entre dichas características está la forma externa del scaffold, adecuada al sitio donde será colocado y la porosidad. A mayor porosidad e interconectividad mayor facilidad de proliferación y migración celular, además de mayor transporte de nutrientes. El tamaño del poro que para aplicaciones en hueso se estima que debe estar entre 100 y 500 µm. En la actualidad los métodos de fabricación convencionales como el lechado de partículas logra buenas características de porosidad pero no hay control de la forma externa y hay gran variabilidad de las propiedades fisicoquímicas entre cada implante hecho aún con los mismos procedimientos. Por otro lado, los métodos de forma libre o prototipado rápido controlan la forma externa pero aun no tienen la resolución para lograr detalles del orden de micras.
Una tercera alternativa a los implantes óseos la constituyen los cementos óseos inyectables. Estos cementos óseos tienen su aplicación principal en la fijación de prótesis y en el relleno de cavidades óseas como en los tratamientos de kifoplastia. Como ventaja su aplicación requiere procedimientos mínimamente invasivos pero su porosidad es muy baja tanto en porcentaje de porosidad como en tamaño del poro.
Además de hacer una revisión sobre materiales y fabricación scaffolds como sustitutos óseos este artículo presenta una propuesta de modulación del porcentaje de porosidad, tamaño de poro e interconectividad de un cemento óseo a partir de la teoría de reacción-difusión propuesta por Turing hacia 1952. Desde entonces, dicha teoría se aplica en muchos campos de la química y la biología, en especial para modelar patrones en seres vivos. Los sistemas reacción-difusión como modelos matemáticos representan uno o más reactivos distribuidos espacialmente que cambian debido a reacciones químicas y se difunden en dicho espacio. Esto permite una configuración estable en el que las concentraciones de las sustancias que componen el sistema no son uniformes en un dominio y genera singularidades que conforman patrones. Esta capacidad de lograr patrones o distribuciones espaciales es lo que permite pensar en un proceso que permita regular la geometría interna de un implante óseo que se obtiene por cemento óseo inyectable, mientras se desarrolla el proceso de curado de este material en la cavidad o defecto óseo donde se aplica.
DESARROLLO
Biomateriales
Un biomaterial se define como: "un material ideado para interaccionar con los sistemas biológicos para evaluar, tratar, aumentar o substituir cualquier tejido, órgano o función del cuerpo" según la Second Consensus Conference on definitions in Biomaterials (Segunda Conferencia para el Consenso de definiciones en Biomateriales), que tuvo lugar en el Reino Unido en 1992.1 Un área de interés para la ingeniería tisular es el desarrollo de materiales que contribuyan en los procesos de regeneración ósea. Estos son necesarios pues las patologías de los huesos representan una porción importante de las causas de incapacidad física sin importar la condición de las personas. ]]>
En un principio, en el enfoque dado a los implantes óseos solo se buscaba aplicar o desarrollar materiales capaces de soportar los esfuerzos mecánicos que originalmente debía soportar el hueso dañado y que no provocaran una reacción de rechazo por parte del organismo en el que se implantaban. En esta categoría de materiales encontramos metales como los aceros inoxidables y aleaciones de titanio en los sistemas de fijación de huesos que con fracturas. Sin embargo, estos sistemas tienen el inconveniente de que requieren intervenciones quirúrgicas para su extracción luego del tratamiento, lo que implica mayores costos y potencializa la infección. Además, todo material que se inserta en un tejido vivo provoca una respuesta, aunque sea leve, por parte de este.En las últimas décadas se desarrollaron biomateriales para cumplir requerimientos específicos en diferentes aplicaciones clínicas. Autores como Ikada,3 Meyer,4 Estrada5 y Barrere6 describen que los materiales para implantes óseos deben observar las siguientes propiedades:
]]>Biocompatibilidad: integrarse al organismo hospedero sin que haya efectos citotóxicos, genotóxicos o respuesta inmune. Esta es una propiedad fundamental de los biomateriales.
Biodegradabilidad: degradarse (mediante hidrólisis) a tasas que sean lo más cercanas posibles a las tasas de formación de nuevo hueso. Esto constituye un reto a la biocompatilidad debido a que los productos de la degradación no deben ser tóxicos.
Resistencia y compatibilidad mecánica: resistir cargas mecánicas según sea la posición del tejido óseo que reemplaza. Las propiedades mecánicas como el módulo de elasticidad, la resistencia a la tracción, a la fractura, a la fatiga y porcentaje de elongación, entre otros, deben ser lo más cercanas posibles a las del tejido que se reemplaza (compatibilidad mecánica) para evitar la osteopenia que se asocia al uso de implantes óseos o "stress shielding".
Osteoinductividad: promover la fijación de la formación de células específicas del tejido óseo. Esto se logra al reclutar células madre mesenquimales y osteoprogenitoras para que posteriormente proliferen y se diferencien hacia la línea osteogénica.
Osteoconductividad: actuar como soporte estructural en la formación y crecimiento de nuevo hueso. Esta propiedad se combina con la biodegradabilidad pues el material del implante debe ser reabsorbido para dar espacio al nuevo tejido que inicialmente ayudó a soportar.
Radiolucidez: diferenciarse radiográficamente con respecto al tejido donde se implantó.
El desarrollo de la ingeniería de tejidos en el área de biomateriales exhibe materiales que cumplen en mayor o menor grado estas propiedades. Existen familias de materiales con características que les hacen útiles para un rango específico de aplicaciones clínicas por lo que según sea la aplicación se debe seleccionar el biomaterial. Los materiales del scaffold se clasifican según sean metálicos, cerámicos, poliméricos u orgánicos. Puede haber materiales compuestos como cerámico-metal o cerámico-polimérico. También pueden clasificarse en sólidos o hidrogeles (si el contenido de agua es mayor al 30 %).
Orgánicos
Los materiales naturales son los que usan tejido óseo del mismo individuo (autoinjertos), de individuos de la misma especie (aloinjertos) o de especies distintas (xenoinjertos). Son los autoinjertos los que cumplen las tres propiedades de osteoinductividad, osteogenicidad y osteoconductividad deseables en el implante. Su inconveniente radica en el costo y complejidad de los procedimientos quirúrgicos requeridos para obtener el tejido como implante, además de las complicaciones postoperatorias propias de cirugías invasivas. Los aloinjertos requieren de tratamientos como liofilización, irradiación, lavado con ácidos, entre otros para evitar el rechazo por parte del receptor y eliminar posibles infecciones en el tejido a implantar. Los xenoinjertos, como los de hueso bovino también presentan el inconveniente de enfermedades contagiosas.
Cerámicos ]]>
En esta categoría de material cerámicos el más usado es la hidroxiapatita la cual es un fosfato de calcio cristalino (Ca10) (PO4)6 (OH)2). Este material, de tipo cerámico, es el componente mineral principal de los huesos en los mamíferos pues entre el 60 y el 70 % del peso del tejido óseo seco es este compuesto. En dependencia de su fuente puede presentar una estructura muy similar al tejido óseo, lo que provee características de osteoconductividad que permite que el tejido conectivo del hueso que le rodea le penetre y realice un proceso de osificación del material.7,8
Luego de estudiarse profundamente la osteoconductividad, comenzaron a realizarse experimentos para establecer además como es que el material del implante promueve la osteoinductividad. Los estudios de Okumura9 muestran cómo la osteogénesis comienza sobre la superficie de los poros del implante y crece en el espacio disponible en los poros por lo que una adecuada densidad de estos es muy importante. La medición de las propiedades mecánicas del implante in vivo se estudiaron por Trecant,10 quien en 1994 diseñó un estudio que mostró como aunque los implantes de fosfato de calcio tienen bajas propiedades mecánicas al momento de colocarse en el organismo, posteriormente mejoran sus propiedades debido al crecimiento de tejido óseo y gracias a la formación de colágeno y apatita biológica.
Si bien diferentes tipos de fosfatos de calcio o variaciones de la HA pueden tener diferentes grados de biodegradabilidad, Kitsugi y Cols.11 mostraron que no hay cambios significativos en las propiedades osteoinductivas del material. En 1996 Zongjian y Cols.12 realizaron implantes en distintos animales y demostraron que la hidroxiapatita y fosfato de calcio pueden generar procesos de ontogénesis aun cuando el implante no se coloque en tejido óseo, sino de manera intramuscular o subcutánea. La velocidad y forma de la generación de tejido varía según sea el tipo de animal. En perros se mostró el crecimiento de tejido vascular conectivo a los 15 días, alojamiento de células mesenquimales a los 30, generación de matriz ósea a los 45 días y remodelado del tejido óseo a los 60 días.
La reactividad en la superficie del implante se estudiada por Ducheyne y Qiu13 pues afecta la fijación, proliferación, diferenciación y mineralización de las células del tejido óseo. Cerroni y Cols.14 llevaron a cabo estudios con hidroxiapatitas sintéticas y expusieron cómo se generaba el tejido óseo en los poros de la cerámica sintética.
Polímeros
En el caso de los polímeros reabsorbibles las investigaciones se centran en los derivados del ácido poliglicólico (PGA) y del ácido poliláctico (PLA). El primer uso de los mismos se reportó en 1960 con el desarrollo de las suturas biodegradables. De los anteriores el que recibe mayor atención es el PLA, polímero termoplástico, amorfo y semicristalino, pues aparte de su aplicación en suturas también se estudia su papel en la liberación controlada de fármacos e implantes óseos reabsorbibles. Hasegawa y Cols.15 comprobó que la velocidad de degradación de los implantes se relaciona con el sitio en donde es implantado, pues las cargas mecánicas que debe soportar el tejido influyen en la cantidad formada de este.
]]>
La revisión bibliográfica muestra en los últimos años una fuerte tendencia en el desarrollo de scaffolds hechos de materiales compuestos cerámico/polímero. Esto se debe a que cerámicos como los fosfatos de calcio tienen excelentes propiedades osteoinductivas pero una baja degradabilidad, baja resistencia mecánica y dificultad en sus procesos de conformación para controlar las características físicas y geométricas requeridas del scaffold. Por otro lado, los polímeros como el ácido poliláctico exhiben baja osteoinductividad pero mejores propiedades mecánicas y de degradabilidad, además de que se pueden conformar mediante varios procesos que permiten controlar mejor sus características geométricas. El desarrollo de compuestos cerámico/polímero permite obtener un material biodegradable, de buena resistencia mecánica, osteoinductivo, osteoconductor y conformable al combinar las propiedades de los materiales base que lo componen como se ve en la tabla 1. Un resumen de los biomateriales y sus aplicaciones se describe en la tabla 2.
Tabla 2. Materiales para implantes óseos. Extractado y adaptado de Ikada.3
| Composición | Tipo | Origen | Aplicaciones clínicas | Propiedades |
| Fosfatos de calcio Ej.: hidroxiapatita, fosfato tricalcico, fosfato de octacalcio | ]]> Cerámico | Sintético | Regeneración ósea, de sitios sin carga mecánica, relleno de defectos óseos (cementos, gránulos, recubrimientos) | Adhesión de tejido óseo (bioactividad), biodegradable, tasa de degradación variable |
| Fosfatos de calcio base silício (biovidrios) | Vidrios cerámicos | Sintético | Regeneración ósea, de sitios sin carga mecánica, relleno de defectos óseos (gránulos, recubrimientos) | Adhesión de tejido óseo (bioactividad), biodegradable |
| Alumina (óxido de aluminio) | ]]> Cerámico | Sintético | Reemplazo de articulaciones (rodilla, hombro) | Alta resistencia a la tensión, resistencia a la fatiga, sin adhesión de tejido óseo, alta resistencia a la fatiga, baja fricción |
| Titanio y sus aleaciones | Metal | Sintético | Reemplazo de hueso en sitios con carga mecánica. Prótesis dentales o de cadera, vertebras | Adhesión de tejido óseo (bioactividad) en algunos casos. Resistente a la corrosión. Alta resistencia mecánica |
| Acero inoxidable, aleaciones de cobalto y cromo | ]]> Metal | Sintético | Reemplazo de hueso en sitios con carga mecánica, prótesis dentales y de cadera, vértebras y fijaciones | Corrosión a largo plazo |
| Polimetilmetacrilato | Polímero | Sintético | Reemplazo de hueso en zonas con carga mecánica, relleno de defectos óseos (cemento óseo). Fijación de prótesis de cadera y vertebroplastia | No degradable |
| Poliesteres como el ácido polilactico, ácido poliglicólico, policaprolactona y poliuretano. | ]]> Polímero | Sintético | Fijación degradable de hueso, hilo de sutura, relleno de defectos óseos, regeneración tejido blando y liberación controlada de fármacos | La tasa de degradación y las propiedades mecánicas se pueden controlar variando su peso molecular |
| Polietileno de ultra alto peso molecular | Polímero | Sintético | Componente de prótesis articulares en la zona de movimiento relativo (junta) | Capacidad de lubricación |
| Tereftalato de polietileno | ]]> Polímero | Sintético | Cemento y relleno de defectos óseos. | La tasa de degradación y las propiedades mecánicas se pueden controlar variando su peso molecular. Bioactivo |
| Polietilenglicol | Polímero | Sintético | Excipiente en fármacos y alimentos. Reparación de tejidos duros y blandos | Gel acuoso inyectable y degradable |
| Coral | ]]> Mineral | Natural (animal) | Relleno de defectos óseos | Alta interconexión, biodegradable |
| Matriz ósea desmineralizada | Proteína | Natural (humano) | Relleno de defectos, regeneración de cartílago | Biodegradable, fuente natural de proteínas osteoinductivas (BMPs) |
| Colágeno | ]]> Proteína | Natural (bovino) | Reparación de tejidos duros y blandos | Biodegradable |
En 1999, las bondades del uso de compuestos de HA y ácido poliláctico se muestran en el estudio de Shikinami17 quien realiza compuestos de estos materiales que son conformados por presión y luego maquinados. Los materiales obtenidos muestran propiedades mecánicas cercanas a las del hueso cortical además de reabsorbibilidad, bioactividad y osteoconductividad. En 2004 Ignjatovic y Uskokovic18 desarrollaron compuestos de HA y acido poliláctico que conformaron por presión en caliente. Al variar la presión del proceso se obtuvo diferentes grados de porosidad en los materiales que se implantaron en ratones, con buena biocompatibilidad y adhesión del tejido al implante. También los efectos de los procesos de esterilización de ácido poliláctico fueron estudiados por Weir y Cols.19 pues cambios en la cristalinidad y el peso molecular que se generan por los procesos de este tipo alteran de manera importante las propiedades mecánicas del material polimérico.
Manufactura de scaffolds
Los procesos de fabricación de scaffolds para tejido óseo buscan controlar la arquitectura de los mismos a diferentes niveles pues tanto la forma externa como la estructura interna son parámetros de diseño de ingeniería necesarios para cumplir los requerimientos clínicos especificados en la primera sección. La arquitectura tiene diferentes propiedades y características según sea la dimensión de un elemento del scaffold. Para describirla se consideran tres escalas básicas que se describen a continuación: ]]>
La macroescala-mesoescala describe la geometría que se mide en mm. Entre sus características están la forma externa del scaffold según el sitio donde será colocado, las propiedades mecánicas, la densidad y la porosidad: como porcentaje de volumen del scaffold que es vacio. A mayor porosidad mayor facilidad de proliferación y migración celular además de mayor transporte de nutrientes.
La microescala: está compuesta por características del orden de µm como: tamaño del poro, interconexión de poros y degradabilidad.
La nanoescala: características en nm, trata de factores como: topología de la superficie de los poros y la fisicoquímica superficial.
Diversos métodos de manufactura se usan para lograr propiedades determinadas a diferentes escalas. Estos métodos se clasifican en convencionales y de prototipado rápido. Los convencionales hacen uso de fenómenos físicos-químicos para lograr estructura internas con un tamaño de poro de entre 100-500 µm mientras logran porosidades hasta del 90 %, tienen como desventaja que la estructura interna está compuesta por trabéculas dispuestas aleatoriamente, el espesor de los scaffolds que se obtienen alcanza hasta unos 8 mm y hay gran variabilidad en propiedades físicas como la permeabilidad en scaffolds hechos de la misma manera. Por su parte, los métodos de prototipado rápido (RP), también llamados modelado de forma libre (SFF), logran scaffolds de mayor tamaño y con estructuras orientadas pero no logran porosidades elevadas ni poros de pequeño tamaño. Un listado de las técnicas de manufactura de scaffold se da en la tabla 3.
]]> Modelamiento computacional de scaffolds
En cuanto a modelamiento de los procesos de regeneración ósea, se ve que en la última década se desarrolló un trabajo tendiente a caracterizar el comportamiento del scaffolds según sea el material y geometría del mismo. Una revisión hecha por Sengers y Cols.20 muestra que las principales áreas de estudio son:
Transporte de nutrientes, proliferación y la síntesis de matriz extra celular (ECM): esta área trata sobre el metabolismo de nutrientes, transporte y utilización, la cinética de formación de la ECM, la proliferación celular y las limitaciones de nutrientes, las interacciones mecánicas y el crecimiento volumétrico y la proliferación y diferenciación de células madre.
Adhesión y migración celular: se considera la colonización de scaffolds, el medio en que se implanta y la diferenciación celular, la movilidad y migración celular, se consideran las interacciones entre las células y el scaffold como las de tipo mecánico.
Formación de colonias: ya sea mediante modelos continuos o de autómatas celulares.
Estructura del scaffold y la adaptación del tejido: se simula el material de los scaffolds, el transporte de sustancias y el tamaño de los poros, la arquitectura de los scaffolds. La técnica de análisis predominante para esto es el análisis por elementos finitos (FEM). Por último también se estudia la diferenciación de tejidos y la remodelación además de la migración de células en superficies del scaffold.
]]> A continuación se consideran algunos trabajos hechos en las áreas mencionadas. Adachi y Cols.21 en su estudio proponen que para el cumplimiento de los requisitos de diseño, la elección del material del scaffold y su microestructura es muy importante. La resistencia mecánica y la permeabilidad están en función de estas y otras variables. La microestructura también afecta el proceso de regeneración ósea a lo largo del tiempo. Es por esto que analiza el scaffold a nivel de microescala (una celda cúbica porosa) para proponer una estructura metodológica para el diseño de scaffolds con aplicaciones clínicas.
Liu y Cols.22 usa el algoritmo de diferenciación de tejido por regulación mecánica con algunas variaciones con respecto al modelo original propuesto por Lacroix. Frente a otros modelos de crecimiento de tejido óseo este distingue el tipo de tejido que crece (conectivo, cartilaginoso u óseo según sea el esfuerzo al que esté sometido el tejido y a los movimientos que ocurren sobre su superficie. Esto ayuda a comprender los resultados experimentales que otros modelos no predijeron. El modelo se basa en la teoría mecanoestática de Frost. En esta teoría el hueso de adapta según sea el esfuerzo al que está sometido o su deformación. Se demuestra que el estímulo genera una mineralización del hueso que a su vez modifica el módulo elástico del mismo.
Sanz-Herrera y Cols.23 modelan in-silico el efecto que el porcentaje de porosidad, tamaño del poro, rigidez inicial del material y cantidad de células cultivadas tiene en el módulo de elasticidad, cinética de remodelamiento y crecimiento de tejido dentro de un scaffold. Se muestra que el porcentaje de porosidad es factor que afecta de manera importante los procesos de flujo en el scaffold así como las propiedades mecánicas del mismo. Porosidades del 75 al 90 % muestran ser las mejores para facilitar la proliferación celular. El tamaño del poro afecta los procesos de velocidad de migración celular. También es importante por afectar la difusión de nutrientes y evacuación de desechos del metabolismo celular. Se encuentra que poros de más de 100 µm son recomendables. También se concluye que la rigidez del material afecta los procesos de remodelación ósea pues zonas con poca deformación muestran reabsorción.
Ruimerman y Cols.24 Hacen una revisión de las teorías sobre adaptación ósea. Muestran que en general todas las teorías propuestas mencionan que la densidad ósea varía por la acción de variables de tipo mecánico debido a la aplicación de cargas externas. Afirman que algunos de los mecanismos o factores más relevantes del proceso de remodelación ya fueron identificados pero aun falta trabajo por realizar pues los modelos existentes dejan de lado aspectos importantes desde el punto de vista biológico.
Milan y Cols.25 presentaron el modelamiento de un scaffold hecho de polímero de ácido poliláctico (PLA) y fosfato de calcio, para ello emplearon las técnicas de FEM y CFD para simular las condiciones de un birreactor en donde está sometido a la acción de un medio de cultivo. Las cargas que se aplican son compresivas y variables pues se relacionan con las condiciones reales de carga de los huesos en mamíferos. Frente a otros modelos tiene como particularidad que la malla o modelo geométrico se realiza con base en la reconstrucción 3D de un scaffold real. Se obtuvo que la compresión dinámica es un método que permite la estimulación de la proliferación celular que podría funcionar mejor que las cargas estáticas y frente a la perfusión tiene la ventaja de estimular áreas más amplias del scaffold.
Galbusera y Cols.26 presenta el modelamiento numérico del comportamiento de un scaffold de hidroxyapatita portador de fármacos. El implante fue probado in-silico en diferentes posiciones dentro de un femur humano. Se comprobó la resistencia mecánica (según el criterio de falla de Tsai-Wu para materiales cerámicos) y la máxima porosidad del scaffold para la cual no ocurre la falla. Se probó el riesgo de desmineralización por blindaje de esfuerzo (en inglés: stress-shielding) y se modeló la cinética de liberación de la droga.
Sistemas de reacción-difusión en biología
La organización o estructura de los tejidos es un aspecto de interés para la mecanobiología. Se tiene por consenso que los mecanismos de organización de un tejido responden esencialmente a estímulos físicos y químicos. En el tejido óseo se identificada un fenómeno de remodelación ósea donde la mineralización del hueso es secundaria a estímulos mecánicos de esfuerzo y deformación, así como a estímulos de hormonas como cuya inestabilididad puede ocasionar procesos como la osteoporosis. Hay que notar que existen múltiples mecanismos que afectan la forma y estructura del tejido óseo por lo que un área de trabajo en la biología computacional es la determinación mediante simulación de los procesos dominantes y la validez de las suposiciones en que se basan los modelos de dichos procesos. ]]>
Dentro de los mecanismos químicos que se estudian están los sistemas de reacción-difusión donde uno o más químicos, llamados morfogeneradores, se difunden en un espacio reaccionando entre sí hasta que un patrón estable de concentraciones químicas es alcanzado. A su vez, dichas concentraciones actúan como un estímulo o señal que activa procesos celulares como la diferenciación o proliferación e influye de esta manera en la organización tisular como lo muestra el trabajo de Garzón27 sobre osificación endocondral.Un sistema reacción-difusión básico se compone de dos sustancias a y b que se difunden en el espacio a diferente velocidad y reaccionan entre sí. En un espacio unidimensional la forma general de un sistema reacción-difusión puede ser como aparece en la siguiente ecuación:
(1)
(2)
La ecuación expresa que la concentración de la sustancia a en un tiempo dado depende de una función F que depende de las concentraciones de a y b más la difusión de a desde la vecindad. La constante Da mide la velocidad de difusión de a mientras que el laplaciano describe la concentración de a en un punto con respecto a la concentración de la misma sustancia en la vecindad; así, si la concentración de a en la vecindad de un punto es mayor que en el punto el laplaciano es positivo y la difusión se da hacia el punto mientras que si la concentración es menor en la vecindad el laplaciano es negativo y la difusión se da hacia la vecindad. La formación de patrones en los sistemas reacción difusión ocurre si una variación de las concentraciones iniciales de las sustancias hacen que el sistema, inicialmente inestable, alcance un estado estable en el que la concentración de las sustancias reactivas o los morfogeneradores varíen en el espacio.
La figura 1 muestra un patrón de Turing generado en un espacio bidimensional. Nótese que la sustancia a toma la forma de puntos. En este sistema hay altas concentraciones de b donde la concentración de a es baja. A la sustancia b se le llama inhibidor por que altos valores de b en un punto evitan que otros puntos con altas concentraciones de b se formen alrededor. En un sistema reacción-difusión de dos sustancias el inhibidor es aquella sustancia que se difunde más rápidamente. Hay que notar que existen otros sistemas que pueden tener más reactivos con los que se obtienen distintos patrones de tal manera que se puede variar la geometría resultante. En la figura 2 se compara el hueso esponjoso humano, el coral y un patrón que se obtuvo mediante un sistema reacción-difusión que se inspiró en el trabajo de Turing, donde se puede notar cierta similitud entre el patrón que se genera y la estructura de los tejidos mineralizados. ]]>
La ingeniería de tejidos tiene el reto de desarrollar scaffolds que cumplan la funcionalidad del hueso e imite sus propiedades y proporcione un soporte temporal que ayude al proceso de regeneración ósea. Existen muchas alternativas de materiales, técnicas de procesamiento y uso en combinación con otras técnicas de ingeniería de tejidos. Esta investigación permite entender los procesos biológicos, físicos y químicos y cuáles son sus mecanismos dominantes para así poder hacer un adecuado desarrollo y selección de materiales y técnicas de fabricación de scaffolds para obtener implantes que sean sustitutos óseos útiles en aplicaciones clínicas.
REFERENCIAS BIBLIOGRAFICAS
1. Gil HB, Ginebra TD, Planell NI. Biomateriales. En ELISAVA TdD. 2008. Disponible en http://tdd.elisava.net/coleccion/20/gil_ginebra_planell-es
2. Kalorama information. Dental Implant and Bone Graft Markets to Approach $ 3.5 Billion in 2010. Disponible en http://www.medicalnewstoday.com/articles/29693.php
3. Ikada DE. Challenges in tissue engineering. En Journal of The Royal Society Interface. 01/11/2006;3(10):589-601
4. Meyer U, Meyer TH, Handschel J, Wiesmann HP. Fundamentals of tissue engineering and regenerative medicine. New York: Springer; 2009.
5. Garzón AA. Ingeniería de tejido óseo: Consideraciones Básicas. Revista EIA. 2006;5:93-100. ISSN 1794-1237.
6. Barrère GU, et al. Advanced biomaterials for skeletal tissue regeneration: Instructive and smart functions. J Materials Science and Engineering. 2008;59:38-71.
7. Groot KD. Bioceramics consisting of calcium phosphate salts. Biomaterials. 1980;1,2:34-41.
8. Christel PAT, Klein JMA, Blieck-Hogemrst JGC, Groot KD. Studies of the solubility of different calcium phosphate ceramic particles in vitro. Biomaterials. 1990;10,4:223-28.
9. Okumura M, Ohgushi H, Tamai S. Bonding osteogénesis in coralline hydroxyapatite combined with bone marrow cells. Biomaterials. 1991;11,2:56-65.
10. M. Trécant, J. Delécrin, J. Royer, E. Goyenvalle, G. Daculsi. Mechanical changes in macro-porous calcium phosphate ceramics after implantation in bone. Clinical Materials. 1994;15,3:22-12.
11. Kitsugi T, Yamamuro T, Nakamura T, Oka M. Transmission electron microscopy observations at the interface of bone and four types of calcium phosphate ceramics with different calcium/phosphorus molar ratios. Biomaterials. 1995;16,3:12-22.
12. Yang Z, Yuan H, Tong W, Zou P, Chen W, Zhang X. Osteogenesis in extraskeletally implanted porous calcium phosphate ceramics: variability among different kinds of animals. Biomaterials. 1996;17,1:30-9.
13. Qiu QD. Bioactive ceramic: the effect of surface reactivity on bone formation and bone cell function. Biomaterials. 1999;20:45-52.
14. Cerroni GY, et al. Growth of osteoblast-like cells on porous hydroxyapatite ceramics: an in vitro study. Biomolecular engineering. 2002;12,2:56-76.
15. Hasegawa S, Ishii S, Tamura J, Furukawa T, Neo M, Matsusue Y, et al. A 5-7 year in vivo study of high-strength hydroxyapatite/poly (l-lactide) composite rods for the internal fixation of bone fractures. Biomaterials. 2006;27,3:167-77.
16. Elisseeff MY. Scaffolding in tissue engineering. LA: CRC Press Taylor & Francis Group; 2006.
17. Shikinami Y, Okuno M. Bioresorbable devices made of forged composites of hydroxyapatite particles and poly-a-lactide: part I. Basic characteristics. Biomaterials. 1999;20:53-62.
18. Ignjatovic N, Uskokovic D. Synthesis and application of hydroxyapatite/polylactide composite biomaterial. Applied Surface Science. 2004;9,1:19-25.
19. Weir NA, Buchanan FJ, Orr JF, Farrar DF, Boyd AE. Processing, annealing and sterilisation of poly lactide. Biomaterials. 2004;25,1:45-52.
20. Sengers BG, Taylor M, Please CP, Oreffo ROC. Computational modelling of cell spreading and tissue regeneration in porous scaffolds. Biomaterials. 2007;28,10:1926-40.
21. Adachi T, Osako Y, Tanaka M, Hojo M, Hollister SJ. Framework for optimal design of porous scaffold microstructure by computational simulation of bone regeneration. Biomaterials. 2006;27:3964-72
22. Liu X, Niebur GL. Bone ingrowth into a porous coated implant predicted by a mechano-regulatory tissue differentiation algorithm. Biomechanics and Modeling in Mechanobiology. 2008;7,4:335-44.
23. Sanz-Herrera JA, Garcia-Aznar JM, Doblare M. On scaffold designing for bone regeneration: a computational multiscale approach. Acta Biomateriales. 2009;5:219-29.
24. Ruimerman R, Huiskes R. Development of a unifying theory for mechanical adaptation and maintenance of trabecular bone. Theoretical Issues in Ergonomics Science. 2005;6,3-4:225-38.
25. Milan JL, Planell JA, Lacroix D. Computational modelling of the mechanical environment of osteogénesis within a polylactic acid_calcium phosphate glass scaffold. Biomaterials. 2009;30:4219-26.
26. Galbusera F, Bertolazzi L, Balossino R, Dubini G. Combined computational study of mechanical behaviour and drug delivery from a porous, hydroxyapatite-based bone graft. Biomechanics and Modeling in Mechanobiology. 2009;8:209-16.
27. Garzón-Alvarado DA, García-Aznar JM, Doblaré M. Appearance and location of secondary ossification centres may be explained by a reaction-diffusion mechanism. Computers in Biology and Medicine. 2009;39:554-61.
28. Deutsch A, Dormann S. Cellular automaton modeling of biological pattern formation: characterization, applications, and analysis. Birkhäuser. 2005;26:334.
29. Ferrer LA, Vergara PS, Oquendo E. Hidroxiapatita como sustituto del tejido óseo. Revista Electrónica de Portales Médicos. 2008. Disponible en http://www.portalesmedicos.com/publicaciones/articles/1054/1/Hidroxiapatita-como-sustituto-del-tejido-oseo
Recibido: 4 de noviembre de 2009.
Aprobado: 30 de noviembre de 2009. ]]>
Prof. Diego Alexander Garzón-Alvarado. Facultad Ingeniería. Universidad Nacional de Colombia-Bogotá. Email: dagarzona@bt.unal.edu.co ]]>