Validación de técnica inmunoquímica para detección de sangre oculta en heces
Validation of an immunochemical technique for the detection of fecal occult blood
Dra. MSc. Olga Marina Hano García, Dra. Mavié Castellanos Gutiérrez, Dr. Luis Calzadilla Bertot, Dr. MSc. Oscar Manuel Villa Jiménez
Instituto de Gastroenterología.
]]>
RESUMEN
Antecedentes: el cáncer colorrectal es prevenible y responde de manera efectiva al tratamiento cuando se diagnostica en etapas tempranas. La determinación de sangre oculta en heces es un método usado para el cribado de este en etapas precoces y de su lesión precursora, el adenoma. ,
Objetivos: 1) determinar la validez y reproducibilidad del test inmunoquímico RapiLat-Hemo en el diagnóstico de cáncer colorrectal y adenomas y comparar con el reactivo de referencia (SPIN-FOB). 2) describir los hallazgos endoscópicos más frecuentes en pacientes con sangre oculta en heces positiva, 3) describir la localización del cáncer colorrectal en los pacientes con test inmunoquímico RapiLat-Hemo positivo.
Métodos: se realizó un estudio de validación de un nuevo test inmunoquímico cubano (RapiLat-Hemo), para detectar SOH, incluyendo a 161 pacientes atendidos en consulta de colon, del Instituto de Gastroenterología de la Habana, en el período 2008-2010, con indicación de colonoscopia, quienes reunieron los criterios de inclusión. A todos los pacientes se les realizó determinación de SOH (RapiLat-Hemo), y se correlacionaron estos resultados con los del reactivo de referencia y la colonoscopia.
Resultados: predominó sexo femenino y ≤ 60 años de edad. Se obtuvo una sensibilidad de la prueba para identificar a pacientes con CCR de 88,2% y una especificidad de 92,4 %; una sensibilidad de 60,0 % para pacientes con adenomas ≥10 mm y una especificidad de 85,3 %.
Conclusiones: el test demostró validez y reproducibilidad adecuadas en el diagnóstico de cáncer colorrectal y adenomas ≥ 10 mm. Hubo concordancia con el reactivo de referencia (SPIN-FOB). Los hallazgos endoscópicos más frecuentes fueron: pólipos, cáncer colorrectal, y divertículos. La localización más frecuente del cáncer colorrectal en pacientes con sangre oculta en heces positiva fue hacia segmentos más distales del colon.
Palabras clave: sangre oculta en heces, colonoscopia, cáncer, colon, validación, sensibilidad, especificidad.
ABSTRACT
Background: colorectal cancer is preventable and responds effectively to treatment when diagnosed at an early stage. Determination of fecal occult blood is a method used to screen for early colorectal cancer and its precursor lesion, the adenoma.
Objectives: 1) determine the validity and reproducibility of the RapiLat-Hemo immunochemical test to diagnose colorectal cancer and adenomas, and compare it with the reference reagent (SPIN-FOB), 2) describe the most frequent endoscopic findings in patients with positive fecal occult blood, 3) describe the location of colorectal cancer in patients with positive RapiLat-Hemo immunochemical tests.
Methods: A validation study was conducted of a new Cuban immunochemical test (RapiLat-Hemo) to detect FOB. The study sample was composed of 161 patients attending colon consultation at the Institute of Gastroenterology of Havana in the period 2008-2010 who were undergoing colonoscopy and met the inclusion criteria. All patients underwent FOB determination (RapiLat-Hemo), and results were correlated with those of the reference reagent and colonoscopy.
Results: There was a predominance of the female sex and the ≤ 60 age group. The test for detection of colorectal cancer had a sensitivity of 88.2% and a specificity of 92.4%. For detection of ≥10 mm adenomas, sensitivity was 60.0% and specificity 85.3%.
Conclusions: The test showed adequate validity and reproducibility for the diagnosis of colorectal cancer and ≥ 10 mm adenomas. There was concordance with the reference reagent (SPIN-FOB). The most common endoscopic findings were polyps, colorectal cancer and diverticula. The most common colorectal cancer location in patients with positive fecal occult blood was the most distal segments of the colon.
INTRODUCCION
El cáncer colorrectal (CCR) es un problema mundial. El número de casos aumentará en las próximas dos décadas como resultado del envejecimiento y la expansión de las poblaciones, tanto en los países desarrollados como en los países en desarrollo. Es la segunda causa en frecuencia de mortalidad por cáncer entre hombres y mujeres.1-4 La mayoría de los CCR aparecen a partir de adenomas esporádicos y unos pocos, a partir de síndromes genéticos de poliposis o enfermedad inflamatoria intestinal (EII).2
En Cuba, los tumores malignos han sido la segunda causa de mortalidad anual desde hace varias décadas; se ha observado un incremento progresivo, que alcanzó en el 2007 la cifra de 20 360 defunciones.5
La mortalidad por CCR en Cuba en 1980 fue de 722 casos, 6,9 % del total de fallecidos por tumores malignos. En el 2003 las defunciones se elevaron por esta causa a 1 568 para el 8,6 % del total de fallecidos. El incremento porcentual entre los años extremos (de los 24 años considerados en un estudio), fue de 25 %, con un aporte dos veces mayor del sexo femenino, con un incremento de la mortalidad en ambas localizaciones (colon y recto) en los últimos años.6
Datos recientes aportados por la Dirección Nacional de Estadísticas de Cuba señalan al CCR en el 2007 como la tercera causa de mortalidad por tumores malignos en nuestro país con 2 032 víctimas, casi 10 % de todas las defunciones por tumores malignos, superado por cáncer del pulmón, en ambos sexos, seguido por el de próstata en el hombre y de mama en la mujer.7
En diversos países se han elaborado programas para realizar pesquisaje en población asintomática para la detección precoz del CCR y lesiones premalignas como los adenomas, con el objetivo de reducir la mortalidad, por lo cual se han elaborado distintas estrategias como la prevención primaria a través de la introducción de hábitos alimentarios adecuados en la población, la realización de ejercicios físicos,8,9 el diagnóstico precoz (pruebas de screening, las cuales se utilizan en el pesquisaje utilizando la detección de sangre oculta en heces [SOH], y el estudio colonoscópico.10-13
Los test de SOH que se usan con mayor frecuencia son los derivados del guayaco (basados en la pseudoperoxidasa). Aunque son prácticos y sencillos, tienen como problema que dada su naturaleza no son específicos para sangre, no gradúan la cantidad del sangrado, ni indican el segmento del tracto digestivo del que proviene. Algunos alimentos o medicamentos pueden afectar los resultados de prueba, por lo cual para disminuir los falsos positivos, el paciente debe evitar tomar al menos 3 días antes, determinados alimentos y medicamentos.14-16
]]> En la actualidad existen tests basados en la detección inmunoquímica de la hemoglobina humana con una alta especificidad para la detección de SOH, estos son recomendados por la mayoría de los estudios para el screening del CCR, y son superiores a los de guayaco, pues no se necesitan restricciones dietéticas ni medicamentosas; son mejor aceptadas por los pacientes y tienen una sensibilidad y especificidad mayores. Por lo cual se utilizan como prueba de primer nivel en el pesquisaje de este cáncer, indicándose estudio endoscópico en los casos con resultado positivo.17-22En la presente investigación se realizó la validación de un test inmunoquímico (RapiLat-Hemo) para la detección de SOH, el cual fue creado por un grupo de investigadores de la Unidad de Desarrollo e Innovación Tecnológica, subordinada a la Empresa de Productos Biológicos (EPB) "Carlos J. Finlay", motivados por las limitaciones técnicas de los métodos químicos utilizados hasta el momento (guayaco) para la detección de SOH en nuestro medio. Los objetivos de este trabajo son: 1) Determinar validez y reproducibilidad del test inmunoquímico RapiLat-Hemo en el diagnóstico de CCR y adenomas. 2) Describir hallazgos endoscópicos más frecuentes en pacientes con SOH positiva 3) Describir localización del CCR en pacientes con test inmunoquímico RapiLat-Hemo positivo.
MÉTODOS
Se realizó un estudio de validación de pruebas diagnósticas, para un nuevo método inmunoquímico cubano para el diagnóstico de SOH, a los pacientes mayores de 18 años, atendidos en la consulta de colon, del Instituto de Gastroenterología (IGE) en el período noviembre 2008 a mayo 2010, que presentaron indicación de realizarse una colonoscopia y estuvieron de acuerdo de participar en la investigación.
La muestra quedó constituida por 161 pacientes adultos, de ellos 119 pacientes tenian ≤60 años de edad, con 84 del sexo femenino y 77 masculinos. Se les realizó previamente determinación de sangre oculta en heces mediante el test inmunoquímico en estudio RapiLat-Hemo (técnica de látex), el cual está diseñado para la determinación cualitativa de hemoglobina humana (Hbh) en heces por aglutinación en lámina.
Determinación de la muestra
Fueron incluidos pacientes que aceptaron voluntariamente participar en la investigación, mayores de 18 años de edad y con indicación clínica de realizarse una colonoscopia procedentes de la consulta de colon. Se excluyeron pacientes con sangramiento rectal macroscópico, con diagnóstico previo de enfermedad inflamatoria intestinal, con cuadro de diarreas disenteriformes (flemas y sangre) y aquellos que tomaban aspirina, antiinflamatorios no esteroideos o anticoagulantes al momento del estudio.
Procedimiento
A estos pacientes se les indicó un test de SOH, para lo cual se les entregó un frasco con una numeración codificada. Dicha muestra se recogió dentro del período de 30 días antes de la preparación para la realización de la colonoscopia. Estas muestras se evaluaron en fresco o fueron almacenadas a -20 ºC en condiciones adecuadas en el laboratorio de investigaciones del IGE, donde se realizó la primera evaluación utilizando el reactivo en estudio (RapiLat-Hemo); por los dos primeros observadores (un observador del IGE y otro de la EPB Finlay), siendo después trasladadas al área de Desarrollo e Innovación Tecnológica de la EPB Finlay donde a dicha muestra se le realizó otra evaluación por un tercer observador. Además en dicho centro se realizó la determinación con el reactivo inmunocromatografico de referencia SPIN-FOB de la firma comercial SPIN-FOB de España, el cual consiste en un inmunotest, el cual muestra una sensibilidad de 50ng hHb/mL de tampón y una especificidad mayor de 99 (e: spinreact@spinreact.com). Una vez recogida la muestra de SOH, se realizó la colonoscopia convencional. Esta constituyó la regla de oro para este estudio de validación. En cuanto a los pólipos se trabajó solamente con adenomas, los cuales se dividieron según su tamaño en menores de 10 mm (<10 mm) y mayores o iguales a 10 mm (≥10 mm). En cuanto al CCR se confirmó histológicamente, incluyéndose todos los casos sin interesar el tipo histológico.
]]> Fundamentación de la técnica de látexEl método se basa en una reacción inmunoquímica donde las partículas de látex sensibilizadas con anticuerpos anti-Hb humana reaccionan con la hemoglobina humana presente en la muestra de heces en forma sensible y específica, produciendo una aglutinación visible macroscópicamente. El test muestra una sensibilidad y especificidad clínicas del 100 % y 99,3 % respectivamente, sensibilidad analítica (límite de detección) de 1 µg/mL y efecto prozona: > 500 µg/L. La técnica de látex, aglutinación en lámina para estos propósitos constituye una de las mejores opciones ya que resulta una técnica rápida y de fácil ejecución, basada en la reacción antígeno-anticuerpo.
Consideraciones éticas
La realización de esta investigación no supuso ningún cambio en las indicaciones para realizar colonoscopia. A todos los pacientes en estudio se les pidió su consentimiento por escrito, explicándoles las características del mismo y los riesgos que conllevaba, así como sus derechos. Este estudio fue conformado de acuerdo a los principios éticos de la Declaración de Helsinki,23 además de ser revisado a priori por el Comité de Ética Médica para los estudios en humanos de esta institución.
Análisis estadístico
Se confeccionó una base de datos automatizada en el sistema Excel 2007. Se determinaron los indicadores de evaluación de una prueba diagnóstica comparando el test de prueba con la colonoscopia (regla de oro) y con un reactivo comercial (SPIN-FOB). Específicamente se determinaron los indicadores para CCR y adenomas. Sensibilidad, especificidad, valor predictivo positivo, valor predictivo negativo, proporción de falsos positivos, proporción de falsos negativos, exactitud. Odds radio diagnóstica, Índice J de Youden (Seguridad diagnóstica), Cociente de probabilidad o razón de verosimilitud, Probabilidad pre-prueba (Prevalencia) La concordancia entre pruebas (RapiLat-Hemo y SPIN-FOB) se evaluó con el Índice de Kappa.
La concordancia entre observadores se evaluó con el Índice de Kappa para más de dos observadores y una variable dicotómica. Se obtuvo el intervalo de confianza por el método de Jackknife. Para la descripción de hallazgos endoscópicos y localización del CCR según resultado de la prueba diagnóstica en validación, se utilizaron medidas descriptivas: frecuencias absolutas y porcentajes. El análisis estadístico se realizó mediante el programa Epidat v3.0.
RESULTADOS
En la tabla 1 se muestran los resultados en cuanto al test inmunoquímico en estudio (RapiLat-Hemo) en relación con el resultado de la colonoscopia, donde de los pacientes 161 pacientes incluidos, 26 presentaron SOH positiva y de estos, todos presentaron alguna patología en la colonoscopia.
]]>
En la tabla 2 se muestran los resultados del RapiLat-Hemo en relación al CCR, donde 17 pacientes presentaron CCR y de estos, 15 tuvieron la SOH positiva. Se obtuvo una sensibilidad de la prueba para identificar a los pacientes con CCR de 88,2 % IC 95 % (65,7 % a 96,7 %) y una especificidad de 92,4 % IC 95 % (86,8 % a 95,7 %).Por lo que demostró una validez y reproducibilidad adecuada para el diagnóstico del CCR.
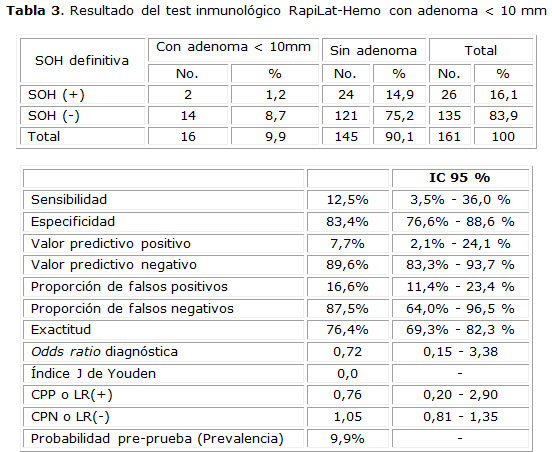
Los adenomas se agruparon según su tamaño. Las tablas 3 y 4 ilustran los resultados del Rapilat-Hemo de acuerdo con este parámetro. Los adenomas ≥10 mm se obtuvieron en 5 pacientes, y de ellos en 3 la SOH resultó positiva.
Se obtuvo una utilidad de la prueba más adecuada para identificar a pacientes con adenomas ≥10 mm de 60,0 % IC 95 % (23,1 % a 88,2 %) Se observó también que la probabilidad de diagnosticar un paciente con adenoma ≥10 mm con la SOH positiva aumenta 4,07 veces IC 95 % (1,81 a 9,14). Por lo que demostró una validez y reproducibilidad adecuada para el diagnóstico de adenomas ≥10 mm.
En la tabla 5 se observa una comparación entre cada reactivo (RapiLat-Hemo y SPIN-FOB), donde se obtuvo 22 pacientes con ambos reactivos positivos. Se halló la concordancia entre pruebas (Índice de Kappa): 0,88 IC 95 % (0,78 a 0,98) la cual resultó estadísticamente significativa. También se halló la concordancia entre tres o más observadores con dos categorías; se obtuvo un índice de Kappa por el método de Jackknife de 0,9536 IC 95 % (0,9007 a 1), lo cual fue estadísticamente significativo.
En la tabla 6 se muestra la localización endoscópica del CCR en pacientes con SOH positiva, donde en 15 pacientes con CCR la localización del mismo predominó hacia los segmentos más distales del colon.
]]>DISCUSIÓN
El CCR es prevenible y responde de manera efectiva al tratamiento cuando se diagnostica en etapas tempranas, por lo que cada día adquieren mayor valor los programas encaminados a la detección temprana del CCR y sus lesiones precursoras.24 Estos pueden producir eliminación de sangre que se puede detectar en heces mucho antes de aparecer síntomas clínicos. Esto ha llevado a la búsqueda de análisis de materiales fecales que permitan una detección temprana y pesquisa del CCR en individuos asintomáticos. El método más común ha sido la detección de sangre oculta en heces utilizándose diferentes test (guayaco e inmunoquímicos), donde la simplicidad de estas pruebas para el paciente varía. El punto de corte óptimo para la sensibilidad en las pruebas inmunoquímicas aún no ha sido validado.2,14 Los test inmunoquímicos utilizan anticuerpos específicos frente a la hemoglobina humana, por lo que sus resultados no están influenciados por factores dietéticos. Su costo es mayor, pero su sensibilidad y especificidad son superiores a los bioquímicos.24
En la literatura internacional se encuentran estudios publicados que demuestran el papel que desempeña la determinación de SOH en la disminución de la mortalidad por CCR.25 En esta investigación se observó un predominio del sexo femenino lo cual concuerda con lo planteado por algunos autores como Torres Vidal 6 que plantea que la mortalidad por CCR ha ido en aumento en Cuba para ambos sexos, con predominio del sexo femenino. A pesar de que en esta investigación no se determinó el predominio del sexo para el CCR, se observó un predominio del sexo femenino, con sintomatología sugestiva de patologías de colon. Estos resultados concuerdan con los reportados por Oort y otros, en un estudio realizado en Amsterdam donde el 56,9 % de las pacientes eran mujeres, así como el realizado en Cuba, en el hospital CIMEQ (2008), donde el 57,7 % de los pacientes correspondió a este sexo.26 En Cuba se observa una sobremortalidad femenina por CCR para todos los años, más marcada a partir de la década de los 90 en que la distancia entre ambos sexos se hace mayor de manera prácticamente permanente con desventaja para las mujeres.9 Resultado diferente, reportado a nivel internacional, donde predomina el sexo masculino.9.13
En esta investigación se obtuvo de manera general, un por ciento bajo de pacientes con SOH positiva (16 %) en relación con otros estudios realizados internacionalmente, lo cual pudiera estar condicionado con el tamaño de la muestra, ya que en ellos se realizó pesquisaje en poblaciones asintomáticas con o sin riesgo, que incluyeron mayor número de pacientes, como el estudio realizado por Greenberg27 que abarcó varios países, donde reunieron un total de 554 pacientes con colonoscopia, y obtuvieron 35,3 % de positividad en la SOH para todas las lesiones encontradas; al igual que Hyun-Soo,28 con 553 pacientes, donde el 25,3 % presentaron SOH positiva y Woo,15 con 85 pacientes reportó resultados superiores a los de la presente investigación con 31,8 % de positividad de la SOH.
La utilización de los tests de SOH se basa en el cribado del CCR, pero también para la detección de su lesión precursora (adenoma). El predominio de la positividad de la SOH para CCR, sobre los adenomas en la investigación no concuerda con lo encontrado en la literatura internacional revisada, donde el por ciento mayor de positividad corresponde a adenomas.27,28 Esta diferencia está en correspondencia al diseño de la investigación, la cual estuvo dirigida a incluir pacientes sintomáticos, por lo cual estos aparecieron como hallazgos endoscópicos.
En cuanto a la sensibilidad y especificidad para CCR, se concuerda con varios estudios internacionales, como el multicéntrico realizado por Greenberg,27 en diferentes universidades de varios países como Estados Unidos, Canadá, Inglaterra, Italia, Alemania y Dinamarca donde compararon dos tests inmunoquímicos (Heme Select y FlesSure OBT) con dos reactivos derivados del guayaco, obteniendo una sensibilidad de 83,3 % y 87,5 % y especificidad de 88,2 % y 86,2 % respectivamente, parámetros que se encuentran por debajo de los obtenidos en esta investigación.
Hyun-Soo Kim,28 obtuvo una sensibilidad del 34,4 %, especificidad del 85,4 % y valores predictivos muy inferiores a los de esta investigación, donde utilizó un reactivo inmunoquímico (i-FOBT). Woo15 en Corea del Sur, realizó la validación de un test inmunoquímico denominado Occul Tech, al compararlo con dos reactivos comerciales, obtuvo una sensibilidad de 83,3 % y especificidad de 75,9 %, discretamente inferior al RapiLat-Hemo. En este mismo estudio se compararon los indicadores del reactivo en validación con dos reactivos comerciales, uno de ellos un reactivo cuantitativo, basado en el método de la aglutinación con látex HM-Jack, con una sensibilidad y especificidad de 50 % y 83,5 % respectivamente, ambos indicadores inferiores en relación con el RapiLat-Hemo. De manera similar, el otro reactivo comercial Instant-View, utilizado mostró indicadores inferiores al RapiLat-Hemo.
Dancourt 29 y otros, en la Universidad de Bourgogne (Francia) compararon un reactivo derivado del guayaco con un inmunoquímico, demostrando que este último tiene una mayor sensibilidad y especificidad para CCR, la cual es similar a la reportada en este estudio. Favennec30 (1992), evaluó la prueba inmunoquímica basada en el método de látex (Hemolex), y obtuvo sensibilidad y especificidad de 70 % y 98 % respectivamente, de manera general, al ser comparada con un reactivo del guayaco. Este reactivo Hemolex al ser comparado con tres reactivos igualmente inmunoquímicos en estudio realizado por Goberts,31 obtuvo valores de 85,7 % y 94,1% respectivamente. Guittet,32 comparó guayaco con un test inmunoquímico; obtuvo para este último, resultados similares a este estudio en cuanto a sensibilidad y especificidad para CCR y adenomas. Castiglione33 utiliza un reactivo inmunoquímico de látex (LAT), y obtiene valores similares a los de este estudio; al comparar el RapiLat-Hemo con el SPIN-FOB se encontró una adecuada concordancia. En la actualidad existen estudios donde se utilizan test inmunoquímicos cuantitativos, los cuales se plantea tienen una eficacia superior,24,34 como el OC-sensor utilizado por Oort, 35 con una sensibilidad de 87,1 % y especificidad de 91,0 %, resultados casi similares al reactivo de látex (RapiLat-Hemo), en la presente investigación.
La prevalencia de pólipos aumenta con la edad que es tal vez el determinante individual más importante, esta se asocia no solo con una mayor tasa de prevalencia, también se correlaciona con una mayor probabilidad de pólipos múltiples, mayor tamaño y adenomas con grados más severos de displasia, de ahí que los programas de pesquisaje vayan dirigidos a población ≥50 años.36 Si bien no hay estudios definitivos, parece ser que la evolución es bastante lenta y requiere más de 10 años, por lo que eliminar adenomas es una estrategia obvia para reducir la incidencia de CCR.37 En cuanto a sensibilidad, especificidad y valores predictivos para los adenomas, este estudio coincide con varios trabajos reportados,27 los cuales, los clasifican por tamaños (<10 mm o ≥10 mm); se observa una mayor eficacia de los reactivos para los adenomas ≥10 mm.
]]> Aunque la prueba de SOH no tiene una buena sensibilidad para detectar adenomas pequeños, sí puede detectar los de mayor tamaño que son precisamente los que tienen más riesgo de malignizar. Greenberg,27 obtuvo una sensibilidad de 37,1 % y 35,9 %; y especificidad de 88,3 % y 85,6 % respectivamente, para todos los adenomas; superiores a los de esta investigación, pero al dividirlos por tamaño encontró que para los ≥10mm aumentó significativamente, lo cual concuerdan con los resultados obtenidos con el RapiLat-Hemo.Hyun-Soo Kim,28 reportó valores inferiores a los resultados en esta investigación, con una sensibilidad para adenomas de 22,9 %, utilizando también un test inmunoquímico (i-FOBT). Woo,15 realizó igualmente la validación del Occul Tech, donde con adenomas >10 mm, obtuvo indicadores inferiores a los del RapiLat-Hemo. Graser,38 en la Universidad de Munich, Alemania, comparó la sensibilidad de los estudios colonoscópicos con los tests de SOH inmunoquímicos, obtuvo una sensibilidad muy similar a esta investigación para adenomas con el test estudiado (32 %).
Haug39 en el Centro médico para el cáncer en Alemania, comparó dos reactivos inmunoquímicos, el inmuno-CARE-C y el FOB advanced, estos mostraron una sensibilidad de 25 % y 27 % y especificidad de 97 % y 93 % respectivamente para adenomas avanzados, definido histológicamente como: adenomas ≥10 mm, vellosos o con displasia de alto grado, cifras superiores a los obtenidos en esta investigación, ya que fueron adenomas avanzados, los cuales tienen mayor probabilidad de sangrar. Dancourt29 y otros, demostraron que el reactivo inmunoquímico tiene una mayor sensibilidad y especificidad, para adenomas avanzados ligeramente superior a lo reportado en este estudio. Tomás Moro,40 en Minnesota, obtuvo valores similares para sensibilidad, especificidad y valores predictivos para el diagnóstico de adenomas.
En cuanto al CCR con SOH negativa, pudiera estar en relación con que estas lesiones suelen sangrar de forma intermitente y de forma no homogénea en las heces, por lo cual una sola determinación no es suficiente, constituyendo quizás un sesgo de esta investigación, donde se recogió sólo una muestra de heces por paciente, lo cual contribuyó a una menor detección de adenomas y CCR con el RapiLat-Hemo.
Con relación a la localización del CCR,12 el 23 % de estas neoplasias afectan el recto, el 10 % unión rectosigmoidea, 25 % sigmoides, 6 % colon descendente, 13 % colon transverso, 8 % colon ascendente y el 15 % el ciego. En este estudio predominó la localización hacia los segmentos más distales del colon, lo que se corresponde con los resultados obtenidos por Yuko Minami,41 donde primaron las neoplasias hacia colon izquierdo con un 45 %. Hechevarría Borrero42 halló igualmente un predominio del cáncer hacia el colon izquierdo con 54 %.
Los resultados obtenidos en esta investigación, donde se encontró una buena sensibilidad y especificidad del RapiLat-Hemo para CCR y adenomas ≥10 mm, con adecuada validez y reproducibilidad diagnóstica demuestran que los tests inmunoquímicos de SOH son una buena opción para el cribado del CCR y su lesión precursora, el adenoma, unido al examen endoscópico, por lo cual recomendamos la inclusión de este método en el cribado de estas lesiones en nuestro medio, sobre todo a nivel de atención primaria de salud.
Agradecimientos
A MSc. Juan Alberto Pérez Carrasco, Dr. C. Mario Álvarez Marcer y MSc. Isabel Giraldino Falero, de la Empresa de producción de Biológicos "Carlos J. Finlay". Área de desarrollo e innovación tecnológica.
]]> REFERENCIAS BIBLIOGRÁFICAS
1. Rex DK, Liangpunsakul S. Detección del cáncer colorrectal. The American College of Gastroenterology. (Consultado junio 2008). Disponible en: http://patients.gi.org/recursos-en-espanol/deteccion-del-cancer-colorectal/
2. Guía de Recomendaciones para la prevención del cáncer colorrectal. Consenso argentino 2004. (Consultado junio 2008). Disponible en: http://www.sacp.org.ar/consenso_argentino_2004.pdf
3. Viñes JJ, Ardanaz E, Aráosla A, Gaminde L. Epidemiología poblacional de cáncer colorrectal: revisión de la causalidad. (Consultado abril 2008). Disponible en: http://www.cfnavarra.es/salud/anales/textos/vol26/n1/salud1a.html
4. Béjar L, Pili M, Díaz V, Ramírez G, López J, Cabanillas JL. Incidence and mortality by colorectal cancer in Spain during 1951-2006 and its relationship with behavioural factors. European Journal of Cancer Prevention. 2009;18:436-44.
5. Cuba. Dirección Nacional de Estadísticas. Anuario estadístico de 2007: Principales causas de muerte de todas las edades. [en línea]. La Habana: MINSAP; 2008. (Consultado mayo 2010). Disponible en: http://bvs.sld.cu/cgibin/wxis/anuario/?IsisScript=anuario/iah.xis&base=anuario&lang=e
6. Torres Vidal RM, Gran Álvarez MA. Impacto del cáncer de colon en la morbilidad de la población cubana,1979-2003. Rev Temas estadísticos de Salud. Dirección Nacional de Estadísticas. MINSAP. 2005;1(1). (Consultado mayo 2008). Disponible en: http://www.sld.cu/galerias/pdf/sitios/dne/ nro1_cancer_colon.pdf
7. MINSAP. Dirección Nacional de Estadísticas. Anuario estadístico de 2007: Mortalidad por algunos tumores malignos según sexo. [en línea]. La Habana: Cuba, 2008 (Consultado marzo 2009). Disponible en: http://bvs.sld.cu/cgibin/wxis/anuario/?IsisScript=anuario/iah.xis&base=anuario&lang=e
8. Marzo-Castillejo M, Bellas-Beceiro B, Nuin-Villanueva M, Cierco-Peguera P, Moreno-Baquerano M, Rubio-Toledano L. Grupo de prevención del cáncer del PAPPS. Actualizaciones 2005. Aten Prim. 2005;36(Supl 2):45-65.
9. Study in The European Journal of cancer Prevention National Bowel Cancer Screening Program. J Med Screen. 2008;15:163-74.
10. Rex DK, Johnson DA, Lieberman DA, Burt RW, Sonnenberg A. Colorectal cancer prevention 2000: screening recommendations of the American College of Gastroenterology. Am J Gastroenterol. 2000;95(4):868-77.
11. Smith RA, Von Eschenbach AC, Wender R, Levin B, Byers T, Rothenberger D. ACS Prostate Cancer Advisory Committee, ACS Colorectal Cancer Advisory Committee, ACS Endometrial Cancer Advisory Committee. American Cancer Society guidelines for the early detection of cancer: update of early detection guidelines for prostate, colorectal, and endometrial cancers. Also: Update 2001-Testing for early lung cancer detection. CA Cancer J Clin. 2001;51:38-75.
12. Asociación Española de Gastroenterología, Sociedad Española de Medicina de Familia y Comunitaria y Centro Cochrane Iberoamericano. Prevención del cáncer colorrectal. Guía de Práctica Clínica. Barcelona, marzo de 2004. (Consultado mayo 2010). Disponible en: http://www.sepd.org
13. Sáenz R, Navarro A. Una proposición de protocolos de diagnóstico y tratamiento para países de Latinoamérica. Cáncer Colorrectal. Reunión de Consenso. 20 de octubre de 2004. Santiago de Chile. (Consultado mayo 2010). Disponible en: http://www.aige.org
14. Ouyang DL, Chen JJ, Getzenberg RH, Schoen RE. Noninvasive testing for colorectal cancer: A review. Am J Gastroenterol. 2005;100(6):1393-403.
15. Woo HY, Mok RS, Park YN, Park DI, Sung IK, Sohn ChI. A prospective study of a new immunochemical fecal occult blood test in Korean patients referred for colonoscopy. Clinical Biochemistry. 2005;38:395-9.
16. Crespil M, Lisi D. Is colorrectal cancer screening by fecal occult blood feasible? Annals of Oncology. 2002;13:47-50.
17. Church TR, Yeazel MW, Jones RM. A randomized trial of direct mailing of fecal occult blood tests to increase colorectal cancer screening. J Natl Cancer Inst. 2004;96:770-80.
18. Ko CW, Dominitz JA, Nguyen TD. Fecal occult blood testing in a general medicine clinic: comparison between guaiac-based and immunochemical based tests. Am J Med. 2003;115:111-4.
19. Imperiale TF. Quantitative immunochemical fecal occult blood tests: is it time to go back to the future? Ann Intern Med. 2007;146:309-11.
20. Morikawa T, Kato J, Yamaji Y, Wada R, Mitsushima T, Shiratori Y. A comparison of the immunochemical fecal occult blood test and total colonoscopy in the asymptomatic population. Gastroenterology. 2005;129:422-8.
21. Bampton PA, Sandford JJ, Cole SR, Smith A, Morcom J, Cadd B, et al. Interval faecal occult blood testing in a colonoscopy based screening programme detects additional pathology. Gut. 2005;54:803-6.
22. Levi Z, Hazazi R, Rozen P, Vilkin A, Waked A, Niv Y. A quantitative immunochemical faecal occult blood test is more efficient for detecting significant colorectal neoplasia than a sensitive guaiac test. Aliment Pharmacol Ther. 2006;23:1359-64.
23. Declaración de Helsinki de la Asamblea Médica Mundial. Principios éticos para las investigaciones médicas en seres humanos. 52a Asamblea General [monografía en Internet]. Escocia: Asamblea Médica Mundial; 2000. (Consultado marzo 2008). Disponible en: http://www.upo.es/general/investigar/otri/otri_docu/pn/Decl_Helsinki.pdf
24. Levi Z, Rozen P, Hazazi R. Sensitivity and specificity of a quantitative immunochemical FOBT for colorectal neoplasia. Ann Intern Med. 2007;146:244-55.
]]>25. McLoughlin RM, Colm AO. Colorectal cancer screening. World J Gastroenterol. 2006;12(42):6747-50.
26. Tusen Y, Chao L, Barroso L, Armas M, Fernández I. Test de sangre oculta y colonoscopia en el diagnóstico del cáncer colorrectal. Rev Investigaciones medicoquirúrgicas. 2009;1(2):5-12.
27. Greenberg PD, Bertario L, Gnauck R, Kronborg O, Hardcastle JD, Epstein MS, et al. A prospective multicenter evaluation of new fecal occult blood tests in patients undergoing colonoscopy. The American Journal of Gastroenterology. 2000;95(5):1331-7.
28. Hyun-Soo K, Kyu Hong K, Jin Heon H, Ki Won C, Jae Woo K, Hye Jung K, et al. Factors affecting the sensitivity or specificity of immunochemical fecal occult blood testing screening for colorectal neoplasia. Gastrointestinal Endoscopy. 2006;63(5):AB214.
29. Dancourt V, Lejeune C, Lepage C, Gailliard MC, Meny B, Faivre J. Immunochemical faecal occult blood tests are superior to guaiac-based tests for the detection of colorectal neoplasms. Eur J Cancer. 2008;44(15):2254-8.
]]>30. Favennec L, Kapel N, Meillet D, Chochillon C, Gobert JG. Detection of occult blood in stools: comparison of three guaiac tests and a latex agglutination test. Ann Biol Clin. 1992;50:311-3.
31. Goberts G. Comparison of two immunochemical methods for faecal occult blood detection. Clin Chem News. 1992;18(6):22-30.
32. Guittet L, Bouvier V, Mariotte N, Vallee JP, Levillain R, Tichet T, et al. Comparison of a guaiac and an immunochemical faecal occult blood test for the detection of colonic lesions according to lesion type and location. British Journal of Cancer. 2009;100:1230-5.
33. Castiglione G, Visioli CB, Ciatto S, Grazzini G, Bonanomi AG, Rubeca T, et al. Sensitivity of latex agglutination faecal occult blood test in the Florence District population-based colorectal cancer screening programme. Br J Cancer. 2007 June 4;96(11):1750-4.
34. Diaz Tasende J, Marín Gabriel C. Cribado del cáncer colorrectal mediante test de sangre oculta en heces. Rev Esp Enferm Dig. 2008;100:315-9.
]]>35. Oort FA, Droste JS, Van der Hulst RW, Van Heukelem HA, Loffeld RJ, Wesdorp IC, et al. Colonoscopy-controlled intra-individual comparisons to screen relevant neoplasia: Faecal immunochemical test vs. Guaiac-based faecal occult blood test. Aliment Pharmacol Ther. 2010;31(3):432-9.
36. Winamer SJ, Zauber AG. Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup. N Engl J Med. 2005;5:329.
37. Roque SF, Navarro LA. Prevención y pesquisa del cáncer colorrectal. Avances en la Gastroenterología en las Américas. Lima, Perú: Ed. Cimagraf; 2005. p. 168.
38. Graser A, Stieber P, Nagel D, Schäfer C, Horst D, Becker CR, et al. Comparison of CT colonography, colonoscopy, sigmoidoscopy and faecal occult blood tests for the detection of advanced adenoma in an average risk population. Gut. 2009;58(2):241-8.
39. Haug U. Immunochemical fecal blood tests differ widely in performance. Ann Intern Med. 2009;150:162-9.
]]>40. Tomás Moros M, García Durán F, Carneros Martín J, Sánchez Prudencio S, Villa Poza J, Ciriza de los Ríos J, et al. Neoplasia avanzada de colon. Estudio comparativo entre pacientes con antecedentes familiares de cáncer colorrectal y la población general. Gastroenterol Hepatol. 2009;32(3):234.
41. Minami Y, Yoshikazu N. Increase of colon and rectal cancer incidence rates in Japan: Trends in incidence rates in Miyagi Prefecture, 1959-1997. Journal of Epidemiology. 2006;16(6):28-35.
42. Hechevarría Borrero P, Meriño T. Características clínicas del cáncer de colon. Estudio de 57 pacientes. MEDISAN. 2003;7(3):4-9. (Consultado febrero 2009). Disponible en: http://bvs.sld.cu/revistas/san/vol7
Recibido: 7 de mayo de 2013.
Aprobado: 22 de mayo de 2013.
]]>
Dra. MSc. Olga Marina Hano García. Lagunas No. 204 entre Lealtad y Perseverancia, Centro Habana. La Habana, Cuba. Teléfono: +537 867-87-66
Correo electrónico: olga.hano@infomed.sld.cu