El cuerpo carotídeo en la homeostasis de la glucosa
The carotid body in glucose homeostasis
Elena Roces Dorronsoro, Mónica Lemus Vidal, Sergio Adrián Montero Cruz
Centro Universitario de Investigaciones Biomédicas. Universidad de Colima. Colima, México.
]]>
RESUMEN
Los cambios en los niveles de glucosa en la sangre periférica o central se detectan por sensores a la glucosa situados en: los núcleos hipotalámicos, el páncreas, el núcleo del tracto solitario, el sistema portal hepático y los receptores del cuerpo carotídeo. El cuerpo carotídeo o glomus caroticum es un órgano quimiosensorial localizado de forma bilateral en la vecindad de la bifurcación de la carótida común. Los cuerpos carotídeos son sensores polimodales, que detectan los niveles de oxígeno, pH, bióxido de carbono, temperatura, osmolaridad, potasio, glucosa e insulina en la sangre que los irriga. El objetivo de esta revisión es describir los trabajos realizados por Ramón Álvarez-Buylla y colaboradores en el Laboratorio de Neuroendocrinología del Centro Universitario de Investigaciones Biomédicas de la Universidad de Colima, y de otros investigadores, relacionados con el estudio de los cuerpos carotídeos en la homeostasis de la glucosa. Los CCs responden a la hipoglucemia a través de la depleción de trifosfato de adenosina, o a cambios en el pH y pO 2, sin depleción de trifosfato de adenosina. Es cada vez más evidente que los CCs juegan un papel fisiológico importante en la homeostasis de este carbohidrato, y que el estrés hipóxico ejerce una influencia tónica en la secreción de diversos neurotrasmisores y hormonas como la arginina-vasopresina, el óxido nítrico, el factor neurotrófico derivado del cerebro, ácido gamma-aminobutírico, glucagón, cortisol y otros, que participan en el procesamiento central de los mecanismos contrarregulatorios en la homeostasis glucémica. Los CCs inician respuestas contrarreguladoras a la hipoglucemia con la participación de la hipófisis, las adrenales, el páncreas y el sistema simpático.
Palabras clave: cuerpo carotídeo, homeostasis, glucosa.
ABSTRACT
Changes in glucose levels in the peripheral or central blood are detected by sensors located on glucose: hypothalamic nuclei, the pancreas, the nucleus tractus solitarius, the hepatic portal system and carotid body receptors. The carotid body or glomus caroticum is a chemosensory organ located bilaterally in the vicinity of the bifurcation of the common carotid. The carotid bodies are polymodal sensors, which detect levels of oxygen, pH, carbon dioxide, temperature, osmolarity, potassium, glucose and insulin in the blood that irrigates. The objective of this review is to describe the work done by Ramon Alvarez-Buylla and colleagues in the Laboratory of Neuroendocrinology at the University Center for Biomedical Research at the University of Colima, and other researchers, related to the study of the carotid bodies in homeostasis glucose. CCs respond to hypoglycaemia through depletion adenosine triphosphate, or to changes in pH and PO2 without depletion adenosine triphosphate. It is increasingly evident that CCs play an important physiological role in the homeostasis of this carbohydrate, and hypoxic stress exerts a tonic influence on the secretion of various neurotransmitters and hormones such as arginine vasopressin, nitric oxide, neurotrophic factor derived from brain gamma-aminobutyric acid, glucagon, cortisol and others involved in the central processing contrarregulatorios mechanisms in glucose homeostasis. CCs initiate counter-regulatory responses to hypoglycemia involving the pituitary, adrenal, pancreas and the sympathetic system.
Keywords: carotid body homeostasis, glucose.
INTRODUCCIÓN
La glucosa constituye, casi en forma exclusiva, la fuente de energía metabólica del cerebro de los mamíferos.1 La incapacidad del sistema nervioso central (SNC) para sintetizar y almacenar este carbohidrato, hace que el cerebro dependa de la circulación arterial para mantener un flujo constante de su fuente primaria de energía.2 Los cambios en los niveles de glucosa en la sangre periférica o central se detectan por sensores a la glucosa situados en: los núcleos hipotalámicos,3 el páncreas,4 el núcleo del tracto solitario (NTS),5 el sistema portal hepático6,7 y los receptores del cuerpo carotídeo (CC).8 En esta revisión se describen los trabajos realizados por Ramón Álvarez-Buylla y colaboradores en el Laboratorio de Neuroendocrinología del Centro Universitario de Investigaciones Biomédicas (CUIB), de la Universidad de Colima, y de otros investigadores, relacionados con: el estudio de los CC en la homeostasis de la glucosa, los mecanismos del CC en la detección de la concentración de glucosa en la sangre que los irriga, la participación del NTS en la respuesta hiperglucemiante con aumento en la retención de glucosa por el cerebro y los órganos efectores de dichas respuestas.
]]>EL CUERPO CAROTÍDEO: ANATOMÍA Y FUNCIÓN
El cuerpo carotídeo o glomus caroticum es un órgano quimiosensorial localizado de forma bilateral en la vecindad de la bifurcación de la carótida común. Aunque la presencia de este órgano se reportó desde el siglo XVIII por Von Haller y Taube, su estudio detallado se inició apenas a principios del siglo XX. El fisiólogo de Köln (Alemania), Heinrich Hering (1923-1927) (citado por De Castro, 2009),9 estudió el reflejo cardio-respiratorio y demostró, de manera elegante, que los estímulos mecánicos o eléctricos al seno carotídeo desencadenan un reflejo, que llamó "reflejo del seno", con bradicardia e hipotensión arterial. Así mismo, Hering descubrió que la región del seno está inervada por una rama del IX par craneal o nervio glosofaríngeo, el nervio del seno carotídeo (nsc) o nervio de Hering, que constituye la base anatómica de dicho reflejo. En paralelo con estos descubrimientos, Jean-François Heymans y su hijo Corneille en Bélgica, continuaron el estudio de la región reflexogénica cardio-aórtica en estudios de parabiosis para proponer que la bradicardia es consecuencia de mecanismos vagales y concluir que la zona cardioaórtica constituye la región principal en la regulación respiratoria (Heymans y Heymans 1927) (citado por De Castro, 2009).9 Aunque ya se conocía la extensa inervación simpática y el suministro de sangre en el glomus caroticum, los detalles precisos de su organización y estructura, así como sus implicaciones fisiológicas, no se conocieron hasta que Fernando De Castro, discípulo de Cajal, describe la estructura detallada y la inervación del CC en 1926;10 como fue la primera descripción de quimiorreceptores arteriales, se considera, entonces, que el cuerpo carotídeo (CC) es un órgano que detecta los cambios químicos de la sangre. En 1938, en plena Guerra Civil Española, Corneille Heymans recibe el Premio Nobel en Fisiología y Medicina, por repetir la hipótesis de De Castro y su demostración.9
De Castro describe al CC como un ovillo de vasos, axones simpáticos y células glandulares, que forman pequeños glomérulos, con minúsculos y complicados plexos de fibras glosofaríngeas que envuelven a los glomérulos.10 De acuerdo con Hering, y sus primeros estudios, De Castro confirma la existencia del nervio y del seno carotídeos en todas las especies animales y edades estudiadas, se descarta que se trata de una malformación patológica propuesta por Binswanger y otros anatomistas a finales del siglo XIX. Además, De Castro describe la inervación sensorial de la región carotídea localizada en la bifurcación de la carótida interna. De igual forma, hace notar que algunas fibras son terminales que se extienden hasta la adventicia de la arteria, y constituyen los barorreceptores propiamente dichos. En estudios con denervaciones tróficas, De Castro concluye que las fibras barorreceptoras que inervan el seno carotídeo son necesariamente sensoriales, sus neuronas proyectan hasta el SNC para mantener la vida, y postula que dichas fibras representan las bases del "reflejo del seno".9
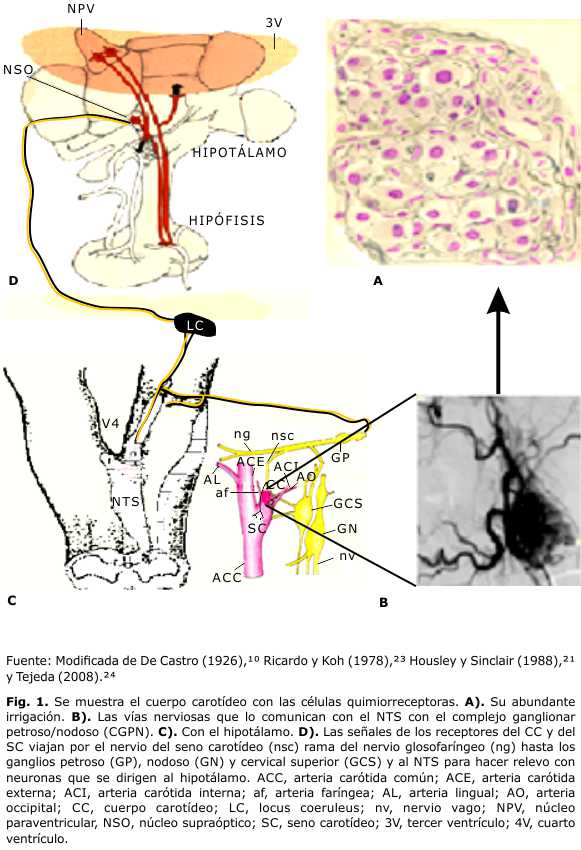
En relación con los quimiorreceptores del CC, De Castro realiza experimentos excepcionales para poner en evidencia cómo las células glómicas reciben inervación simpática que parte de neuronas simpáticas de la neuroglía presente en el glomus. Las células glómicas (núcleos coloreados) están rodeadas por inervación sensitiva, pero estas fibras no forman plexos cerrados alrededor del cuerpo carotídeo (Fig. 1A).10
Experimentos en perros con sección de los nervios glosofaríngeos y vagos, De Castro demuestra que las terminales nerviosas que inervan el glomus pertenecen a neuronas sensoras de los núcleos de ambos nervios, y lanza la hipótesis del carácter quimiorreceptor de las células del glomus caroticum. Postula que dichas células son distintas de las barorreceptoras, y señala, además, que realizan su función a través de procesos protoplásmicos al ponerse en contacto con la sangre. El elevado flujo sanguíneo (1,4 - 2,0 L/100 g de tejido/min) de los CC y alta tasa metabólica por g de tejido, hacen que tengan una maquinaria metabólica acelerada y exigente, susceptible a pequeños cambios químicos de la sangre que los irriga.11
¿Cómo se define el conocimiento del seno y cuerpo carotídeos en la actualidad? Se acepta que el nsc o de Hering, rama del glosofaríngeo, está formado por fibras barorreceptoras presentes en las paredes del seno carotídeo, y por fibras procedentes de los quimiorreceptores situados en los CCs.12 Las fibras del nervio carotídeo pasan de largo por el CC para terminar en el seno carotídeo. Ambas estructuras reciben, además, inervación simpática procedente del ganglio cervical superior por los nervios ganglio-glomerulares. 10 Los CCs son dos pequeñas estructuras, de 12 mg en humanos adultos y solo 1 mg en el gato, derivados de la cresta neural, localizados en la bifurcación carotídea (Fig. 1C).
Los CCs están constituidos por glomérulos que contienen, además de las fibras nerviosas señaladas, dos tipos de células: tipo 1, glomerulares o epitelioides, propiamente quimiorreceptoras, con intensa fluorescencia natural debido a su alto contenido de catecolaminas; tipo 2, o sustentaculares, glía-semejantes, que rodean a las células tipo 1. La función primordial de los CCs es regular los niveles del oxígeno requerido por el organismo de los mamíferos para activar el centro respiratorio y producir hiperventilación cuando las condiciones de este gas en la sangre son deficientes (hipoxemia).13,14
La localización estratégica de los CCs, en la iniciación de la circulación cerebral, hace que estos pequeños órganos se comporten como vigilantes de las condiciones de la sangre que recibe el cerebro. Los CCs son sensores polimodales, y pueden detectar, en la sangre que los irriga, niveles de oxígeno (O2), pH, bióxido de carbono (CO2), temperatura, osmolaridad,15 potasio, 16 glucosa8,13,17 e insulina.18 En el seno carotídeo, localizado en la bifurcación de la carótida común en el inicio de la carótida interna, se encuentran los barorreceptores carotídeos alojados entre la adventicia y las fibras musculares de estos vasos. Los impulsos procedentes de los CCs cursan por los nervios glosofaríngeo y vago, cuyos cuerpos celulares se encuentran en el complejo ganglionar petroso-nodoso (CGPN). Los axones aferentes baro- quimiorreceptores entran al CGPN con los nervios correspondientes, y viajan a lo largo del paquete sensorial del tracto solitario antes de formar sinapsis con neuronas en el núcleo del tracto solitario (NTS)19 (Fig. 1C). Los estudios anatómicos muestran que la porción dorsomedial del NTS recibe la inervación de los barorreceptores, mientras que la parte medial del área caudal al calamus escriptorius (NTS comisural-NTSc) es el sitio de entrada de los aferentes quimiorreceptores.20 En el NTS se encuentran las sinapsis iniciales para el procesamiento de la información sensorial que llega de los receptores viscerales (neuromodulación) y que incide sobre los reflejos de presión arterial, frecuencia cardiaca, frecuencia respiratoria, hipo e hiperglucemia, actividad nerviosa simpática, etc; esta información se dirige al locus coeruleus (LC) y de ahí al hipotálamo (Fig. 1D). Se sugiere que el NTS modula las señales aferentes que recibe, por mecanismos presinápticos en las propias terminales, o postsinápticos en los cuerpos neuronales.21
]]>La unión de baro- y quimiorreceptores carotídeos, forman el conjunto encargado de la detección de las dos variables que aseguran la perfusión y el metabolismo del SNC: cantidad y calidad de la sangre que recibe. Descensos en las concentraciones de glucosa activan a los quimiorreceptores del cuerpo carotídeos (QRCC) para iniciar respuestas contrarregulatorias que elevan la concentración de glucosa en la sangre y previenen el daño cerebral.24,25 Por el contrario, un descenso en la presión o en el flujo del seno carotídeo disminuye la actividad de los barorreceptores y desencadena una respuesta simpática para elevar la presión arterial y aumentar el flujo sanguíneo cerebral, por acción vasodilatadora del simpático sobre estos vasos, que mantiene la perfusión cerebral con substratos metabólicos y niveles de O2 adecuados. En resumen, baro- y quimiorreceptores del seno-cuerpo carotídeo participan en la regulación de las dos variables importantes para el metabolismo del SNC, glucosa y oxígeno. Las respuestas cardiovasculares y ventilatorias están muy estudiadas. 26 Sin embargo, el análisis detallado de la participación de los QRCC en la homeostasis de la glucosa se inició con los trabajos de Álvarez-Buylla y colaboradores8 y otros investigadores como Koyama y colaboradores.17
EL CUERPO CAROTÍDEO (CC) EN LA HOMEOSTASIS DE LA GLUCOSA
En los últimos años el estudio del CC y su relación con la regulación de la glucosa ha despertado gran interés.27 Los primeros estudios sobre la participación del CC en la homeostasis de la glucosa fueron hechos por Álvarez-Buylla y de Álvarez-Buylla, 8 que consiguen desarrollar una ingeniosa preparación para aislar circulatoriamente el seno carotídeo in vivo (SCA). Estos investigadores demuestran que la inyección de glucosa en el seno carotídeo vascularmente aislado, reduce la actividad eléctrica de los QRCC en un 20 % (Fig. 2), e incrementa su umbral a la hipoxia en gatos anestesiados. En los experimentos de control, la inyección de manitol (misma concentración y volumen) no cambia las descargas quimiorreceptoras. La estimulación eléctrica del cabo central del nsc en gatos induce efectos semejantes a los obtenidos con el NaCN; dos min después del estímulo, la diferencia arterio-venosa de glucosa hepática y la retención de glucosa cerebral (RGC) aumentan, y permanecen elevadas durante 16 min. Es decir, los QRCC, tónicamente activos bajo condiciones normales de glucosa, incrementan su actividad después de las aplicaciones de NaCN o de la estimulación central del nsc, para elevar la RGC; observaciones que concuerdan con las obtenidas en estudios anteriores por Álvarez-Buylla y colaboradores,28 donde se muestra un aumento en las concentraciones de glucosa en el líquido cefalorraquídeo después de la estimulación de los QRCC.
La disminución de la actividad de los barorreceptores por oclusión de ambas carótidas (Reflejo de Hering-HR) o la estimulación de los quimiorreceptores con NaCN produce incrementos inmediatos de la salida de glucosa por el hígado, así como un aumento de la diferencia venosa-arterial de glucosa hepática en comparación con su basal para inducir un aumento en la RGC en gatos, perros y ratas. Es decir, tanto la estimulación de los barorreceptores del seno carotídeo como de los QRCC provoca un reflejo hiperglucemiante con retención de glucosa cerebral (RHRGC).8
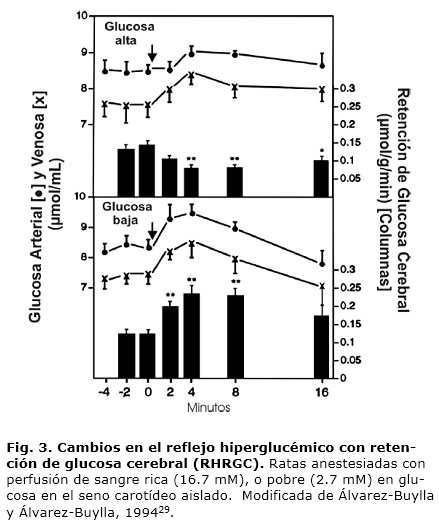
En gatos adrenalectomizados, o con sección de ambos nsc, no se produce el reflejo mencionado, que se restablece al estimular el cabo central del nsc; en estas condiciones, las respuestas respiratorias ante la estimulación QRCC son menores después de perfundir el CC con una solución de glucosa. Los cambios en la presión arterial no son significativos después de la estimulación QRCC, sola o precedida por la infusión de glucosa. La infusión de glucosa en el seno carotídeo no cambia las descargas barorreceptoras, y confirma la presencia de un efecto selectivo de este carbohidrato sobre la función quimiorreceptora. Es decir, la disociación entre baro-y quimiorreceptores refuerza la participación de los QRCC en el efecto glucémico. La estimulación baro-quimiorreceptora induce una secreción selectiva de epinefrina o norepinefrina de la médula adrenal, que desaparece en animales adrenalectomizados.28 Estudios diseñados para investigar los efectos de la estimulación QRCC en la circulación cruzada entre dos ratas (RGC) muestran que la perfusión del seno carotídeo con sangre rica en glucosa induce una disminución en la RGC, mientras que la perfusión con sangre pobre en glucosa produce un aumento en la RGC29 (Fig. 3).
]]>
Estudios de Koyama y colaboradores17 corroboran la participación del CC en la homeostasis de la glucosa en perros con extirpación de ambos CC. Estos autores utilizan un modelo de pinzamiento hipoglucémico-hiperinsulinémico (que mantiene la glucemia en 65 mg/dL aprox.) y encuentran que en estas condiciones, los animales presentan una hipoglucemia mayor ante la perfusión de insulina, en comparación con los perros normales. Es decir, los perros con extirpación de los CCs requieren una velocidad de infusión de glucosa mayor para mantener la euglucemia.
La ausencia de los mecanismos contrarregulatorios (respuesta hiperglucemiante desencadenada por la hipoglucemia insulínica), por la falta de los QRCC, motiva el incremento en la infusión de glucosa en los perros sin CC. Resultados consistentes con el papel glucosensor de los CCs.8 Koyama y colaboradores,17 encuentran que en condiciones normales, la hiperglucemia refleja, ante el estímulo hipoglucemiante en los CCs, se debe a un aumento en la secreción de glucagón y cortisol.
¿CÓMO DETECTAN LA HIPOGLUCEMIA LOS CUERPOS CAROTÍDEOS?
El proceso de la transducción quimiosensorial en los quimiorreceptores arteriales está poco estudiado. Según la hipótesis metabólica de la quimiorrecepción,30 es evidente la relación entre la quimiorrecepción y la producción de energía. Una disminución de la pO2 arterial produce una disminución en el contenido de trifosfato de adenosina (ATP) en las células quimiosensoriales tipo 1 del CC que conduce a la liberación de un neurotransmisor con aumento en la actividad neuronal sensorial. Es probable que esta hipótesis metabólica se aplique, también, a la hipoglucemia en los CCs, pues una baja perfusión de este carbohidrato produce una disminución de ATP y un aumento de ADP en los CCs.8 Obeso y colaboradores,31 al estudiar la hipótesis metabólica en preparaciones in vitro del CC de gato, con 2-desoxi-D-glucosa (0,25 mM y 2-4 mM) como agente depletor de ATP, encuentran un incremento en la actividad eléctrica del nsc con liberación paralela de dopamina en estos receptores, dependiente de Ca2+ extracelular; se concluye, entonces, la presencia de una sensibilidad diferenciada en las células quimiorreceptoras, que responden a la hipoglucemia a través de la depleción de ATP, o a cambios en el pH y pO2, sin depleción de ATP.
En preparaciones in vitro en cultivos de rebanadas delgadas del CC de rata, se observa que un descenso de glucosa en el medio induce la secreción de catecolaminas de las células glómicas, directamente proporcional a la entrada de Ca2+ extracelular vía canales de Ca2+ tipo L. La glucosa baja inhibe los canales de K+, induce despolarización y la apertura de los canales de Ca2+ tipo L. En las células glómicas, los niveles bajos de glucosa e hipoxia convergen para elevar la [Ca2+] citosólico y la liberación de transmisores, para conseguir la estimulación de las fibras aferentes sensoras, que desencadenan la activación de la respuesta simpático-adrenal. Esta acción sinérgica en la detección de glucosa y O2, supone una ventaja adicional en el proceso contrarregulatorio en los casos de hipoglucemia o hipoxemia agudos. Los efectos de baja glucosa e hipoxia sobre la secreción de catecolaminas son aditivos. A niveles arteriales de pO2∼90 mmHg la actividad de las células tipo 1 se modula por concentraciones de glucosa en el rango fisiológico (5 mmol/L ó 90 mg/dL); la actividad elevada de estas células durante la hipoxia (PO2 25 mmHg) a 0 mM de glucosa, se reduce con la presencia de glucosa a una concentración de 5-10 mM.32
Estudios posteriores demuestran que la remoción de glucosa extracelular inhibe las corrientes salientes de K+, se genera un potencial de receptor despolarizante, se incrementa la entrada de Na+, y después de Ca2+, con un aumento en la secreción del neurotransmisor en las células tipo 1 del CC. La secreción se elimina con la remoción de Na+ extracelular y con el bloqueo de los canales de Ca2+ de la membrana plasmática. Esto significa que la glucopenia produce un influjo de Ca2+ transmembranal con el consecuente incremento intracelular de este ion para la secreción del transmisor en las células tipo 1 de los CC. Se postula, entonces, que la asociación de transportadores a la glucosa Glut 2 y glucocinasa no parece ser necesaria para la detección de los niveles bajos de glucosa por los QRCC.33
Para profundizar en el problema de la estimulación de los QRCC ante niveles bajos de glucosa y dilucidar si los efectos de la glucopenia sobre la estimulación son directos o indirectos, Zhang y colaboradores34 utilizaron cocultivos de células glómicas y neuronas aferentes del ganglio petroso (GP) de ratas, con registros en célula completa (parche perforado). La caída de glucosa hasta 0-2 mM en el medio, produjo una descarga sensorial en las neuronas del GP. Sin embargo, con niveles de pO2 a 90 mm Hg (sangre arterial), fue posible producir quimioexcitación con niveles glucémicos de 3.3-4 mM (hipoglucemia fisiológica). La inhibición de dichas respuestas por una combinación de bloqueadores purinérgico y nicotínico, sugiere que el neurotransmisor en esta respuesta es el ATP o la ACh. En el registro pareado de la célula tipo 1 y el GP, la respuesta aferente coincide con la despolarización de la célula tipo 1. La hipoglucemia, igual que la hipoxia, estimula la liberación de 5-HT y ácido gama-aminobutírico (GABA), neurotransmisores que modulan, en forma opuesta, la función de las células tipo 1 a través de un mecanismo "push-pull" autocrino/paracrino con un potencial de receptor, y una despolarización postsináptica con una respuesta en las neuronas sensoriales del GP y actividad de espiga breve. El potencial de receptor se asocia con una disminución en la resistencia de entrada al inyectar una corriente hiperpolarizante constante durante las aplicaciones de glucosa 3,3 mM ó 0,1 mM en las células tipo 1. Es decir, la concentración baja de glucosa actúa como estímulo directo en el CC y produce una descarga aferente con activación de vías autonómicas contrarregulatorias.34
]]>En base a los datos presentados, se esquematiza en la figura 4 el mecanismo y vías utilizadas para obtener una respuesta contrarregulatoria ante una hipoglucemia y/o hipoxemia. La despolarización por el cierre de los canales de potasio de las células tipo 1 motiva un influjo de Ca 2+ transmembranal por canales tipo L dependientes de voltaje y la disminución de ATP intracelular, factores clave para la secreción del neurotransmisor por las células tipo 1 para estimular las terminales nerviosas sensitivas e incrementar la actividad de los impulsos de las neuronas sensitivas del nervio del seno carotídeo.
PARTICIPACIÓN CENTRAL EN LA RESPUESTA HIPERGLUCEMIANTE INDUCIDA POR EL ESTÍMULO HIPÓXICO DE LOS QUIMIORRECEPTORES DEL CUERPO CAROTÍDEO
Hasta aquí se ha visto que los niveles de glucosa sanguínea se controlan, en parte, dentro del SNC, integrándose la información de receptores periféricos.8,35,36 Varios grupos de células nerviosas o núcleos, en particular el NTS, participan en esta regulación.37 La mayor parte de los aferentes de los QRCC terminan en el NTS, principalmente en sus porciones medial y comisural. Durante los últimos años, el laboratorio de Neuroendocrinología del CUIB estudia cómo estos núcleos centrales y los neurotransmisores involucrados, interaccionan con los receptores periféricos para asegurar los niveles apropiados de glucosa circulante; y analizan la participación del NTS y el hipotálamo en el procesamiento del reflejo hiperglucemiante con aumento en la retención de glucosa por el cerebro (RHRGC).
ARGININA-VASOPRESINA (AVP) Y REGULACIÓN DE LA GLUCOSA EN RESPUESTA A LA ESTIMULACIÓN DE LOS RECEPTORES DEL CUERPO CAROTÍDEO CON CIANURO DE SODIO (NACN)
La vasopresina constituye un mediador único en la homeostasis de la glucosa, incide en los hepatocitos, en las células alfa del páncreas y en la médula adrenal cuando se libera como hormona neurohipofisiaria.38 El AVP, al ligar endógeno del receptor V1a de AVP, se sintetiza en muchos sitios del cerebro, como el núcleo paraventricular del hipotálamo (HPV), donde la AVP participa en la homeostasis de la glucosa como neurotrasmisor o neuromodulador.39 Es interesante observar que los axones procedentes de neuronas hipotalámicas del núcleo HPV terminan, precisamente, en el NTS.40 La administración directa de micro-dosis de AVP en el NTS en ratas despiertas eleva significativamente el RHRGC, mientras que la infusión de un antagonista de AVP disminuye el reflejo.41 Esta observación se sustenta en la activación de los receptores V1a hepáticos por la vasopresina, esencial en la respuesta glucogenolítica del hígado después de la estimulación de los QRCC con NaCN.42,43
]]>
ACTIVACIÓN DE LOS RECEPTORES GABA-B EN EL NTS Y BLOQUEO DE LA RESPUESTA GLUCÉMICA INDUCIDA POR LA ESTIMULACIÓN DE LOS RECEPTORES DEL CUERPO CAROTÍDEODiversos estudios demuestran que el NTS contiene neurotrasmisores que participan en el procesamiento de los mensajes aferentes de los QRCC. En particular, este núcleo presenta una alta densidad de terminales nerviosas que contienen GABA, neurotrasmisor inhibitorio importante en el SNC, así como receptores GaBAA y GABAB.44 Estos antecedentes hicieron que el grupo de Álvarez-Buylla y colaborades8,29,28 iniciara estudios sobre los efectos de neurotrasmisores GABAérgicos en el RHRGC post-estimulación anóxica de los QRCC. 45 La microinyección de baclofén (agonista de los receptors GABAB) en el NTS, reduce significativamente el RHRGC observado después de la estimulación de los QRCC, mientras que antagonistas de los receptores GABAB como el faclofén y el CGP55845A en el NTS producen el efecto contrario. En contraste, el muscimol y la bicuculina (agonista y antagonista respectivamente de los receptores GABAA) en el NTS, antes de la estimulación de los QRCC, no inducen cambios significativos en los niveles de glucosa en la sangre. Estos experimentos demuestran la presencia de un mecanismo inhibitorio tónico en el NTS a través de la activación de receptores GABAB, que modularía la respuesta hiperglucemiante.45 Es notorio observar cómo pequeñas alteraciones en la función GABAérgica en un núcleo del tallo cerebral, tienen profundos efectos en los niveles de glucosa plasmáticos y en la retención de este carbohidrato por el cerebro.
EL ÓXIDO NÍTRICO EN EL NTS COMISURAL (NTSC) Y EN EL EJE HIPOTÁLAMO-HIPOFISIARIO MODIFICAN LA GLUCEMIA DESPUÉS DE LA ESTIMULACIÓN DE LOS RECEPTORES DEL CUERPO CAROTÍDEO CON CIANURO EN RATAS
Como se ha señalado, el NTS constituye el enlace central clave en el control de múltiples reflejos homeostáticos, en el mismo sentido, muchos estudios demuestran que el óxido nítrico (NO) es una molécula señalizadora importante que participa en una amplia variedad de funciones en el SNC, incluida el metabolismo de la glucosa.46
Experimentos en ratas en el Laboratorio de Neuroendocrinología del CUIB demuestran que el nitroprusiato de sodio (NPS) (donador de NO) y el YC₁ (activador de la enzima guanilato ciclasa soluble, receptor natural para NO), infundidos en el NTSc antes de la estimulación de los QRCC, incrementan la glucemia arterial en relación con los resultados obtenidos en ratas control que reciben líquido cefalorraquídeo artificial en el NTSc. Por el contrario, la infusión de L-NAME (bloqueador de la enzima NO sintasa) en el NTSc antes de la estimulación de los QRCC, disminuye la glucemia arterial. En estos experimentos, la identificación de la proteína FOS, por inmunohistoquímica, permitió analizar la actividad neuronal en el NTSc en relación con el RHRGC inducido por la estimulación anóxica de los QRCC. El NPS en el NTSc incrementó el número de células Fos-ir en el NTSc/mm2 en comparación con el L-NAME o después de LCRa en el NTSc en ratas con estímulo anóxico de los QRCC. Se encuentra una relación positiva entre las neuronas inmuno-reactivas (c-Fos positivas) y el RHRGC, es decir, la activación de neuronas nitrinérgicas en el NTSc aumenta significativamente ante la estimulación anóxica de los QRCC.47,48 Por otro lado, la infusión de NPS en la cisterna magna antes de la estimulación de los CCs con NaCN, incrementó la concentración de nitritos en el plasma y en el tejido hipotálamo-hipofisiario, así como su expresión génica de iNOS y nNOS, aunque se observa un descenso en la glucemia. Ocurre el efecto opuesto después de la infusion de L-NAME. Estos resultados indican que el NO en el tejido hipotálamo-hipofisiario puede estar involucrado en los cambios en la glucemia después de la estimulación anóxica de los CCs.49
EL FACTOR NEUROTRÓFICO DERIVADO DEL CEREBRO (BDNF) EN EL NÚCLEO DEL TRACTO SOLITARIO MODULA LA HOMEOSTASIS DE LA GLUCOSA DESPUÉS DE LA ESTIMULACIÓN DE LOS QUIMIORRECEPTORES DEL CUERPO CAROTÍDEO EN RATAS
El BDNF juega un papel importante en el sistema endocrino de los mamíferos, y es notoria la participación de esta neurotrofina en el metabolismo de la glucosa.50 Con estos antecedentes, trabajos recientes del laboratorio de Neuroendocrinología analizan la participación del BDNF en el RHRGC evocado por estimulación anóxica de los QRCC. La infusión de BDNF en el NTSc, aumenta el RHRGC provocado por la estimulación de los QRCC, y por el contrario, la infusión de K252a (inhibidor del receptor TrkB del BDNF) en el NTSc, antes de la estimulación de los QRCC, disminuye ambas variables de glucosa (hiperglucemia y retención de glucosa cerebral), experimentos que ponen de manifiesto la participación del BDNF en el NTSc en la homeostasis de la glucosa.51
]]> LA SOMATOSTATINA (SS) EN EL NÚCLEO DEL TRACTO SOLITARIO COMISURAL (NTSC) MODULA LA RETENCIÓN DE GLUCOSA CEREBRAL POSTESTIMULACIÓN ANÓXICA DE LOS QUIMIORECEPTORES CAROTÍDEOS EN RATAS
La somatostatina (SS), neuromodulador inhibitorio importante en la homeostasis respiratoria y energética,52 se encuentra distribuido en el organismo (páncreas, NTS e hipotálamo).53 Se sugiere que este neuropéptido ejerce múltiples funciones endocrinas y paracrinas sobre distintos órganos blanco. Participa en la diferenciación y proliferación celular, y es un neurotransmisor importante, que inhibe la secreción de hormonas y neurotransmisores y modula la actividad y excitabilidad neuronales.54
El efecto inhibidor que ejercen la SS y sus receptores en el NTS indica que esta hormona en el NTSc modula a la baja el RHRGC después de la estimulación QRCC con NaCN. En efecto, la infusión de SS en el NTSc 4 min antes del estímulo anóxico disminuye el RHRGC 10 min después del estímulo anóxico.55,56
LA ACTIVACIÓN DE RECEPTORES GLUTAMATÉRGICOS EN EL NÚCLEO DEL TRACTO SOLITARIO COMISURAL (NTSc) MEDIA LA RETENCIÓN DE GLUCOSA POR EL CEREBRO EN RESPUESTA A LA ESTIMULACIÓN ANÓXICA DE LOS QUIMIORRECEPTORES DEL CUERPO CAROTÍDEO EN RATAS
Se sabe que los receptores AMPA participan en la vía glutamatérgica central para modular las señales entrantes de los quimiorreceptores extracraneales, sin embargo, son pocos los estudios que examinan su papel en el control del metabolismo energético.57 La activación de los receptores AMPA en el NTS, y la transmisión sináptica en los reflejos cardiorrespiratorios, desencadenan un reflejo simpatoexcitador, 58 que sugiere la participación de receptores ionotrópicos AMPA como moduladores clave en la respuesta ventilatoria.59 La activación de estos receptores incrementa, también, la respuesta de los quimiorreceptores evocada por la estimulación hipóxica intermitente.60 El glutamato se libera en el NTS por las terminales centrales del glosofaríngeo y del bulbo ventrolateral rostral (BVLR), que participa en la regulación de la actividad simpática de los baro-quimiorreflejos en la función respiratoria.61 En estudios de este laboratorio se centró la investigación en las señales glutamatérgicas, a través de los receptores AMPA, y la homeostasis de la glucosa alterada por la estimulación anóxica de los QRCC (Fig. 5). El AMPA en el NTSc antes de la estimulación de los QRCC inhibió la respuesta hiperglucemiante y la retención de glucosa por el cerebro observada en las ratas que recibieron LCRa en el NTSc. Sin embargo, el bloqueador de los receptores AMPA/kainato (NBQX) en el NTSc, aunque no modificó la respuesta hiperglucemiante, inhibió significativamente la retención de glucosa por el cerebro a los 20 y 30 min del estímulo anóxica en el SCA. Estos resultados muestran que las fibras glutamatérgicas, a través de los receptores AMPA en el NTSc, modulan el RHRGC después del estímulo QRCC en ratas. 51
CONSIDERACIONES FINALES
En base a los trabajos analizados por los autores citados en este capítulo, es cada vez más evidente que los CCs juegan un papel fisiológico importante en la homeostasis de la glucosa, y que el estrés hipóxico ejerce una influencia tónica en la secreción de diversos neurotrasmisores y hormonas como la AVP, el NO, el BDNF, el glutamato y otros. Los CCs deben incluirse, por tanto, en el grupo de los receptores extracraneales sensibles a los cambios en las concentraciones de glucosa, como el páncreas, el hígado y la vena porta hepática. El CC desempeña un papel primordial en la iniciación de los reflejos hiperglucemiantes para desencadenar respuestas contrarreguladoras a la hipoglucemia, originada in vivo cuando los niveles de glucosa en la sangre caen por debajo de 65mg.dL-1. El papel contrarregulatorio de los CCs tiene implicaciones clínicas, y se tienen evidencias sobre deficiencias de la función de los CCs en pacientes diabéticos, que presentan fallas en las respuestas ventilatorias a la hipoxia.62 En la respuesta contrarregulatoria participan, también, la hipófisis, las adrenales, el páncreas y el sistema simpático con aumento en la liberación de vasopresina, catecolaminas, glucagón y cortisol. Este estudio complementa la idea del papel fisiológico de los CCs en la homeostasis de la glucosa sugerido desde el año 1953 por Petropavlovskaya.63
]]>REFERENCIAS BIBLIOGRÁFICAS
1. Sokoloff L. Quantitative measurements of cerebral blood flow in man. Methods Med Res. 1960;8:253-61.
2. Strachan MW. Physiological responses to hypoglycaemia-not all 'just in the head. J Physiol. 2007;582:457-6.
3. Biggers DW, Myers SR, Neal D, Stinson R, Cooper NB, Jaspan JB, et al. Role of brain in counterregulation of insulininduced hypoglycemia in dogs. Diabetes. 1989;38:7-16.
4. Cook DL, Taborsky GJ. Beta-cell function and insulin secretion. En Ellenberg y Rifkin's Diabetes Mellitus. Porte D, Sherwin R, Eds. Stamford, CT: Appleton y Lange; 1997. p. 49-74.
5. Dallaporta M, Himmi T, Perrin J, Orsini JC. Solitary tract nucleus sensitivity to moderate changes in glucose level. Neuroreport. 1999;10:2657-60.
6. Donovan CM, Halter JB, Bergman RN. Importance of hepatic glucoreceptors in sympathoadrenal response to hypoglycemia. Diabetes. 1991;40:155-8.
7. Hevener AL, Bergman RN, Donovan CM. Novel glucosensor for hypoglycemic detection localized to the portal vein. Diabetes. 1997;46:1521-25.
8. Alvarez-Buylla R, de Alvarez-Buylla E. Carotid sinus receptors participate in glucose homeostasis. Resp Physiol 1988;72:347-60.
9. De Castro F. Towards the Sensory Nature of the Carotid Body: Hering, De Castro and Heymans† Front Neuroanat. 2009;3:23.
10. De Castro F. Sur la structure et l'innervation de la glande intercarotidienne (glomus caroticum) de l'homme et des mammifères, et sur un nouveau système d'innervation autonome du nerf glosopharyngien. Trav Lab Rech Biol. 1926;24:365-432.
11. Daly MB, Lambertsen CJ, Schweitzer A. Observations on the volume of blood flow and oxygen utilization of the carotid body in the cat. J Physiol Lond. 1954;125:67-89.
12. Nonídez JF, Windle WF. Textbook of Histology. McGraw-Hill book co. New York; 1953. p. 528.13. López-Barneo J. Oxygen and glucose sensing by carotid body glomus cells. Curr Opin Neurobiol. 2003;13:493-9.
14. Weir EK, Lopez-Barneo J, Buckler KJ, Archer SL. Acute oxygen-sensing mechanisms. New Engl J Med. 2005;353:2042-55.
15. Eyzaguirre C, Zapata P. Perspectives in carotid body research. J Appl Physiol. 1984;57:931-57.
16. Kumar P, Bin J. Adequate stimuli of the carotid body: more than an oxygen sensor? Respir Physiol Neurobiol. 2007;157:12-21.
17. Koyama Y, Coker R, Stone E, Lacy D, Jabbour K, Williams P, et al. Evidence that carotid bodies play an important role in glucoregulation in vivo. Diabetes. 2000;49:1434-42.
18. Conde SV, Sacramento JF, Guarino MP, Gonzalez C, Obeso A, Diogo LN, et al. Carotid body, insulin, and metabolic diseases: unraveling the links. Front Physiol. 2014;5:1-14.
19. Finley JC, Katz DM. The central organization of carotid body afferent projections to the brainstem of the rat. Brain Res. 1992;572:108-16.
20. Chitravanshi VC, Sapru HN. Chemoreceptor sensitive neurons in commissural subnucleus of nucleus tractus solitarius of the rat. Am J Physiol Regul Integr Comp Physiol. 1995; 268:R851-8.
21. Housley GD, Sinclair JD. Localization by kainic acid lesions of neurones transmitting the carotid chemoreceptor stimulus for respiration in rat. J Physiol. 1988;406:99-114.
22. McDonald DM, Mitchell RA. The innervation of glomus cells, ganglion cells and blood vessels in the rat carotid body: a quantitative ultrastructural analysis. J Neurocytol. 1975;4:177-230.
23. Ricardo JA, Koh ET. Anatomical evidence of direct projections from the nucleus of the solitarius tractus to the hypothalamus, amygdala and other forebrain structures in the rat. Brain Res. 1978;153:1-26.
24. Tejeda R. Efecto concomitante del óxido nítrico y el cianuro de sodio en el seno carotídeo in vivo sobre el reflejo hiperglucémico en ratas normales y diabéticas [Tesis de Doctorado]. CUIB, Universidad de Colima; 2008.
25. Auer RN, Wieloch T, Olsson Y, Siesjo BK. The distribution of hypoglycemic brain damage. Acta Neuropathol. 1984;64:177-91.
26. Guyton AC. Anatomía y fisiología del sistema nervioso. 2ª Ed. Madrid, España: Editorial Médica Panamericana; 1994.
27. Nurse C. Neurotrasmitter and neuromodulatory mechanisms at peripherial arterial chemoreceptors. Exp Physiol. 2010;95(6):657-67.
28. Alvarez-Buylla R, de Alvarez-Buylla E, Mendoza H, Montero S, Alvarez-Buylla A. Pituitary and adrenals are required for hyperglycemic reflex initiated by stimulation of CBR with cyanide. Am J Physiol. 1997;272:R392-9.
29. Alvarez-Buylla R, Alvarez-Buylla E. Changes in blood glucose concentration in the carotid body-sinus modify brain glucose retention. Brain Res. 1994;654:167-70.
30. Anichkov SV, Belen'kii ML. Pharmacology of the Carotid Body Chemoreceptors. New York: Macmillan; 1963.
31. Obeso A, Almaraz L, Gonzalez C. Effects of 2-deoxy-d-glucose on in vitro cat carotid body. Brain Res. 1986;371:25-36.
32. Pardal R, López-Barneo J. Low glucose-sensing cells in the carotid body. Nat Neurosci. 2002;5:197-8.
33. García-Fernández M, Ortega-Sáenz P, Castellano A, López-Barneo J. Mechanisms of low-glucose sensitivity in carotid body glomus cells. Diabetes 2007;56:2893-900.
34. Zhang M, Buttigieg J, Nurse CA. Neurotransmitter mechanisms mediating low-glucose signalling in cocultures and fresh tissue slices of rat carotid body. J Physiol. 2007;578:735-50.
35. Frohman L. CNS peptides and glucoregulation. Annu Rev Physiol. 1983;45:95-107.
36. Niijima A. Afferent impulse discharges from glucoreceptors in the liver of the guinea pig. Ann N Y Acad Sci. 1969;157:690-700.
37. Silver IA, Erecinska M Glucose-induced intracellular ion changes in sugar-sensitive hypothalamic neurons. J Neurophysiol. 1998;79:1733-45.
38. Grazzini E, Boccara G, Joubert D, Trueba M, Durroux T, Guillon G, et al. Vasopressin regulates adrenal functions by acting through different vasopressin receptor subtypes. Adv Exp Med Biol. 1998;449:325-34.
40. Duan YF, Kopin IJ, Goldstein DS. Stimulation of the paraventricular nucleus modulates firing of neurons in the nucleus solitary tract. Am J Physiol. 1999;277:R403-11.
41. Yarkov AV, Montero S, Lemus M, Roces de Álvarez-Buylla E, Álvarez-Buylla R. Arginine-vasopressin in nucleus of the tractus solitarius induces hyperglycemia and brain glucose retention. Brain Res. 2001;902:212-22.
]]>42. Montero SA, Yarkov A, Lemus M, de Alvarez-Buylla ER, Alvarez-Buylla R. Carotid chemoreceptor reflex modulation by arginine-vasopressin microinjected into the nucleus tractus solitarius in rats. Arch Med Res. 2006;37:709-16.
43. Montero S, Yarkov A, Alvarez-Buylla R. Carotid chemoreceptors participation in brain glucose regulation. Role of arginine-vasopressin. Adv Exp Med Biol. 2000;475:749-60.
44. Bowery NG, Enna SJ. Animobutyric acid B receptors: first of the functional metabotropic heterodimers. J. Pharmacol Exp Ther. 2000;292:2-7.
45. Lemus M, Montero SA, Cadenas JL, Lara JJ, Tejeda-Chavez HR, Álvarez-Buylla R, et al. GabaB receptors activation in the NTS blocks the glycemic responses induced by carotid body receptor stimulation. Auton Neurosci. 2008;141:73-82.
46. Almeida A, Cidad P, Delgado-Esteban M, Fernández E, García-Nogales P, Bolaños JP, et al. Inhibition of mitochondrial respiration by nitric oxide: its role in glucose metabolism and neuroprotection. J Neurosci Res. 2005;79:166-71.
]]>47. Montero S, Lemus M, Luquin S, Garcia-Estrada J, Melnikov V, Leal CA, et al. Nitric oxide in the commissural nucleus tractus solitarii regulates carotid chemoreception hyperglycemic reflex and c-Fos expression. Nitric Oxide. 2014;36:87-93.
48. Lemus M, Montero SA, Leal CA, Portilla-de Buen E, Luquin S, Garcia-Estrada J, et al. Nitric oxide infused in the solitary tract nucleus blocks brain glucose retention induced by carotid chemoreceptor stimulation. Nitric Oxide. 2011;25:387-95.
49. Cadenas JL, Montero SA, Leal C, Lemus M, Portilla-de Buen, Alvarado BA, et al. Nitric oxide in the hypothalamus-pituitary axis mediates increases in brain glucose retention induced by carotid chemoreceptor stimulation with cyanide in rats. Nitric Oxide. 2010;22:296-303.
50. Krabbe KS, Nielsen AR, Krogh-Madsen R, Plomgaard P, Rasmussen P, Erikstrup C, et al. Brain-derived neurotrophic factor (BDNF) and type 2 diabetes. Diabetologia 2007;50:431-8.
51. Cuéllar R, Montero S, Luquín S, García-Estrada J, Dobrovinskaya O, Melnikov V, et al. Glutamatergic Receptor Activation in the Commissural Nucleus Tractus Solitarii (cNTS) Mediates Brain Glucose Retention (BGR) Response to Anoxic Carotid Chemoreceptor (CChr) Stimulation in Rats. Adv Exp Med Biol. 2015;860:301-8.
]]>52. Jacquin T, Champagnat J, Madamba S, Denavit-Saubié M, Siggins GR. Somatostatin depresses excitability in neurons of the solitary tract complex through hyperpolarization and augmentation of IM, a non-inactivating voltage-dependent outward current blocked by muscarinic agonists. Proc Natl Acad Sci. 1988;85:948-52.
53. Patel YC. Somatostatin and its receptor family. Front Neuroendocrinol. 1999;20:157-98.
54. Tallent M, Siggins G. Somatostatin acts in CA1 and CA3 to reduce hippocampal epileptiform activity. J Neurophysiol. 1999;81(4):1626-35.
55. Montero S, Lemus M, Figueroa J, Ceja C, Morales P, Pacheco J, et al. La somatostatina en el núcleo del tracto solitario comisural modula la retención de glucosa cerebral postestimulación anóxica de los quimioreceptores carotídeos en ratas. Rev Cubana Invest Biomed. 2013;32:74-82.
56. Mojarro de Dios C. "Efecto de la somatostatina en el núcleo del tracto solitario comisural sobre la hiperglucemia con retención de glucosa cerebral inducida con cianuro de sodio en el seno carotídeo aislado in vivo en ratas normo e hiperglucémicas" [Tesis de Maestría] CUIB, Universidad de Colima; 2014.
57. Pang ZP, Han W. Regulation of synaptic functions in central nervous system by endocrine hormones and the maintenance of energy homeostasis. Biosci Rep. 2012;32:423-32.
58. Lin L. Glutamatergic neurons say NO in the nucleus tractus solitarii. J Chem Neuroanat. 2009;38:154-65.
59. Ohtake PJ, Torres JE, Gozal YM, Graff GR, Gozal D. NMDA receptors mediate peripheral chemoreceptor afferent input in the conscious rat. J Appl Physiol. 1998;84:853-61.
60. De Paula PM, Tolstykh G, Mifflin S. Chronic intermittent hypoxia alters NMDA and AMPA-evoked currents in NTS neurons receiving carotid body chemoreceptor inputs. Am J Physiol Regul Integr Comp Physiol. 2007;292:R2259-65.
61. Koshiya N, Guyenet PG. NTS neurons with carotid chemoreceptor inputs arborize in the rostral ventrolateral medulla. Amer J Physiol. 1996;270:R1273-8.
62. Ikegaya N, Yonemura K, Suzuki T, Kato-Ohishi H, Taminato T, Hishida A, et al. Impairment of ventilatory response to metabolic acidosis in insulin-dependent diabetic patients with advances nephropathy. Ren Fail. 1999;21:495-8.
63. Petropavlovskaya AA. "Reflex hyperglycemia" in The Pharmacology of New Therapeutic Substances (Leningrad:Medgiz). 1953;30-2.
Recibido: 5 de diciembre de 2015.
Aprobado: 7 de enero de 2016.
Elena Roces Dorronsoro. Centro Universitario de Investigaciones Biomédicas. Universidad de Colima. Colima, México. ]]>
Correo electrónico: che_colima_5@yahoo.com.mx ]]>