La multifuncional célula estrellada del hígado y su papel en la fibrosis hepática
The multifunctional stellate cell of the liver and its role in hepatic fibrosis
Aleida Josefa Herrera Batista
Héctor Juan Ruiz Candina
Alicia Borroto Leiseca
Universidad de Ciencias Médicas de La Habana ICBP "Victoria de Girón". La Habana, Cuba.
]]>
RESUMEN
Introducción: La comprensión de la célula estrellada del hígado y su participación en la fibrosis hepática ha emergido con el desarrollo de métodos de investigación que han posibilitado aislarla y caracterizarla.
Objetivo: Analizar los aspectos más novedosos de estas células reportados por la literatura profundizando en su participación en la génesis de la fibrosis hepática.
Métodos: Se realizó una búsqueda bibliográfica utilizando los buscadores: SciELO, Central Pud Med y Scholar Google; se emplearon publicaciones científicas de preferencia de la modalidad "revisiones bibliográficas".
Resultados: Esta célula recibió diferentes denominaciones: pericitos hepáticos, células de Ito, células intersticiales, lipocito. En 1995 se tomó el acuerdo de llamarla "Célula hepática estrellada". Representó del 5-8 % de las células del hígado y presenta forma ahusada, con prolongaciones, núcleo oval, moderado retículo endoplasmático rugoso, pequeño aparato de Golgi, abundantes gotas lipídicas, filamentos intermedios de citoqueratina. Almacenan vitamina A y sintetizan matriz extracelular, además elaboran varios tipos de factores de crecimiento y citoquinas. Cuando recibe una señal agresiva viral o tóxica, se activan experimentando un proceso de trans-diferenciación transformándose en miofibroblastos, incrementando su capacidad para sintetizar matriz extracelular generando una cicatriz temporal en el sitio del daño, con vistas a proteger la glándula; pero sí la agresión persiste, estas continúan aumentando de tamaño y causando fibrosis; caracterizada por la formación de escaras o cicatrices de gran tamaño provocando perturbación tanto de la arquitectura, como en la función normal del hígado.
Conclusiones: La célula estrellada es una célula multifuncional, con un papel protagónico en la fibrosis hepática.
Palabras clave : célula estrellada hepática; célula de Ito; fibrosis hepática; miofibroblasto; cicatrización de heridas.
ABSTRACT
]]> Introduction: The understanding of the stellate cell of the liver and its participation in hepatic fibrosis has emerged with the development of research methods that have made it possible to isolate and characterize it.Keywords: hepatic stellate cell; Ito cell; liver fibrosis; myofibroblast; wound healing.
INTRODUCCIÓN
La comprensión de la célula estrellada del hígado (CEH), su participación en el daño hepático y en la fibrosis solo ha emergido después del desarrollo de sofisticados métodos de investigación, que han posibilitado aislarla y caracterizarla. El paradigma que convierte a una célula quiescente, almacenadora de vitamina A, en una célula proliferativa, contráctil, con un papel protagónico en la fibrosis hepática, es decir un miofibroblasto, ha deslumbrado a hepatólogos, patólogos, histólogos y fisiólogos por muchos años y solo recientemente ha podido ser dilucidado. El progreso en esta área del saber se debe al desarrollo de:
En condiciones fisiológicas las CEH comprenden ≈ el 15 % del total de células residentes en el hígado. Su principal función es el almacenamiento y homeostasia de la vitamina A y otros retinoides, los cuales se almacenan en el citoplasma en forma de gotas lipídicas como ésteres de retinol. Estas células regulan el flujo sanguíneo en los capilares sinusoidales, producen apolipoproteínas, prostaglandinas, factores de crecimientos y citoquinas, lo cual contribuye a la homeostasia de la matriz extracelular (MEC). La síntesis y degradación de la MEC es esencial para la integridad del espacio perisinusoidal o espacio de Disse y para la comunicación intra e intercelular entre células vecinas.2,3
La CEH ha emergido en los últimos 30 años como una célula versátil, multifuncional y enigmática célula mesenquimatosa, que es la protagonista esencial del proceso de fibrosis después de un daño infringido al hígado. Por tales razones la presente revisión bibliográfica se propone como objetivo analizar los aspectos más novedosos de estas células reportados por la literatura profundizando en su participación en la génesis de la fibrosis hepática.
MÉTODOS
Se realizó una búsqueda bibliográfica a través de los buscadores de información y plataformas: SciELO, Central Pud Med y Scholar Google. El resultado de la búsqueda mostró un aproximado de 120 artículos que fueron filtrados; se utilizaron 30 publicaciones científicas de preferencia de la modalidad "revisiones bibliográficas".
]]>
DESARROLLO
La primera descripción de las células estrelladas como almacenadoras de vitamina A fue realizada por Kϋpffer en 1876, utilizando como método el oro coloidal y las denominó "Sternzellen" que significa "estrella" en alemán y a la cual le adjudicó una función fagocítica.1,4-6 Su identidad fue confirmada en 1882 por Rothe.6 Las observaciones iniciales de Kϋpffer fallaron en distinguir entre la CEH con la clásica célula fagocítica residente del hígado, que pertenece a la familia monocito macrófago y conocida hoy como "Célula de Kϋpffer". Irónicamente, estudios recientes han confirmado que la CEH es capaz de fagocitar cuerpos apoptóticos, aunque el método utilizado por Kϋpffer no las reconoció a ellas sino a aquellas otras que hoy llevan su nombre.
La CEH ha sido estudiada con diferentes técnicas y de acuerdo a estas ha recibido diferentes denominaciones. Las mismas fueron estudiadas con el método de plata de Golgi -por Zimmerman y denominadas por este investigador como "pericitos hepáticos". En 1955 Ito, con la técnica apropiada, pudo detectar lípidos en su interior y a partir de ese momento fueron conocidas como "células almacenadoras de lípidos" o simplemente como "células de Ito".1 Suzuki las estudió con impregnación argéntica, denominándolas "células intersticiales" y más recientemente, en 1966 Bronfenmajer, Schaffner, and Popper, proponen el nombre de "lipocito" para denotar su contenido en grasa (vitamina A). 1 Por último Wake en 1988, utilizando técnica de cloruro de oro, proporcionó la descripción definitiva de la célula estrellada in situ y estableció que las células peri sinusoidales son las mismas descritas por Kϋpffer 100 años atrás.7 Debido a la existencia de una amplia variedad de denominaciones en el año 1996 se tomó el acuerdo, ampliamente aceptado, de llamarla "Célula hepática estrellada" en lugar de los sinónimos: Célula de Ito, Lipocito, célula almacenadora de lípidos o célula perisinusoidal.1
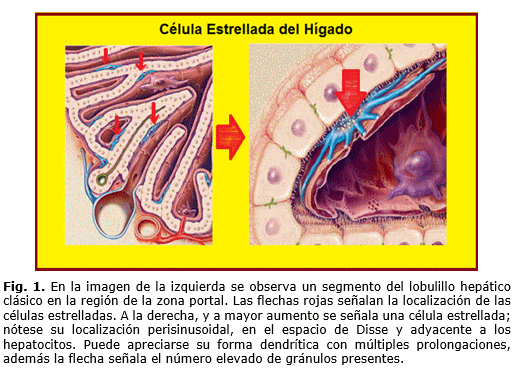
Las CEH se localizan en el espacio de Disse, entre las células endoteliales de los capilares sinusoidales y los hepatocitos, es decir son células perisinusoidales (Fig.1). Representan del 5-8 % de las células del hígado, así como el 30 % de las células no parenquimatosas de este órgano. Presenta forma ahusada, con el cuerpo celular angular o redondeado, con un núcleo oval o elongado, moderado retículo endoplasmático rugoso y un pequeño aparato de Golgi yuxta nuclear, abundantes filamentos intermedio de citoqueratina; expresa además marcadores de células neurales: proteína acídica fibrilar de la glía (GFAP), la sinemina y la sinaptofisina; también expresa desmina, CD146, el factor de crecimiento hepático (HGF) y el factor de crecimiento neural (NGF).8-10
La CEH se caracteriza por poseer numerosas prolongaciones dendríticas, que se extienden entre las células endoteliales, abrazándolas y que poseen micro proyecciones espinosas (Fig. 2). Por la superficie antiluminal se extienden múltiples procesos a través del espacio de Disse para hacer contacto con los hepatocitos. Estos contactos facilitan el transporte intercelular de mediadores solubles y citoquinas. Además, se asocian a las terminaciones nerviosas. En el hígado saludable son células quiescentes y contienen numerosas gotas lipídicas y de vitamina A, es decir son verdaderas células almacenadoras de vitamina A, constituyendo el mayor reservorio de esta vitamina en el cuerpo y realizan otras funciones relacionadas con el desarrollo hepático, la regeneración, el metabolismo de lipoproteínas y retinol, la regulación del sistema inmune y fibrogénesis en respuesta a la injuria hepática.8-12
Cuando el hígado recibe una agresión mediante una infección viral o toxinas hepáticas, las células estrelladas reciben señales desde los hepatocitos dañados, las células endoteliales, las células de Kϋpffer, las plaquetas y desde las células inmunes, lo cual la activan provocándoles una trans-diferenciación que las transforma en células similares a miofibroblastos. Al ser las CEH las células productoras de matriz extracelular (MEC) en el hígado, su reacción primaria es generar una cicatriz temporal, en el sitio del daño, con vistas a proteger a la glándula de la agresión y de daños posteriores.13,14
]]>Además, las CEH secretan citoquinas y factores de crecimiento que favorecen la regeneración de las células epiteliales hepáticas. Sin embargo en las enfermedades hepáticas crónicas que se prolongan y que favorecen la activación mantenida de las CEH, estas aumentan de tamaño (Fig. 3) y causan fibrosis, caracterizada por la formación de escaras o cicatrices de gran tamaño provocando perturbación tanto de la arquitectura, como de la función normal del hígado.13-15 Estudios recientes, tanto clínicos como experimentales, revelan que el proceso de fibrosis hepática es totalmente reversible, si se eliminan los factores causales, señalándose que la CEH activada se torna drásticamente reducida y lentamente regresa a la normalidad, o muere por apoptosis.16-19
EL PAPEL DE LA CÉLULA ESTRELLADA EN LA FIBROSIS HEPÁTICA
La fibrosis hepática es una consecuencia patológica de estímulos crónicos: virales, autoinmunes, inducido por drogas, entre ellas el alcohol, así como de las enfermedades colestáticas y metabólicas. Puede ser definida como el resultado de la acumulación progresiva de la matriz extracelular (MEC) y disminución de su remodelado por las enzimas metaloproteasas, lo cual altera la arquitectura normal del hígado. Cuando la injuria y la reacción inflamatoria aguda asociada, causan necrosis celular moderada y daño de la matriz extracelular, se produce una reacción de reparación y en respuesta a las células parenquimatosas perdidas por necrosis o apoptosis, se produce auto replicación, regeneración y sustitución de las células muertas. No obstante, ante la agresión mantenida los mecanismos se desregulan y falla la regeneración llegándose a la fibrosis hepática.10-12
Si no se trata esta glándula progresa a la cirrosis, al fallo de órgano y por último a la muerte. Esta complicación consiste en un incremento anómalo de tejido conectivo, con el consiguiente aumento de las proteínas de la matriz extracelular, entre ellas las colágenas tipo I, las cuales son depositadas fundamentalmente por las CEH al activarse ante el estímulo agresor; esta activación es promovida por el factor de necrosis tumoral alfa (TNF-α), los factores transformadores β y α (TGF β y TGF α) y las especies reactivas del oxígeno producidas por los hepatocitos que mueren por apoptosis;20 en estas circunstancias las CEH comienzan a expresar α actina (α-SMA) típica del músculo, así como citoquinas pro inflamatorias y factores de crecimientos, tales como el HGF, para promover regeneración. Las CEH juegan un papel fundamental en la respuesta inmune hepática,21 pueden funcionar como células presentadoras de antígenos y de hecho pueden modular la proliferación de los linfocitos T; aunque su papel mejor conocido es su participación en el proceso de fibrosis hepática. Otros miofibroblastos hepáticos contribuyen en el proceso fibrótico, pero hoy se sabe que las CEH participan en un 80 %.11,12,20,21
En resumen, la fibrosis hepática es la resultante de un daño crónico con acumulación de proteínas de la MEC, lo cual es una característica de la mayoría de enfermedades hepáticas crónicas. La fibrosis hepática, como proceso pasivo e irreversible, ha sido considerada como un modelo de "cicatrización de heridas" como respuesta a la injuria hepática crónica. 14 Los reportes clínicos recientes han confirmado que la fibrosis hepática avanzada es potencialmente reversible y actualmente se plantea que al eliminarse las noxas se revierte el proceso y el hígado pasa a la normalidad, proceso en el cual, al parecer, un número elevado de CEH mueren por apoptosis.22-24
Durante el proceso de injuria crónica se produce la activación de las CEH, lo cual es considerado un evento central en el proceso de fibrogénesis hepática. Las CEH aumentan en talla y adquieren el fenotipo de un miofibroblasto con regulación de la angigénesis y activación y amplificación de la respuesta inmune, a través de secreción de citoquinas y quimoquinas; con una pérdida ostensible de los gránulos intracelulares e incrementando su capacidad para la síntesis de la MEC.13 La composición de esta cambia con un incremento y acumulación de las proteínas, entre ellas las colágenas que forman fibras I, III V y XI y entre las que forman láminas la IV y la VI; colágenas asociadas a fibras, como la XIV y colágenas de la familia de las multiplexinas, la XVIII; además elabora elastina, hialuronato, proteoglicanos, como el perlecano, la decorina, el agrecan y la fibromodulina; así como glicoproteínas como la fibronectina, laminina y tenascina.24-28
Este tipo de matriz tiene la capacidad de acelerar la activación de las CEH, provocando la pérdida de las microvellosidades (Fig. 4) por los hepatocitos adyacentes y desaparición de las fenestraciones a nivel de las células endoteliales. Según plantean los investigadores este cambio en la arquitectura de las células endoteliales empeora el transporte de solutos desde los capilares sinusoidales a los hepatocitos, contribuyendo a la disfunción de estos; además la acumulación de la MEC favorece la amplificación de la fibrosis. Por otra parte, las alteraciones en la misma provocan cambios en la expresión de los receptores de integrina de la membrana. La acumulación de este componente tisular se debe a dos hechos fundamentales: el incremento de la síntesis y disminución de la degradación.24-26
]]> Fig. 4. En la imagen de la izquierda se muestra el espacio de Disse de una célula normal donde se aprecian las microvellosidades de los hepatocitos, las CEH con abundantes gránulos, así como las fenestraciones entre las células endoteliales. En el esquema de la derecha se observan los cambios que ocurren ante la agresión mantenida al hígado. Nótese un incremento en el grosor del espacio de Disse o espacio subendotelial, donde se aprecia un gran incremento de los componentes de la MEC. A nivel de los hepatocitos han disminuido las microvellosidades y las células endoteliales aparecen firmemente adheridas.Se sabe que en condiciones normales la matriz es una estructura dinámica y que se encuentra en constante síntesis y remodelación, y que su homeostasis depende del balance entre dos grupos enzimáticos: las metaloproteasas (MMPs) y sus inhibidores (TIMPs). El exceso de matriz en el hígado es controlado por las MMPs (1, 2, 8 y 13), mientras que el marcado incremento de esta se debe a los inhibidores (TIMP-1 and TIMP-2). La TIMP 1, en particular posee un efecto antiapoptótico sobre el fenotipo fibrótico de la CEH, con lo cual se alarga su supervivencia favoreciendo todos los efectos a favor del incremento de la fibrosis hepática.24,29
La angiogénesis es otra respuesta a la injuria crónica del hígado28 que lleva al remodelado sinusoidal y al incremento y activación de los pericitos o CEH y consecuentemente muchos potentes mediadores angiogénicos participan en la respuesta exagerada de cicatrización de heridas durante la agresión crónica al hígado, trayendo como consecuencia la excesiva acumulación de la MEC y esta puede afectar también a la célula incrementando indirectamente la liberación de citoquinas que incluyen el factor de crecimiento transformador β (TGF-β), el factor de crecimiento derivado de las plaquetas (PDGF), el HGF, el factor de crecimiento del tejido conectivo (CTGF), el TNF-α, el factor de crecimiento del fibroblasto (b FGF) y el factor de crecimiento del endotelio vascular (VEGF).24,30
Se plantea que el fenotipo contráctil de la CEH contribuye a la angiogénesis y a la hipertensión portal, que es una característica de la cirrosis hepática. Como se sabe la localización de estas células en el espacio perisinusoidal, favorece que sus largos procesos ejerzan un efecto regulador sobre la resistencia pericapilar y de este modo puedan regular el flujo sanguíneo intrahepático mediante la vía de su fenotipo contráctil.28
CONSIDERACIONES FINALES
La célula estrellada es una célula multifuncional, almacenadora de vitamina A, con un papel protagónico en la fibrosis hepática
]]> Conflicto de intereses
Los autores declaran que no existe conflicto de intereses.
REFERENCIAS BIBLIOGRÁFICAS
1. Friedman S L. Hepatic Stellate Cells: Protean, Multifunctional, and Enigmatic Cells of the Liver. Physiol Rev. 2008 January;88(1): 125-72.
2. Vera M, Nieto N. Hepatic stellate cells and alcoholic liver disease. Rev. esp. enferm. dig. 2006 Sep [citado 2018 Jul 05];98(9):674-84. Disponible en: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1130-01082006000900005&lng=es .
3. Friedman SL. Stellate cells: a moving target in hepatic fibrogenesis. Hepatology. 2004;40:1041-3.
]]> 4. Blaner WS, O'Byrne SM, Wongsiriroj N, Kluwe J, D'Ambrosio D, Jiang H, et al. Hepatic stellate cell lipid droplets: a specialized lipid droplet for retinoid storage. Biochim Biophys Acta. 2009 June;1791(6):467-73.5. Aterman K. The parasinusoidal cells of the liver: a historical account. Histochem J. 1986;18:279-305.
6. Wake K. Perisinusoidal stellate cells (Fat-storing cells, interstitial cells, lipocytes), their related structure in and around liver sinusoids, and vitamin A storing cells in extrahepatic organs. Int Rev Cytol. 1980;66:303-53.
7. Wake K. Liver perivascular cells revealed by gold and silver impregnation methods and electron microscopy. In: Motta PM, editor. Biopathology of the Liver, an Ulrastructural Approach. Dordrecht: Kluwer; 1988: 23-36.
8. Blaner WS. Hepatic stellate cell lipid droplets: a specialized lipid droplet for retinoid storage. Biochim Biophys Acta. 2009;1791(6):467-73.
9. Schuppan D, Kim YO. Evolving therapies for liver fibrosis. J Clin Invest. 2013. 123(5):1887-901.
10. Arriazu E, ,Ruiz de Galarreta M, Cubero FJ, Varela-Rey M, Pérez de Obanos MP, Leung TM, et al. Extracellular Matrix and Liver Disease. Antioxid Redox Signal. 2014 Sep 1;21(7):1078-97.
11. Kisseleva T, Brenner D. A. Anti-fibrogenic Strategies and the regression of fibrosis. Best Pract Res Clin Gastroenterol. 2011 April;25(2):305-17.
12.Mio K, Bloomston MP. Hepatic Stellate Cells and microRNAs in Pathogenesis of Liver Fibrosis. J Clin Med. 2016 Mar;5(3):38.
13. Chunyue Yin , Kimberley J. Evason, Kinji Asahina, Didier YR. Stainier. Hepatic stellate cells in liver development, regeneration, and cancer. J Clin Invest. 2013 May 1;123(5):1902-10.
14. Crespo Yanguas S, Cogliati B, Willebrords J, Maes Mi, Colle I, van den Bossche B, et al. Experimental models of liver fibrosis. Arch Toxicol. 2016 May;90(5):1025-48.
15. Lee UE, Friedman SL. Mechanisms of hepatic fibrogenesis. Best Pract Res Clin Gastroenterol. 2011;25(2):195-206.
16. Ellis EL, Mann DA. Clinical evidence for the regression of liver fibrosis. J Hepatol. 2012;56(5):1171-80.
17. Troeger JS. Deactivation of hepatic stellate cells during liver fibrosis resolution in mice. Gastroenterology. 2012;143(4):1073-83.
18. Wells RG. The Portal Fibroblast-Not Just a Poor Man's Stellate Cell. Gastroenterology. 2014 Jul;147(1):41-47.
19. Schuppan D, Kim YO. Evolving therapies for liver fibrosis. J Clin Invest. 2013;123(5):1887-901.
20. Bataller R, Brenner DA. Liver fibrosis. J Clin Invest. 2005;115:209-18.
21. Russell JO, Monga SP. Wnt/β-Catenin Signaling in Liver Development, Homeostasis, and Pathobiology. Annu Rev Pathol. 2018 Jan 24;13:351-78.
22. Ramachandran P, Iredale JP. Reversibility of liver fibrosis. Ann Hepatol. 2009;8:283-91.
23. Puche JE, Saiman Y, Friedman SL. Hepatic stellate cells and liver fibrosis. Compr Physiol. 2013;3:1473-92.
24. Gülsüm Özlem E. Cellular and molecular mechanisms in the pathogenesis of liver fibrosis: An update. World J Gastroenterol. 2014 Jun 21;20(23):7260-76.
25. Henderson NC, Arnold TD, Katamura Y, Giacomini MM, Rodriguez JD, McCarty JH, et al. Targeting of αv integrin identifies a core molecular pathway that regulates fibrosis in several organs. Nat Med. 2013;19:1617-24.
]]> 26. Ray K. Liver: Key role for αv integrins in myofibroblasts in liver fibrosis. Nat Rev Gastroenterol Hepatol. 2014;11:4.27. Eulenberg VM, Lidbury JA. Hepatic Fibrosis in Dogs. J Vet Intern Med. 2018 Jan-Feb;32(1):26-41.
28. Lee UE, Scott L. Friedman. Mechanisms of Hepatic Fibrogenesis. Best Pract Res Clin Gastroenterol. 2011 April;25(2):195-206.
29.Fowell AJ, Collins JE, Duncombe DR, Pickering JA, Rosenberg WM, Benyon RC, et al. Silencing tissue inhibitors of metalloproteinases (TIMPs) with short interfering RNA reveals a role for TIMP-1 in hepatic stellate cell proliferation. Biochem Biophys Res Commun. 2011;407:277-82.
30. Johnson A, DiPietro LA. Apoptosis and angiogenesis: an evolving mechanism for fibrosis. FASEB J. 2013;27:3893-901.
]]> Recibido: 10 de agosto de 2018.
Aleida Josefa Herrera Batista. Universidad de Ciencias Médicas de La Habana ICBP "Victoria de Girón". La Habana, Cuba. Correo electrónico: aleidajosefa@infomed.sld.cu
]]>