y estudiar algunas de las variables que influyen en la reacción, así como la estabilidad del radioinmunoconjugado en presencia de otros agentes quelatantes.]]>
and study some of the variables that influence in the labelling reaction, as well as the stability of the radioimmunoconjugate in presence of other chelating agents.]]>
Nuevo radioinmunoconjugado ![]() -dota-h-r3. Sintesis y radiomarcaje
-dota-h-r3. Sintesis y radiomarcaje
New radioimmunoconjugate ![]() -dota-h-r3. synthesis and radiolabeling
-dota-h-r3. synthesis and radiolabeling
Denis R. Beckford Vera, Abmel Xiques Castillo, Rene Leyva Montana, Marylaine Perez Malo Cruz, Edgar Casanova Gonzalez, Minely Zamora Barrabi
Omar García1, Julio Medina2
]]> Centro de Isotopos (CENTIS). La Habana, CUBARESUMEN
El marcaje de anticuerpos monoclonales con metales radiactivos para diagnóstico y terapia generalmente involucra el uso de agentes quelatantes bifuncionales que contienen una función reactiva para conjugarse con las proteínas y un grupo capaz de enlazar fuertemente al metal formando complejos fisiológicamente estables. El objetivo del trabajo fue modificar el anticuerpo monoclonal humanizado (h-R3) con el ácido 1,4,7,10-tetraazaciclododecano-N,N´,N´´,N´´´-tetraacético (DOTA) en solución acuosa, realizar el marcaje de los conjugados obtenidos con ![]() y estudiar algunas de las variables que influyen en la reacción, así como la estabilidad del radioinmunoconjugado en presencia de otros agentes quelatantes.
y estudiar algunas de las variables que influyen en la reacción, así como la estabilidad del radioinmunoconjugado en presencia de otros agentes quelatantes.
ABSTRACT
Labelling of monoclonal antibodies with radioactive metals for cancer diagnosis and therapy has usually been accomplished by the use of bifunctional chelating agents, which contain both a reactive functionality for covalent attachment to proteins and a strong metal-binding group capable of forming a physiologically stable complex with the radionuclide. The objective of the present work was to modify the humanized monoclonal antibody (h-R3) with the 1,4,7,10-tetraaza-cyclododecane N,N´,N´´,N´´´-tetraacetic acid (DOTA) in aqueous solution, achieve the labelling of the obtained conjugates with ![]() Y and study some of the variables that influence in the labelling reaction, as well as the stability of the radioimmunoconjugate in presence of other chelating agents.
Y and study some of the variables that influence in the labelling reaction, as well as the stability of the radioimmunoconjugate in presence of other chelating agents.
Key words: monoclonal antibodies, diagnosis, neoplasms, labelled compounds, yttrium 90
INTRODUCCION
A pesar de los retos, los anticuerpos monoclonales marcados con radiometales emisores ![]() - continúan siendo una opción viable para la radioinmunoterapia del cáncer. Sin embargo, la terapia de tumores sólidos continúa siendo un desafío para la comunidad científica, ya que las dosis que son efectivas en los tumores hematológicos son insuficientes en los tumores epiteliales más comunes; a pesar de que los ensayos clínicos han demostrado avances en tratamientos locoregionales y de metástasis residuales mínimas [1].
- continúan siendo una opción viable para la radioinmunoterapia del cáncer. Sin embargo, la terapia de tumores sólidos continúa siendo un desafío para la comunidad científica, ya que las dosis que son efectivas en los tumores hematológicos son insuficientes en los tumores epiteliales más comunes; a pesar de que los ensayos clínicos han demostrado avances en tratamientos locoregionales y de metástasis residuales mínimas [1].
Generalmente, el marcaje de anticuerpos monoclonales (mAb) con radionúclidos metálicos involucra el uso de agentes quelatantes bifuncionales (AQBFs) con el objetivo de formar radioinmunoconjugados con una alta estabilidad bajo condiciones fisiológicas [2-5,6]. Los derivados del ácido dietilentriaminopentaacético (DTPA) y el DOTA han sido los agentes quelatantes bifuncionales más empleados para el marcaje de biomoléculas con radisótopos metálicos, principalmente radiolantánidos.
Lewis y cols [7,8] desarrollaron un método simple, eficiente y económico para enlazar agentes quelatantes bifuncionales a proteínas. A partir de entonces, esta metodología ha sido empleada con éxito por otros autores para el marcaje de anticuerpos monoclonales, principalmente con radiolantánidos [9].
MATERIALES Y METODOS
Anticuerpo monoclonal
El anticuerpo monoclonal anti-EGF humanizado h-R3 (TheraCIMR®), proteina de isotipo IgG1 que reconoce con elevada especificidad el dominio externo del EGF-R, fue suministrado por el Centro de Inmunologia Molecular (CIM, Cuba).
Reactivos
Los ligandos DOTA y DOTA-NHS se adquirieron de Macrocyclics Dallas TX. La 1-etil-3-[3-(dimetilamina) propil] carbodiimida (EDC) y la N-hidroxisulfosuccinimida (sulfo-NHS) se adquirieron de la firma Pierce, Rockford, IL. Se empleó agua ultrapura (18,2 M![]() /cm, EURO 60-integra plus, Alemania). El
/cm, EURO 60-integra plus, Alemania). El ![]() se obtuvo a partir de un generador cromatográfico
se obtuvo a partir de un generador cromatográfico ![]() (CENTIS).
(CENTIS).
Instrumentacion general
La cromatografia liquida de alta resolucion (HPLC) se realizo con un equipo Shimadzu (Japon), equipado con un inyector manual Rheodyne, bombas LC-6A, desgasificador DGU-3A, detector UV SPD-6AV, integrador CROMATOPAC CR4AX y un colector de fracciones 2112 REDIRAC (BROMMA). La concentracion del anticuerpo monoclonal se determino en un espectrofotometro UV-visible (spectronic GENESYS, Milton Roy, USA). La medicion de la actividad se realizo en un contador de centelleo liquido (LKB-WALLAC-RacBeta 1209, Finlandia) y en un calibrador de dosis CMR 35 (Capintec, EEUU).
Conjugacion del anticuerpo monoclonal h-R3
DOTA-OSSu-h-R3 (método in situ). Para conjugar el anticuerpo monoclonal h-R3 con DOTA se empleó una variante del método de Lewis y cols [7, 8]. Una solución de DOTA (20 mg, 0,049 mmol) en 500 µl de agua se mezcló con 100 µl de sulfo-NHS (10,7 mg, 0,049 mmol) también disuelto en agua y se ajustó el pH de la mezcla de ambas soluciones a ~5,8 con 110 µl de NaOH 1M, la solución resultante se enfrió a 4ºC. A la mezcla anterior se le adicionó 153 µl de una solución de EDC (9,5 mg, 0,049 mmol) preparada momentos antes de utilizarla. La mezcla de reacción se agitó por 45 min a 4ºC, el pH se ajustó a 7,0 con ![]() 0,2 M pH-9,0 y se mezcló sin previa purificación con la solución concentrada del anticuerpo monoclonal h-R3 (10,5-11,7 mg/mL).
0,2 M pH-9,0 y se mezcló sin previa purificación con la solución concentrada del anticuerpo monoclonal h-R3 (10,5-11,7 mg/mL).
Se estudiaron tres relaciones molares AQBF:mAb en cada caso, 600:1, 500:1 y 200:1. A las mezclas de reacción se les ajustó el pH hasta 8,0 con una solución saturada de ![]() y se incubaron toda la noche a 4ºC. La purificación de los DOTA-conjugados se realizó empleando cromatografía de exclusión molecular en una columna empaquetada con Sephadex G-50 (280 x 5 mm) previamente lavada con una solución de HCl 0,5 M para eliminar la presencia de posibles cationes metálicos, posteriormente se equilibró con buffer acetato
y se incubaron toda la noche a 4ºC. La purificación de los DOTA-conjugados se realizó empleando cromatografía de exclusión molecular en una columna empaquetada con Sephadex G-50 (280 x 5 mm) previamente lavada con una solución de HCl 0,5 M para eliminar la presencia de posibles cationes metálicos, posteriormente se equilibró con buffer acetato ![]() 0,1 M (1,0% HSA) pH-7,0, se eluyó con buffer acetato de amonio 0,1M pH-7,0 y se colectaron fracciones de 0,5 mL. La concentración de la proteína modificada se determinó empleando el ensayo de Bradford. Para determinar los agregados de alto peso molecular que se pudieran formar en el proceso de conjugación y la integridad de los conjugados se utilizó HPLC de exclusión molecular (HPLC-EM) empleando una columna Protein Pack SW300 Waters (7,5 x 300 mm, 10 µm, Waters), se inyectaron 20 µl de la muestra, como fase móvil se utilizó NaCl 0,9% con un flujo de 1mL/min.
0,1 M (1,0% HSA) pH-7,0, se eluyó con buffer acetato de amonio 0,1M pH-7,0 y se colectaron fracciones de 0,5 mL. La concentración de la proteína modificada se determinó empleando el ensayo de Bradford. Para determinar los agregados de alto peso molecular que se pudieran formar en el proceso de conjugación y la integridad de los conjugados se utilizó HPLC de exclusión molecular (HPLC-EM) empleando una columna Protein Pack SW300 Waters (7,5 x 300 mm, 10 µm, Waters), se inyectaron 20 µl de la muestra, como fase móvil se utilizó NaCl 0,9% con un flujo de 1mL/min.
Determinación del numero promedio de agente quelatante bifuncional enlazado a una molécula de anticuerpo monoclonal
Para determinar la cantidad de grupos DOTA enlazados a una molécula de anticuerpo monoclonal h-R3 se empleó una variante del método de Meares y colaboradores [11]. Se mezcló 53 µl de una solución de ![]() (555 µM, 0.029.µmoles) que tenía ~5,5 x 106 cpm/µl; 53 µl de buffer acetato de amonio 0,5 M, pH-7,0 y 90 µl, (0,0024-0,0029 µmoles) de DOTA-h-R3. La mezcla se hizo reaccionar por 3 horas a 42oC y posteriormente se le añadió 22 µl de DTPA 10 mM pH-6 y se incubó 15 min a temperatura ambiente. Posteriormente se aplicó 1,5 µl de la mezcla de reacción sobre una tira de ITLC-SG (1x10 cm) y se desarrolló en
(555 µM, 0.029.µmoles) que tenía ~5,5 x 106 cpm/µl; 53 µl de buffer acetato de amonio 0,5 M, pH-7,0 y 90 µl, (0,0024-0,0029 µmoles) de DOTA-h-R3. La mezcla se hizo reaccionar por 3 horas a 42oC y posteriormente se le añadió 22 µl de DTPA 10 mM pH-6 y se incubó 15 min a temperatura ambiente. Posteriormente se aplicó 1,5 µl de la mezcla de reacción sobre una tira de ITLC-SG (1x10 cm) y se desarrolló en ![]() (10% m/v): Metanol (1:1). La tira se cortó 1 cm por encima del punto de aplicación y ambas fracciones se midieron en un contador de centelleo líquido.
(10% m/v): Metanol (1:1). La tira se cortó 1 cm por encima del punto de aplicación y ambas fracciones se midieron en un contador de centelleo líquido.
Radiomarcaje
En un tubo Eppendorf se mezclaron alícuotas de ![]() (3-14 mCi, 3-12 µl) en una solución de HCl 0,05 N, entre 100 y 150 µl de buffer acetato de amonio 0,5 M pH-7,0 y 100 µl (~0,400 mg) del conjugado DOTA-h-R3. La mezcla de reacción se incubó a 42°C por 1 h, transcurrido este tiempo se le adicionó 1/9 del volumen de reacción de una solución de DTPA 10 mM pH-6,0 para acomplejar el 90Y que no reaccionó y se incubó por 15 min a temperatura ambiente. Utilizando diseños experimentales se evaluó la influencia del tiempo de incubación y el pH del buffer en el rendimiento de marcaje. Las relaciones molares escogidas fueron 500:500:500:1 (método in situ) y 200:1(conjugación directa). Se mezclaron 3 mCi de
(3-14 mCi, 3-12 µl) en una solución de HCl 0,05 N, entre 100 y 150 µl de buffer acetato de amonio 0,5 M pH-7,0 y 100 µl (~0,400 mg) del conjugado DOTA-h-R3. La mezcla de reacción se incubó a 42°C por 1 h, transcurrido este tiempo se le adicionó 1/9 del volumen de reacción de una solución de DTPA 10 mM pH-6,0 para acomplejar el 90Y que no reaccionó y se incubó por 15 min a temperatura ambiente. Utilizando diseños experimentales se evaluó la influencia del tiempo de incubación y el pH del buffer en el rendimiento de marcaje. Las relaciones molares escogidas fueron 500:500:500:1 (método in situ) y 200:1(conjugación directa). Se mezclaron 3 mCi de ![]() en una solución de HCl 0,05 N, 100 µl de buffer acetato de amonio pH-7,0 o pH-8,0 y ~0,3 mg de cada conjugado. Las mezclas de reacción se incubaron a 42°C y la determinación del rendimiento de marcaje se realizó a 1 h y 3 h. Los datos obtenidos se analizaron con el software estadístico STAGRAPHICS® Plus versión 5.1.
en una solución de HCl 0,05 N, 100 µl de buffer acetato de amonio pH-7,0 o pH-8,0 y ~0,3 mg de cada conjugado. Las mezclas de reacción se incubaron a 42°C y la determinación del rendimiento de marcaje se realizó a 1 h y 3 h. Los datos obtenidos se analizaron con el software estadístico STAGRAPHICS® Plus versión 5.1.
Determinación del rendimiento de marcaje
El rendimiento de marcaje se determino utilizando cromatografia instantanea de capa delgada (ITLCTM SG, Silica Gel Impregnated Glass Fiber Sheets, Pall) 1 x 10 cm, se uso una mezcla de acetato de amonio (10% m/v) y metanol (1:1) como fase movil. En este sistema el radioinmunoconjugado se mantiene en el punto de aplicación (Rf=0), mientras que el 90Y acomplejado por el DTPA migra hasta Rf=0,5-0,9. También para algunos casos el rendimiento de marcaje se chequeó por HPLC utilizando una columna TSK-Gel SW3000 (7,5 x 300 mm, 10 µm, TosoHass) usando NaCl (0,9%, 0,05% ![]() ) en régimen isocrático como fase móvil. Se colectaron fracciones de 0,5 mL y se midieron en un contador de centelleo líquido.
) en régimen isocrático como fase móvil. Se colectaron fracciones de 0,5 mL y se midieron en un contador de centelleo líquido.
Estudio de estabilidad in vitro en exceso de DTPA
El radioinmunoconjugado ![]() -DOTA-h-R3 (20-80 µL, >156 µCi) previamente purificado se adicionó a 1 mL de DTPA 1 mM en NaCl 0,9% y se incubó a 37oC. Se aplicaron alícuotas de 1-4 µL sobre tiras de papel ITLC/SG y se desarrollaron en MeOH:
-DOTA-h-R3 (20-80 µL, >156 µCi) previamente purificado se adicionó a 1 mL de DTPA 1 mM en NaCl 0,9% y se incubó a 37oC. Se aplicaron alícuotas de 1-4 µL sobre tiras de papel ITLC/SG y se desarrollaron en MeOH:![]() (10% m/v) 1:1, posteriormente la tira se cortó 1 cm por encima del punto de aplicación y ambas fracciones se midieron en un contador Rackbeta. De la misma forma fue comprobado por HPLC-EM utilizando buffer
(10% m/v) 1:1, posteriormente la tira se cortó 1 cm por encima del punto de aplicación y ambas fracciones se midieron en un contador Rackbeta. De la misma forma fue comprobado por HPLC-EM utilizando buffer ![]() 0,01 M como fase móvil. Las muestras se analizaron en intervalos de 24-72 h por un periodo de nueve días.
0,01 M como fase móvil. Las muestras se analizaron en intervalos de 24-72 h por un periodo de nueve días.
Conjugación del anticuerpo monoclonal h-R3
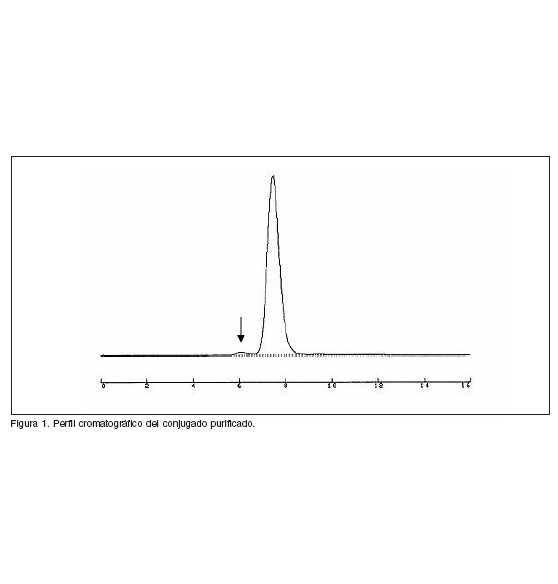
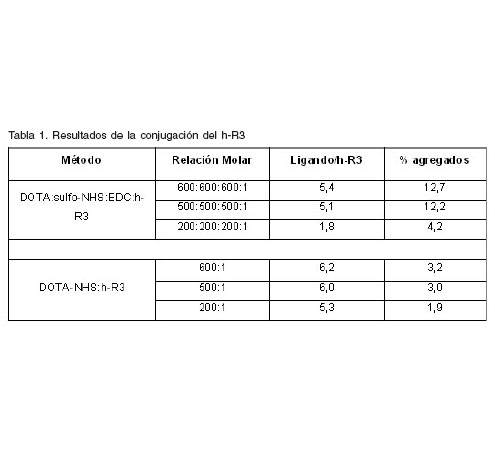
El porcentaje de agregados moleculares formados se tomo como el area debajo del pico anterior al pico correspondiente al conjugado como se aprecia en la figura 1. En ningun caso se observo la formación de fragmentos como consecuencia de la reaccion de conjugacion. Los resultados de la cantidad de moleculas de AQBF enlazadas a una molecula de anticuerpo monoclonal y el nivel de formacion de agregados moleculares se muestran en la tabla 1.
Radiomarcaje
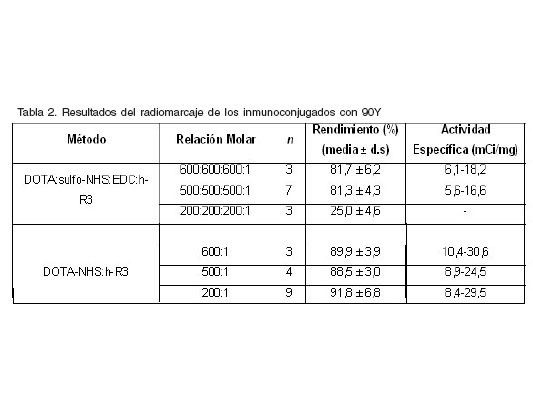
Se realizaron marcajes de todos los conjugados obtenidos por las dos vías utilizadas para modificar el h-R3 con DOTA. Los resultados del radiomarcaje se muestran en la tabla 2. Después de la purificación la pureza radioquímica para todos los radioinmunoconjugados obtenidos por la primera variante fue superior a 97% y superior a 98% para la segunda, determinado por ITLC-SG y chequeado por HPLC-EM. Las condiciones óptimas de marcaje se identificaron como 1,5 h y pH-8,0. Bajo estas condiciones se obtuvieron rendimientos de marcaje de 88,5 ± 1,9% (n=5) para el conjugado obtenido por el método in situ y 92,1 ± 3,1% (n=5) para el conjugado obtenido por la modificación del h-R3 con DOTA-NHS.
Estudio de estabilidad en exceso de DTPA
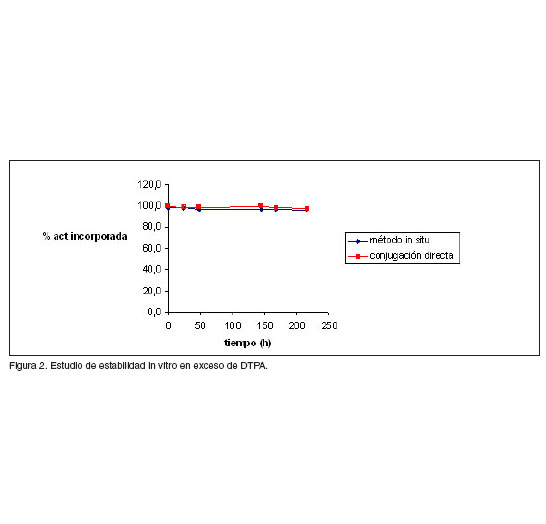
La estabilidad del radioinmunoconjugado ![]() -DOTA-h-R3 se evaluo en presencia de exceso de DTPA. La relación molar DTPA: 90Y-DOTA-h-R3 fue 24503:1 para el caso del conjugado obtenido por el metodo in situ y 20900:1 para el conjugado obtenido por reaccion directa del DOTA-NHS con el h-R3. Los resultados obtenidos se muestran en la figura 2.
-DOTA-h-R3 se evaluo en presencia de exceso de DTPA. La relación molar DTPA: 90Y-DOTA-h-R3 fue 24503:1 para el caso del conjugado obtenido por el metodo in situ y 20900:1 para el conjugado obtenido por reaccion directa del DOTA-NHS con el h-R3. Los resultados obtenidos se muestran en la figura 2.
DISCUSION
]]> El ácido 1,4,7,10-tetraazaciclododecano-N,N´,N´´,N´´´-tetraacetico y sus derivados se han empleado con exito en el radiomarcaje de anticuerpos monoclonales con 90Y debido a que forman complejos altamente estables en medio fisiológico con este radionuclido [7, 8, 12, 13].Generalmente la activacion del DOTA involucra más de un paso de sintesis, como consecuencia escogimos el metodo desarrollado por Lewis colaboradores [7,8] para activar el grupo carboxilo del agente quelatante bifuncional (DOTA) posteriormente modificar el anticuerpo monoclonal h-R3. Este metodo ofrece conjugados de hasta 5,6 quelatos por molecula de anticuerpo para relaciones molares AQBF:mAb hasta 408:1, preservando la inmunoreactividad del anticuerpo modificado superior al 90% [14]. Teniendo en cuenta que en el metodo descrito nos resulta dificil conocer la concentracion real del DOTA activado, decidimos usar tambien DOTA-NHS comercial para modificar el anticuerpo monoclonal h-R3.
Las relaciones molares estudiadas están basadas en estudios realizados anteriormente en nuestro laboratorio, donde se activo el grupo carboxilo del DOTA empleando NHS y DCC en medio de DMSO, resultando que solo cuando la relacion molar AQBF:mAb fue mayor que 400:1 los resultados del marcaje, expresados en pureza radioquimica, fueron satisfactorios manteniendo la inmunoreactividad por encima del 90% [15].
La purificación de la mezcla de conjugación es una etapa muy importante en el desarrollo del inmunoconjugado, ya que es donde se elimina el agente quelatante en exceso que no se enlazo a la proteina, garantizando en lo adelante que no exista, o al menos se reduzca al minimo, la competencia del AQBF no conjugado por el radionuclido. Varios metodos se han reportado para lograr dichas separaciones, las mas empleadas son: dialisis, exclusion molecular por centrifugacion y exclusion molecular por columna. La dialisis, metodo mas utilizado, garantiza la separacion casi completa del AQBF no quelatado empleando chelex 100 y numerosos cambios de buffer. En este proceso Lewis y cols [7,8] y Berger y cols [13] utilizaron ~150 y ~90 h respectivamente. Coliva, Zacchetti y cols [16] reportaron la purificacion del conjugado Bz-DOTA-mAb mediante cromatografia de exclusion molecular usando columnas comerciales PD-10, proceso que se realiza en pocos minutos con resultados satisfactorios. En nuestro caso decidimos emplear cromatografia de exclusion molecular utilizando una columna empaquetada con Sephadex G-50 de dimensiones 0,5 x 28 cm, con la cual se logro una buena separación del AQBF que no reacciono comprobado por HPLC-EM.
La cantidad de grupos DOTA enlazados a una molécula de anticuerpo monoclonal se vio influenciada por el exceso de AQBF empleado para modificar la biomolecula. Sin embargo no existe diferencia sustancial para las relaciones molares AQBF/mAb 500:1 y 600:1, lo cual sugiere que ocurre una saturacion de los grupos ![]() -amino de los residuos de lisina, grupo fundamental donde se espera se produzca el enlace amida entre el agente quelatante bifuncional y la proteina. Los rendimientos de marcaje obtenidos en nuestros experimentos son satisfactorios y se corresponden con los datos reportados por otros autores [8,12,17], sin embargo, para la relacion molar DOTA:sulfo-NHS:EDC:h-R3 (200:200:200:1) los rendimientos no superaron el 25%, lo cual esta relacionado con la cantidad de grupos DOTA enlazados a una molecula de h-R3.
-amino de los residuos de lisina, grupo fundamental donde se espera se produzca el enlace amida entre el agente quelatante bifuncional y la proteina. Los rendimientos de marcaje obtenidos en nuestros experimentos son satisfactorios y se corresponden con los datos reportados por otros autores [8,12,17], sin embargo, para la relacion molar DOTA:sulfo-NHS:EDC:h-R3 (200:200:200:1) los rendimientos no superaron el 25%, lo cual esta relacionado con la cantidad de grupos DOTA enlazados a una molecula de h-R3.
Los resultados obtenidos en la incubacion del radioinmunoconjugado en exceso de DTPA evidencian su estabilidad, corroborando los resultados reportados por otros autores [9,18]; para radioinmunoconjugados basados en anticuerpos monoclonales marcados con ![]() , empleando DOTA y sus derivados como agentes quelatantes bifuncionales. El 90Y que no se mantiene asociado al conjugado se pudiera deber a la presencia de pequeñas cantidades de agentes quelatantes que no se lograron separar en el proceso de purificación y que no se detectan por los metodos empleados.
, empleando DOTA y sus derivados como agentes quelatantes bifuncionales. El 90Y que no se mantiene asociado al conjugado se pudiera deber a la presencia de pequeñas cantidades de agentes quelatantes que no se lograron separar en el proceso de purificación y que no se detectan por los metodos empleados.
CONCLUSIONES
La metodología descrita permitio obtener de forma rapida y sencilla el conjugado DOTA-h-R3 modificando el anticuerpo monoclonal humanizado (h-R3) con DOTA por dos vias sin afectar la integridad de la molécula. Los conjugados obtenidos presentan entre 1,8 y 6,7 moleculas de DOTA enlazadas a una molécula de anticuerpo monoclonal h-R3 y se logró un marcaje estable de los conjugados obtenidos con ![]() con rendimientos y estabilidad satisfactorios.
con rendimientos y estabilidad satisfactorios.
REFERENCIAS BIBLIOGRAFICAS
1. SHARKEY RM, GOLDENBERG D M. Perspectives on Cancer Therapy with Radiolabeled Monoclonal Antibodies. J Nucl Med. 2005;( 46): 115S-127S.
2. MCCALL MJ, DIRIL H, MEARES CF. Simplified Method for Conjugation Macrocyclics Bifunctional Chelating Agents to Antibodies via 2-Iminothiolane. Bioconjugate Chem. 1990;( 1): 222-226.
3. LI M, MEARES CF. Synthesis metal chelate stability studies and enzyme digestion of a peptide-linked DOTA derivative and its corresponding radiolabeled immunoconjugates. Bioconjugate Chem. 1993; (4): 275-283.
4. PANWAR P, IZNAGA-ESCOBAR N, MISHRA P, SRIVASTAVA V, SHARMA KR, CHANDRA R, MISHRA AK. Radiolabeling and biological Evaluation of DOTA-Ph-Al Derivative Conjugated to Anti-EGFR Antibody ior egf/r3 Targeted tumor Imaging and Therapy. Cancer Biology and Therapy. 2005; 4 ( 8): e63-e69.
5. MOHSIN H, JIA F, SIVAGURU G, HUDSON MJ, SHELTON TD, HOFFMAN TJ, CUTLER CS, KETRING AR, ATHEY PS, SIMON JR, FRANK K, JURISSON SS, LEWIS MR. Radiolanthanide-Labeled Monoclonal Antibody CC49 for Radioimmunotherapy of Cancer: Biological Comparison of DOTA Conjugates and 149Pm, 166Ho, and 177Lu. Bioconjugate Chem. 2006; (17): 485-492.
6. LIU S, EDWARDS DS. Bifunctional chelators fortherapeutic lanthanide radiofarmaceuticals. Bioconjugate Chem. 2001; (12): 7-34.
7. LEWIS MR, RAUBITSCHEK A, SHIVELY JE. A Facile Water-Soluble Method for Modification of Proteins with DOTA. Use of Elevated Temperature and Optimized pH To Achieve High Specific Activity and High Chelate Stability in Radiolabeled Immunoconjugates. Bioconjugafe Chem. 1994; (5): 565-576.
8. LEWIS MR, JIM YK, ANNE-LINE JA, SHIVELY JE, RAUBITSCHEK A. An improved method for conjugating monoclonal antibodies with N-hidroxysulfosuccinimimidyl DOTA. Bioconjugate Chem. 2001; (12): 320-324.
9. GRIFFITHS GL, GOVINDAN SV, SHARKEY RM, FISHER DR, GOLDENBERG DM. 90Y-DOTA-hLL2: An Agent for Radioimmunotherapy of Non-Hodgkin’s Lymphoma. J. Nucl. Med. 2003; (44): 77-84.
10. BRADFORD MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem. 1976;( 72): 248.
11. MEARES CF, MCCALL MJ, REARDAN DT, GOODWIN DA, DIAMANTI CI, MCTIGUE M. Conjugation of Antibodies with Bifunctional Chelating Agents Isothiocyanate and Bromoacetamide Reagents Methods of Analysis and Subsequent Addition of Metal Ions. Anal Biochem. 1984;( 142): 68-78.
12. SERENGULAN VG, LISA BS, GOLDENBERG DM, ROBERT MS, HABIBE K, JOSEPH ED, MICHELE JLH, GARY LG. 90Yttrium-labeled complementary-determining-region-grafted monoclonal antibodies for radioimmunotherapy: radiolabeling and animal biodistribution studies. Bioconjugate Chem. 1998; (9): 773-782.
13 BERGER MA, MASTERS GR, SINGLETON J, SCULLY MS, GRIMM LG, SOLTIS DA, ALBONE EF. Pharmacokinetics, Biodistribution and Radioimmunotherapy with Monoclonal antibody 776.1 in a Murine Model of Human Ovarian Cancer. Cancer biotherapy & Radiopharmaceuticals. 2005; 20 (6): 589-601.
14. SMITH A, ALBERTO R, BLAEUENSTEIN P, NOVAKHOFER I, MAECKE HR, SCHUBIGER PA. Preclinical Evaluation of 67Cu-labeled Intact and Fragmented Anti-Co-lon Carcinoma Monoclonal Antibody MAb35. Cancer Res. 1993; (53): 5727-5733.
15. LEYVA R, PERERA A, XIQUES A, HERNANDEZ I, LEON M. Labeling of humanized MAb h-R3 with 90Y. World J. Nucl. Med. 2002; (1): s186 (abst.).
16. COLIVA A, ZACCHETTI A, LUISON E, TOMASSETTI A, BONGARZONE I, SEREGNI E, BOMBARDIERI E, MARTIN F, GIUSSANI A, FIGINI M, CANEVARI S. 90Y Labeling of monoclonal antibody MOv18 and preclinical validation for radioimmunotherapy of human ovarian carcinomas. Cancer Immunol Immunother. 2005; (54): 1200-1213.
17. KUKIS DL, DENARDO SJ, DENARDO GL, O’DONNELL RT, MEARES CF. Optimized conditions for chelation of yittrium-90-DOTA immunoconjugates. J. Nucl. Med. 1998; (39): 2105-2110.
18. HANCOCK RD, MARTELL AE, MOTEKAITIS RJ. Factors affecting stabilities of chelate, macrocyclic and macrobicyclic complexes in solution. Coord. Chem. Rev. 1994; (133): 39-65.
Centro de Isotopos (CENTIS) Ave. Monumental y Carretera La Rada, Guanabacoa, Ciudad de La Habana, Cuba beckford@centis.edu.cu