Detection of mixed infections in sugarcane genotypes from Cuba
ISubdirección de Fitomejoramiento. Instituto de Investigaciones de la Caña de Azúcar (INICA). Carretera CUJAE Km 2 1/2. Boyeros. La Habana. Cuba.
IIInstituto Cubano de Investigaciones de los Derivados de la Caña de Azúcar (ICIDCA-Sede Boyeros). Carretera CUJAE Km 2 1/2. Boyeros. La Habana. Cuba.
IIICentro Nacional de Sanidad Agropecuaria (CENSA). Autopista Nacional Km 23 ½ y Carretera de Tapaste. Apartado 10. San José de las Lajas. Mayabeque. Cuba.
IVCentro de Cibernética Aplicada a la Medicina (CECAM). Calle 146 Esq. 31 #3102. Playa. La Habana. Cuba. ]]>
RESUMEN
Los síntomas de amarilleamiento y clorosis presentan alta incidencia en el Banco de Germoplasma de la Caña de Azúcar de Cuba. El objetivo de este trabajo fue determinar su asociación con fitoplasmas, Xanthomonas albilineans (Ashby) Dowson, los virus del mosaico y de la hoja amarilla. Para ello se seleccionaron del Banco de Germoplasma aquellos genotipos que manifestaron síntomas de amarilleamiento y clorosis de forma sostenida durante el ciclo de vida del cultivo. Se diagnosticaron ambos virus empleando la técnica Reverso Transcriptasa-Reacción en Cadena de la Polimerasa (RT-PCR), mientras que X. albilineans y fitoplasmas fueron estudiados por PCR anidada. Del total de muestras, ocho resultaron positivas al virus de la hoja amarilla, tres al mosaico, ocho a fitoplasmas y nueve a X. albilineans. En el 76,2% de los genotipos se observó la presencia de al menos un patógeno y en el 42,8% de los casos se evidenció infección múltiple. Mediante el análisis de conglomerados jerárquicos se detectaron cuatro grupos con patrones de infección diferentes. Este estudio permitirá rescatar a través de métodos de saneamiento los genotipos infectados además contribuirá a perfeccionar los métodos de hibridación del Programa Cubano de Mejoramiento Genético del cultivo.
Palabras clave: Saccharum spp., virus, fitoplasmas, Xanthomonas albilineans.
ABSTRACT
Yellowing and chlorosis were observed among the symptoms with higher incidence in the Cuban Germplasm Bank of Sugar Cane. The aim of this study was to determine whether these symptoms were associated with the presence of phytoplasmas, Xanthomonas albilineans (Ashby) Dowson as well as with sugarcane mosaic and yellow leaf viruses. Those individuals showing yellowing and chlorosis during the whole crop life cycle were selected from the Cuban Germplasm Bank. The technique Reverse Transcriptase-Polymerase Chain Reaction (RT-PCR) was used to diagnose both viruses, and the nested PCR for X. albilineans and the phytoplasmas. Eight samples were evaluated as positive to Yellow Leaf Virus, three to Mosaic Virus, eight to phytoplasmas and nine to X. albilineans. From the total of samples, 76,2% were infected with, at least, one pathogen and 42,8% presented multiple infections. By using cluster analysis, four groups were detected with different infection patterns. This study will allow recovering of infected genotypes by sanitation methods, in addition to contribute to the improvement of hybridization methods for the Breeding Program of this crop in Cuba.
Key words: Saccharum spp., virus, phytoplasmas, Xanthomonas albilineans.
]]>
INTRODUCCIÓNEl Banco de Germoplasma de la Caña de Azúcar de Cuba cuenta con 3 332 individuos entre ellos: formas originales de Saccharum, géneros afines, F1 interespecíficos de Saccharum, híbridos y otros. Uno de los principales síntomas determinados son clorosis y amarilleamiento (1) que pueden estar enmascarando la presencia de los virus del mosaico y de la hoja amarilla de la caña, fitoplasmas, Xanthomonas albilineans (Ashby) Dowson, entre otras (2, 3, 4).
El virus del mosaico de la caña de azúcar (VMCA), perteneciente a la familia Potyviridae, provoca zonas decoloradas y amarillentas en la lámina foliar (5). Estos virus son responsables de importantes pérdidas en los rendimientos azucareros. Actualmente, en Cuba, el VMCA se encuentra erradicado de las áreas de producción, sin embargo, se debe mantener la vigilancia fitosanitaria ya que en los centros de pruebas de resistencia a esta enfermedad se han encontrado aislados virales con variaciones en su patogenicidad (6).
Los síntomas de amarilleamiento foliar de la caña de azúcar pueden ser causados por un virus de la familia Luteoviridae, como el virus de la hoja amarilla de la caña azúcar (VHACA). En 1999 se informó su existencia por primera vez en Cuba (7) pero actualmente se desconoce su incidencia y distribución. Las plantas enfermas pueden mostrar amarilleamiento intenso en el nervio central aún cuando la lámina esté verde; también, acortamiento de los entrenudos y necrosis de las hojas viejas, no obstante, estos síntomas también pueden deberse a factores ambientales (4, 8). Por ello el diagnóstico visual provoca sesgos en la identificación de la enfermedad (9, 10).
Otra causa de amarilleamiento es la infección con fitoplasmas (3, 11), la que fue informada por primera vez en Cuba en 1999 (12), estableciéndose las regiones centrales y del Este de Cienfuegos como las más afectadas en el país (3). En esa ocasión se encontró que el subgrupo 16SrI-A del Grupo del Amarilleamiento del Áster era el que predominaba y desde entonces se ha informado la presencia de este patógeno asociado a plantas asintomáticas y sintomáticas (3).
La escaldadura foliar, causada por el patógeno X. albilineans, aunque se informó su presencia en Cuba en 1978, estuvo latente hasta inicios de 1998, época en que la enfermedad se manifestó de forma agresiva debido a la presencia de los serovares I y III (13, 14). Esta puede cursar por cuatro fases, que van desde asintomática, clorosis, hasta la muerte del plantón (14). Actualmente en el país, la escaldadura se comporta de forma variable en cuanto a sintomatología y patogenicidad, lo que se atribuye a la susceptibilidad mostrada por las variedades comerciales y/o a posibles variaciones intraespecíficas de la bacteria, sin descartar los cambios ambientales (resultados no publicados).
Las enfermedades mencionadas por sí solas causan grandes estragos y pérdidas productivas, y cuando se combinan los daños suelen ser mucho mayores. Hasta la fecha, se han realizado varios estudios encaminados a la búsqueda de infecciones mixtas causantes de: cambios en la patogenicidad (15, 16, 17), sintomatología (9, 16) y manifestaciones, según la época del año (17).
El objetivo de este trabajo fue determinar, mediante métodos de diagnóstico molecular, los fitopatógenos asociados a los genotipos de la Colección del Banco de Germoplasma de la Caña de Azúcar que presentan síntomas de clorosis y amarillamiento de forma sostenida en el ciclo de vida del cultivo.
Material vegetal: ]]>
Se seleccionaron 21 genotipos de la Colección del Banco de Germoplasma de la Caña de Azúcar de Cuba, ubicado en la provincia de Matanzas, que manifestaron síntomas de amarilleamiento y clorosis sostenidos durante el ciclo de vida del cultivo (B34104, CP31-294, RB80-6043, Q124, C97-105, My645, C87-260, Laica 96, Java 51, CSG403-92, B42231, C91-81, Ja64-20, Ja64-19, C120-78, C87-51, B6368, C323-68, C86-12, C90-530 y C86-156). Los síntomas fueron determinados según la escala propuesta por Jorge et al. (1). Se colectó la hoja (+1) de plantas con nueve meses de edad. Se realizó el diagnóstico molecular para la detección de X. albilineans, VMCA, VHACA y fitoplasmas.Diagnóstico de microorganismos:
X. albilineans: Se maceraron 100mg de material vegetal, se adicionaron 100µL de agua libre de nucleasas y se trató térmicamente a 100oC (10 min). Se tomó 1µL de este material para realizar la PCR anidada siguiendo el procedimiento utilizado por Díaz (13). Se realizó una primera reacción con los cebadores XF3/XR3 (13). Posteriormente una segunda amplificación con los cebadores XF4/XR4 (13), tomando 1µL (10ng) del producto de la primera amplificación. En ambas reacciones se empleó el mismo programa: 95oC (4min), 94oC (30s), seguido de 30 ciclos a 57oC (30s), 72oC (1min) y 10 min de extensión final a 72oC (13).
VMCA y VHACA: Para la identificación de estos dos virus se utilizó la RT-PCR. Para la obtención del ARN total se partió de 200mg de tejido de la lámina de la hoja de caña de azúcar macerados en nitrógeno líquido, utilizando el juego de reactivos RNeasy® Plant Mini Kit. A partir de 2µL de este se sintetizó el ADNc utilizando el kit RT (Promega), con Random Primers como cebadores y la enzima reverso transcriptasa AMV RT (HC), según recomendaciones del fabricante.
Para identificar la presencia del VMCA se utilizó el procedimiento descrito por Marie-Jeane et al. (18) con los cebadores específicos oligo 1n/oligo 2n que amplifican el segmento de la proteína de la cápsida. Se partió de 25ng de ADNc. El programa de reacción utilizado fue el siguiente: 50oC por 30 min, 95oC por 15 min, seguido de 30 ciclos a 94oC (1min), 55oC (1min) y 72oC (30s), seguido de una extensión final de 72oC por 10 min (18).
Para la detección del VHACA se partió de 1,5µL de ADNc (25ng). La reacción de amplificación se realizó con los cebadores YF1/YR1 propuestos por Girard et al. (19). Se utilizó el siguiente programa de reacción: 45oC por 45 min, 95oC por 2 min, seguido de 35 ciclos: 95oC por 30 seg, 61oC por 45 seg y 72oC por 1 min, seguido de una extensión final de 72oC por 10 min.
Fitoplasmas: Para la detección de fitoplasmas se utilizó la PCR anidada combinada con RFLP/ Hae III (11). Se tomaron 200 mg de la lámina de la hoja, se maceraron en nitrógeno líquido y se procedió a extraer el ADN utilizando el juego de reactivos Wizard Genomic DNA purification Kit (Promega). Posteriormente, se realizó la PCR anidada. Se partió de 25ng de ADN para realizar la primera reacción de amplificación, utilizando los cebadores P1/P7 (20, 21) con el siguiente programa: 95oC (4min), seguido de 30 ciclos: 95oC (30s), 53oC (75s) y 72oC (90s), y de una extensión final de 72oC (10min). Para la segunda reacción se utilizaron 25ng del producto de la primera amplificación, se usaron los cebadores R16F2n/R16R2 (22) con el siguiente programa 95oC (4min), seguido de 35 ciclos: 94oC (30s), 56oC (1min) y 72oC (2min), y una extensión final de 72oC por 10 min (11). Posteriormente, se realizó digestión con la enzima de restricción HaeIII al producto de la segunda reacción, según recomendaciones del fabricante (SIGMA).
Todos los productos de las PCR se aplicaron en gel de agarosa al 1%, se tiñeron con bromuro de etidio (0,5µg.ml-1), los productos obtenidos se visualizaron en un transiluminador; de acuerdo a lo descrito por Sambrook et al. (23).
Análisis estadístico:
Los genotipos de caña de azúcar fueron agrupados de acuerdo a la presencia/ausencia de infección por los diferentes patógenos (VHACA, VMCA, X. albilineans y fitoplasmas), mediante un Análisis de Conglomerado con el método UPGMA (24) y la distancia DSSI específica para datos binarios que proviene del coeficiente de similitud de Sokal y Sneath (CSSSI): ]]>
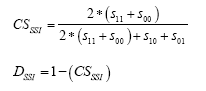
S00: Cantidad de agentes patógenos que infectan a dos cultivares dados de caña de azúcar.
S11: Cantidad de agentes patógenos que infectan dos cultivares dados de caña de azúcar.
S10 y S01: Cantidad de agentes patógenos que infectan a un cultivar de caña de azúcar pero no a otro, en un sentido u otro.
Para el análisis estadístico se empleó el software R versión 2.12.0. (25).
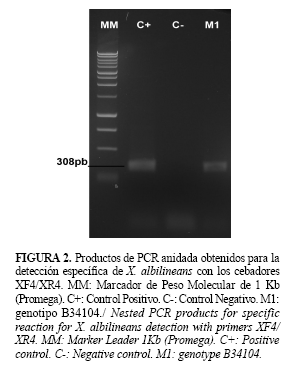
Se determinó que más del 75% de los 21 genotipos evaluados estaban infectados con al menos uno de los patógenos estudiados (Tabla 1). De ellos, ocho con VHACA y tres con VMCA (Fig. 1), nueve con X. albilineans (Fig. 2) y ocho con fitoplasmas (Fig. 3). Se encontraron cinco genotipos con ausencia de los cuatro microorganismos (23,8 %). Se observó además, que nueve del total de individuos tenían infecciones mixtas, para un 42,8% (Tabla 1).
Asimismo, se encontró que todas las plantas positivas al VMCA mostraron una infección concomitante con el VHACA; por lo que este virus (VMCA) no se encontró en infección simple. Por otra parte, solo dos de las ocho muestras infectadas con el VHACA tuvieron infección simple (25%) (Tabla 1). ]]>
El análisis mediante RFLP/ Hae III de las muestra positivas a fitoplasmas (Figura 3), evidenció que las mismas correspondían al subgrupo 16SrI-A del Amarilleamiento del Áster (resultados no mostrados).El análisis de conglomerados jerárquicos reveló una división clara en dos grupos, G0 y G1 (Fig. 4). El primero (G0) se pudo subdividir a su vez en dos subgrupos relevantes, G2 y G3.
G1: Es el grupo más numeroso e incluyó 13 genotipos: cinco no afectados por ninguna de las enfermedades estudiadas (Ja64-20, C87-51, C90-530, Java 51, C87-260), tres simultáneamente infectados por X. albilineans y fitoplasmas (RB80-6043, Ja64-19, C120-78), cuatro por X. albilineans (C97-105, B6368, C323-68, C86-156) y uno por fitoplasmas (C86-12) (Figura 4). Este grupo se distingue por el hecho de tener una baja cantidad de pruebas con resultados positivos, 21,1% en total (de cada 100 pruebas de diagnóstico, 21 fueron positivas para X. albilineans y/o fitoplasmas).
G2: contiene seis cultivares afectados por virus, sea VHACA o VMCA y/o por fitoplasmas. Este grupo se distingue por el hecho de tener una mediana cantidad de pruebas con resultados positivos, 41,6 % en total.
G3: Grupo que incluye sólo dos cultivares infectados con múltiples patógenos. B34104 se distinguió de manera negativa, pues estaban presentes en él todos los patógenos estudiados (virus, X. albilineans y fitoplasmas), seguido en este sentido de Q124, que estaba infectado con todos los patógenos excepto VMCA. Este grupo sobresale por el hecho de tener una alta cantidad de pruebas con resultados positivos, 87,5 % en total.
G0: Es un gran grupo que incluye a ocho cultivares que se destacan por estar infectados con los virus estudiados y/o con fitoplasmas o por ser estar infectados con casi todo los patógenos estudiados.
Muchas enfermedades que afectan a la caña de azúcar cursan en alguna etapa de la infección expresando síntomas de clorosis y amarilleamiento. Las estudiadas en este trabajo forman parte de este grupo y son responsables de grandes pérdidas en la industria azucarera a nivel internacional. Varios autores plantearon que cuando las plantas se infectan simultáneamente por mosaicos y amarilleamiento foliar, entre otras enfermedades, su crecimiento y producción se reducen de modo más severo que cuando son infectadas solo por uno de estos patógenos (2, 16).
En el presente trabajo se observó que el 42,6% de las muestras estaban colonizadas por más de un patógeno, lo que representa un alto porcentaje de infección (cercano al 50%) teniendo en cuenta que la planta una vez infectada puede desarrollar resistencia sistémica adquirida mediada por ácido jasmónico, respuesta que generalmente la protege contra una segunda infección (26). No obstante, el proceso de infección es muy complejo, pues depende también de otros factores como: el estadío de la enfermedad primaria, la predisposición genética a una infección secundaria, posible estrés abiótico, entre otros (10, 15, 26). Por otra parte, se ha observado que los efectos sinérgicos que se producen como resultado de una infección mixta, unidos a la interacción con factores abióticos, pudieran explicar también el incremento en la severidad del amarilleamiento foliar (16).
X. albilineans resultó ser el microorganismo de mayor frecuencia en las muestras tomadas, y se encontró asociado a infecciones simples en mayor número de genotipos (Tabla 1), manifestando síntomas similares a los hallados en plantas con infecciones múltiples, lo que enfatiza la importancia de contar con métodos de diagnóstico como los empleados, que eliminan el sesgo provocado por la manifestación de los síntomas visuales. ]]>
También, se apreció que cinco de los genotipos que expresaban síntomas de amarilleamiento y clorosis no se encontraban infectados por ninguno de los patógenos estudiados, lo que concuerda con lo planteado por Viswanathan et al. (2), acerca de la multifactorialidad de eventos que provocan estos síntomas, entre los que se encuentran factores bióticos y abióticos, los que pudieron estar incidiendo en el banco de germoplasma.Además se evidenció que el subgrupo de fitoplasmas encontrado se correspondía con el 16SrI-A del Grupo del Amarilleamiento del Áster, lo que concuerda con resultados previos que plantearon que en este Banco de Germoplasma el 95% de los casos de fitoplasmas tenían un 99% de similitud con la secuencia intergénica del ARN 16/23S del fitoplasmas que causa amarilleamiento del perejil, en Alberta, Canadá (3, 11).
La presencia mayoritaria de infección mixta de VMCA y VHACA pudiera deberse al hecho de que los virus penetran por heridas causadas por vectores o por daños mecánicos en los cultivos, de manera que, al haber daño penetró no solo un virus, sino varios microorganismos. Elemento a tener en cuenta a la hora de evaluar la presencia viral; por lo que una vez detectado un virus, es más probable, según nuestros resultados, encontrar una segunda infección. Todo ello demuestra la necesidad de buscar estos virus en el banco de germoplasma para evitar que se propaguen a través de la semilla botánica en los lotes de cruzamiento.
Los cuatro conglomerados observados pueden ser evidencia de una tendencia a la interacción entre determinados patógenos cuando colonizan un cultivar dado y/o de mecanismos biológicos comunes o distintivos de infección. Así vemos que el grupo G1 incluye a cultivares infectados con X. albilineans y/o fitoplasmas (Fig. 4); en cambio, el G2 incluye básicamente a los cultivares infectados por virus y en algunos casos por fitoplasmas. Esto puede ser consecuencia de que la susceptibilidad a fitoplasmas comparte características comunes con la suceptibilidad a X. albilineans y a los virus estudiados. Además, se observa una tendencia creciente del G1 al G3 a la presencia de infecciones mixtas; en G1 se observaron tres cultivares de un total de 13 con la infección de dos patógenos, en G2 cuatro de seis cultivares también mostraron infección con dos patógenos y en G3 los dos cultivares de este grupo presentaron infecciones mixtas de tres o de los cuatro patógenos estudiados (Fig.4).
En general, estos resultados permitieron conocer las causas que provocaron amarilleamiento y clorosis en genotipos del Banco de Germoplasmas de la Caña de Azúcar; además permite brindar a los mejoradores una herramienta de gran valor a la hora de manejar en los progenitores, la herencia de las resistencias a enfermedades en los programas de cruzamiento. Por otra parte, estos resultados sugieren la necesidad de aplicar métodos de saneamiento a los materiales afectados, como es el caso del cultivo in vitro de los micromeristemos procedentes de los genotipos infectados por estos virus.
Se agradece por su incondicional ayuda en el estudio de fitoplasmas a la Técnico Berta E. Piñol Pérez del Centro Nacional de Sanidad Agropecuaria.
REFERENCIAS
1. Jorge H, Jorge IM, Mesa JM, Bernal NA. Normas y Procedimientos del Programa de Fitomejoramiento de la Caña de Azúcar en Cuba. 2da Ed. Boletín Especial Cuba&Caña. 2011; 348p.
2. Viswanathan R, Balamuralikrishnan M, Karuppaiah R. Identification of three genotypes of sugarcane yellow leaf virus causing yellow leaf disease from India and their molecular characterization. Virus Genes. 2008;37(3):368-379.
3. Arocha Y, Jones P. Phytoplasma Diseases in Sugarcane and Papaya Crops in Cuba. Rev Protección Veg. 2006;21(3):137-148.
4. Rott P, Mirkov TE, Schenk S, Girard JC. Recent advances in research on Sugarcane yellow leaf virus, the causal agent of sugarcane yellow leaf. Sugar Cane International. 2008;26(3):18-22.
5. Viswanathan R, Karuppaiah R, Balamuralikrishnan M. Identification of new variants of SCMV causing sugarcane mosaic in India and assessing their genetic diversity in relation to SCMV type strains. Virus Genes. 2009;39(3):375-386.
6. La O M, Fernández E, González R, Mesa J, Zardón MA, Girard JC. Strain differentiation of sugarcane Mosaic Virus in Cuba by RT-PCR and direct sequenciation. En: Memorias del IX Simposio Internacional de Biotecnología Vegetal. Villa Clara. Cuba. 2010; 64p.
7. Aday OC, Díaz FR, García H, Barroso F. Comportamiento de genotipos de caña de azúcar, introducidos y cubanos, ante el síndrome de la hoja amarilla. Centro Agrícola. 2003;30(1):46-50.
8. Abu Ahmad Y, Costet L, Daugrois JH, Nibouche S, Letourmy P, Girard JC, et al. Variation in infection capacity and in virulence exists between genotypes of Sugarcane yellow leaf virus. Plant Dis. 2007;91:253-259.
9. Viswanathan R, Karuppaiah R, Malathi P, Ganesh Kumar V, Chinnaraja C. Diagnosis of Sugarcane yellow leaf virus in asymptomatic sugarcane by RT-PCR. Sugar Tech. 2009;11(4):368-372.
10.Grisham MP, Johnson RM, Zimba PV. Detecting Sugarcane yellow leaf virus infection in asymptomatic leaves with hyperspectral remote sensing and associated leaf pigment changes. J Virol Methods. 2010;167(2):140-145.
11.Arocha Y, López M. Candidatus Phytoplasma graminis' and `Candidatus Phytoplasma caricae', two novel phytoplasmas associated with diseases of sugarcane, weeds and papaya in Cuba. International Journal of Systematic and Evolutionary Microbiology. 2005;55:2451-2463.
12.Arocha Y, González L, Peralta EL, Jones P. First report of virus and phytoplasma pathogens associated with Yellow Leaf Syndrome of sugarcane in Cuba. Plant Disease. 1999;83:1171.
13.Díaz M. Escaldadura Foliar de la Caña de Azúcar en Cuba: caracterización, diversidad y diagnóstico molecular de su agente causal Xanthomonas albilineans Ashby (Dowson). Tesis presentada en opción al grado científico de Doctor en Ciencias Agrícolas. Universidad Agraria de La Habana. Cuba. 2000; 78p.
14.La O M, Llanos M, Jerez F, Sánchez B. Caracterización serológica de Xanthomonas albilineans para la obtención de material sano de caña de azúcar. Ciencias Biológicas. 2001;32(2):127-128.
15.Bharathi V, Kishan R, Nagamalleswari P. Mixed infection of sugarcane streak mosaic and sugarcane yellow leaf virus infecting sugarcane crops in A.P. India Sugar. 2006;56:37-42.
16.Singh D, Tewari AK, Rao GP, Karuppaiah R, Viswanathan R, Meenasksi A, et al. RT-PCR/PCR analysis detected mixed infection of DNA and RNA viruses infecting sugarcane crops in different state of India. Sugar Tech. 2009;11(4):373-380.
17.Ryan RP, Vorhölter FJ, Potnis N, Jones JB, Van Sluys MA, Bogdanove AJ, et al. Pathogenomics of Xanthomonas: understanding bacterium-plant interactions. Nat Rev Microbiol. 2011;9(5):344-355.
18.Marie-Jeanne V, Ioos R, Peyre J, Alliot B, Signoret P. Differentiation of Poaceae Potyviruses by reverse transcription polymerase chain reaction and restriction analysis. J Phytopathol. 2000;148:141-151.
19.Girard JC, Fernandez E, Daugrois JH, Roques D, Roumagnac P, Rott P. Genetic diversity of Sugarcane yellow leaf virus in a sugarcane selection plot in Guadeloupe (FWI). Proceedings of the 27th Congress of the International Society of Sugar Cane Technologists (ISSCT), Veracruz, Mexico. 2010; 9 p.
20.Deng S, Hiruki C. Amplification of 16S rDNA genes from culturable and non-culturable mollicutes. J Microbiol Methods. 1991;14:53-61.
21.Schneider B, Cousin M, Klinkong S, Seemüller E. Taxonomic relatedness and phylogenetic positions of phytoplasmas associated with diseases of faba bean, sunhemp, sesame, soybean and eggplant. Plant Dis. 1995;102:225-232.
22.Smart C, Schneider B, Blomquist C, Guerra L, Harrison N, Ahrens U, et al. Phytoplasma specific primers based on sequences of the 16/23S rRNA spacer region. Appl Environ Microbiol. 1996;62(8):2988-2993.
23.Sambrook J, Fritsch EF, Maniatis T. Molecular Cloning: A Laboratory Manual. 2da Ed. Cold Spring Harbor Laboratory, New York, USA. 1989. 31-33p.
24.Jain AK, Murty MN, Flynn PJ. Data Clustering: A Review. ACM Computing Surveys. 1999;31(3):264-323.
25.R Development Core Team, R Foundation for Statistical Computing. R: A Language and Environment for Statistical Computing Vienna, Austria. 2010. http://www.R-project.org.
26.Vasiukova NI, Chalenko GI, Gerasimova NG, Valueva TA, Ozeretskovskaia OL. Activation of elicitor defensive properties by systemic signal molecules during the interaction between potato and Phytophthora. Prikl Biokhim Mikrobiol. 2008;44(2):236-240.
]]>
Recibido: 23-10-2011.
Aceptado: 4-3-2012.
*Autor para correspondencia: María L. La O. Subdirección de Fitomejoramiento. Instituto de Investigaciones de la Caña de Azúcar (INICA). Carretera CUJAE Km 2 1/2. Boyeros. La Habana. Cuba. Correo electrónico: lao@inica.minaz.cu. ]]>