- Persistente: significa que los síntomas están presentes
- Más de cuatro días a la semana. y durante más de cuatro semanas.
- Leve: significa que no están presentes ninguna de las circunstancias siguientes:
Trastornos del sueño.
Deterioro de las actividades diarias de ocio y deportivas.
Impedimento de la asistencia a la escuela o al trabajo.
Síntomas molestos.
- ]]>
Moderada/grave: significa que están presentes una o más de las circunstancias siguientes:
Trastornos del sueño.
Deterioro de las actividades diarias de ocio y deportivas.
Impedimento de la asistencia a la escuela o al trabajo,
]]>Síntomas molestos.
Pacientes sensibles al alergeno D. pteronyssinus se demostró por prueba de punción cutánea positiva (diámetro del promedio del habón > 3 mm) con el extracto alergénico Valergen-DP a 20 000 UB/ml, prueba de provocación con el extracto Valergen DP a evaluar a diferentes dosis (2, 20, 200,2000UB/ml) y así confirmar de que la prueba cutánea positiva es clínicamente relevante y no es tan sólo una demostración de alergia latente y conteo de eosinófilos mayor al 20 %.9
Criterios de inclusión
- Pacientes alérgicos riníticos con una historia clínica positiva de síntomas alérgicos provocados por el polvo de casa.
- Prueba cutánea positiva con el extracto alergénico de D. pteronyssinus, Valergen DP a 20 000 UB/ml.
- La citología de secreciones nasales positiva para eosinófilos, por encima del 20 %. ]]> Edad entre 18-45 años de edad.
- Los pacientes que expresen su consentimiento por escrito.
Criterios de Exclusión
- Pacientes tratados previamente con inmunoterapia con extractos alergénicos en los dos años anteriores.
- Pacientes que tengan asociado un asma persistente severa.
- Pacientes con diagnóstico de enfermedad autoinmune.
- Eczema severo generalizado.
- Paciente con el diagnóstico de enfermedad tumoral. ]]> Pacientes con tratamiento con beta-bloqueadores.
- Enfermos con trastornos psiquiátricos.
- Alteraciones estructurales a nivel nasal.
- Enfermedades respiratorias en las últimas cuatro semanas.
- Cirugía nasal en las ocho semanas previas.
- Falta de cooperación del paciente.
- Embarazo y lactancia.
- Pacientes donde el uso de la adrenalina este contraindicado (Hipertensión arterial).
Criterios de interrupción del tratamiento
]]>- Pacientes con reacciones sistémicas a la primera dosis del esquema de
tratamiento.
- Pacientes que no respondan adecuadamente a la vacunación al presentar eventos adversos focales sistémicos reincidentes.
- Durante la inmunoterapia desarrollen alguna de las condiciones descritas en los criterios de exclusión.
Las variables de respuesta (para determinar la eficacia) fueron las siguientes: puntuación por síntomas clínicos, puntuación por consumo de medicamentos, reactividad cutánea, provocación nasal y citología de secreciones nasales.
]]>La seguridad se midió a través del comportamiento de los eventos adversos.
El sistema SPSS 12.0 para Windows fue utilizado para la entrada de los datos y procesamiento de los mismos.
Se realizó el análisis estadístico en dos momentos a los seis meses y al año.
Se calculó la mediana de cada una de las variables en cada grupo y sus respectivos intervalos de confianza del 95 %. El comportamiento de todas las variables se comparó entre el grupo tratado y el control empleando la prueba no paramétrica de Mann-Whitney U, para comparar medianas, comprobando de esa forma la hipótesis del estudio. La comparación dentro de cada grupo con respecto a los niveles basales pretratamiento se realizó mediante la prueba no paramétrica de Wilconxon con pares signados para muestras pareadas. En el caso de la reactividad cutánea, se calculó la media geométrica y el intervalo del 95 % de confianza, para los valores finales e iniciales del tratamiento.
RESULTADOS
]]> Al comparar el comportamiento de los síntomas. Se observó que en el grupo con tratamiento activo hubo una disminución significativa en la media de los síntomas durante el transcurso del tratamiento, de 178.50 al inicio a 1,50 en la medición final y en el grupo con tratamiento placebo se presentaron aumentos significativos en los valores de las medias, de 112. 85 basal a 130. 55 al terminar el estudio. En el grupo con tratamiento activo las disminuciones promedio fueron de 156.3 en los síntomas basales con un intervalo de confianza para el 95 % de (IC, 142.9; 169.7). (Gráfico 1)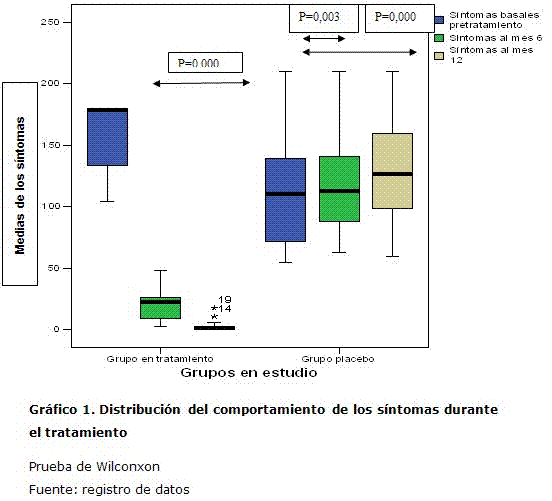
Al evaluar el uso de medicamentos basales, con estos mismos a los 6 y 12 meses, en el grupo con tratamiento activo se dieron disminuciones significativas a medida que avanzó la inmunoterapia, no así en el grupo placebo que se observaron aumentos significativos en el consumo de medicamentos. En los medicamentos usados la disminución promedio fue de 43.5 con un intervalo de confianza para el 95 % de (IC, 36.6:50.8). (Gráfico 2)

Según el comportamiento de los valores de la prueba cutánea. Se encontró reducción significativa en la media de las determinaciones del grupo activo, de 7.00 a 4. 40 en la última medición, lo que indicó una disminución en la sensibilización alergeno específica. Esta variable no se comportó igual en el grupo placebo donde la media aumentó de 5,40 a 6.60. Los valores de la reacción cutánea disminuyeron como promedio en un 2.6 % con un intervalo de confianza para el 95 % de (IC, 2.3 %:2.9 %). (Gráfico 3)

Con respecto a la vacunación se presentaron cuatro eventos adversos, tres fueron sistémicos ligeros y se presentaron en la tercera semana del tratamiento para un 15 %, y uno fue inespecífico en la segunda semana para un 5 %.Todos fueron inmediatos sin peligro para la vida, no se presentó eventos adversos focales, sistémicos severos, ni sistémicos generalizados, durante el período de inmunoterapia. Los pacientes que presentaron estos eventos adversos continuaron tratamiento sin recaídas. (Gráfico 4)

DISCUSIÓN
En investigaciones realizadas en otros países como es el estudio farmacoeconómico de Renato Ariano10 en Italia, al evaluar el comportamiento de los síntomas en dos grupos, uno con inmunoterapia y otro con placebo, se observó la existencia de una diferencia significativa a favor del grupo que recibió inmunoterapia a partir del primer año de la administración de ésta. Al revisar el metanálisis realizado por el Dr. Wilson et al, 11 donde se incluyeron 32 ensayos y 959 pacientes, se aprecia una reducción significativa de los síntomas (DME -0,34; intervalo de confianza del 95 %: 0,69 a -0,15; p = 0,002). En Cuba está el trabajo del Dr. Olimpio Rodríguez Santos12 en la provincia de Camagüey, donde se observó una disminución en la asistencia a los cuerpos de guardias por exacerbación de la enfermedad. A criterio de la autora, esto esta dado, porque a medida que avanzamos en este proceder, el paciente se va desensibilizando, iniciando con la degranulación paulatina de las células cebadas, que provoca reducción en la sintomatología, al exponerse el individuo al alergeno.
En el metanálisis realizado por el Dr. Wilson11 en 2003, hay una disminución del uso de medicamentos de un 43 %. Esto coincide con otras investigaciones como la del Dr. Domínguez 13 en México, que resultó ser efectiva al reducir el uso de medicamentos. El Dr. Marogna 14 en Italia, observó similares efectos a los antes expuestos y la existencia de una diferencia significativa en favor del grupo que recibe inmunoterapia a partir del primer año de la administración de esta. En cambio, el Dr. Renato10 en su estudio encuentra que a partir del tercer año es que la diferencia alcanza importancia estadística. Por su parte, la revisión de todos los estudios realizados hasta octubre del 2005, de la Dra Cox, et al, 15 muestra que parece haber una tendencia a mejor la eficacia con dosis más altas en la inmunoterapia, sin embargo se encontraron dos ensayos clínicos que con el uso de dosis bajas mostraron eficacia en la disminución del uso de medicamentos.4 En la investigación se constató que a pesar de que la dosis administrada no fue tan alta como la observada por otros estudios hubo una reducción importante en el consumo de medicamentos por los pacientes, relacionado con la mejoría de los síntomas a medida que avanzamos en la inmunoterapia.
]]>Al analizar el comportamiento de la reactividad cutánea, se consultaron varias bibliografías como la de Ko-Huang Lue16 de la universidad y hospital Taichung en Taiwán, que demostraron que se produce una negativización de la prueba cutánea en pacientes tras el uso de la inmunoterapia. En el estudio realizado por Beato17 en el Hospital Universitario de Getafe, Madrid, se encuentra el 53 % de negativización de los valores del prick test con clínica negativa. Por su parte existen otras literaturas como el metanálisis realizado por Wilson, et al, 11 donde este dato no es tan evidente pues no hay disminuciones significativas, pero en cambio refieren una mejoría clínica de los pacientes. En el estudio se obtuvo una disminución en los valores del prick, lo cual coincide con lo antes expuesto y demuestra la eficacia de esta modalidad terapéutica como hiposensibilizante y en la inducción de tolerancia por la vía oral.
Estudios más recientes muestran como la actuación de esta modalidad terapéutica sobre el sistema inmune es dosis y tiempo dependiente, con incrementos en los niveles de IgG4 específica IgA. 18 Todos coinciden que estos cambios están en relación con las transformaciones inmunológicas que tienen lugar en el paciente al iniciar la inmunoterapia y con los posteriores beneficios que reporta para la evolución de su desorden alérgico. 18, 19
Se pudo apreciar el número de eventos adversos en relación con las dosis aplicadas fueron ínfimos, no presentamos ningún paciente con evento sistémico severo durante la inmunoterapia, lo cual avala la seguridad de esta modalidad terapéutica. El motivo por el cual los pacientes no presentaron eventos adversos y la buena aceptación del medicamento, esta avalado por los experimentos que se han realizado con extractos alergénicos marcados con isótopos radiactivos administrados por vía sublingual. Donde no se observó ninguna absorción en la cavidad oral del alergeno marcado, lo que tranquiliza, en el sentido de no temer por eventos adversos sistémicos; Además, se constató que una parte del alergeno marcado persistía en la región sublingual durante al menos 48h lo que hace reflexionar al autor, que esta persistencia juega un cierto papel en el mecanismo de acción de la ITSL, y que tendrá lugar una lenta absorción y procesamiento del alergeno localmente retenido a través del sistema inmune local.4, 20
CONCLUSIONES
Se observa disminución significativa de los síntomas, así como del uso de medicamentos en el grupo con tratamiento activo en relación al grupo placebo. La reactividad cutánea se reduce con el uso de la ITSL. No se producen eventos adversos fatales.
]]> REFERENCIAS BIBLIOGRÁFICAS
1. Hoz B, Cólas C, Rodríguez M, Grupo Freedom. Calidad de la vida en pacientes con rinitis alérgica: estudio comparativo con la hipertensión arterial en el ámbito de al atención primaria. An Sist Sanit Navar. 2009; 32(2):169-81.
2.Aguilar D. Rinitis alérgica. En: Mendez J, Huerta J, Bellanti JA, Ovilla R, Escobar A. Alergia: Enfermedad Multisistémica. Aspectos básicos y clínicos. 1ª ed. México: Editorial Panamericana; 2008.p.99-103.
3. Castro R, Álvarez M, Ronquillo M, Rodríguez J, García I, Gómez M, et al. Sensibilización a tres especies de ácaros en pacientes alérgicos de la zona costera de la ciudad de La Habana. Rev Alergia Mex. 2009; 56(2):31-5.
4.Larenas-Linneman D, Marco F, Enrique E. Inmunoterapia Sublingual. En: Mendez J, Huerta J, Bellanti JA, Ovilla R, Escobar A, editores. Alergia: Enfermedad Multisistémica. Aspectos básicos y clínicos. 1ª ed. México: Editorial Panamericana; 2008.p.411-7.
5. Neffer H, Solé D, Máspero J, Ortiz I, Cherrez I, Caballero F, et al. Rinitis alérgica en Latinoamérica. Manejo actual y estrategia para la adopción de guías de diagnóstico y tratamiento. Drugs of Today. 2009; 45(4):1-9.
6. Olaguibel M, Alvarez P. Efficacy of sublingual allergen vaccination for respiratory allergy in children. Concluions from one meta- analysis. J Investig Allergol Clin Immunol. 2005; 15(1):9-16.
7. Pham-Thi N, Scheinmann P, Fadel R, Combebias A, Andre X. Assessment of sublingual immunotherapy efficacy in children with house dust mite-induced allergic asthma optimally controlled by pharmacologic treatment and mite-avoidance measures. Pediatr Allergy Immunol. 2007; 18:47-57.
8. Lozano A, Croce V, Cavallo A, Bandín G, Bozzola M, García J, et al. Consenso nacional de rinitis alérgica en pediatría. Arch Argent Pediatr. 2009; 107(1):67-81.
9. Ferri NB, Sola PJ. Citología exfoliativa de la cavidad nasal. En: Negro J M, Alvarez MR, Buendía E, Amoros LM, Belchí J, Caballero L, et al, editores. Rinitis Alérgica Mecanismos y tratamiento. Barcelona: MRA ediciones; 2004.p.237-40.
10. Renato A, Patrizia B, Daniela T, Cristoforo I, Franco F. Pharmacoeconomics of allergen immunotherapy compared with symptomatic drug treatment in patients with allergic rhinitis and asthma. J Allergy Clin Immunol. 2006; 27(2):159-63.
11. Wilson R, Torres M, Durham S. Sublingual immunotherapy for allergic rhinitis: systematic review and meta-analysis. Allergy. 2005; 60:4-12.
12. Rodriguez O. Inmunoterapia Sublingual en rhinitis alérgica y asma en niños de dos a cinco años sensibilizados a ácaros. Rev Alergia Mex. 2008; 55(2):71-5.
13. Domínguez T, Hernández O, Santa A, Mendoza L. Eficacia clínica de la seguridad de la inmunoterapia sublingual con extractos estandarizados en el tratamiento del asma alérgica ocasionada por Dermatophagoides en la población mexicana pediátrica. Rev Sanid Milit [serie en Internet]. 2007 [citado 12 ago 2008]; 56(6):[aprox. 9 p.]. Disponible en: http://www.imbiomed.com/1/1/articulos.php?id_revista=16&id_ejemplar=129.
14. Marogna M, Tomassetti D, Bernasconi A, Colombo Massolo F, Rienzo Businco A, Canonica G, et al. Preventive effects of sublingual immunotherapy in childhood: an open randomized controlled study. J Allergy Clin Immunol. 2005; 101(2):206-11.
15. Cox LS, Larenas-Linneman D, Nolte H, Weldon D. Sublingual immunotherapy: a comprehensive review. J allergy Clin Immunol. 2006; 117:1021-35.
]]>16. Lue KH, Lin YH, Sun KH, Lu KH, Hsieh JC, Chou MC. Clinical and immunologic effects of sublingual immunotherapy in asthmatic children sensitized to mites: a double-blind, randomized, placebo-controlled study. Pediatr Allergy Immunol. 2006; 17:408-15.
17. Beato A, Ayala M, Molina Q, Comenero R, Sanz R. Inmunoterapia en la rinitis alérgica estacional. Revisión de 30 pacientes. Acta de otorrinolaringol Esp. 2005; 56:112-5.
18. Harold N. Inmunoterapia para alergenos ¿En dónde está ahora?. JACI. 2007; 119:769-77.
19. Passalasqua G, Guerra L, Fuamagali F, Canonca GW. Safety of sublingual inmunotherapy. Treat Respir Med. 2006; 5:225-34.
20. Passalacqua G, Valovirta E. Adverse effects associated with sublingual immunotherapy. En: Clinical allergy and immunology series. Allergens and allergen immunotherapy. 4 ed. New York: Editorial Informa Helthcare; 2008.p.469-75.
]]>Recibido: 5 de enero de 2011
Aprobado: 3 de mayo de 2011
Dra. Adianez Sugrañes Montalván. Email: cacho@finlay.cmw.sld.cu ]]>