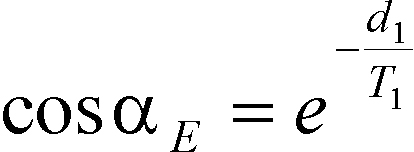
ARTÍCULO ORIGINAL
Resonancia magnética nuclear: nuevas aplicaciones en la cuantificación y la evaluación de intermediarios de vacunas basadas en polisacáridos
Nuclear Magnetic Resonance: new applications in the quantification and assessment of polysaccharide-based vaccine intermediates
Raine Garrido,* Herman Vélez, Vicente Vérez
Centro de Química Biomolecular, Ave. 21 y 200. Atabey, Playa, La Habana, Cuba.email: raine.garrido@cqb.cu
* Lic. en Química. Laboratorio de Análisis Espectroscópico.
RESUMEN
La resonancia magnética nuclear (RMN) constituye una fuerte alternativa para estudios estructurales, evaluación de identidad y cuantificación de ingredientes farmacéuticos activos (IFA). En las dos últimas décadas la aplicación de la resonancia magnética nuclear cuantitativa (RMNc) tuvo un creciente impacto en la cuantificación de compuestos, fundamentalmente orgánicos. Varios resultados obtenidos mediante la RMNc han ido creando un lugar para la técnica en la industria biofarmacéutica. La RMNc incluye experimentos de RMN con algunos parámetros modificados, con el objetivo de obtener señales cuantificables. Basada en algunos de los reportes más relevantes, la presente revisión aborda algunas de las aplicaciones de la RMN para vacunas basadas en polisacáridos o glicoproteínas. El trabajo hace especial énfasis en detallar algunos aspectos que caracterizan la RMNc, así como sus aplicaciones.
Palabras clave: RMN, análisis cuantitativo, vacuna, polisacárido.
ABSTRACT
Nuclear Magnetic Resonance has become the choice for structural studies, identity assays and simultaneous quantification of active pharmaceutical ingredient of different polysaccharide-based vaccine. In the last two decades, the application of quantitative Nuclear Magnetic Resonance had an increasing impact to support several quantification necessities. The technique involves experiments with several modified parameters in order to obtain spectra with quantifiable signals. The present review is supported by some recent relevant reports and it discusses several applications of NMR in carbohydrate-based vaccines. Moreover, it emphasizes and describes several parameters and applications of quantitative Nuclear Magnetic Resonance.
Key words: NMR, quantitative analysis, vaccine, polysaccharide.
]]> INTRODUCCIÓN
Breve reseña histórica del desarrollo de la resonancia magnética nuclear
La resonancia magnética nuclear (RMN) constituye una técnica con un amplio y reconocido espectro de aplicaciones en el campo del análisis estructural. Tuvo sus inicios a principios de la década de 1950, cuando se comercializaron los primeros espectrómetros para la obtención de espectros de protones, tras el descubrimiento en 1945 de la resonancia. Este fenómeno plantea que los núclidos sometidos a un campo magnético externo absorben radiación electromagnética en el orden de las radiofrecuencias. Como la frecuencia exacta de esta absorción depende del entorno químico de los núclidos, el espectro de señales de absorción de los mismos revela una valiosa información sobre la estructura de la molécula.
Con el desarrollo de la RMN transformada de Fourier (RMN-TF), desde comienzos de los años 1970, se aumentó la sensibilidad en los espectrómetros y posibilitó el registro rutinario de núclidos de poca abundancia natural como el 13C. Un desarrollo vertiginoso tuvo lugar desde ese entonces y hasta la actualidad (1). Una gran aplicabilidad en técnicas posteriores tuvo la introducción del concepto de transferencia de polarización, combinando la secuencia para el eco de spines, propuesta por Hahn en 1954. Así mismo, la aplicación de técnicas bidimensionales (2D-RMN) resuelve un número importante de interrogantes estructurales en el campo de las biomoléculas (2). Adicionalmente, las posibilidades teóricas de la técnica para la cuantificación de compuestos, desde la década de 1960, crearon las bases para el desarrollo de la resonancia magnética nuclear cuantitativa (RMNc) (3). Con la utilización de gradientes de campo magnético (Pulse Field Gradient, PFG) se alcanzó una reducción importante en los tiempos de adquisición de la señal de resonancia, también conocida como caída de inducción libre (FID, siglas en inglés) y permitió para el caso de las moléculas en disolución, a través de la técnica DOSY (Diffusion Order SpectroscopY), la medición de la difusión a lo largo de los tres ejes (X,Y y Z), así como la dirección y velocidad de flujo (4).
Un número de técnicas desarrolladas en la década de 1990 extendió el empleo de experimentos de 2D-RMN como el TOCSY (TOtal Correlation SpectroscopY) y el ROESY (Rotating frame Overhauser Enhancement SpectroscopY), empleados para evaluar los acoplamientos escalares y sus homólogos dipolares entre protones, respectivamente, a experimentos híbridos mayormente conocidos como 3D-RMN (4). Esto favoreció el avance de los estudios de los sitios de interacción entre biomoléculas.
Con la introducción de la triple resonancia se incrementaron los estudios estructurales en las ciencias biológicas. De esta manera fue posible la obtención de una mayor información de núclidos como el 15N y el ya mencionado 13C (4). Lo anterior fortaleció el diseño acelerado del conjunto de técnicas que constituyen la base para la RMN de proteínas, incluso permitió el desarrollo de accesorios para espectrómetros, especializados en este tipo de estudio, como las sondas triple _ inversa (1H, 13C y 15N). Para el 2002, Kurt Wuttrich (Suiza) había recibido el premio Nobel de Química por sus aportes al estudio de la estructura tridimensional de las biomoléculas. El desarrollo alcanzado por la técnica permite su empleo en la evaluación cualitativa y cuantitativa de diferentes tipos de compuestos (5).
Algunas aplicaciones de la RMN para la evaluación de intermedios en vacunas
Existen numerosas vacunas comerciales y candidatos vacunales multivalentes basados en polisacáridos que protegen contra varias bacterias. Los análisis asociados a los procesos de producción y control de la calidad de estas vacunas resultan extremadamente complejos y en muchos casos la RMN se encuentra insertada entre las técnicas comúnmente empleadas (6).
Desde hace más de 30 años comenzaron a aparecer un número creciente de publicaciones con asignaciones de los núclidos de protones y carbono de muchos de los carbohidratos que hoy conforman las vacunas licenciadas para uso humano basadas en polisacáridos (7).
La aplicación de la RMN como método de caracterización para vacunas, con el ingrediente farmacéutico activo (IFA) de naturaleza glicosacarídica o glicoproteica es amplia (8, 9). La vacuna multivalente antineumocócica Pneumovax® 23 emplea un método por RMN para confirmar la identidad estructural de cada uno de los polisacáridos capsulares empleados en el IFA (10).
]]> La selectividad y la reproducibilidad de los métodos de RMN empleados para este fin resulta superior a la de prácticas usuales, como los análisis espectrofotométricos. Ensayos similares son empleados para la evaluación de otros polisacáridos bacterianos como: el polisacarido Vi de Salmonella enterica serovar typhi, los serogrupos A, C, Y y W135 de Neisseria meningitidis, los serotipos 5 y 8 de Streptococcus aureus y al serotipo b de Haemophilus influenzae (9, 11).Con el licenciamiento en el 2004 de la primera vacuna obtenida por síntesis química (Quimi-Hib) contra el serotipo b de Haemophilus influenzae, la RMN presentó nuevas posibilidades para la obtención y evaluación de los intermediarios del IFA (12). Como parte de la obtención del IFA los procesos de síntesis cuentan con varios pasos donde se aplican las posibilidades de la RMN de 1H y de 13C como control de proceso y control de la calidad de los intermedios de síntesis y los reactivos residuales (13). La evaluación de los conjugados monovalentes de un candidato vacunal contra los serogrupos A, C, Y y W135 de Neisseria meningitidis también encontraron solución en la técnica (14). Mediante el empleo de RMN de protones los autores compararon el patrón de señales de varios lotes de los cuatro glicoconjugados.
El polisacárido común de la pared celular de los neumococos (PoliC) es uno de los contaminantes más frecuentes en vacunas neumocócicas. El mismo constituye una impureza polisacarídica resultante de los procesos de fermentación para la obtención de los polisacáridos capsulares de Streptococcus pneumoniae.
La caracterización estructural de esta impureza fue realizada a través de la combinación del experimento de correlación (Heteronuclear Multiple Quantum Coherence, HMQC), para evaluar el acoplamiento escalar heteronuclear, la RMN de 13P y de 1H (15). Este trabajo permitió la selección de la señal correspondiente al sustituyente de fosfocolina como huella reveladora de la presencia de esta impureza.
La combinación de varias técnicas de 2D-RMN son usadas para numerosos estudios estructurales sobre la composición de los polisacáridos capsulares empleados en vacunas. Recientemente se completó a través de experimentos de correlación heteronuclear (Heteronuclear Single Quantum Coherence, HSQC) la evaluación de las señales de protones, carbonos y el núcleo de fósforo del polisacárido capsular correspondiente al serogrupo X de Neisseria meningitidis (Fig. 1) (16). Análogamente, un estudio basado en los experimentos de correlación TOCSY para acoplamiento escalar de protones y HSQC para acoplamiento 13C-1H, permitió la evaluación satisfactoria del polisacárido del serotipo 1 de Streptococcus pneumoniae (17).
Una alternativa por RMN de protones combinada con métodos estadísticos fue evaluada para la clasificación de varios grupos de bacterias aisladas de pacientes (18). El método propuesto se comparó con los métodos convencionales empleados para estos propósitos con resultados satisfactorios.
La relevancia de los residuos O-acetilo y fosfoglicerol en la efectividad de la respuesta inmunológica inducida por un conjugado monovalente del serotipo 18c Streptococcus pneumoniae fue evaluada mediante un estudio asistido, entre otras, por técnicas de 2D-RMN tales como: HMQC sin desacoplamiento durante la adquisición y TOCSY (19).
Sin embargo, la RMN desde sus inicios se ha visto más restringida para las evaluaciones cuantitativas de principios activos e impurezas de vacunas. De hecho, en los años de 1960, debido a la marcada variabilidad que mostraban los reportes, se estimó que la RMN no sería factible para evaluaciones cuantitativas.
Por factores como la diferencia entre los tiempos de relajación de los núclidos analizados, los experimentos de rutina no son capaces de concentrar cuantitativamente toda la información del sistema que se analiza. El desarrollo de numerosas herramientas para la obtención de los espectros ha ido corrigiendo lo anterior y haciendo posible el desarrollo de la RMNc (20).
Resonancia magnética nuclear cuantitativa
]]> Consideraciones generalesVarios métodos han ido ocupando un lugar como parte de las baterías de análisis desarrolladas para los controles de calidad y proceso de los productos intermedios en la producción de vacunas, en dependencia de la complejidad estructural de cada producto y la disponibilidad de equipamiento analítico en cuestión. Generalmente, son muy utilizados los métodos basados en la espectrofotometría. Estos incluyen la transformación cuantitativa de los productos de interés analítico para obtener un derivado con un máximo de absorbancia sin interferencias en las regiones ultravioleta y visible del espectro. Estos métodos se enfocan en la evaluación de monosacáridos específicos (pentosas, hexosas, desoxi-azúcares, ácidos urónicos, etc.) y grupos funcionales (21, 22).
En muchos casos el producto de interés se encuentra mezclado o impurificado con otros de igual naturaleza, tales como isómeros o productos de degradación. En estos casos los métodos espectrofotométricos quedan limitados para su evaluación. En este punto varios métodos cromatográficos ofrecen la capacidad de separar el producto de interés de sus impurezas para su posterior detección. Luego, desde el cromatograma resultante se realiza la cuantificación del mismo. Por su parte, los carbohidratos se caracterizan por una sensibilidad limitada ante los métodos comunes de detección cromatográfica (ultravioleta, índice de refracción, entre otros). Como variante específica para la cuantificación de productos sacarídicos se desarrolló y se ha generalizado la detección amperométrica pulsada (DAP) (23).
Aún con el desarrollo de las técnicas cromatográficas muchos métodos de cuantificación no alcanzan una adecuada separación y en consecuencia arrojan una notable variabilidad en sus resultados. La RMNc ha permitido disponer de una alternativa que admite cuantificar con resultados confiables en cada uno de estos escenarios, incluso allí donde la complejidad estructural no garantiza una adecuada precisión con otros métodos de cuantificación.
La capacidad de la RMN para ensayos cuantitativos es discutida desde la década de 1960 (3). La RMNc parte del principio de que el área bajo cada lorentziana en el espectro es directamente proporcional al número de núclidos con igual corrimiento químico.
La RMN, aunque resulta una técnica costosa en comparación con las anteriores, permite optimizar parámetros para cuantificar biomoléculas de elevada complejidad. No requiere necesariamente la destrucción o transformación de la muestra. La posibilidad de emplear varios núclidos como 1H, 31P, 19F y 13C extiende la capacidad de la técnica para posibles análisis en muestras de alta complejidad estructural, como polisacáridos y glicoproteínas. Cuando la señal de interés está solapada con otras, la técnica brinda la posibilidad de descomponer la señal desde el espectro para hacer efectiva la cuantificación. A través del empleo de gradientes de campo y las técnicas basadas en la velocidad de difusión de los componentes de la muestra, la RMN permite la separación en el espectro final de dichos componentes y la cuantificación del componente de interés (24). Existen cromatógrafos acoplados a equipos de RMN, los cuales constituyen sistemas especializados para las mediciones cuantitativas a flujo continuo (25).
La RMNc se recomienda para determinar la pureza de ingredientes farmacéuticos activos y revelar la presencia de impurezas que pueden interferir en la acción de los anteriores (5, 26). Se sugiere como alternativa para elucidar la estructura de las impurezas, seguir el curso de la descomposición de un producto, evaluar el contenido de disolventes residuales y determinar relaciones molares entre diferentes productos de una mezcla.
Para la obtención de los experimentos de RMNc, los trabajos realizados desde la década de 1960 advirtieron de un conjunto de parámetros generales a comprobar, con el objetivo de garantizar el éxito del resultado cuantitativo (5).
Preparación de muestras para resonancia magnética nuclear cuantitativa
Para preparar la muestra, inicialmente se debe realizar una adecuada elección del disolvente. Los materiales empleados en la preparación (tubos para RMN, pipetas, espátulas, etc.) deben estar perfectamente limpios y secos. Las señales del disolvente, en lo posible, no deben interferir con las del analito. La viscosidad de la disolución resultante no debe ser alta para evitar problemas con la resolución del espectro final. Para las muestras apolares se recomienda emplear, fundamentalmente, cloroformo deuterado (CDCL3) y para el caso de las muestras más polares, metanol deuterado (metanold4), antes que dimetilsulfóxido hexadeuterado (DMSOd6). La disolución deberá ser homogénea y en lo posible debe estar filtrada (20).
]]> Con el objetivo de validar los ensayos cuantitativos de la RMN y de llevar a término la cuantificación en sí, frecuentemente se emplea un compuesto de referencia como estándar interno. Estos compuestos necesariamente son de elevada pureza, estables, químicamente inertes, poco volátiles y no deben ser higroscópicos. Las señales del compuesto de referencia no deben interferir con las señales del analito. Por este motivo no existe una referencia universal (20). Los compuestos de referencia también pueden ser insertados en la muestra como estándar externo. Esto se logra insertando en el tubo de RMN de la muestra, un capilar con la sustancia de referencia (5). Esta alternativa se emplea principalmente en aquellos casos donde la sustancia de referencia elegida presenta interacciones químicas con la muestra. También es muy empleada en evaluaciones por RMNc de fósforo y flúor de muestras biológicas (27). En este caso se recomienda controlar el volumen de la muestra respetando el área de observación de la sonda para evitar una alta variabilidad en los resultados de la determinación (28).Recientemente, se han venido explorando con éxito algunas alternativas de RMNc con el empleo de referencias electrónicas artificiales. Los método ERETIC (Electronic REference To access In vivo Concentrations) (29) y PULCON ((PUlse Length-based CONcentration measurements) incluyen el empleo de señales sintéticas como referencias virtuales (5, 30).
Parámetros de interés para la adquisición del experimento cuantitativo
La diferencia en el tiempo de relajación transversal (T1) entre los núclidos analizados es una de las principales causas de que los experimentos comunes de RMN no se puedan emplear para cuantificar. La secuencia propuesta para los experimentos de RMNc comienza con un tiempo (d1), con el objetivo de garantizar el recobrado total de los núclidos analizados. Posteriormente se genera un pulso con la frecuencia adecuada para la excitación de los anteriores. Finalmente el equipo registra la señal decreciente generada por los núcleos como parte de los procesos de relajación (Fig 2) (20). Esta secuencia se repite hasta acumular una adecuada relación señal/ruido. El ajuste de un grupo de parámetros de adquisición sirve como herramienta para la obtención de la señal espectroscópica, con más de un 99% de la información del analito. Dicho de otra manera, se garantiza que la señal registrada tenga toda la información requerida para el análisis cuantitativo.
Los resultados de un estudio para la evaluación del recobrado de los núclidos en función del d1 mostraron que: para d1= 3T1 el recobrado fue de 95,00%, para d1= 5T1 fue 99,30% y para d1= 7T1 el valor de recobrado fue de 99,91% (31). Por tal motivo no pocos autores recomiendan usar un valor cinco veces mayor que el máximo tiempo de relajación transversal de los núclidos evaluados (5T1max), fundamentalmente para pulsos de 90° (32). Por otro lado, se recomienda que el FID se registre sin rotación y eliminando el acoplamiento entre los núcleos de 13C y 1H durante la adquisición de la señal de RMN, principalmente mediante la secuencia GARP (Globally Optimized Alternating-phase Rectangular Pulses) incluida en el desacoplador de los espectrómetros modernos (Fig. 2) (20).
El pulso (pw) correcto para obtener un máximo de sensibilidad en el espectro debe ser de 90°. Sin embargo, resulta conveniente para el caso de los experimentos cuantitativos que el ángulo sea menor (32, 33). Este parámetro es conocido como ángulo de Ernst (aE) (34). El mismo está definido según:
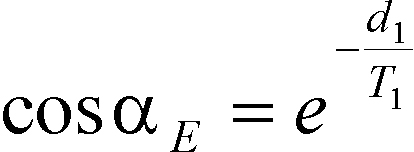
El tiempo que tarda la digitalización de la FID es conocido como tiempo de adquisición (aq). El mismo está relacionado con la ventana espectral (sw) y el número de puntos a registrar en el dominio tiempo (td) según:

El tiempo de adquisición se debe fijar adecuadamente, tomando en consideración que durante esta fase está recomendado desacoplar en un segundo canal (f2) del espectrómetro, lo cual suele provocar un calentamiento en la muestra (Fig. 2) Frecuentemente valores entre 2 y 4 segundos se emplean para los experimentos cuantitativos (32, 35).
]]> Otro parámetro a tomar en consideración es la ventana espectral (sw). Se recomienda para establecer un adecuado valor de sw, adicionar 2 ppm a las señales extremas del espectro de la muestra a evaluar. Este ajuste se sugiere para evitar la atenuación de señales que produce el filtro analógico de los espectrómetros en los límites del espectro, así como evitar la aparición de señales desdobladas fuera de la ventana espectral (32, 35). El número de acumulaciones es igualmente un factor a tomar en consideración con vistas a obtener una adecuada relación señal/ruido (s/r) en los espectros de RMNc. Puede ser empleado como parámetro para determinar los límites de detección y cuantificación de los experimentos de RMNc (36).Parámetros de interés para el procesamiento y obtención del espectro cuantitativo
Con el objetivo de mejorar la calidad del espectro resultante tras la transformación de Fourier numerosas funciones matemáticas se emplean como herramientas en el tratamiento de la FID. En las prácticas de rutina comúnmente se emplea la multiplicación exponencial. Para el caso de mezclas complejas donde se requiere mejorar la resolución, se recomienda la multiplicación con una función lorentziana-gaussiana. Esta función tiene un impacto en la reducción del ancho de los picos, aunque con alguna disminución en la relación s/r del espectro (32).
Un ajuste manual de las fases en el espectro se debe realizar en la mayoría de los casos. Seguidamente se recomienda un ajuste de la línea de base. De la calidad del espectro resultante tras estas operaciones depende la exactitud de los valores de áreas de las señales a evaluar y en consecuencia el éxito del análisis.
En un espectro correctamente procesado, donde los errores sistemáticos son mínimos, el mayor error de la integral proviene de la incertidumbre entre el comienzo y el final de la señal de RMN a medir, dado por la naturaleza intrínseca de la lorentziana.
La Figura 3 muestra el espectro de protones del intermediario 5-O-Alil-1-O-(2,5-di-O-bencil-b-D-Ribofuranosil)-2,3,4-tri-O -bencil-D-Ribitol (DSD) de la vacuna Quimi-Hib y la evaluación de un disolvente residual por integración (32, 37). Un procedimiento de integración llamado bucketing, también conocido como binning, permite agrupar las señales de interés en diferentes cuadrantes y ayuda a eliminar la contribución de los artefactos y las pequeñas variaciones provenientes de las condiciones de la muestra (38).
La determinación del área en picos solapados no se puede llevar a cabo con exactitud por los procedimientos de integración clásica. Sin embargo, esto encuentra solución con el procedimiento de deconvolución o line-fitting, como también se le conoce en el campo de la RMN.
La deconvolución simula uno o varios espectros únicamente con los picos de interés, empleando el método de los mínimos cuadrados. De esta manera es posible calcular el área de estas señales desde el espectro artificial con suficiente exactitud. Otras alternativas en la aplicación del procedimiento de line-fitting son: el método de mínimos cuadrados pesados (39), el método de mínimos cuadrados lineales, con el empleo de valores simples de descomposición (SVD, por sus siglas en inglés)(40) y la denominada CTLS (Contrained total-line-shape) (41).
Cálculos cuantitativos a partir del espectro
Para obtener la concentración absoluta de un compuesto en una mezcla, el área de una de las señales del compuesto se compara con la integral de la señal correspondiente a una referencia de concentración conocida. Si el espectro se obtiene en condiciones cuantitativas el valor de la concentración se puede calcular según la relación:
]]>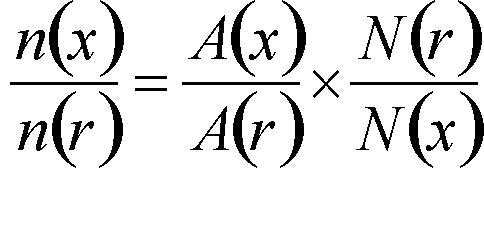
Donde n es el valor correspondiente a la cantidad de sustancia, N el número de núcleos que contribuyen a la misma y A es el área de la señal para el analito (x) y la referencia (r).
A partir de esta fórmula se pueden explotar dos métodos alternativos de análisis.
El método relativo, a través del cual se pueden evaluar los diferentes componentes (m) de una mezcla y permite conocer la relación de dichos componentes según el despeje:

El método absoluto que permite calcular la pureza o la concentración de un componente en la muestra a través de la adición de una referencia de concentración conocida según:

Donde M(x) y M(r) resultan ser las masas molares del analito y la referencia P(x) y P(r) los valores de pureza de ambos m(r) es la masa de la referencia añadida y m es la masa de la muestra.
Algunas aplicaciones de la resonancia magnética nuclear cuantitativa en vacunas
En la última década, la aplicación de la RMNc ha tenido un creciente impacto en la industria farmacéutica. Varios trabajos han ido solucionando diferentes problemas analíticos en la preparación de vacunas o candidatos. Un estudio de validación se reportó en 2005 para un método de cuantificación por qHNMR del polisacárido derivatizado de la vacuna PedvaxHIB (42). A través del estudio y siguiendo las recomendaciones de las Conferencia Internacional para la Armonización de requerimientos técnicos para el registro de fármacos en humanos (ICH, siglas en ingles) y de la Enciclopedia de Estadísticas Biofarmacéutica, se demostró precisión, exactitud, consistencia, linealidad, robustez y especificidad para el ensayo propuesto (43). Un estudio similar se realizó para la evaluación de un método que permite cuantificar el contenido de N,N dimetilformamida residual en el intermediario DSD (37) Estos métodos constituyen herramientas valiosas en los controles de la calidad de ambas vacunas. El Poli C presenta como parte de su estructura al menos un residuo de fosfocolina; el mismo constituye un elemento de identidad estructural que se emplea para evaluar la presencia de esta impureza.
]]> Una alternativa mediante el empleo de un método de RMN de 31P con PFG se propuso para la cuantificación de fosfocolinas en muestras biológicas (44). Por otra parte, otro método recomienda la evaluación cuantitativa de Poli C a través de la diferencia en su velocidad de difusión con respecto al polisacárido capsular, empleando la técnica bidimensional DOSY (Diffusion Order Spectroscopy) (24).El método, que emplea experimentos basados en pulsos de gradientes de campo magnético permite la diferenciación, según los radios hidrodinámicos, entre el Poli C no enlazado y el enlazado a los polisacáridos capsulares de un candidato vacunal contra Streptococcus pneumoniae.
El contenido de O-Acetatos de muchos polisacáridos constituye un aspecto fundamental en la efectividad de la respuesta inmunológica generada por estos.
En el año 2000 un método basado en RMNc de protones fue validado para el análisis cuantitativo por RMN del contenido de O-Acetato en el serovar typhi de Salmonella enterica (45). Una posterior extensión posibilitó la aplicación del método para cuantificar el contenido de O-Acetato a cuatro polisacáridos capsulares correspondientes a serogrupos de Neisseria meningitidis (46). Se reportó un método basado en RMN de protones para la cuantificación del polisacárido del serogrupo X de Neisseria meningitidis (16). Un método absoluto patentado en el 2011, como parte de una batería analítica, permite a través del empleo de ácido cítrico como referencia interna, la cuantificación del polisacárido Vi de Salmonella enterica serovar typhi, antes mencionado (47). El método permite evaluar el contenido de O-Acetatos en el polisacárido y en el IFA.
CONCLUSIONES
Muchos problemas analíticos comunes de la fabricación de vacunas encontraron solución en el uso creciente de la RMNc. La misma, por su rendimiento y su versatilidad, se ha convertido en la técnica de elección para la cuantificación de compuestos orgánicos con un creciente uso en la industria biofarmacéutica. El ajuste certero de varios parámetros permite la obtención de métodos que dan solución a varios requerimientos de cuantificación de materias primas, productos de alto valor agregado o impurezas, altamente recomendados en la producción de vacunas. Mediante el mismo experimento de RMNc, el espectro obtenido puede brindar información cuantitativa del compuesto analizado, además de la información estructural cualitativa intrínseca del mismo.
REFERENCIAS
1. Holzgrabe U, Diehl B, Wawer I. NMR spectroscopy in pharmaceutical analisys. 1st ed. Holzgrabe U, Diehl B, Wawer I, editors. Amsterdan: Elsevier; 2008.
]]>2. Chary KVR, Govil G. NMR in Biological Systems. Dordrecht: Springer; 2008.
3. Hollis DP. Quantitative Analysis of Aspirin, Henacetin, and Caffeine Mixtures by Nuclear Magnetic Resonance Spectrometry. Anal Chem 1963;35(11):1682-4.
4. Jacobsen NE. NMR Spectroscopy Explained: Simpli?ed Theory, Applications and Examples for Organic Chemistry and Structural Biology. Hoboken: John Wiley & Sons, Inc.; 2007.
5. Bharti SK, Roy R. Quantitative 1H NMR Spectroscopy. Trends Anal Chem 2012;35:5-26.
6. Frasch CE. Preparation of Bacterial Polysaccharide_Protein Conjugates: Analytical and Manufacturing Challenges. Vaccine. 2009;27:6468-70.
7. Jones C, Whitley C, Lemercinier X. Full Assignment of the Proton and Carbon NMR Spectra and Revised Structure for the Capsular Polysaccharide from Streptococcus pneumoniae Type 17F. Carbohyd Res 2000;325:192-201.
8. Lemercinier X, Jones C. Full `H NMR Assignment and Detailed O-Acetylation Patterns of Capsular Polysaccharides from Neisseria meningitidis Used in Vaccine Production. Carbohyd Res 1996;296:83-96.
9. Jones C. NMR Assays for Carbohydrate-Based Vaccines. J Pharm Biomed Anal 2005;38(5):840-50.
10. Abeygunawardana C, Williams TC, Summer JS, Hennessey JP. Development and Validation of an NMR-Based Identity Assay for Bacterial Polysaccarides. Anal Biochem 2000;279:226-40.
11. Jones C. NMR assays for carbohydrate-bassed vaccines. Journal of Pharmaceutical and Biomedical Analysis 2005;38:4894-900.
12. Vérez V, Fernández V, Hardy E, Toledo ME, Rodríguez MC, Heynngnezz L, et al. A Synthetic Conjugate Polysaccharide Vaccine Against Haemophilus in?uenzae type b. Science 2004;305:522-5.
13. Vérez V, Roy R, Rodríguez MC, Villar A, Fernández V, García E, et al. Haemophilus influenzae type b Conjugate Vaccine with a Synthetic Capsular Polysaccharide Antigen: Chemical View. In: René Roy, editor. Carbohydrate-Based Vaccines. ACS Symposium Series. New York: American Chemical Society; 2008. p. 71-84.
14. Bardotti A, Averani G, Berti F, Berti S, Carinci V, D'Ascenzi S, et al. Physicochemical Characterisation of Glycoconjugate Vaccines for Prevention of Meningococcal Diseases. Vaccine. 2008;26:2284-96.
15. Vialle S, Sepulcri P, Dubayle J, Talaga P. The Teichoic Acid (C-polysaccharide) Synthesized by Streptococcus Pneumoniae serotype 5 has a Speci?c Structure. Carbohyd Res 2005;340:91-6.
16. Garrido R, Puyada A, Fernández A, González M, Ramírez U, Cardoso F, et al. Quantitative nuclear magnetic resonance analysis and total assignment of the capsular polysaccharide Neisseria meningitidis serogroup X. Journal of Pharmaceutical and Biomedical Analysis 2012;70:295-300.
17. Stroop CJM, Xu Q, Retzlaff M, Abeygunawardana C, Busha CA. Structural Analysis and Chemical Depolymerization of the Capsular Polysaccharide of Streptococcus pneumoniae type 1. Carbohyd Res 2002;337:335-44.
18. Bourne R, Himmelreich U, Sharma A, Mountford C, Sorrell T. Identification of Enterococcus, Streptococcus, and Staphylococcus by Multivariate Analysis of Proton Magnetic Resonance Spectroscopic Data from Plate Cultures. J Clin Microbiol 2001;39(8):2916-23.
19. Chang J, Serrano Y, Garrido R, Rodríguez LM, Pedroso J, Cardoso F, et al. Relevance of O-Acetyl and Phosphoglycerol Substituent in the Antigenicity of Streptococcus pneumoniae serotype 18C Capsular Polysaccharide. Vaccine 2012;30:7090-6.
20. Pauli GF, Jaki BU, Lankin DC. Quantitative 1H NMR: Development and Potential of a Method for Natural Products Analysis. J Nat Prod [Reviews] 2005;68(1):133-49.
21. Porro M, Viti S, Antoni G, Neri P. Modifications of the Park-Johnson Ferricyanide Submicromethod for the Assay of Reducing Groups in Carbohydrates. Analytical Biochemistry 1981;118:301-6.
22. Dubois M, Gilles KA, Hamilton JK, Rebers PA, Smith F. Colorimetric Method for the Determination of Sugars and Related Substances. Anal Chem 1979;28:350-6.
23. Riccia S, Bardottia A, D'Ascenzia S, Ravenscroft N. Development of a New Method for the Quantitative Analysis of the Extracellular Polysaccharide of Neisseria meningitidis serogroup A by Use of High-Performance Anion-Exchange Chromatography with Pulsed-Amperometric Detection. Vaccine 2001;19:1989_97.
24. Xu Q, Abeygunawardana C, Nga AS, Sturgessa AW, Harmonb BJ, Hennessey JP. Characterization and Quantification of C-polysaccharide in Streptococcus pneumoniae Capsular Polysaccharide Preparations. Anal Biochem 2005;336:262-72.
25. Silva MV. LC-NMR and other Hyphenated NMR Techniques. Hoboken: John Wiley & Sons; 2012.
26. Pauli GF, Jaki BU, Lankin DC, Walter JA, Burton IW. Quantitative NMR of Bioactive Natural Products. In: Colegate S, Molyneux R, editors. Bioactive Natural Products. 2nd ed. New York: Taylor & Francis; 2007.
27. Martino R, Gilard V, Desmoulin F, Malet-Martino M. Fluorine-19 or Phosphorus-31 NMR Spectroscopy: A Suitable Analytical Technique for Quantitative In Vitro Metabolic Studies of Fluorinated or Phosphorylated Drugs. J Pharm Biomed 2005;38(5):871-81.
28. Henderson T. Quantitative NMR Spectroscopy Using Coaxial Inserts Containing a Reference Standard: Purity Determinations for Military Nerve Agents. Anal Chem 2002;74(1):191-8.
29. Akoka S, Barantin L, Trierweiler M. Concentration Measurement by Proton NMR Using the ERETIC Method. Anal Chem 1999;71:2554-67.
30. Wider G, Dreier L. Measuring Protein Concentrations by NMR Spectroscopy. JACS 2006;128:2571_6.
31. Griffiths L, Irving AM. Assay by Nuclear Magnetic Resonance Spectroscopy: Quantification Limits. Analyst. 1998;123:1061-9.
32. Soininen P. Quantitative 1H NMR Spectroscopy, Chemical and Biological Applications [dissertation]. Kuopio: University of Kuopio; 2008.
33. Beyer T, Diehl B, Holzgrabe U. Quantitative NMR Spectroscopy of Biologically Active Substances and Excipients. Bioanal Rev. 2010; 33:2402-10.
34. Ernst RR, Anderson WA. Application of Fourier Transform Spectroscopy to Magnetic Resonance. Rev Sci Instrum 1966;37(1):93-101.
35. Pauli GF, Jaki BU, Lankin DC. A Routine Experimental Protocol for qHNMR Illustrated with Taxol. J Nat Prod 2007;70:589-95.
36. Expert Working Group ICH. Harmonised Tripartite Guideline. Validation on Analytical Procedures: Text and Methodology Q2(R1). Geneva: ICH; 2005. p. 1-13.
37. Garrido R, Cardoso F, Rodríguez MC, Fernández V, Vélez H, Vérez V. Quantitative proton magnetic resonance determination of N,N dimethylformamide in one intermediate of the Quimi Hib vaccine. Magn Reson Chem 2012;50(8):525-8.
38. De Meyer T, Sinnaeve D, Van Gasse B, Tsiporkova E, Rietzschel ER, De Buyzere ML, et al. NMR Based Characterization of Metabolic Alterations in Hypertension Using an Adaptive, Intelligent Binning Algorithm. Anal Chem 2008;80:3783-90.
39. Gipson GT, Tatsuoka KS, Sweatman BC, Connor SC. Weighted Least-Squares Deconvolution Method for Discovery of Group Differences Between Complex Biofluid 1H NMR Spectra. J Magn Reson 2006;183:269-7.
40. Xu Q, Sachs JR, Wang TC, Schaefer WH. Quantification and Identification of Components in Solution Mixtures from 1D Proton NMR Spectra Using Singular Value Decomposition. Anal Chem. 2006;78:7175-85.
41. Soininen P, Haarala J, Vepsäläinen J, Niemitz M, Laatikainen R. Strategies for Organic Impurity Quanti?cation by 1H NMR Spectroscopy: Constrained Total-Line-Shape Ftting. Anal Chim Acta 2005;542(2):178_85.
42. Xu Q, Klees J, Teyral J, Capen R, Huang M, Sturgess AW, et al. Quantitative Nuclear Magnetic Resonance Analysis and Characterization of the Derivatized Haemophilus influenzae type b Polysaccharide Intermediate for PedvaxHIB. Anal Biochem. 2005;337(2):235-45.
43. Zhong B, Qiu C, Tang D. Validation of Quantitative and Qualitative Assays. In: Shein-Chung C, editor. Encyclopedia of Biopharmaceutical Statistics. Secound ed. New York: Marcel Dekker; 2003. p. 1-14.
]]>44. Loening NM, Chamberlin AM, Zepeda AG, Gonzalez RG, Cheng LL. Quantification of Phosphocholine and Glycerophosphocholine with 31P edited 1HNMR Spectroscopy. NMR in Biomedicine 2005;18(7):413-20.
45. Lemercinier X, Martínez I, Jones C. Use and Validation of an NMR Test for the Identity and O-Acetyl Content of the Salmonella typhi Vi Capsular Polysaccharide Vaccine. Biologicals 2000;28:17-24.
46. Jones C, Lemercinier X. Use and Validation of NMR Assays for the Identity and O-Acetyl Content of Capsular Polysaccharides from Neisseria meningitidis Used in Vaccine Manufacture. J Pharm Biomed Anal 2002;30:1233-46.
47. Berti F, Micoli F, Proietti D, inventors; Analysis of Vi Saccharides patent US2011/0159602 A1. 2011 jun. 30.
]]> Recibido: Agosto de 2012