Validación de la técnica de determinación de proteínas totales por el método microcoomassie a doble longitud de onda para la muestra de producto terminado del antígeno de la nucleocápsida del virus de la hepatitis C
Validation of the technique of determination of total proteins by microcoomassie method to double wave longitude for the sample of Finished Product of hepatitis C core antigen
Maelys Miyares,* Joana González, Dinorah Torres, Lázara Muñoz, Yanelys Pestana, Sheila Padrón, Inalvis Herrera, Ileana Rosales, Marbelis Linares
Centro de Ingeniería Genética y Biotecnología (CIGB) Ave. 31 entre 158 y 190, Cubanacán, Playa, La Habana, Cuba. CP10600. email: maelys.miyares@cigb.edu.cu
* Licenciada en Tecnología de la Salud, Especialista en Control Analítico.
RESUMEN
En el Centro de Ingeniería Genética y Biotecnología se obtuvo una formulación para un candidato vacunal del virus de la hepatitis C (VHC). Es un plásmido para la inmunización con ADN que contiene los genes de los tres antígenos estructurales del virus, mezclado con una variante truncada recombinante de la nucleocápsida del VHC como adyuvante molecular. Ambos compuestos se formularon en bulbos separados y se mezclaron en el momento de la inmunización. En el laboratorio de Desarrollo Analítica se validó la técnica de determinación de proteínas totales por el método de microcoomassie para la muestra de producto terminado (PT) del antígeno de la nucleocápsida del virus de la hepatitis C (HCcAg). Los parámetros validados fueron: especificidad, linealidad, rango, exactitud, precisión y estabilidad de la muestra de PT, bajo dos condiciones diferentes de almacenamiento. El método resultó ser específico para la cuantificación del HCcAg, sin interferencias del placebo de la muestra, a diluciones superiores a 1:8. La curva del microcoomasie fue lineal en el rango de trabajo de 5-40 µg/mL. Se demostró la exactitud del método (recuperación 100 ± 10%). En la evaluación del sistema se cumplieron los criterios de aceptación establecidos para la precisión: repetibilidad (CV £ 5%) y precisión intermedia (CV £ 10%). El PT es estable a (4 ºC y 22-25 ºC) durante los tiempos estudiados sin alteración en la concentración del HCcAg. La validación fue satisfactoria y el método fue adecuado para cuantificar proteínas en la muestra de PT. Este resultado permite dar cumplimiento a las especificaciones establecidas para este producto.
Palabras clave: hepatitis C, microcoomassie, validación.
ABSTRACT
A formulation was obtained for a vaccinal candidate of hepatitis C virus (VHC) in the CIGB. It is a plasmid for the immunization with DNA contianing the genes of the three structural antigens of the virus, blended with a recombinant truncated variant of the protein of the core of the VHC, as molecular adjuvant. Both compounds were formulated in separate vials and were mixed at the moment of the immunization. In the laboratory of Development-analytic the technique of determination of total proteins was validated by the microcoomassie method for the sample of Finished Product (FP) of Hepatitis C core antigen (HCVcoreAg). The validated parameters were: Specificity, Linearity and Range, Accuracy, Precision, Stability of the FP sample under two different conditions of storage. The method was specific for the quantification of the HCcAg without interferences of sample placebo of FP to superior dilutions at 1:8. The curve of the microcoomassie for the FP was lineal in the range of work of 5-40 µg/mL. It demonstrated the accuracy of the method (100±10% recovery). In the evaluation of the system, the established acceptance criteria were completed for Precision: Repeatability (CV £ 5%) and Intermediate Precision (CV £ 10%). Temperatures studied in stability did not cause alteration in HCcAg concentration, and the FP can be stored for 15 days. Validation was satisfactory. The method is adequate to quantify the sample of the FP. This result allows us to comply with the specifications established for this product.
Key words: hepatitis C, Microomasie, validation.
]]>
INTRODUCIÓN
La infección por el virus de la hepatitis C (VHC) es un problema de salud en el ámbito mundial (1). El virus causante de la enfermedad fue identificado como un virus de ARN de simple cadena positiva, perteneciente a la familia Flaviviridae. El virión posee un diámetro entre 36 y 72 nm y es envuelto con epícula (2).
En el Centro de Ingeniería Genética y Biotecnología fue clonada la región estructural del genotipo 1b, principal circulante en Cuba, y esta es la base de los candidatos vacunales en desarrollo. El enfoque más avanzado es una formulación vacunal basada en un plásmido para la inmunización con ADN, que contiene los genes de los tres antígenos estructurales del virus, mezclado con una variante truncada recombinante de la proteína core del VHC, como adyuvante molecular. Este candidato de vacuna de ADN induce respuestas humoral y celular específicas, fuertes y sostenidas en diferentes modelos animales, con marcada protección en ratones en un modelo de reto con virus sustituto. Con esta formulación vacunal se ha concluido satisfactoriamente la fase preclínica (3).
Se concluyó de forma satisfactoria un estudio clínico Fase I en pacientes cubanos crónicamente infectados con el VHC de genotipo 1b, no respondedores a tratamientos previos con interferón más ribavirina (4).
Está en curso un estudio clínico Fase II, en escenario terapéutico, y también se inició un estudio Fase I/II, en escenario preventivo, en pacientes con insuficiencia renal crónica. Teniendo en cuenta los requerimientos reguladores se validó la técnica de determinación de proteínas totales por el método de microcoomassie (5) para la muestra de producto terminado (PT) del antígeno de la nucleocápsida del virus de la hepatitis C (HCcAg).
Esta técnica consiste en un método colorimétrico basado en la unión del colorante azul de Coomassie a la estructura de la proteína, formando un complejo coloreado azul oscuro después de adicionada la proteína, debido a la estabilización de la forma aniónica del colorante por interacciones iónicas e hidrofóbicas. Se realiza la determinación de las absorbancias de las muestras a dos longitudes de ondas: 620 y 450 nm, respectivamente, lo cual mejora considerablemente la sensibilidad y linealidad de la curva de calibración a pequeñas concentraciones de proteínas. Este resultado permite dar cumplimiento a las especificaciones establecidas para el PT, ya que este método forma parte de los cuatro procederes analíticos para la caracterización del HCcAg.
MATERIALES Y MÉTODOS
Muestras y soluciones empleadas ]]>
· Material de referencia: Bulbo con albúmina de suero bovino liofilizado (MR BSA 06-1109), suministrada por el Grupo de Estabilidad de la Unidad de Control de Calidad del CIGB.· Producto terminado: Antígeno de la nucleocápsida del virus de la hepatitis C (HCcAg) del lote experimental CHC1101, suministrada por el Departamento de Desarrollo de Purificación del CIGB.
· Placebo de la muestra del PT: PBS 1X 0,2 mM; EDTA 6 mM; Tween 20 al 0,05%.
· Solución de Coomassie 1X: ácido ortofosfórico 10% v/v; etanol absoluto 5% v/v; Coomassie G 250 0,01% m/v.
· Agua para inyección.
Parámetros de validación: Se evalúan la especificidad, linealidad, rango, exactitud, precisión (6, 7) y estabilidad de la muestra de PT bajo dos condiciones diferentes de almacenamiento.
Especificidad: Se realizó la evaluación de la interferencia del placebo empleado en la formulación de la muestra de PT. Se aplicaron seis réplicas de diferentes diluciones del placebo (desde puro hasta 1:256) y seis réplicas del control negativo (agua) que se tomó como referencia. Se compararon los valores medios de absorbancia obtenidos y la desviación estándar con la respuesta del blanco del ensayo mediante una prueba F y prueba t de Student, para determinar si existían diferencias significativas entre ellos, para una probabilidad de 95%.
Linealidad y rango del sistema: Se realizaron tres experimentos independientes y se determinaron los parámetros para evaluar la linealidad del sistema: Coeficiente de determinación (R2) (³; 0,98), ANOVA de significación de la pendiente (P £; 0,01) (8).
Para establecer el rango de trabajo se analizó la precisión (repetibilidad y precisión intermedia), y la exactitud de cada uno de los puntos del rango lineal de la curva de regresión. Se determinó la precisión mediante el cálculo del coeficiente de variación (CV) expresado en por ciento. Se consideró como criterio de aceptación para la repetibilidad (intraensayo) un CV £ 5%, calculado a partir de la concentración media y desviación estándar de cada punto de la curva ensayada en el mismo día. Para la precisión intermedia (interensayo) se consideró como criterio de aceptación un CV £ 10%. Se calculó a partir de la concentración media global de cada punto de la curva de calibración entre días diferentes. Para evaluar la exactitud se calculó la recuperación expresada en por ciento (criterio de aceptación 100±10%), y se aplicó la prueba t de Student, para determinar si el valor medio obtenido y el valor teórico esperado de la concentración de los puntos de la curva no diferían significativamente, para un 95% de confianza.
Exactitud: Se realizó mediante la evaluación de la adición de patrón MR BSA 06-1109 a la muestra de PT (9). Teniendo en cuenta los resultados del estudio de especificidad, la muestra de PT se diluyó 1:13, la cual quedó preparada a una concentración tal que su absorbancia se correspondió con el rango medio de la curva de calibración. Se prepararon muestras mezclas (Mm) adicionando a la muestra de PT cantidades diferentes del MR de BSA, correspondientes a los rangos RA (19), RM (11,3) y RB (7,1 µg/mL) de la curva de calibración. Se aplicó tres réplicas independientes en cada punto. A los valores de absorbancia obtenidos se les restó el valor de la muestra de PT. Se obtuvieron los valores de concentración (valores experimentales u observados), los cuales se compararon con los valores esperados. Se analizaron los porcentajes de recuperación de cada preparación. Se realizó la prueba G de Cochran para determinar si existían diferencias significativas entre el valor medio obtenido y el valor teórico esperado, para un 95% de confianza. Se analizó la influencia en la variabilidad de los resultados, calculando la media: D.E y (CV £; 10%) de todas las recuperaciones obtenidas. ]]>
Precisión: Se ensayó la muestra de PT en los rangos alto, medio y bajo de la curva de calibración, con seis réplicas independientes (10). Para estudiar la repetibilidad (intraensayo), se realizó el ensayo bajo las mismas condiciones de operación por un analista en el mismo día. Se determinó la variabilidad de la concentración media y la desviación estándar de la muestra en todos los rangos (CV £ 5%). Para el estudio de la precisión intermedia (interensayo) se realizó el ensayo anterior indistintamente durante tres días por dos analistas, bajo condiciones de operación y reactivos diferentes, en el mismo laboratorio. Se determinó la variabilidad por cada analista en días diferentes (CV £ 10%) (6, 8, 9).Estabilidad: Para analizar la influencia de la temperatura en la estabilidad de la muestra respecto al contenido de antígeno de la nucleocápsida del virus de la hepatitis C, se diseñó un estudio preliminar de estabilidad en condiciones aceleradas (4 ºC y temperatura ambiente 22-25 ºC). Se determinó el ANOVA de significación de la pendiente (P ³0,05).
RESULTADOS Y DISCUSIÓN
La validación de los métodos analíticos utilizados en las actividades de control desempeña un papel determinante, pues de ellos depende la comprobación confiable y reproducible de los índices de calidad de las materias primas y productos, lo cual contribuye notablemente al aseguramiento de la calidad, seguridad y eficiencia de los mismos (10). Es importante contar con una técnica como la validada en este trabajo, que sea sensible en la cuantificación del contenido de HCcAg y que permita evaluarlo en los estudios de estabilidad.
El método analítico establecido se clasificó como ensayo cuantitativo, de acuerdo con la clasificación de las agencias reguladoras del uso de medicamentos (8, 9), por tratarse de un ensayo destinado a cuantificar el PT HCcAg. El diseño de la validación empleado se realizó teniendo en cuenta la clasificación reguladora, por lo que se evaluaron los parámetros siguientes: especificidad, linealidad, rango del sistema, precisión (precisión intraensayo e interensayos) y exactitud (6, 8, 9).
Se estudió la especificidad del método mediante el análisis de la interferencia del placebo de la muestra de PT (Tabla 1). Se observó que el placebo presentó interferencia, donde se obtuvieron valores de absorbancia superiores al valor de la referencia, pero estos disminuyeron al diluirlo. Con una dilución 1:8 es posible eliminar las interferencias del placebo, ya que no existen diferencias significativas con relación a la referencia (blanco del ensayo) (p=0,36).
Se evaluó la linealidad del sistema que resultó satisfactoria (Tabla 2). Se observó que los resultados de los análisis estadísticos en todos los casos cumplieron con el criterio de aceptación propuestos para cada prueba: R2 = 0,99, probabilidad asociada al valor de F para la ANOVA de significación de la pendiente (P £ 0,01. El Rango de trabajo establecido fue de 5 a 40 µg/mL. Los cinco puntos de la curva de calibración tuvieron una precisión (repetibilidad y precisión intermedia) y exactitud aceptadas. Para la precisión intraensayo e interensayo se cumplió con el criterio de aceptación establecido respectivamente: CV £ 5% y CV £ 10% (Tabla 3). Se observó para la exactitud un por ciento de recuperación entre 100±10% entre el valor calculado y el esperado. Según los resultados obtenidos todos los puntos de la curva cumplieron con el criterio de aceptación establecido (Tcalc = Tteo) para un 95% de confianza (6, 8, 9). Se estudió la exactitud sobre la muestra de PT.
Concluimos que el factor concentración no tiene influencia en la variabilidad de los resultados (p=0,87) (Tabla 4). Se determinaron los porcentajes de recuperación de cada preparación. Se obtuvo el valor medio de 99%, no existiendo diferencias significativas entre este valor y el 100% (para la muestra de PT). El CV global fue de 9,4%. Se calcularon los intervalos de confianza para el por ciento de recuperación medio, encontrándose entre 92% y 106%, los cuales incluyen el 100%, por lo que se cumple con el criterio de aceptación para esta prueba.
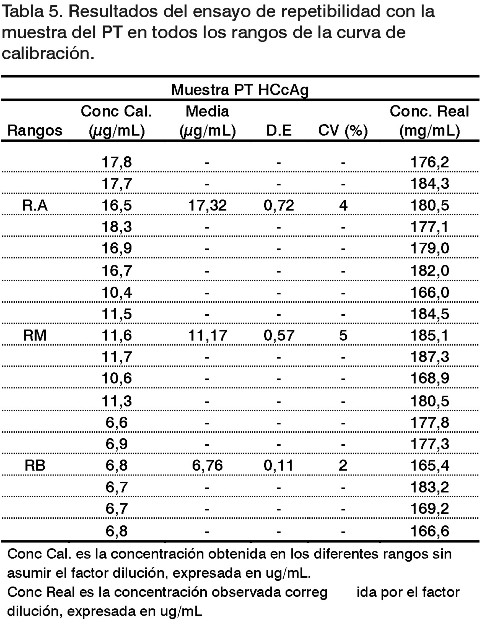
La evaluación de la precisión del sistema se realizó sobre la muestra de PT. En los resultados obtenidos en la repetibilidad se observa que cada uno de los rangos cumplió con el criterio de aceptación para esta prueba (CV £ 5%) (Tabla 5). La variabilidad del valor de concentración al diluir la muestra se encuentra en los límites establecidos (CV global = 4%) donde se obtuvo un valor medio de 177,3 µg/mL. Los resultados obtenidos para la precisión intermedia se muestran en la Tabla 6. El mayor CV obtenido fue de 9,4%. Lo que indica que en todos los casos, hay cumplimiento del criterio de aceptación en todo el rango estudiado (CV £ 10%) (6, 8, 9). ]]>
Se analizó un estudio de estabilidad preliminar de la muestra de PT, exponiendo un bulbo a 4 ºC y T.A con una frecuencia de 0, 1, 3, 7,15 días. Se evidenció que la concentración del HCcAg no se afectó durante el almacenamiento en todo el tiempo de estudio (Fig. 1). Los valores de concentración obtenidos del PT se encuentran dentro del criterio de aceptación del producto (entre 0,15-0,25 mg/mL) y no existe significación de la pendiente a 4 ºC (P=0,45) y a TA (P=0,82), por lo que la característica medida es estable durante todo el tiempo de estudio.
Los resultados de la validación del método demostraron que es apropiado para la cuantificación de HCcAg en la muestra de PT, al cumplir con los requisitos analíticos para ser empleado en el control de la calidad de este producto. Este método es uno de los cuatro procederes analíticos validados para el control de la proteína del Core de HC en muestras de producto terminado. También ha constituido una valiosa herramienta para los estudios de estabilidad y la liberación de lotes utilizados en la clínica.
REFERENCIAS
1. Francki RIB, Fauquet CM, Knudsen DL, Brown F, editores. Classification and nomenclature of viruses. Fifth report of the International Committee on Taxonomy of Viruses. Archives of Virology, suppl. 2. New York: Springer-Verlag; 1991.
2. Choo QL, Richman KH, Han JH, Berger K, Lee C, Dong C, et al. Genetic organization and diversity of thehepatitis C virus. Proc Natl Acad Sci 1991;88:2451-5. ]]>
3. Álvarez-Lajonchere L, Guerra I, Musacchio A, Aguilar JC, Falcon V, Soria Y, et al. Recombinant in vitro assembled hepatitis C virus core particles induce strong specific immunity enhanced by formulation with an oil-based adjuvant. Biol Res 2009;42(1):41-56.
4. Grakoui A, Wychowski C, Lin C, Feinstone S, Rice CM. Expression and identification of hepatitis C virus polyprotein cleavage products. J Virol 1993;67:1385-95.
5. Tsaffrir Zor, Zvi Selinger. Linearization of the Bradford Protein Assay Increasses Its Sensitivity: Theorical and Experimental Studies. Analytical Biochemistry 1996;236:302-08.
6. Chaloner-Larsson G, Anderson R, Egan A. A WHO guide to good manufacturing practice (GMP) requirements. Part 2: Validation. Validation of analytical assays. Geneva: WHO;1997.
7. Steven Walfish. Analytical Methods: A Statistical Perspective on the ICH Q2A and Q2B Guidelines for Validation of Analytical Methods. BioPharm International 2006;19(12). Disponible en: http://www.biopharminternational.com/biopharm/article /articleDetail. jsp?id=392483
8. Centro para el Control Estatal de la Calidad de los Medicamentos (CECMED). Validación de Métodos Analíticos. Regulación No.41. La Habana: CECMED; 2007. ]]>
9. Harmonised Tripartite Guideline (ICH). Validation of analytical procedures: Text and Methodology. London: ICH; 2005.
Recibido: Septiembre de 2012
Aceptado: Noviembre de 2012
]]>