Caracterización estructural del factor estimulador de colonias de los granulocitos, Hebervital
Structural Characterization of Granulocyte Colony Stimulating Factor, Hebervital
Natacha Pérez,* Yaí Cruz, Galina Moya, Lourdes Costa, Lázaro Betancourt, Vladimir Besada, Joel Ferrero, Jorge Luis López
Centro de Ingeniería Genética y Biotecnología (CIGB), PO Box 6162, Código Postal 10600. La Habana. Cuba. Telef: (537)-271 6022.
RESUMEN
El factor estimulador de colonias de granulocitos (G-CSF) es un medicamento que pertenece a un grupo de proteínas hematopoyéticas. Se obtiene por vía recombinante en el Centro de Ingeniería Genética y Biotecnología, de Cuba, desde el año 2000 y es comercializado como Hebervital. Se indica a pacientes con neoplasias afectados de neutropenia febril, con tratamiento mielosupresor, seguido de trasplante de la médula ósea, entre otros. Induce alteraciones en la actividad biológica de los neutrófilos maduros que pudieran aumentar la defensa del huésped en respuesta a patógenos, como bacterias y hongos. En este trabajo se realizó un análisis específico del G-CSF para determinar su pureza y caracterización; además, se demostró su posible comparabilidad con productos de otras firmas comerciales. El patrón de bandas de las muestras en la electroforesis, así como el porcentaje del área y los perfiles cromatográficos bajo la curva en la cromatografía líquida de alta resolución, fueron similares entre los diferentes productos. La digestión enzimática y la separación proteolítica de los péptidos generaron mapas peptídicos reproducibles y de elevada similitud con el Neupogen.
Palabras clave: factor estimulador de colonias de granulocitos, G-CSF, neutropenia, Hebervital.
ABSTRACT
Granulocyte Colony Stimulating Factor (G-CSF) is member of haemopoietic proteins group used in medication. It is obtained by recombination technique since 2000 at the Center for Genetic Engineering and Biotechnology of Cuba, and it is commercialized as Hebervital. It is recommended for patients with malignant tumors, affected by febrile neutropenia, bone marrow suppressor treatment followed by bone marrow transplant, among others. It induces disorders in the biological activity of the mature neutrophils that could increase host defense in response to pathogens like bacterial and fungal infections. The objective of this project was to perform a specific analysis to determine G-CSF purity and characterization and to demonstrate its comparability with other commercial products. The sample bands pattern in SDS-PAGE, the area percentage and the chromatographic profiles under the curves, in reverse phase high performance liquid chromatographic were similar. The enzymatic digestion and separation by proteolysis of peptides generated reproduces peptide's maps of great similarity with Neupogen.
Key words: granulocyte colony stimulating factor, G-CSF, neutropenia, Hebervital.
INTRODUCCIÓN ]]>
Los factores estimuladores de colonias hematopoyéticas se utilizan en diferentes tratamientos médicos y se encuentran en curso ensayos clínicos donde se utilizan como adyuvantes en vacunas antitumorales (1) y para mejorar los efectos de la vacunación, por ejemplo, contra la hepatitis B (2). El factor estimulador de colonias de granulocitos (G-CSF) humano recombinante es uno de los más aplicados en estudios clínicos que se efectúan por diferentes laboratorios y hospitales, en los que se verifica su amplio espectro de uso en pacientes con cáncer (3), sepsis abdominal, sepsis neonatal y neumonía (4), entre otras afecciones. Este medicamento estimula la activación, diferenciación y proliferación de las células hematopoyéticas en el organismo (5), al aumentar la defensa del huésped en respuesta a patógenos, puesto que tiene, además, efecto antiinflamatorio e inmunomodulador (6, 7).El G-CSF se obtiene por vía recombinante en la bacteria Escherichia coli desde 1986 (8). Tiene una secuencia aminoacídica idéntica a la G-CSF humano endógeno, solo diferente en la presencia de un residuo metionina N-terminal, necesario para la expresión del gen G-CSF en la bacteria E. coli y la ausencia de glicosilación, porque el sistema de expresión en bacterias carece de esa capacidad. Los estudios cristalográficos refieren que estas modificaciones están físicamente muy alejadas de los sitios que influyen en la actividad biológica (9).
El G-CSF es una hormona glicoproteica producida por monocitos, fibroblastos y células endoteliales, polipéptido de una sola cadena de 175 aminoácidos y peso molecular de 18800 daltons. Su pH isoeléctrico es de 6,1. Su estructura está formada por cuatro alfa hélices antiparalelas, con dos puentes disulfuro en las cisteínas C37-C43 y C65-C75. La reducción de alguna de estas uniones disulfuro causa una disminución de la actividad. Contiene una cisteína libre en la posición 18, la cual no se requiere para su actividad biológica y 5 histidinas (10).
En este trabajo se realizó una caracterización del G-CSF que se obtuvo en el Centro de Ingeniería Genética y Biotecnología de La Habana, Cuba (CIGB), Hebervital, teniendo en cuenta los requisitos y exigencias de las regulaciones internacionales y las técnicas específicas para la verificación de la estructura primaria; además, se compara este producto con muestras de G-CSF de una firma comercial (Neupogen), con el objetivo de demostrar su integridad y similitud.
MATERIALES Y MÉTODOS
Obtención de G-CSF
El proceso fermentativo se realizó utilizando la cepa de E. coli BL21 (DE3) transformada con el plásmido que contiene la información genética que codifica para esta proteína bajo el control del promotor T7. La proteína de interés se expresó intracelularmente en el precipitado del cultivo. La obtención de los cuerpos de inclusión se realizó por un proceso de ruptura de las células del precipitado (11), en homogenizador de alta presión. Los cuerpos de inclusión se separaron de las proteínas citoplasmáticas solubles por centrifugación, se recolectó el sedimento y se sometió a diferentes pasos de lavado para su semipurificación. La extracción de la proteína se realizó con un agente desnaturalizante, renaturalizada por filtración en gel y se purificó por cromatografía de intercambio catiónico. Al material eluido se le realizó una cromatografía de filtración en gel para llevar la proteína a la solución tampón final NaAc 20 mM pH 4. Los lotes obtenidos se formularon, llenaron y envasaron, a una concentración 30 MUI/bulbo, para dar lugar a los lotes de Hebervital 6V3011 y 6V3021, de los cuales se tomaron muestras para este estudio comparativo.
Determinación de la concentración de proteínas
A las muestras procedentes de los pasos de fermentación, ruptura y lavados se les determinó la concentración de proteínas por modificación de la técnica de Lowry (12). A las muestras de los ingredientes farmacéuticos activos (IFA) y del producto terminado se les determinó la concentración al leer la absorbancia a 280 nm en espectrofotómetro (Genesys) a través del coeficiente de extinción porcentual (0,86 en este caso), se utilizó para ello la ley de Lambert-Beer de forma similar a la caracterización que se le realizó al Neupogen (13). ]]>
Determinación de pureza por electroforesis en gel de poliacrilamida (SDS-PAGE)Se realizó según procedimiento modificado del método descrito en el Manual (14).
Muestras analizadas
1-Neupogen B1054, 2-Neupogen B1055, 5-Hebervital (6V3011/0), 6-Hebervital (6V3021/0)
Preparadas empleando tampón de tratamiento reductor (2XR). Se aplicó 20 µg para todos los lotes; para leer las bandas se utilizó el Software "Molecular Analyst" versión 1.4.1 Bio-Rad y un scanner Imagingdensitometer Model GS-700. El material de referencia que se utilizó en el análisis fue MRG-CSFe-01-0301, producido en el CIGB. El criterio de aprobación de la muestra fue ≥ 95% de pureza.
Cromatografía líquida de alta eficacia en fase reversa (CLAR)
La pureza de las muestras se determinó por un procedimiento modificado del método desarrollado por Carr (15).
Equipamiento: Inyector Rheodyne 7725i con "loop" de 1 mL, desgasificador, Knauer; Bomba: L-7100, Merck-Hitachi; Detector: UV de longitud de onda variable Knauer; Horno Knauer, Columna: C8 4,6 x 250 mm, Vydac; microcomputadora COMPAQ DESKPRO con el programa de adquisición y procesamiento de datos Model D-7000, Chromatography Data Station Software, HPLC System Manager, Versión 3.1 Merck-Hitachi.
Procesamiento de datos: Se realizó mediante el sistema LaCrom. El reporte incluyó datos de identificación, cromatogramas, tiempo de retención (tr) para cada uno de los picos detectados, área y por ciento (%) del área total de las diferentes muestras. A partir del tiempo de retención de la muestra control se identificó el pico de G-CSF de la muestra a analizar. El criterio de aprobación fue ≥ 95% de pureza. El criterio de aprobación fue ≥ 95% de pureza.
Análisis estadísticos: Con los resultados de pureza obtenidos se realizó un análisis de varianza (ANOVA, factor simple) entre las muestras de Hebervital y Neupogen, para comparar por estadística básica utilizando el programa Minitab 15, los resultados dentro de grupos, dos muestras de un mismo producto, y entre grupo, muestras de cada producto, para determinar diferencias entre las purezas por cromatografía líquida de alta resolución. ]]>
Actividad biológicaSe realizó teniendo en cuenta las pautas que establece la European Pharmacopea (16), se basó en la proliferación de la línea celular Gnfs-60 (leucemia mieloide murina retroviralmente inducida) mediada por G-CSF. Las muestras y el material de referencia de laboratorio se analizaron por duplicado en una placa de 96 pocillos de fondo plano. La curva dosis-respuesta comenzó a 1 ng/mL. Control negativo (células no tratadas con G-CSF). Se cuantificó la actividad biológica de las muestras, al utilizar un programa de cálculo de líneas paralelas (PARLIN). Las muestras se analizaron en paralelo con el material de referencia que se realizó en el CIGB, al calibrar contra el material de referencia internacional 88/502 del NIBSC. Se repitió este ensayo al menos en cuatro días diferentes para las mismas muestras, se calculó la media geométrica, que se corresponde con el valor final de potencia asignado para cada muestra. Criterio de aprobación: Intervalo de confianza para una probabilidad del 95%, la cual no debió ser menor o igual de 74% y no mayor de 136%.
Detección de ADN de E. coli contaminante por técnica de hibridación
Se determinó en las muestras de IFA. El ADN de E. coli se purificó según el método de Sambrook (17) y se aplicó sobre un filtro de nylon Hybon N (Amersham, Inglaterra), al utilizar un equipo Manifold (Biorad, USA), para una curva patrón con diluciones 1:2, partiendo de 1 ng, así como 100 µg de proteínas de la muestra a ensayar y 100 µg de BSA Fracción V como control negativo, que se desnaturalizaron con anterioridad durante 5 min a 95 °C en un bloque térmico. El filtro de nylon se trató con solución de NaCl 1,5M, 0,5M NaOH, durante 5 min a temperatura ambiente y se dejó secar 30 min al aire antes de exponerlo a la luz UV. Envuelto, posteriormente se colocó en un transluminador (Bioblock, Francia) a 320 nm durante 3 min. El filtro se colocó con solución prehibridadora (0,9M NaCl, 0,12M citrato de sodio, 0,1% Ficoll 400, 0,1% polivinilpirrolidona, 1 mg/mL BSA Fracción V, 0,5% SDS, 50% formamida) y 100 µg/mL de tRNA, durante 2 h a 42 °C. La hibridación se realizó en una sonda marcada con 32P (CIGB, Cuba), a razón de 106 cpm/mL, en la solución de prehibridación de 14 -16 h a 42 °C. El filtro se lavó con una solución de NaCl 0,3M, 0,04M Citrato de Sodio, 0,1% SDS y posteriormente se lavó con 0,03M NaCl, 0,0004M y 0,1%. El filtro envuelto fue expuesto a un film de rayos X a -70 °C durante 48 h. La cantidad de ADN contaminante presente en la muestra se determinó al comparar la intensidad de su señal con diferentes puntos de la curva de ADN de E. coli.
La pureza microbiológica, así como la pirogenicidad, se determinó según modificaciones de métodos descritos en United State Pharmacopoeia USP 35, vigente (18).
Determinación de proteínas contaminantes por técnica de Inmunodot
Método semicuantitativo que se basó en la identificación inmunológica con antisueros específicos contra el patrón de proteína de la célula hospedera, se realizó como modificación del método descrito como protocolo (19).
Determinación de identidad de la proteína de interés por el método de Western blot
Se basó en una modificación de un protocolo original (20). Se montó una electroforesis en gel de poliacrilamida al 15% en presencia de SDS con la proteína a transferir. Se electrotransfirió la proteína a una membrana de nitrocelulosa en presencia de buffer de transferencia con SDS durante 1 h. Se incubó la membrana en buffer fosfato salino (PBS) 1x + 5% de leche descremada durante toda la noche. Se incubó la membrana con 1 µg/mL del anticuerpo policlonal de conejo anti-G-CSF, diluido en 1% de PBS, durante 1 h a una temperatura de 37 oC. Se realizaron tres lavados a la membrana en tres pasos consecutivos: 1) PBS 0,1% por 5 min, 2) Tween 0,1% por 10 min y 3) PBS 0,1% por 5 min.
Las membranas con una mezcla de peroxidasa-proteína se incubaron durante 1 h 37 oC y luego se reveló el Western con diaminobenzidina (15 mL de PBS; 0,0075 g de diaminobenzidina; 15 µL de peróxido). ]]>
Comparación de la estructura primaria de los G-CSF: Hebervital y NeupogenFueron realizados varios ensayos para determinar la identidad, dentro de ellos el análisis de la estructura primaria al caracterizar los extremos N y C terminal, para así demostrar la integridad de la molécula, los ensayos realizados se describen a continuación:
Muestras analizadas
CIGB: Hebervital 6V3021/0 - Amgen: Neupogen B1054
S-carbamidometilación de cisteínas libres
La alquilación de las cisteínas libres se realizó por resuspensión de la proteína (100 µg) en 100 µL de una solución tampón que contenía cloruro de guanidinio 6 M, Tris 0,3 M, pH 8,6 y iodoacetamida. Este último reactivo se empleó en un exceso de cincuenta veces con relación a los moles de proteína presentes (5 nmoles). La mezcla se incubó durante 20 min a temperatura ambiente en atmósfera de N2. Al finalizar la reacción la proteína se purificó inmediatamente por CLAR.
Digestión enzimática y separación de péptidos proteolíticos
Cada muestra de proteína carbamidometilada se resuspendió en 80 µL de solución NH4HCO3 al 1%, urea 2 M y se digirió durante 4 h con tripsina; posteriormente las muestras se diluyeron (2 x) y se añadió endoproteinasa Glu-C. La muestra se incubó seguidamente durante 4 h. Ambas proteasas se emplearon en una relación enzima-sustrato de 1:50. Al término de la digestión, la mezcla de péptidos se acidificó al añadir ácido fórmico hasta una concentración de 5% y los péptidos que se generaron se separaron por CLAR (LKB Pharmacia) en columna RP-C18 (Vydac, 4.6 x 250 mm), al utilizar un gradiente lineal desde 0 % hasta 60% de la solución B en 90 min. Las soluciones que se utilizaron para generar el gradiente fueron:
A: H2O / TFA 0,1% y B: acetonitrilo / TFA 0,05%.
Las muestras de proteína se purificaron en igual sistema cromatográfico, se empleó una columna de RP-C4 (JT Baker, 4,6 x 50 mm), se utilizó un gradiente desde 15% hasta 60% de la solución B en 20 min. ]]>
Análisis por espectrometría de masasESI-MS: Los espectros de masas se adquirieron en un espectrómetro de masas híbrido con geometría ortogonal QTOF-2 (Micromass, UK). El espectrómetro se calibró con una solución salina compuesta por una mezcla de yoduros de sodio y cesio en el rango m/z de 50-2000 Th y las mediciones se realizaron en un rango de m/z de 400 hasta 2000 Th. El software de procesamiento de los espectros de masas que se empleó fue el MassLynx versión 3,5 (Micromass, UK).
ESI-MS/MS: Los péptidos se secuenciaron por ESI-MS/MS al ajustar el rango de masas para cada caso. Estas mediciones se realizaron con el primer cuádruplo, al fijarse a una resolución de 3 a 4 Th para seleccionar el ion precursor a fragmentar. El gas de colisión fue argón y la energía de colisión que se empleó osciló entre 20 y 45 eV hasta lograr un espectro de masas con suficiente información estructural que permitió una secuenciación confiable del péptido.
RESULTADOS Y DISCUSION
Proceso de producción del IFA de Hebervital
Las fermentaciones del cultivo tuvieron una estabilidad plasmídica de 90%, una concentración celular 27 g/L de cultivo y una expresión 28%. La biomasa celular obtenida, además de la proteína de interés liberó al medio un grupo de componentes de las células hospederas, como proteínas y ácidos nucleicos. La pureza del producto de esta etapa fue mayor del 40%, la cual se determinó por el método de electroforesis en gel de poliacrilamida SDS-PAGE al 15%.
El proceso de purificación posterior eliminó los contaminantes derivados de las células hospederas y de otras fuentes. Los ensayos que determinan las características organolépticas y las pruebas de seguridad tuvieron resultados satisfactorios (Tabla 1).
Los lotes cumplieron con las especificaciones establecidas, el producto terminado que se elaboró a partir de estos se sometió a ensayos de identidad comparativos con los lotes de producto de la competencia como se muestra a continuación.
Caracterización del producto terminado ]]>
A continuación se muestran los resultados del estudio comparativo que se realizó con el producto terminado contra muestras de otro laboratorio.Estudio comparativo por electroforesis
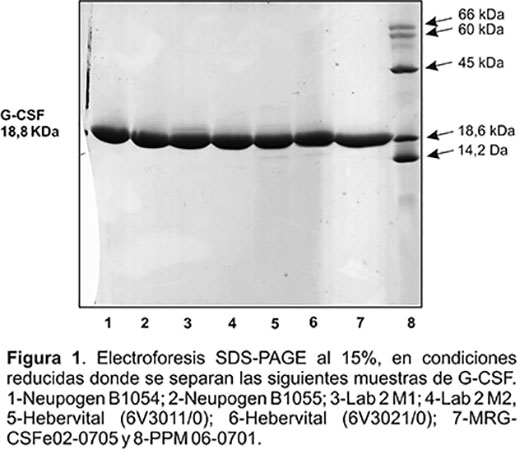
En la Figura 1 se observa la separación de las muestras de G-CSF en una electroforesis en gel de poliacrilamida en presencia de SDS al 15%.
Los resultados cualitativos muestran que el patrón de bandas de las muestras ensayadas es similar, la banda principal se encuentra en todas a la misma altura y por consiguiente concuerdan con la talla molecular del GCSF al compararlas con el material de referencia (procedente del CIGB) empleado en el estudio (carril 7). El carril 8 corresponde a patrones de pesos moleculares, provenientes de la firma SIGMA:
· Albúmina (BSA) 66 kDa
· Fumarasa (60 kDa)
· Ovoalbúmina (45 kDa)
· Lisozima (18,6 kDa)
· Alpha-Lactoalbúmina (14,2 kDa) ]]>
Al procesar la imagen para determinar los porcentajes de pureza de las muestras de interés se obtuvo que los resultados fueron superiores al 99%.Estudio comparativo por cromatografía en fase reversa
En los perfiles cromatográficos de las muestras ensayadas, al realizar la determinación del porcentaje del área bajo la curva, de cada muestra ensayada (Tabla 2) se obtuvo que la pureza es superior al 97%.
La comparación estadística de pureza de los resultados mostró un valor estadístico de p 20,05; esto fue válido en la pureza que se determinó en los cromatogramas entre grupos y dentro de grupo, por lo que se puede afirmar que no hubo diferencias significativas entre los resultados de pureza de los 2 productos.
Actividad biológica
Se llevaron a cabo al menos cuatro ensayos diferentes, los resultados se muestran en la Tabla 3.
En el Hebervital los lotes tienen un valor asignado de 30 millones de unidades/mL. En el Neupogen la presentación en jeringuilla es a razón de 30 millones de unidades en 0,5 mL; por tanto, la potencia que se asignó es de 60 millones de unidades/mL. El valor que se obtuvo para todas las muestras se encuentra entre el 90-110% del valor nominal, con resultados muy similares entre cada una.
Estudio comparativo de la estructura primaria
El primer paso fue la alquilación de la cisteína libre por reacción con iodoacetamida, ya que según lo planteado por otros autores (10), el G-CSF es una proteína de 175 aminoácidos, que consta de cinco cisteínas de las cuales cuatro forman puentes de disulfuro (Cys37-Cys43 y Cys65-Cys75), mientras que la Cys18 se encuentra libre. Este reactivo reacciona específicamente con los grupos tioles libres, lo cual facilita el análisis por espectrometría de masas de la proteína, además de evitar el intercambio de puentes de disulfuro durante el proceso de digestión enzimática. ]]>
Las muestras de proteína carbamidometilada se purificaron por CLAR y se analizaron por ESI-MS. Los espectros de masas obtenidos se muestran en la Figura 2.Teniendo en cuenta la secuencia del ADN, la formación de puentes de disulfuro y la modificación introducida por la reacción con iodoacetamida, el peso molecular esperado para el G-CSF debe ser de 18855,93 Da. Los espectros de masa demostraron una alta concordancia de los valores de masas experimentales con el valor de masas esperado para el G-CSF carbamidometilado (Tabla 4).
Las muestras de proteína carbamidometilada se digirieron con tripsina y endoproteinasa Glu-C. Este tratamiento permite obtener en péptidos independientes, a la cisteína carbamidometilada y a las implicadas en la formación de puentes de disulfuro.
En la Figura 3 se muestra los perfiles obtenidos por CLAR. Se observa alta reproducibilidad entre todos los mapas peptídicos.
Se señalan las fracciones correspondientes a los péptidos N- y C-terminal, a los puentes de disulfuro entre las cisteínas 37 y 43 y entre las cisteínas 65 y 75, y la presencia de la cisteína 18 en forma libre, como corresponde a la estructura primaria del G-CSF natural. Las fracciones a, b y c indican la presencia de cisteínas libres y puentes S-S incorrectamente formados.
También se analizaron por espectrometría de masas las fracciones 1-5 y las fracciones minoritarias a, b y c. Los valores de m/z obtenidos para cada una y su asignación a péptidos del G-CSF se muestran en la Tabla 5.
En las fracciones 1 y 4 los péptidos eluyeron reproduciblemente de m/z 565,31 y 894,00, los cuales se asignaron a los extremos N y C del G-CSF, respectivamente. En la fracción 2 se obtuvo una señal de m/z de 402,70 correspondiente al péptido 18Ccm-Arg23 (Ccm: cisteína carbamidometilada) con su masa incrementada en 57 Da, producto de la alquilación de Cys18. Las fracciones 3 y 5 portaron péptidos con los puentes de disulfuro correctamente formados entre las cisteínas 37Cys-Cys43 y 65Cys-Cys75.
En los espectros de masas de las fracciones a y b se observaron las señales de m/z 392,67 y 378,20, que luego de su secuenciación se asignaron a los péptidos 42Leu-Glu47 y 36Leu-Lys41 que contenían a la Cys43 y Cys37 carbamidometiladadas. La presencia de las cisteínas 37 y 43 en forma de carbamidometilcisteína no fue producto de una alquilación excesiva de la proteína, ya que si se comparan el peso molecular de la proteína no derivatizada (18798,98 Da) y los valores de masa observados (Tabla 4) se corrobora la alquilación de una sola cisteína por molécula de proteína y que esta, además, se encontró en forma de cisteína libre.
En la fracción se eluyeron los péptidos de m/z 736,33 y 721,86. La señal de m/z 736,33 se asignó a los péptidos Cys18-Arg23 y Leu42-Glu47 unidos por un puente de disulfuro entre las cisteínas 18 y 43, mientras que la señal de m/z 721,86 se asignó a los péptidos Cys18-Arg23 y Leu36-Lys41 enlazados también mediante puente de disulfuro entre las cisteínas 18 y 37. Estos resultados indicaron la presencia, en las preparaciones de GCSF analizadas, de puentes disulfuro incorrectamente formados entre las Cys18-Cys37 y Cys18-Cys43. No obstante, en la explicación de este fenómeno no se descarta la posibilidad excepcional de que el proceso de modificación química a pH básico, promueva un intercambio de puentes de disulfuro y que esta reacción ocurrió más rápidamente que la alquilación con iodoacetamida de la proteína. Tabla 5. Valores de m/z de cada fracción cromatográfica analizada de la digestión con tripsina y Glu-C del G-CSF y su asignación a regiones de la proteína.
Los experimentos realizados no permitieron la cuantificación de las especies moleculares con formación incorrecta de puentes de disulfuro. Sin embargo, las fracciones cromatográficas donde se detectó esta modificación son realmente minoritarias, además de ser similares en cada mapa peptídico. Este resultado sugiere que la presencia de moléculas con formación incorrecta de puentes de disulfuro corresponde a una mínima fracción de las muestras y que este fenómeno se comporta de manera similar en cada una. ]]>
Se demostró que el G-CSF que se utilizó en este trabajo cumple con las especificaciones establecidas por USP y la Pharmacopeia Europea para el Neupogen en cuanto a pureza, sin diferencias significativas con el mismo. La digestión con tripsina y endoproteinasa Glu-C del G-CSF derivatizado con iodoacetamida y la separación de los péptidos proteolíticos generó mapas peptídicos reproducibles y de elevada similitud entre cada una de las muestras analizadas. La verificación de los extremos N y C, y la obtención de los espectros ESI-MS de la proteína carbamidometilada, demostraron la integridad de cada una de las muestras de proteína. Se detectó los puentes de disulfuro entre las cisteínas 37 y 43 y entre las cisteínas 65 y 75, y la presencia de la cisteína 18 en forma libre, como corresponde a la estructura primaria del G-CSF natural. La caracterización demostró su integridad ya que la masa molecular de la proteína coincide con el valor esperado, se secuenciaron los péptidos N y C y no se encontró degradación por los extremos, lo que también demuestra que el proceso que se desarrolló genera un producto de buena calidad, de acuerdo a la caracterización tanto del IFA como del producto terminado.El conjunto de resultados de esta investigación indica que la estructura primaria del G-CSF producido en el CIGB (Hebervital) y el Neupogen, de la compañía Amgen, son similares.
AGRADECIMIENTOS
El colectivo de autores agradece el trabajo realizado por los coautores y colaboradores pertenecientes a los departamentos de Producción, Control de la Calidad, e Investigaciones Biomédicas en la fabricación y caracterización estructural del Hebervital, así como a la Dirección General del CIGB y los Departamentos de Negocios y Comercialización de la Empresa Heber Biotec S.A., por la labor en la obtención del Neupogen, medicamento innovador que se utilizó como patrón en el estudio comparativo.
REFERENCIAS
1. Shoemaker CW, Ayres MS, Grenvik GA, Holbrook RP. Factores estimulantes de colonias hematopoyéticas. En: Tratado de Medicina Crítica y Terapia Intensiva. 4ta Edición. México D.F: Editorial Médica Panamericana; 2000. p. 531-9.
2. Tanwar S, Thursz M. Granulocite colony-stimulating factor as a novel adjunct to improve hepatitis B vaccination. World J Hepatol 2010;2(3):136-8.
3. Saab BY, Sharaf L, Zeidan I, Bizri A. Filgrastim use: evaluation in cancer and critically ill non-cancer patients. Cancer Therapy 2003;1:191-6.
4. Bernstein HM, Pollock BH, Calhoun DA, Christensen RD. Administration of Recombinant Granulocyte Colony-Stimulating Factor to Neonates with Septicemia: A Meta-Analysis. Journal of Pediatrics 2001;138(6):917-20.
5. Metcalf D. Hemopoietic regulators. Trends Biochem Sci 1992;17(8):286-9.
6. Hartung T. Anti-inflammatory effects of granulocyte colony-stimulating factor. Curr Opin Hematol 1998;5(3):221-5.
7. Hartung T. Immunomodulation by colony-stimulating factors. Rev Physiol Biochem Pharmacol 1999;136:1-164.
8. Souza LM, Boone TC, Gabriole J, Lai PH, Zsebo KM, Murdock DC, et al. Recombinant human granulocyte colony-stimulating factor: effects on normal and leukemic myeloid cells. Science 1986;232:61-5.
9. Lieschke GJ, Burguess AW. Granulocyte-Macrophage Colony-stimulating Factor. New England Journal of Medicine 1992;327:28-35.
10. Herman A, Boone T, Lu H. Characterization, Formulation, and Stability of Neupogen (Filgrastim), a Recombinant Human Granulocyte-Colony Stimulating Factor. Pharmaceutical Biotechnology 2002;9:303-28.
11. Georgiou G, Valax P. Isolating inclusion bodies from bacteria. Methods Enzimology 1999;309:48-58.
12. Lowry OH, Rosebrough NJ, Farr AL, Randall RJ. Protein measurement with the follin phenol reagent. J Biol Chem 1951;193:265-75.
13. Herman AC, Boone TC. Characterization, formulation and stability of Neupogen (filgrastim), a Recombinant Human Granulocyte-Colony Stimulating Factor. Pharm Biotechnol 1996;9:303-28.
14. Westermeier R. Electrophoresis in Practice. Fourth revised and enlarged edition. Wenham: Wiley-VCH Verlag GmbH & Co. KGaA; 2005.
15. Carr D. HPLC as a tool to Purify and Isolated. In: The Handbook of Analysis and Purification of Peptides and Proteins by Reversed-Phase HPLC. 3rd Edition. Hesperia, California: Grace Vydac; 2002.p.40-9.
16. European Pharmacopeia. Directorate for Quality of Medicines. Filgrastim concentrate solution (2206). European Pharmacopeia 2009;6(3):4142-4.
17. Sambrook J, Rusell DW. Molecular Cloning: a laboratory manual, Ch 9; 3rd edition. New York: Cold Spring Harbor Laboratory; 2001.
18. United States Pharmacopeia 35-NF 30. Pharmaceutical Compounding Sterile Preparations, Chapter 797. Rockville: USP-NF General; 2012.p.1-38.
19. Millipore Corporation. Protein Blotting Applications Guide. Technical Protocol TP001. Bedford (MA): Millipore Corporation; 1997. Disponible en: http://www.fisher.co.uk/techzone/life/hints/Millipore1.pdf
20. Towbin H, Staehelin T, Gordon J. Electrophoretic transfer of proteins from polyacrylamide gels to nitrocellulose sheets: procedure and some applications. Proc Natl Acad Sci USA 1979;76(9):4350-4.
Recibido: Mayo de 2013 ]]> Aceptado: Julio de 2013
]]>