ARTÍCULO ORIGINAL
Evaluación de los Anticuerpos Monoclonales anti-polisacárido capsular de Neisseria meningitidis serogrupos A, C, Y, W y X para su uso en los ensayos de identidad
Evaluation of monoclonal antibodies to the capsular polysaccharide of Neisseria meningitidis serogroups A, C, Y, W and X to be used in the identity assays
Elizabeth González-Aznar,1* Oscar Otero-Alfaro,1 Osmir Cabrera-Blanco,1 Fidel Ramírez-Bencomo,1 Abel Fajardo-Sánchez,2 Aleida Mandariote-Llanes,3 Maribel Cuello-Pérez1
1 Departamento de Anticuerpos Monoclonales y Diagnosticadores, Dirección de Investigación-Desarrollo, Instituto Finlay. Cuba.
]]> 2 Facultad de Biología, Universidad de La Habana. Cuba.3 Departamento de Control de la Calidad, Instituto Finlay. Cuba.
email: elygonzalez@finlay.edu.cu
* Médico General.
RESUMEN
Los serogrupos A, B, C, W, Y y X de Neisseria meningitidis (Nm) son los principales responsables de la enfermedad meningocóccica y contra ellos va dirigido actualmente el desarrollo de vacunas para la prevención de la enfermedad. El Instituto Finlay se encuentra desarrollando vacunas antimeningocóccicas polisacarídicas contra los serogrupos A, C, W, Y y X. En el desarrollo de estas vacunas, el ensayo de identidad constituye un requisito obligatorio para la liberación final del producto. Este ensayo se realiza mediante la técnica Dot Blot, utilizando anticuerpos policlonales (AcP) comerciales; sin embargo, el Instituto Finlay cuenta en este momento con una plataforma de Anticuerpos Monoclonales (AcM) contra los cinco polisacáridos (PsC) de Nm. El objetivo del trabajo fue evaluar la sensibilidad y especificidad de estos AcM para su uso en los ensayos de identidad de las vacunas antimeningocócicas polisacarídicas, con vista a sustituir los AcP comerciales empleados hasta el momento. La sensibilidad de los AcM se evaluó frente al PsC homólogo y la especificidad frente al resto de los PsC de Nm. Se realizó el ensayo de identidad por Dot Blot a cuatro vacunas polisacarídicas multivalentes, usando los AcM comparativamente con los AcP. Todos los AcM evaluados mostraron una alta sensibilidad y especificidad, no encontrándose reactividad cruzada y siendo capaces de identificar en las formulaciones vacunales multivalentes la presencia del PsC homólogo. Concluimos que los AcM obtenidos en nuestro instituto pueden ser usados para los ensayos de identidad de las vacunas.
Palabras claves: ensayo de identidad, Dot Blot, anticuerpos monoclonales, Neisseria meningitidis
ABSTRACT ]]>
Neisseria meningitidis serogroups A, B, C, W, Y and X are the main responsible of meningococcal disease. Vaccines are necessary to prevent this disease. The Finlay Institute is developing polysaccharide vaccines against serogroups A, C, W, Y and X. In the development of vaccines, the identity assay is a mandatory requirement for final product release. This test is performed by Dot Blot technique using commercial polyclonal antibodies (PAb). However, the Finlay Institute has monoclonal antibodies (mAbs) against capsular polysaccharides from N. meningitidis (CPs). The objective of this work was to use these mAbs in identity tests to replace commercial PAb. The specificity of the mAbs, the cross-reactivity with other CPs and the identity of the CPs present in four multivalent polysaccharide vaccines, were evaluated. All tested mAbs showed high specificity, and no cross-reactivity was found. Also all mAbs were able to identify the presence of homologous PsC in multivalent vaccine formulations. We conclude that the mAbs obtained in our institution can be used for identity assays of vaccines.Keywords: identity asay, Dot Blot, monoclonal antibodies, Neisseria meningitidis.
INTRODUCCIÓN
La enfermedad meningocócica (EM) es uno de los grandes problemas de salud a nivel mundial, que afecta principalmente a los niños y adolescentes, con una elevada morbilidad y mortalidad. Tiene como agente etiológico la bacteria Gram negativa Neisseria meningitidis (Nm), patógeno exclusivo del hombre, que utiliza como puerta de entrada al organismo la nasofaringe (1). Se han descrito 13 serogrupos según las características antigénicas de los polisacáridos de la cápsula (PsC); sin embargo, son los serogrupos A, B, C, Y, X y W los principales responsables de la enfermedad (2). La distribución epidemiológica por serogrupos varía, siendo a nivel mundial los serogrupos A, B y C los más frecuentes. No obstante, la mayor incidencia de la EM se encuentra en el llamado cinturón africano de la meningitis, donde los serogrupos más frecuentes son el A, C, Y, W y X (3).
Los primeros intentos de vacunas contra Nm se realizaron a principio del siglo XX cuando Davis, en 1907, se realizó una autoinoculación subcutánea de suspensiones de meningococos completos inactivados por calor, lo cual resultó ser muy reactogénico (1). Desde entonces varias han sido las estrategias llevadas a cabo para el desarrollo de vacunas, dentro de las que podemos citar: vacunas basadas en vesículas de membrana externa (VME) o Proteoliposomas (PL) (4), vacunas basadas en los PsC (Vacunas Polisacarídicas conjugadas o no), vacunas basadas en ingeniería genética (Vacunas Recombinantes) y combinaciones entre ellas (5). Las estrategias vacúnales actuales están dirigidas al desarrollo de vacunas multivalentes contra los serogrupos A, C, Y, W y X (6). El Instituto Finlay, centro dedicado a la investigación, desarrollo y producción de vacunas y pionero en el desarrollo de la primera vacuna contra el meningococo B, se encuentra inmerso en el desarrollo de vacunas polisacarídicas contra los serogrupos A, C, Y, W y X de Nm.
Los procesos de desarrollo y producción de vacunas llevan consigo la aplicación de métodos que permitan identificar o cuantificar los principios activos presentes en las formulaciones (el PsC en este caso) como requisito obligatorio para la liberación final del producto (7). Dentro de los ensayos que se realizan para la liberación de lotes se encuentran: potencia, inocuidad, identidad, esterilidad, pureza, pirogenicidad, por citar algunos (6, 7). Los ensayos de identidad deben ser capaces de identificar los compuestos del producto analizado, así como discriminar entre compuestos parecidos o de estructura relacionada que formen parte de la formulación. Estos ensayos de identidad se hacen más complejos en las vacunas antimeningocócicas polisacarídicas multivalentes, debido a la similitud de grupos funcionales en la estructura química de estos PsC (8).
Varios son los métodos usados para la realización de los ensayos de identidad, aunque por lo general se recomienda el uso de métodos inmunoquímicos (ELISA (Enzyme-Linked-Immunosorbent Assay), Western Blot y Dot Blot) pues además de su alta especificidad y sensibilidad son métodos rápidos y de fácil realización (7, 9). En el Instituto Finlay los ensayos de identidad de las vacunas antimeningocócicas polisacarídicas se realizan mediante la técnica de Dot Blot y en el caso de la identidad del PsC de Nm serogrupo C en la vacuna VA- MENGOC-BC® se realiza por la técnica de aglutinación con partículas de látex. Ambos métodos ofrecen un importante ahorro de tiempo; sin embargo, su limitante ha sido la adquisición de los sueros policlonales y de los reactivos látex, que generalmente son comerciales.
Los Anticuerpos policlonales (AcP) son mezclas heterogéneas, con diferentes afinidades y especificidades, lo que unido a la variabilidad de lote a lote, constituye una desventaja. Los anticuerpos monoclonales (AcM) sin embargo, tienen propiedades que los hacen excepcionales: especificidad, reproducibilidad y constituyen una fuente inagotable. Los AcM con sus grandes ventajas han revolucionado el desarrollo de las investigaciones en el campo de la Inmunología, las técnicas analíticas, diagnósticas, la seroterapia y los procesos industriales (10).
]]> El Grupo de AcM del área de Investigaciones del Instituto Finlay ha obtenido AcM contra varios antígenos (Ag) de diferentes bacterias, actualmente usados para el control de la calidad de vacunas (11). Recientemente, Reyes y col obtuvieron AcM contra los cinco PsC de Nm serogrupos A, Y, C, W y X (12,13) y validaron su uso en la cuantificación de estos PsC de Nm en vacunas polisacarídicas multivalentes, mediante ELISA tipo sándwich (14). De igual forma estos anticuerpos pueden ser usados en el ensayo de identidad por Dot Blot de las vacunas polisacaridicas contra Nm serogrupos A, C, Y, W y X.El objetivo de este trabajo fue evaluar la sensibilidad y especificidad de los AcM anti PsC de Nm, para su uso en los ensayos de identidad por Dot Blot, de las vacunas meningocócicas multivalentes desarrolladas en el Instituto, con vista a sustituir el uso de AcP comerciales.
MATERIALES Y MÉTODOS
Muestras
Polisacáridos capsulares: Los PsC de Nm (Polisacárido capsular para el control interno, PCI), serogrupos A (PACI), C (PCCI), W (PWCI), Y (PYCI) y X (PXCI) fueron suministrados por el grupo de materiales de referencias del Instituto Finlay. Todos se prepararon a una concentración de 1mg/mL en agua destilada.
Anticuerpos Monoclonales: Los AcM murinos anti polisacárido capsular de Nm utilizados fueron: 7E1F7 AcM-anti PsC serogrupo A, 7E12B3 AcM-anti PsC serogrupo C, 5C11F1 AcM-anti PsC serogrupo W, 5H10D9 AcM-anti PsC serogrupo Y y 10B5F10 AcM- anti PsC serogrupo X, todos obtenidos por el grupo de Anticuerpos Monoclonales del Instituto Finlay.
Anticuerpos policlonales: Como AcP se emplearon los sueros aglutinantes (Meningococcus Agglutinating Sera (MAS)), Remel Europe Ltd, Reino Unido. Estos sueros son los que se emplean en el Instituto para los ensayos de identidad de las vacunas antimeningocóccicas. MAS-ZM37 anti Nm serogrupo A, MAS-ZM39 anti Nm serogrupo C, MAS-ZM44 anti Nm serogrupo W, MAS-ZM41 anti Nm serogrupo X y MAS-ZM42 anti Nm serogrupo Y.
Vacunas: Vacuna Antimeningocóccica BC, VA- MENGOC-BC®, Instituto Finlay, Lote 0016. Vacuna Polisacarídica Antimeningocóccica A, C, W, Finlay/ Bio Manguinhos, Lote 113VMW002Z. Vacuna Polisacarídica Antimeningocóccica, DF-Men ACWY, Instituto Finlay, Lote 102 y Vacuna Polisacarídica Antimeningocóccica DF-Men ACWXY, Instituto Finlay, Lote 104.
Dot Blot
]]> Para la realización del Dot Blot, se utilizó un equipo Minifold II S&S (Alemania) acoplado a bomba de vacío y se empleó membrana de nitrocelulosa (MNC) de 0,2 µm (Bio-Rad, EUA). Se realizaron tres Dot Blot con los siguientes objetivos: seleccionar las concentraciones óptimas de AcM y de PCI a emplear; evaluar la sensibilidad y especificidad de los AcM comparativamente con los AcP y realizar el ensayo de identidad de vacunas polisacarídicas multivalentes usando los AcM.Selección de las concentraciones óptimas de los PsC y de los AcMs a utilizar: Para la inmovilización de los diferentes PCI (A, C, W, X y Y) de Nm a la MNC, se aplicaron 2, 5 y 10 µg de PCI por pozo bajo presión de vacío. Posteriormente se extrajo la MNC del equipo y se procedió al proceso de bloqueo de los sitios activos remanentes con Solución Salina Tamponada de Fosfato (SSTF) y Leche descremada (LD) al 3% durante 30 min a 37°C. Después de tres lavados de 5 min cada uno con SSTF/Tween 20 al 0,05%, se recortó la MNC en tiras verticales (cuatro tiras por cada PCI), para ser incubadas durante 1 h a 37°C, con 5 mL de cuatro concentraciones (1, 2, 5 y 10 µg/mL) de su respectivo AcM. Pasado este tiempo y tras tres lavados de similares características se incubaron todas las tiras 1 h a temperatura ambiente (TA) con un segundo anticuerpo (anti IgG de ratón conjugado a peroxidasa, AmershamTM, Reino Unido) a una dilución de 1:4000 en SSTF-LD 1% según fabricante. Seguidamente se realizaron 5 lavados de 3 min y se procedió al revelado para lo cual se cubrió cada tira con SSTF/3,3-tetrahidrocloro Diaminobenzidina (DAB) al 0.04% y peróxido de hidrógeno (H2O2) al 0,5%, durante 20 minutos. La reacción se detuvo realizando varios cambios con agua destilada.
Evaluación de la especificidad de los AcM: La especificidad se determinó mediante la técnica de Dot Blot. Se inmovilizaron 5 µg de cada PCI (A, C, W, X y Y) en una misma tira de MNC y cada tira se incubó con un AcM (5ug/mL) o con un AcP (dilución 1:25). Como segundo anticuerpo para los AcP se empleó el anti-IgG de conejo HRP (Sigma-Aldrich, EUA) a una dilución de 1:2000 en SSTF-LD 1% según fabricante.
Ensayo de identidad de las vacunas multivalentes: Para el ensayo de identidad se realizó un Dot Blot siguiendo el mismo procedimiento ya descrito. En este caso, en cada tira de MNC se inmovilizaron las cuatro vacunas (una vacuna por pozo) a una concentración de 100 µg/mL de PsC total (5 µg/pozo). Se emplearon 10 tiras, 5 para ser enfrentadas a cada AcM y 5 para ser enfrentadas a cada AcP. El resto de los procedimientos de bloqueo, lavado y revelado fueron similares al Dot Blot anterior. El ensayo de identidad de las vacunas evaluadas se realizó por triplicado, para confirmar los resultados obtenidos.
Captura y procesamiento de las imágenes: Las imágenes de los Dot Blot fueron capturadas y procesadas utilizando un densitómetro GS-800 (Bio-Rad, EUA) con software de cuantificación (Quantity One).
RESULTADOS Y DISCUSIÓN
Selección de las concentraciones óptimas de los PsC y de los AcMs en el Dot Blot
Para determinar la identidad por Dot Blot, se procedió como primer paso a determinar las concentraciones óptimas de: inmovilización de cada PCI y de detección de cada AcM a utilizar en la técnica. (Fig. 1).
Se puede observar la presencia de manchas oscuras donde existe reconocimiento del PCI por su respectivo AcM. Cuanto mayor es el reconocimiento, mayor es la intensidad del color. Para los PACI (Fig 1 A) y PYCI (Fig 1 D) se observan manchas oscuras en todas las concentraciones de PsC aplicadas (2, 5 y 10 µg/pozo) no observándose variación al incrementar la concentración del AcM. Sin embargo, en el caso de PCCI (Fig 1 B), PWCI (Fig 1 C) y PXCI (Fig 1 E) las manchas oscuras se comienzan a observar a partir de los 5 µg/pozo de PsC aumentando la intensidad de la señal con el incremento de la concentración del AcM empleado, llegando a ser la concentración de 10 µg/mL, donde se observó la mancha con mayor intensidad de color. De esta forma se seleccionó la cantidad de 5 µg/pozo de PsC como la optima para la inmovilización y 5 µg/mL de AcM como la concentración òptima de reconocimiento.
]]> En los ensayos inmunoenzimáticos como el Dot Blot, donde hay una etapa de inmovilización o captura de una biomolécula, determinar la concentración óptima de la misma a inmovilizar (en este caso el PsC) es un factor de suma importancia. Igualmente lo es la selección de las concentraciones óptimas de la molécula reactante (el AcM en este caso). Estos parámetros influyen en la formación de los complejos Ag-Ac, donde la concentración de ambas moléculas tienen que estar en el rango de la zona de equivalencia (9).Las elevadas concentraciones del material de captura pueden provocar alteraciones en la sensibilidad y en el límite de detección del ensayo (efecto "gancho") por la formación de sobrecapas de biomoléculas débilmente adsorbidas, que se liberan fácilmente en los pasos siguientes, inhibiendo los inmunorreactantes en la fase liquida (9). Concentraciones entre 1-10 µg/mL son reportadas como suficientes (9), lo cual concuerda con los resultados aquí obtenidos donde con 5 µg de PCI y 5 µg/mL de AcM para la captura y la detección respectivamente se evidenció reconocimiento.
Especificidad de los AcM
Una vez establecidas las concentraciones de trabajo de los PsC y del AcM, otro aspecto importante a evaluar fue la especificidad de los AcM utilizados. La Figura 2 muestra los resultados obtenidos en el ensayo de especificidad. En este ensayo cada AcM se enfrentó a una tira de MNC en la cual fueron inmovilizados los cinco PCI de Nm (A, C, W, X y Y). El objetivo de este ensayo fue demostrar que cada AcM era capaz de reconocer solamente al PsC homólogo (especificidad) y no a los PsC de los restantes serogrupos (reactividad cruzada) presentes en la MNC. Comparativamente se evaluó la especificidad de los AcP (Remel, UK) como control de la técnica por ser los que se usan en los ensayos de identidad de las vacunas.
Como se muestra en la Figura 2 tanto los AcM (Fig. 2A) como los AcP (Fig. 2B) reconocen en la MNC solamente al PsC homologo. Dicho reconocimiento se evidencia por la presencia de manchas oscuras (señal) solamente en el pozo donde se encuentra inmovilizado el PsC homólogo. Sin embargo, en el resto de los pozos donde se encuentran los otros PsC no se observa señal, no evidenciándose reactividad cruzada. Este resultado concuerda con los obtenidos por Reyes y col en el 2013 donde utilizaron estos anticuerpo monoclonales, A, C W X y Y en ensayos de identidad y cuantificación de vacunas polisacarídicas múltiples por ELISA con adecuada especificidad (14).
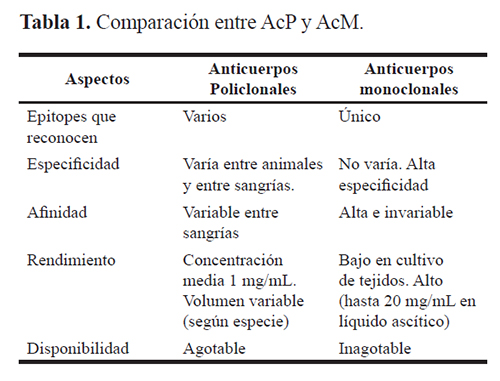
Si bien no se encontró diferencias en cuanto a la especificidad de los AcM respecto a los AcP empleados, es importante recordar que existen otros aspectos que constituyen las grandes ventajas que sobre los AcP presentan los AcM. (Tabla 1) (10).
En el año 2010, los AcM cumplieron 30 años desde su invención, por lo que si bien su obtención no constituye una novedad por estos días, en nuestro caso, el ser propietarios de los hibridomas productores de todos estos AcM, únicos en nuestro país, representa una ventaja indudable. Su uso no estaría condicionado a la compra en el mercado, así como podría resultar más económica la implementación de su uso para esta prueba en la liberación de los lotes de vacunas.
Ensayo de identidad
Una vez conocida la especificidad de los AcM, se procedió a evaluar su uso en el ensayo de identidad de varias vacunas polisacarídicas multivalentes contra Nm comparándolos con los AcP.
]]> En la Figura. 3 se muestra que los AcM (Fig. 3A) al igual que los AcP (Fig. 3B) fueron capaces de identificar en cada formulación evaluada, su correspondiente PsC de forma especifica, no evidenciándose señal en los pozos donde la vacuna aplicada no contenía el PsC homólogo, discriminando a los PsC de otros serogrupos.La identificación de los PsC de Nm, sobre todo en formulaciones multivalentes, es un proceso complejo, debido a la similitud de grupos funcionales en la estructura química que existe entre ellos (Tabla 2). Por lo que contar con AcM capaces de identificar al PsC homólogo (especificidad) discriminando entre compuestos parecidos o de estructura relacionada como son los PsC heterólogos, constituye sin duda una gran herramienta para estos ensayos, sobre todo si tenemos en cuenta las ventajas que tienen sobre los AcP.
En el caso de la vacuna VA-MENGOC-BC®, vacuna basada en el proteolipososma de Nm serogrupo B y en el PsC del serogrupo C adsorbida en hidróxido de aluminio, el resultado del ensayo de identidad del PsC, tiene además otra importancia y es el hecho de que el ensayo de identidad de esta vacuna, lleva un paso intermedio de preparación de la muestra donde se necesita desadsorber los ingredientes activos de la vacuna para llevar a cabo el ensayo, pues el hidróxido de aluminio presente en la formulación interfiere con los resultados.
En nuestro estudio, sin embargo, para realizar el Dot Blot no hubo necesidad de realizar este paso sino que se aplicó la vacuna directamente sobre la MNC.
CONCLUSIONES
Los ensayos de identidad de las vacunas constituyen un aspecto importante para la liberación de lotes y control de la calidad de las mismas. Garantizar los reactivos necesarios para su realización tanto en cantidad como en calidad también es un aspecto necesario.
Si bien estos ensayos se han venido realizando con el uso de AcP comerciales, contar con una batería de AcM (única en el país) con una alta especificidad, reproducibilidad y de producción institucional, es un gran logro.
Estos AcM además pueden ser usados con otros fines que no sean solo el de ensayos de identidad.
]]>REFERENCIAS
1. Ochoa RF, Sierra G, Martínez I, Cuevas I. Enfermedad meningocócica. Diagnóstico microbiológico. En: Prevención de la Enfermedad Meningocócica. La Habana: Finlay Ediciones; 2010.p.3-6.
2. Harrison LH, Trotter CL, Ramsay ME. Global epidemiology of meningococcal disease. Vaccine 2009;27(Suppl 2):51-63.
3. WHO. Meningococcal disease in countries of the African meningitis belt, 2012 – emerging needs and future perspectives. WHO 2009. Properties 2013.Weekly Epidemiological Record 2013;88:129-36.
4. Holst J, Martin D, Arnold R, Huergo CC, Oster P, O’Hallahan J, et al. Properties and clinical performance of vaccines containing outer membrane vesicles from Neisseria meningitidis.Vaccine 2009;27(Suppl 2):3-12.
5. Healy M, Baker C. The Future of Meningococcal Vaccines. Pediatric Infectious Disease Journal 2005;24(2):175-6.
6. Danzig L. Meningococcal Vaccines. Pediatric Infectious Disease Journal 2004;23(12):285-92.
7. CECMED. Requisitos para la liberación de lotes de vacunas. Regulación No.19-2000. La Habana: CECMED; 2000.
8. Cook MC, Bliu A, Kunkel JP. Quantitation of serogroups in multivalent polysaccharide-based meningococcal vaccines: optimisation of hydrolysis conditions and chromatographic methods. Vaccine 2013;31(36):3702-11.
9. Ochoa RF. Técnicas inmunoenzimáticas en el desarrollo clínico de vacunas. La Habana: Finlay Ediciones; 2013.
10. Goding JW. Monoclonal Antibodies: Principles and practice. San Diego: Academic Press; 1996.
11. Falero G, Rodríguez BL, Rodríguez I, Campos J, Ledon T, Valle E, et al. Production and characterization of monoclonal antibodies to E1 Tor toxin co-regulated pilus of Vibrio cholerae. Hybrid Hybridomics 2003;22(5):315-20.
12. Reyes F, Amin N, Otero O, Aguilar A, Cuello M, Valdés Y, et al. Four monoclonal antibodies against capsular polysaccharides of Neisseria meningitidis serogroups A, C, Y and W135: its application in identity tests. Biologicals 2013;41(4):275-8.
13. Reyes F, Otero O, Camacho F, Amin N, Ramírez F, Valdes Y, et al. A novel monoclonal antibody to Neisseria meningitidis serogroup X capsular polysaccharide and its potential use in quantitation of meningococcal vaccines. Biologicals 2014;42(6):312-5.
14. Reyes F, Otero O, Cuello M, Amin N, García L, Cardoso D, et al. Development of four sandwich ELISAs for quantitation of capsular polysaccharides from Neisseria meningitidis serogroups A, C, W and Y in multivalent vaccines. J Immunol Methods 2014;407:58-62.
]]> Recibido: Noviembre de 2014 Aceptado: Febrero de 2015 ]]>