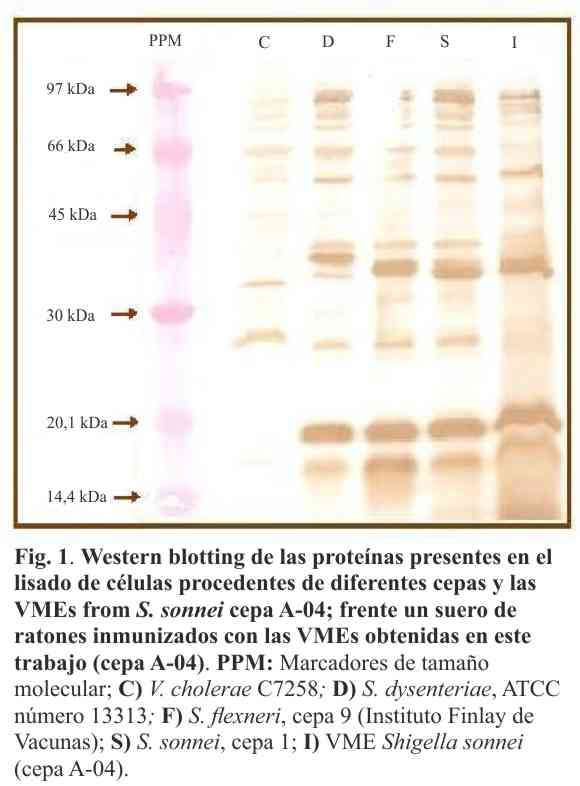
Caracterización proteómica de vesículas de membrana externa extraídas de Shigella sonnei
Proteomic characterisation of outer membrane vesicle extracted from Shigella sonnei
María de los A Padrón-Collaz1*, Ileana Martínez-Cabrera2, Wheeler J3, Sonia Nisar3, Luis A Riverón-Martínez1, Miguel E Martínez-Pozo1, Carmen R Soto-Rodríguez1, Olga M Martínez-Fernández1, Ranset Diez-Martin1, José L Pérez-Quiñoy1, Luis García-Imia1, Arturo Talavera-Coronel1, Gustavo V Sierra-González1, Christopher Jones3
1 Instituto Finlay de Vacunas. Ave 27, No 19805, La Lisa, La Habana, Cuba.
2 Departamento de Biología Fundamental y Ciencias de la Salud. Universidad de las Islas Baleares. España.
]]> 3 Laboratory for Molecular Structure. National Institute for Biological Standards and Control, Blanche Lane, South Mimms, Herts EN6 3QG, UK.
email: mapadron@finlay.edu.cu
* Máster en Ciencias y Tecnólogo de II nivel.
RESUMEN
Las vacunas compuestas por vesículas de membrana externa (VMEs) previenen de manera exitosa la enfermedad meningocócica del serogrupo B. Esta plataforma tecnológica de obtención puede ser aplicada para otros patógenos bacterianos Gram negativos. Una vacuna de VMEs desarrollada contra Shigella sonnei fue obtenida a través de una extracción de componentes celulares y su caracterización por electroforesis en geles de poliacrilamida unidimensional (1D). Se estudiaron las mejores condiciones de solubilización de las muestras, separación electroforética e identificación a través de espectrometría de masas acoplada a cromatografía de alta presión después del corte de las bandas y su tratamiento enzimático con tripsina. En esta etapa se identificaron un total de 57 proteínas en 23 bandas (2,5 proteínas por banda escindida), 47 de las proteínas no repetidas. Las proteínas inmunogénicas presentes en VMEs de S. sonnei fueron cuantificadas en cuanto a masa molecular por 1D-Western blotting en membranas de nitrocelulosa con anticuerpos obtenidos a partir de ratones inmunizados con las VMEs. Como que las bandas electroforéticas 1D contenían más de una proteína, se estudiaron las mejores condiciones de separación por el método de electroforesis bidimensional (2D) para el establecimiento del mapa proteico; tal que el incremento del tamaño de las tiras, el tiempo de focalización y la aplicación catódica garantizaron la mayor resolución.
Palabras clave: Shigella sonnei, vacunas, métodos proteómicos, proteínas de membrana externa.
ABSTRACT
Outer membrane vesicles (OMVs) vaccines successfully prevent Group B meningococcal disease. This platform technology may be applied against other Gram negative bacterial pathogens. An OMV vaccine against Shigella sonnei was prepared by detergent extraction of cells and characterised by one-dimensional polyacrylamide gel electrophoresis (1D). The protein components were quantified by staining and scanning and the composition of bands were defined by coupled high-performance low chromatography/electrospray ionization tandem mass spectrometry after band excision and in-gel trypsin digestion. 57 proteins contained in 23 bands (2.5 proteins/split band) were detected, 47 of them were not repeated. The S. sonnei OMVs immunogenic proteins were identified by 1D-immunoblotting, after transfer of proteins to a nitrocellulose membrane and treatment with antibodies generated by immunisation of mice with the OMVs. The bands detected by 1D had more than a single proteins, that is why we studied the best conditions for molecular separation by two-dimension electrophoresis (2D) for establishing the protein map; such that the increase of strips size, time of isoelectric focusing (IEF) and cup-cathodic loading guaranteed the highest resolution.
]]> Keywords: Shigella sonnei, vaccines, proteomic, outer membrane proteins.
INTRODUCCIÓN
Las infecciones bacterianas continúan siendo la causa de un gran número de niños fallecidos, especialmente en países en desarrollo; de ahí la necesidad de obtener vacunas efectivas, de bajo costo contra los principales patógenos. La shigellosis causada por Shigella sonnei, S. flexneri y S. dysenteriae es uno de los mayores problemas de la salud pública en niños pequeños y jóvenes en estos países (1, 2).
En América Latina, la resistencia de Shigella a los antibióticos se ha incrementado desde la década de los 90, principalmente contra S. sonnei (3). A pesar de que se han obtenido vacunas múltiples de diferentes serotipos de Shigella (a partir de su lipopolisacárido modificado) y que se han probado exitosamente en ensayos clínicos (4-6); no están comercialmente disponibles. Algunas vacunas de subunidades de Shigella aún están en fase preclínica; incluyendo una vacuna parenteral compuesta por proteína/ARN ribosomal (5) y una vacuna de proteosoma administrada por vía nasal compuesta por micelas de proteínas de membrana externa de Neisseria meningitidis serogrupo B unidas a lipopolisacáridos (LPS) de Shigella (7). Un ensayo preclínico con una vacuna intranasal de Invaplex 50 S. flexneri 2a demostró que era segura, inmunogénica y eficaz (8).
El Instituto Finlay de Vacunas ha sido de los primeros en desarrollar vacunas bacterianas compuestas por VMEs que contienen proteínas de membrana externa (PMEs) extraídas con detergentes a partir de las células, con el objetivo de proteger contra infecciones meningocócicas producidas por el serogrupo B ya que las vacunas de polisacárido B no son inmunogénicas (9, 10). La separación proteómica de los componentes proteicos de las VMEs presentes en estas vacunas ha permitido que se pueda evaluar su complejidad en términos de su identificación y cuantificación, lo cual ha permitido establecer el patrón proteico y preparar las condiciones para evaluar la consistencia del proceso de producción (10-12).
Martínez y colaboradores (13) seleccionaron una cepa de S. sonnei (A-04) aislada de pacientes como el mejor candidato para explorar si la tecnología de VMEs puede ser aplicada al desarrollo de una vacuna que proteja contra esta bacteria. Previamente se estudiaron 34 cepas aisladas a partir de heces fecales de pacientes con shigellosis que vivían en Ciudad de La Habana (entre los años 1999 y 2000). Las pruebas realizadas en modelos animales (Test de Sereny e inoculación nasal), nivel de expresión de proteínas determinado a través de electroforesis en geles de poliacrilamida (SDS-PAGE) sugirieron que la virulencia era adecuada, los síntomas y el perfil de histopatológico de la cepa A-04 eran adecuados para desarrollar una nueva vacuna (13). En un trabajo reciente realizado para demostrar el efecto de nueva vacuna compuesta por VMEs procedentes de S. flexneri, esta vacuna fue capaz de proteger contra la infección cuando se administró por vía mucosal (14, 15).
En estos trabajos se identificaron ocho proteínas: dos de estas proteínas fueron previamente descritas como IpaD y OmpA. Las proteínas identificadas como AnsB, TolC, Ggt, TolB se localizaron en la extracción de proteínas de membrana y en la fracción de proteínas solubles; mientras que GroEL, Spa33 e IpaD fueron detectadas exclusivamente como proteínas solubles inmunogénicas (15). Establecer estos patrones proteicos en nuestras preparaciones de VMEs permitirá consolidar el sistema de control de calidad de nuevos candidatos para el desarrollo de vacunas. El objetivo de este trabajo es la extracción de componentes proteicos de la membrana externa de la cepa de producción A-04 de S. sonnei, con un detergente para la obtención de VMEs, la identificación de las proteínas componentes a través de métodos proteómicos y la caracterización de las proteínas inmunoquímicas por Western blot.
]]> MÉTODOS
Preparación de las muestras en el Instituto Finlay
La cepa A04 de S. sonnei creció en un medio sintético optimizado de 20 L, a través de condiciones de fermentación discontinua tipo “batch”, a 37°C y con pH controlado a 7,4. Los cultivos se centrifugaron por espacio de 30 min, a 17700 x g, a 4°C. El sedimento lavado se resuspendió en tampón Tris 30 mM-EDTA 2 mM pH 8,5 hasta una concentración de 140 mg/mL. Las células se resuspendieron con una solución de duodecilsulfato de sodio (SDS) hasta una concentración final de 2 % w/v y se agitó suavemente en un baño de hielo, durante 1 h. Las suspensiones se centrifugaron a 17700 x g, a 4°C, durante 30 min.
Los sobrenadantes se trataron con una mezcla de DNAsa-RNAsa (0,1 mg/20 mL), a 37°C, durante 1 h y se centrifugó a 33300 x g, a 4°C, durante 15 min.
Los sobrenadantes se centrifugaron a 65000 x g, durante 8 h a 4°C y las PME sedimentadas se resuspendieron en Tris 30 mM EDTA 2 mM pH 8,5 y posteriormente se precipitaron con etanol (80 %) y se guardaron a –20°C.
Preparación de la mezcla de sueros contra VMEs de S. sonnei en el Instituto Finlay
Los anticuerpos contra las VMEs de S. sonnei fueron obtenidos por inmunización intramuscular de la pata izquierda de ratones Balb/c (peso entre 20-25 g), con 50 µg de proteínas (determinado por el método de Lowry) en tres dosis a tiempo: 0, 14 y 28 días. Los ratones se desangraron a los 14 días después de la última inoculación y se separó el suero por centrifugación a 2300 g en una centrífuga modelo BBVV (JOAN LAB, Francia). Se unieron los sueros de 10 ratones y se conservaron a -20°C para su uso en el método de Western blotting.
Minielectroforesis y electrotransferencia a membranas de nitrocelulosa a través del método de immunoblotting, realizado en el Instituto Finlay
Se aplicaron 20 µg de proteína en cada pocillo en un gel concentrador al 5% y un gel separador al 10%, con tampón de corrida (Tris-HCl 25 mM pH 8,3; glicina 192 mM; SDS 0,1%) en una cámara electroforética (Pharmacia LKB, USA) acoplada a una fuente (Multidrive Pharmacia LKB, Suecia) y corriente constante de 30 mA. Las proteínas separadas fueron transferidas a membranas de nitrocelulosa 0,45 µm, utilizando un tampón Tris 0,02 M; glicina 0,15M; SDS 0,1%; pH 8,3 y un sistema de transferencia (Mini Blot, BioRad), a temperatura y corriente constantes (8°C, 350 mA), durante 2 h. Las membranas se incubaron en tampón PBS-Tween con anticuerpos (dilución 1/1000) presentes en una mezcla de sueros de ratones inmunizados previamente con VMEs extraídas de S. sonnei y éstos fueron detectados con antisuero anti-IgG conjugado a peroxidasa de rábano (Sigma). Las muestras se visualizaron con un sistema de desarrollo de color diaminobenzidineH2O2. Se evaluaron las VMEs extraídas de S. sonnei obtenidas en este trabajo y las proteínas de las células lisadas de Vibrio cholerae C7258; S. dysenteriae ATCC número 13313; S. flexneri (cepa 9), S. sonnei (cepa 1) a partir de preparados denominados STA (12).
Electroforesis en geles de poliacrilamida en una dimensión con un sistema macro electroforético en el National Institute for Biological Standard and Control (NIBSC, Reino Unido)
]]> La proteínas fueron solubilizadas en un tampón de lisis [Urea 7M; tiourea 2M; CHAPS 2% (3-[(3-Cholamidopropyl)dimethylammonio]-1-propanesulphonate); Tritón X-100 0,5%; glicerol 15%; ditiotreitol (DTT) 1%; Pharmalyte 3-10 1% con inhibidor de proteasas], se calentaron a 100°C y se conservó a -20°C, hasta su uso. La concentración de proteína se determinó a través del kit de Bio-Rad (BioRad, Hemel Hempstead, UK). La electroforesis en geles (SDS-PAGE) se realizó en un sistema Electro Hoefer SE 600 acoplado a una fuente de corriente ECPS 3000/150 (40 mA) y un sistema termostato (Tempette TE-80), con una temperatura constante a 13°C. Las muestras fueron tratadas con un tampón para sistema Laemmli (Bio-Rad) e incubadas a 95°C, durante 5 min. Se aplicaron 30 µg en un gel 12% (1,5 mm x 12 cm x 15,5 cm) y finalmente se visualizó con un sistema de tinción de plata o sistema Coomassie.Electroforesis en gel en segunda dimensión realizada en el NIBSC
La focalización isoeléctrica (FI) se llevó a cabo utilizando tiras de poliacrilamida e inmovilinas y un sistema IPGphor II System (Amersham, US). Las tiras de pH 3-11 NL (13 cm, 18 cm o 24 cm) se rehidrataron con tampón de lisis (como se describe anteriormente) conteniendo bromofenol azul (325, 450 o 600 µL, respectivamente) y las muestras (de 40 o 100 µg) se aplicaron de varias formas (directamente en tampón de lisis, con aplicación anódica con copa o con aplicación catódica). La FI se realizó a 4°C con 45, 60 o 100 KVh. Cada tira fue equilibrada en 10 mL de tampón 1 de equilibración (Tris-HCl 50 mM pH 8,8; tiourea 2 M; urea 7 M; glicerol 30% v/v; SDS 2%, DTT 20 mg/mL: bromofenol azul), durante 10 min y en 10 mL de tampón 2 de equilibración (Tris-HCl 50 mM pH 8,8, tiourea 2M, urea 7M, glicerol 30% v/v, SDS 2%, iodoacetamide 48 mg/mL, bromofenol azul), durante 5 min. La electroforesis bidimensional (12% SDS-PAGE) se realizó a 40 mA. Las condiciones utilizadas fueron: a) 13 cm, aplicación en gel, 45 KVh; b) 13 cm, aplicación anódica en copa, 45 KVh; c) 18 cm, aplicación catódica en copa, 45 KVh; d) 18 cm, aplicación en gel, 45 KVh; 18 cm, aplicación catódica en copa, 60 KVh; e) 18 cm, aplicación en gel, 100 KVh. Los geles se revelaron con un sistema de tinción con plata y se escanearon en un densitómetro SI Scanner (Molecular Dynamics 375, Amersham Pharmacia).
Digestión del gel, análisis por espectrometría de masas y búsqueda en bases de datos realizados en el NIBSC
Las bandas electroforéticas de las VMEs de S. sonnei obtenidas por macroelectroforesis 1D y teñidas con el sistema Coomassie fueron cortadas y digeridas con tripsina. Los fragmentos se separaron e identificaron por espectrometría de masas acoplada a cromatografía de alta presión (HPLC-EM), a través de la secuenciación peptídica y el análisis de la información acerca del proteoma completo de S. sonnei contenido en las bases de datos proteicas Swiss-Prot y TrEMBL. Las secuencias de aminoácidos generadas obtenidas y cotejadas en las bases de datos permitieron identificar el tipo de proteína de Shigella sin necesidad de utilizar anticuerpos monoclonales específicos.
RESULTADOS
Preparación de inmunógenos de VMEs
Las vesículas de membrana externa (VMEs) se obtuvieron a partir de una cepa de S. sonnei (A-04) clínicamente aislada de un paciente; extraídas con detergente SDS 2% a partir de su fermentación a una escala de 20L. Estos preparados obtenidos se analizaron a través de electroforesis 1D (SDS-PAGE) a escala analítica e immunoblotting, usando un suero inmune generado por inmunización con VMEs de esta preparación (Fig. 1). Las proteínas de las células lisadas (STA) a partir de otras cepas de V. cholerae C7258; S. dysenteriae ATCC número 13313; S. flexneri, cepa 9 y S. sonnei cepa 1, se evaluaron en paralelo con las VMEs de S. sonnei obtenidas en este trabajo. Se detectaron inmunoproteínas comunes a todas las especies con tamaños moleculares: 17,2; 22,1; 27,5; 38,7; 41,2; 43,8; 59,3; 66,8; 75-86 kDa. Algunas de estas bandas con tamaños moleculares cercanos al de las proteínas referidas (38; 58; 65 kDa) por Martínez y col. (12), cuando analizaron la extracción celular STA de esta cepa, durante la selección de las cepas candidatas para desarrollar una vacuna.
]]> Separación de los componentes proteicos por electroforesis unidimensional (escala preparativa) y análisis por espectrometría de masasEn nuestro trabajo se utilizó un tampón de lisis y tratamiento de las proteínas de VMEs de mayor complejidad que el utilizado por Martínez y col. (12) en el estudio previo para el análisis de STA de células de S. sonnei cepa A-04, donde refirieron como proteínas mayoritarias las de tamaños: 35, 38, 58, 65 y 101 kDa.
Por otra parte, en nuestro tratamiento incluimos la incubación previa con el tampón de lisis a 100°C, durante 5 min, su congelación, posterior descongelación y finalmente el ajuste de la concentración e incubación con tampón Laemmli (Bio-Rad) nuevamente a 95°C (5 min). Adicionalmente en nuestro trabajo se modificó la concentración del gel separador a escala preparativa a 12% para favorecer la separación de proteínas con tamaños moleculares inferiores. Los resultados para el análisis de estas modificaciones utilizando la tinción con plata se muestran en las Figuras 2A y 2B. Las muestras calentadas a 100°C mostraron una menor abundancia en cuanto a proteínas con tamaños moleculares entre 34–38 kDa, probablemente porque se favorece la separación de proteínas hidrofóbicas.
Se detectaron además, dos bandas mayoritarias con 37 y 40 kDa y otras bandas múltiples de menor intensidad. Estas condiciones separan complejos de proteínas de altos tamaños moleculares con una baja movilidad y cadenas peptídicas de proteínas. La aplicación de cantidades de muestras de 20 a 40 µg en los geles de poliacrilamida y su tinción con Coomassie (Fig. 3) permitió una resolución aceptable para la posterior digestión de las bandas y su análisis por espectrometría de masas. Una parte del gel fue teñido con Coomassie y las bandas se cortaron manualmente (Fig. 3) para ser digeridas con tripsina y proceder a la identificación proteica por HPLC-EM. Los resultados de la secuenciación y comparación de los fragmentos con la información que brindan las bases de datos del proteoma de Shigella se resumen en la Tabla 1.
En muchos de los casos, las bandas simples contenían múltiples componentes proteicos, como se refirió previamente por Uli y col. para vacunas de VMEs meningocócicas (10). Se identificaron cuarenta y siete proteínas individuales no repetidas (57 en total), con algunas proteínas presentes en más de una banda (23 bandas), con una media de 2,5 proteínas por banda escindida.
Las bandas más intensas S12 y S13 contenían las proteínas de membrana: proteína de membrana externa A (OMP A), proteína de membrana externa porina C (PorC), proteína de membrana externa 1b (OMP 1b), la proteína hipotética Q3Z0B3, la proteína porina de membrana externa Q3Z1L6 entre otras; así como dos enzimas metabólicas de la glicolisis (gliceraldehído-3 fosfato deshidrogenasa A presente en citoplasma) y de la transferencia de fosfato en el metabolismo de fructosa y manosa (Mannose-1-phosphate guanyltransferase GDP). Las bandas S2, S3, S4 y S5 con menor intensidad contenían la proteína de membrana externa X (Tabla 1).
Electroforesis en gel bidimensional (2D) de los componentes de las vesículas de membrana externa
La electroforesis 2D requiere su optimización para la separación de ciertas proteínas hidrofóbicas de membrana que tienden a agregarse en el paso de FI. Las condiciones iniciales de solubilización propuestas en este trabajo se basaron en las utilizadas de manera exitosa para el análisis de la vacuna antimeningocócica de vesículas de membrana externa, según como lo describieron Uli y col. (10). La conservación de las muestras en el tampón de rehidratación permitió evitar la pérdida de resolución debido a interacciones entre las PMEs y los lípidos de membrana sin ningún tipo de agregación y precipitación. En el presente trabajo se investigaron una serie de condiciones de aplicación y corrida isoeléctrica de las muestras en las tiras.
]]> La Figura 4 muestra los mejores resultados obtenidos con las tiras de FI de pH 3 a 11, con 13 cm de longitud y un tiempo de FI de 45 kVh, aplicando la muestra en el gel (Fig. 4A); además, una segunda variante en la que se reduce la precipitación de las proteínas básicas en tiras de mayor dimensión (18 cm), con un incremento del tiempo de FI hasta 60 kVh y utilizando la aplicación catódica con copa, permitieron la óptima separación de las proteínas de membrana en las condiciones investigadas (Fig. 4B). Los productos innovadores (primero en su clase) tienen un alto costo y riesgo de fracaso, pero debido a que resuelven por primera vez una necesidad médica no satisfecha su valor en el mercado suele ser alto.De igual modo, cuenta con personal talentoso con conocimiento de los procesos asociados y de las buenas prácticas, que puede satisfacer las demandas del mercado y las necesidades de investigación. Estas fortalezas se respaldan por las oportunidades que facilitan el interés creciente de clientes foráneos por comercializar los productos del CIM como son: el apoyo de la dirección del país, el prestigio y compromiso de la ciencia en Cuba (de la que el CIM forma parte), el trabajo conjunto de la institución con otros componentes de la comunidad científica por cubrir necesidades médicas no satisfechas con productos biológicos de calidad, en una concertación estratégica directa con el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CECMED).
DISCUSIÓN
Muchos de los trabajos inmunoproteómicos publicados han identificado proteínas inmunorreactivas, las cuales inducen respuesta de anticuerpos cuando las células enteras (S. flexneri y S. dysenteriae) se utilizan como inmunógenos en ratones y en conejos. Jenninson y col. (15) detectaron diferentes proteínas en estudios proteómicos; cinco proteínas en la fase de extracción de proteínas de membrana externa: OmpA, AnsB, TolC, Ggt y TolB; las proteínas OmpA, TolC y AnsB se detectaron también como proteínas solubles y otras tres proteínas fueron identificadas como inmunogénicas solubles frente a sueros de pacientes infestados con Shigella: GroEL, Spa33 y IpaD. La proteína OmpA es probablemente una de las proteínas de membrana externa inmunorreactivas mayoritarias, identificada como la proteína de 35 kDa en los análisis del inmunoproteoma (16-18). Este tipo de trabajo no es frecuente en S. sonnei.
En nuestro trabajo, esta proteína se detectó por secuenciación de dos de las bandas electroforéticas de 34,3 y 36,8 kDa; compartiendo movilidad electroforética con la proteína de membrana externa porina C (identificada por secuenciación) y la proteína de membrana externa 1b (identificada también por secuenciación). Esta última también se presentó en bandas con 40,9 y 50,5 kDa. Detectamos la proteína chaperonina 60 kDa por secuenciación (conocida como GroEL con localización en el citoplasma) en las bandas electroforéticas S20 y S21 de 73,5 y 76,2 kDa, respectivamente.
Como muestran los resultados, las proteínas de membrana externa son mayoritarias; pero también están presentes proteínas características del citoplasma y que de alguna manera durante el proceso de extracción de las vesículas, podrían estar relacionadas con los lípidos de membrana o con el detergente de extracción SDS o quedar atrapadas en el interior de la vesícula. Estas bandas fueron reconocidas como inmunorreactivas por Western blotting con anticuerpos de ratón inducidos por las VMEs, lo que confirma la importancia de la presencia de las mismas en nuestras preparaciones. A la pregunta: ¿Pudiera afirmarse absolutamente la identidad de una proteína con electroforesis, sin el empleo de anticuerpos monoclonales?. Sí, es posible siempre que se utilice como parte del sistema de identificación proteómico. Esta herramienta no sólo incluye métodos electroforéticos como procedimientos de separación; también la aplicación de HPLC a los fragmentos de las proteínas presentes en las bandas previamente separadas por SDS-PAGE que son digeridas con la enzima tripsina por sitios específicos. En los fragmentos separados se identifican las secuencias por espectrometría de masas el cual es uno de los métodos que sigue siendo de los más exactos para estos fines.
La información obtenida se introduce en plataformas informatizadas en constante actualización que recogen todas las secuencias registradas acerca de los dominios proteicos característicos de especies. Aunque varios autores cuestionan la garantía de la exactitud en la identificación, como Tsiatsiani y Heck (19) y otros afirman la necesidad de utilizar complementariamente métodos inmunoquímicos para garantizar una adecuada cuantificación (20); el hecho es que los avances en la proteómica basada en la espectrometría de masas permiten estudios de expresión de isoformas, tasa de rotación, localización subcelular, modificaciones postraduccionales e interacciones entre proteínas (gracias al análisis multidimensional del proteoma, integración y visualización e intercambio de datos) (21), lo que hace que este sistema sea más específico que cuando se utilizan solo anticuerpos monoclonales.
En este trabajo, la combinación de la extracción con detergente SDS a partir de la etapa de fermentación del microorganismo, la solubilización posterior de las VMEs con mezclas de detergentes y urea a altas temperaturas, su conservación a bajas temperaturas, su posterior tratamiento con tampón de lisis para corrida electroforética a altas temperaturas permitió una adecuada separación e identificación de los fragmentos proteicos. Estas proteínas, estrechamente asociadas a lípidos, podrían perderse si se utilizan tratamientos destinados a remover los fosfolípidos, como por ejemplo, con dietil éter. En nuestros resultados, la utilización de la solubilización y conservación de las muestras de VMEs en el tampón de lisis propuesto evitó los efectos de fondo de los lípidos en el gel teñido.
En nuestros experimentos realizados en Western blotting la evaluación de la reactividad inmunológica cruzada se observó en muestras de lisados celulares de Shigella y Vibrio cholerae, reconociendo proteínas tales como: proteína de membrana externa X (S5), proteína de membrana externa A, proteína de membrana externa porina C, proteína de membrana externa 1b, chaperonina 60 kDa, proteína de membrana externa 3a, entre otras; que pudieran valorarse como candidatos vacunales contra shigellosis y cólera. Como la muestra de VMEs de Shigella contiene proteínas con una amplia gama de valores de puntos isoeléctricos (pI), el aumento de la longitud de las tiras y el tiempo de focalización beneficiaron la resolución de las proteínas ácidas y neutras; mientras que la resolución de las proteínas básicas resultó ser mejor con la forma de aplicación catódica y con el incremento de la cantidad de proteína. Esta metodología que proponemos, permitirá el desarrollo de estudios futuros para establecer condiciones de crecimiento microbiano y criterios en el control de calidad de futuras vacunas. Las condiciones propuestas para la 2D serán útiles para la determinación del perfil proteico inmunoquímico, que garantice el control de la calidad de una nueva vacuna que proteja contra S. sonnei.
]]> Estos resultados constituyen un punto de partida en el Instituto Finlay de Vacunas para el desarrollo de estudios proteómicos en VMEs de S. sonnei, aisladas a partir de cepas clínicas (pacientes) para su uso como vacuna. Aun hoy, estos resultados mantienen vigencia por cuanto se continúa refiriendo la alta incidencia de shigellosis a nivel mundial, sin que se haya logrado una vacuna altamente protectora y barata, destinada a países de Asia y América Latina que continúan sufriendo de esta enfermedad e incluso, contra otras enfermedades entéricas. El método propuesto para el aislamiento y purificación a escala piloto de VMEs a partir de la cepa A04 aislada de pacientes infectados de S. sonnei, así como la metodología proteómica que proponemos, permitieron obtener un proteoma representado por las proteínas de membrana externa más importantes, descritas por su papel inmunogénico como candidatas para su uso como vacunas. Muchas de estas proteínas resultaron ser reconocidas inmunoquímicamente por anticuerpos inducidos por la inoculación en ratones Balb/c de las propias VMEs, anticuerpos que reconocieron además, proteínas de otras cepas de S. dysenteriae, S. flexneri y V. cholerae.
AGRADECIMIENTOS
Agradecemos a la Royal Society (Reino Unido) por la financiación concedida en el año 2007 para el desarrollo de la evaluación de las muestras de VMEs de S. sonnei en el National Institute for Biological Standard and Control (Reino Unido), lo cual permitió que se llevara a cabo parte de este proyecto.
REFERENCIAS
1. Jones C. Vaccines based on the cell-surface carbohydrates of pathogenic bacteria. An Bras Acad Ciênc 2005;77:293-324.
2. Kotloff KL, Winickoff JP, Ivanoff B, Clemens JD, Swerdlow DL, Sansonetti PJ, et al. Global burden of Shigella infections: implications for vaccine development and implementation of control strategies. Bull World Health Organ 1999;77:651-66.
]]>3. Farfán M, Flores O, Navarro N, Prado V, Mora G, Toro C. Caracterización molecular de mecanismos de resistencia a cloranfenicol en cepas de Shigella flexneri aisladas en niños chilenos con diarrea aguda. Rev Méd Chile 2002;130(3). Disponible en: http://www.scielo.cl/scielo.php?pid=S0034-98872002000300005&script=sci_arttext.
4. Pozsgay V, Chu C, Pannell L, Wolfe J, Robbins JB, Schneerson R. Protein conjugates of synthetic saccharides elicit higher levels of serum IgG lipopolysaccharide antibodies in mice than do those of the O-specific polysaccharide from Shigella dysenteriae type 1. Proc Natl Acad Sci USA 1999;96:5194-7.
5. Shim DH, Chang SY, Park SM, Jang H, Carbis R, Czerkinsky C, et al. Immunogenicity and protective efficacy offered by a ribosomal-based vaccine from Shigella flexneri 2a.Vaccine 2007;25:4828-36.
6. Phalipon A, Tanguy M, Grandjean C, Guerreiro C, Bélot F, Cohen D, et al. A synthetic carbohydrate-protein conjugate vaccine candidate against Shigella flexneri 2a infection. J Immunol 2009;182:2241-7.
7. World Health Organization (WHO). State of the art of new vaccines and development. Department of Immunization, Vaccines and Biologicals. Geneva: WHO; 2006.
]]>8. Tribble D, Kaminski R, Cantrell J, Nelson M, Porter C, Baqar S, et al. Safety and immunogenicity of a Shigella flexneri 2a Invaplex 50 intranasal vaccine in adult volunteers. Vaccine 2010;28:6076-85.
9. Sierra GV, Campa HC, Varcacel NM, Garcia IL, Izquierdo PL, Sotolongo PF, et al. Vaccine against group B Neisseria meningitidis: protection trial and mass vaccination results in Cuba, NIPH Ann 1991;14:195-207.
10. Uli L, Castellanos-Serra L, Betancourt L, Dominguez F, Barbera R, Sotolongo F, et al. Outer membrane vesicles of the VA-MENGOC-BC vaccine against serogroup B of Neisseria meningitidis: analysis of protein components by two-dimensional gel electro-phoresis and mass spectrometry. Proteomics 2006;6:3389-99.
11. Sotolongo F, Campa C, Casanueva V, Fajardo EM, Cuevas IE, González N. Cuban Meningococcal BC Vaccine: Experiences & Contributions from 20 Years of Application. International Journal of Cuban Health and Medicine. MEDICC Review 2007;9(1)16-22.
12. Vipond C, Suker J, Jones C, Tang C, Feavers IM, Wheeler JX. Proteomic analysis of a meningococcal outer membrane vesicle vaccine prepared from the group B strain NZ98/254. Proteomics 2006;6:3400-13.
]]>13. Martínez OM, Riverón L, Alemán A, Talavera A, Montano I, Soto C, et al. Selección de cepas de Shigella sonnei para el desarrollo de una vacuna efectiva contra la shigellosis. VacciMonitor 2008;17 (3):13-20.
14. Camacho AI, de Souza J, Sánchez-Gómez S, Pardo-Ros M, Irache JM, Gamazo C. Mucosal immunization with Shigella flexneri outer membrane vesicles induced protection in mice. Vaccine 2011;29:8222-9.
15. Jennison AV, Raqib R, Verma NK. Immunoproteome analysis of soluble and membrane proteins of Shigella flexneri 2457T. World J Gastroenterol 2006;12:6683-8.
16. Peng X, Ye X, Wang S. Identification of novel immunogenic proteins of Shigella flexneri 2a by proteomic methodologies. Vaccine 2004;22:2750-6.
17. Ying T, Wang H, Li M, Wang J, Wang J, Shi Z, et al. Immunoproteomics of outer membrane proteins and extracellular proteins of Shigella flexneri 2a 2457T. Proteomics 2005;5:4777-93.
]]>18. Ying T, Wang J, Wang H, Feng E, Wei K, Huang L, et al. Immunoproteomics of membrane proteins of Shigella flexneri 2a 2457T. World J Gastroent 2005;11:6880-3.
19. Tsiatsiani L, Heck AJR. Proteomics beyond trypsin. FEBS Journal 2015;282:261226.
20. Wilson R. Sensitivity and specificity: twin goals of proteomics assays. Can they be combined?. Expert Rev Proteomics. 2013;10(2):135-49.
21. Larance M, Lamond AI. Multidimensional proteomics for cell biology. Nat Rev Mol Cell Biol 2015;16:26980.
Recibido: Julio de 2016 Aceptado: Octubre de 2017
]]>