REVIEW
Reacción en cadena de la polimerasa cuantitativa de la expresión génica en el desarrollo preclínico y clínico de medicamentos anticancerosos
Quantitative polymerase chain reaction of gene expression in the preclinical and clinical development for anticancer drugs
]]> Damián Mainet-González
Departamento de Farmacogenómica, Subdirección de Investigaciones Biomédicas, Centro de Ingeniería Genética y Biotecnología, CIGB. Ave. 31 e/ 158 y 190, Cubanacán, Playa, CP 11600, La Habana, Cuba.
RESUMEN
En la aparición del cáncer influyen factores físicos, químicos y biológicos que alteran el genoma de los individuos. Esta enfermedad afecta la morbilidad y la mortalidad en países desarrollados y en Cuba. El proceso de desarrollo de medicamentos es largo, costoso y con un índice de fallo mayor en cáncer que en otras enfermedades. Por ello se continúan investigando diagnosticadores con elevada confiabilidad, para conocer el posible éxito de nuevos candidatos terapéuticos, desde las etapas más tempranas del desarrollo preclínico y clínico. Así, la decisión de emplearlo o desecharlo no se tomaría en las etapas finales del desarrollo, cuando se han gastado varios recursos. Los diagnosticadores genómicos son evaluadores indirectos de la respuesta a medicamentos, menos costosos y más fáciles para determinar y específicos que los diagnosticadores proteómicos en el cáncer. La reacción en cadena de la polimerasa cuantitativa se ha empleado para determinar la expresión de ácidos ribonucleicos codificantes y la confirmación y validación de diagnosticadores genómicos. En este artículo se discuten su alta sensibilidad y especificidad, las posibilidades de automatización, y su empleo independiente o complementario a tecnologías genómicas de alto flujo, para la obtención de medicamentos anticancerosos en países en desarrollo. La reacción en cadena de la polimerasa puede aplicarse con una adecuada relación beneficio-costo en distintas etapas de este proceso, y en la confección de bases de datos farmacológicas y toxicológicas más confiables. Ello favorecerá el conocimiento de esta enfermedad para la generación de medicamentos más seguros y eficaces.
Palabras clave: reacción en cadena de la polimerasa cuantitativa, medicamentos anticancerosos, diagnosticador, desarrollo de medicamentos.
ABSTRACT
Cancer starts from changes in the individual’s genome which are caused by physical, chemical or biological factors. This complex disease increases the mortality and morbidity variables in developed countries, and also in Cuba. Anticancer drug development is a long and expensive process, with a failure rate higher than in other diseases. For that reason, some biomarkers are being implemented for a more efficacious prediction of new therapeutic candidates at early phases of preclinical or clinical development. Then, decision making on stopping or proceeding with a biologically active compound does not applies to final phases of development when a great amount of resources has been spent. Genomic biomarkers are surrogate indicators to measure drug response in the cancer, and also cheaper, of easier analysis and more specific than proteomic biomarkers. In this context, the quantitative polymerase chain reaction (qPCR), has been used to determine gene expression and to confirm and validate other genomic biomarkers. Here we discuss its high analytical sensitivity and specificity, and its possible automation for high throughput analysis of the expression of coding RNA. qPCR could be used alone or complementary to high flow genomic technologies for anticancer drug development in developing countries. Its increased use will be determined by an adequate cost-benefit ratio at the different phases, the generation of more reliable pharmacological and toxicological databases and by increasing the knowledge on this disease to obtain safer and more efficacious drugs.
Keywords: quantitative polymerase chain reaction, anticancer drugs, biomarker, drug development.
INTRODUCCIÓN
]]> El cáncer es un conjunto de enfermedades complejas y multifactoriales que pueden provocar la muerte de una de cada ocho personas afectadas. Su incidencia es de más de 12 millones de nuevos casos anuales en el mundo [1]. Constituyó la segunda causa de muerte en Cuba en 2012 (más de 22 000) y la de mayor años de vida potencialmente perdidos con una tasa de 34.5 años por cada 1000 habitantes [2]. De ahí que la mayoría de los esfuerzos se centren en el desarrollo de nuevos fármacos para combatir su incidencia y aumentar la calidad de vida de los pacientes, así como de nuevos sistemas de diagnóstico más eficaces y de uso más temprano en las diferentes fases del proceso de desarrollo de medicamentos (PDM).El PDM es largo, ineficiente y costoso. De los medicamentos en desarrollo, solamente el 11 % llega a ser comercial; de los medicamentos anticancerosos, únicamente el 5 % de los inicialmente desarrollados [3]. Además, estos últimos tienden a una eficacia menor y más reacciones adversas que los medicamentos destinados a otras enfermedades. La introducción de un medicamento con eficacia y buena seguridad en el mercado requiere de 10 a 15 años y un costo de más de 300 millones de dólares por producto [4, 5]. Ese costo y tiempo de generar un nuevo medicamento va en aumento por la aplicación de tecnologías más complejas y la búsqueda de compuestos más eficaces y seguros para enfermedades incurables de causas multifactoriales. Entre un tercio y la mitad de los costos del desarrollo de medicamentos ocurre en la etapa de ensayos clínicos [6]. El 90 % de los fallos de candidatos terapéuticos durante el desarrollo clínico se debe a tres razones fundamentales: la deficiente farmacocinética, la ausencia de eficacia y los efectos adversos en seres humanos [7, 8]. Existen reacciones idiosincrásicas y alérgicas tóxicas muy peligrosas y tan poco frecuentes (1/10 000) que no se detectan durante el PDM, que a veces obligan a la retirada del producto del mercado cuando su obtención y aprobación ha costado mucho dinero [9, 10]. Una manera de enfocar este problema es la investigación de uno o más diagnosticadores al inicio de las fases preclínicas y clínicas, mediante ensayos fáciles, rápidos, de alto flujo y una razonable relación costo-beneficio, que favorezca la selección de los candidatos terapéuticos con mayor efectividad y seguridad. El objetivo de este artículo es profundizar en cómo la Reacción en cadena de la polimerasa cuantitativa (RCPc), mediante la cuantificación de la expresión de genes, puede favorecer la selección de los candidatos anticancerosos más efectivos y seguros, y discriminar la población enferma más susceptible a la acción farmacológica de estos, mediante el hallazgo de diagnosticadores con alto nivel de predicción en el PDM.
CARACTERÍSTICAS Y ETAPAS DEL PDM
El PDM es largo e ineficiente y consta de dos grandes etapas: la búsqueda y mejoramiento de un compuesto con actividad biológica, y la demostración y promoción de ese nuevo candidato terapéutico como un medicamento comercial eficaz, seguro y novedoso. En la primera etapa se incluyen las fases de identificación de la diana terapéutica, la selección temprana de los compuestos con actividad biológica, y la optimización de estos en diferentes ciclos de síntesis química o biológica. En la segunda etapa se evalúan esos compuestos en experimentos de efectividad, y de toxicología en animales de experimentación (fase preclínica) y en seres humanos (fase clínica).
Para disminuir el tiempo, los gastos y el índice de fallo tardío de los candidatos a fármacos de este proceso, y aumentar la productividad y la innovación de la industria farmacéutica e introducir de manera más rápida y competitiva un nuevo medicamento [11, 12], se toman algunas medidas. Primero, seleccionar las mejores dianas moleculares de importancia capital para la sobrevivencia de las células cancerosas y, por otro lado, la posibilidad de la obtención de un agente modificador de su actividad con efectos mínimos o nulos sobre el funcionamiento de células normales. Segundo, estudiar cada compuesto con actividad biológica desde etapas tempranas del PDM, según un conjunto de parámetros (absorción, distribución, metabolismo, excreción y toxicidad, potencia y selectividad), mediante ensayos biológicos para seleccionar aquellos con mayores probabilidades de conversión en un medicamento comercial después de varios ciclos de optimización o refinamiento estructural. Tercero, desarrollar modelos de animales modificados genéticamente con mayor semejanza a las manifestaciones fundamentales o de mayor interés de esta enfermedad en seres humanos y mejorar su índice de predicción en el PDM. Cuarto, investigar la determinación de uno o más diagnosticadores lo más temprano posible en la fase preclínica y clínica del PDM mediante ensayos fáciles, rápidos, de alto flujo y una razonable relación costo-beneficio, que favorezca la selección de los pacientes con mayores probabilidades de responder a ese candidato terapéutico de una manera segura y efectiva [8, 13]. Quinto, confeccionar grandes bases de datos con los perfiles de absorción, distribución, metabolismo, excreción, toxicidad, potencia y selectividad de cada uno de los candidatos terapéuticos en los experimentos con líneas celulares. A continuación, y mediante el uso de herramientas bioinformáticas, se pronostican o correlacionan sus propiedades farmacocinéticas, toxicológicas y farmacodinámicas en los modelos animales de experimentación y en los ensayos clínicos. Esto permite priorizar adecuadamente aquellos compuestos con mayores probabilidades de éxito en el PDM [14]. Recientemente se ha aplicado la RCPc para mejorar la eficiencia de ese proceso mediante el desarrollo de diagnosticadores preclínicos y clínicos que puedan disminuir el índice de rechazo a los candidatos terapéuticos.
COMPLEJIDAD FISIOPATOLÓGICA DEL CÁNCER Y SU INFLUENCIA EN EL DESARROLLO DE TRATAMIENTOS Y DIAGNOSTICADORES EFECTIVOS
]]> El cáncer es provocado por un desarreglo genético hereditario o adquirido. En su evolución influyen factores químicos, físicos, biológicos y ambientales, como la edad, la no realización de ejercicios físicos, la dieta, el tratamiento, los agentes tóxicos y biológicos, las radiaciones, entre otros, por lo que es una enfermedad multifactorial y compleja [15]. El PDM de fármacos anticancerosos se dificulta por la inestabilidad genómica, la ausencia de un modelo animal con un adecuado índice de predicción, el diagnóstico tardío de esta enfermedad, la mayor incidencia en edades avanzadas y la similitud antigénica y estructural entre las células tumorales y las normales. La inestabilidad genómica origina varias poblaciones celulares dentro del tumor en distintos estadios de diferenciación y en diferentes etapas del ciclo celular. Esta proliferación anárquica puede favorecer la aparición de clones de células malignas resistentes al tratamiento farmacológico y alterar la formación y morfología de los vasos sanguíneos, que dificulta la llegada de los medicamentos a las células tumorales. El valor de predicción de los tumores de líneas celulares humanas en xenotransplantes de ratones inmunodeficientes es tan bajo, que solamente el 11 % de tales candidatos terapéuticos probados en ese modelo animal logran llegar a ensayos clínicos y la aprobación por la agencia estadounidense reguladora de alimentos y fármacos (FDA) [16]. La supervivencia global a 5 años, de los pacientes con un diagnóstico tardío de cáncer pulmonar de células no pequeñas es del 15 %. Un 60 % de esos pacientes es por enfermedad avanzada o metástasis. Sin embargo, esa supervivencia puede llegar a 50 % en los pacientes diagnosticados más tempranamente con posibilidad de tratamiento quirúrgico [17]. Los problemas en el metabolismo y excreción de los medicamentos y el estado hipofuncional del sistema inmune de los pacientes ancianos, disminuyen la posibilidad de emplear mayor cantidad de medicamentos para tratar esta enfermedad.Los antígenos y receptores usados como dianas terapéuticas contra las células tumorales son estructuralmente iguales en las células normales. Esa es la causa de las reacciones adversas; no solo en las células hematopoyéticas y gastrointestinales en división, sino también en células que no se están dividiendo. Eso explica que los medicamentos anticancerosos modificadores directos de procesos fisiológicos esenciales de las células, tengan una proporción entre las dosis tóxicas y las dosis terapéuticas muy cercana a la unidad [18]. Sin embargo, pueden constituir una opción terapéutica efectiva contra esta enfermedad. Existe otro grupo de medicamentos, los modificadores indirectos de esos procesos, como los antitransductores de señales intracelulares, que son más seguros o inocuos, pero no llegan a tener la efectividad de los primeros [19]. Para mejorar la eficacia de estos últimos medicamentos y la búsqueda de anticancerosos más seguros y efectivos, se plantean tres condiciones. La primera, lograr encontrar una o más dianas moleculares no esenciales para las células normales, pero sí para la supervivencia de las células tumorales, mediante el estudio de los cambios genéticos y epigenéticos que tienen lugar dentro de la célula tumoral, en el cual su estado fisiopatológico es diferente a la célula normal. Y el examen del microambiente tumoral para lograr influir en la interacción de las células tumorales con la matriz extracelular y las células estromales. La segunda, encontrar candidatos terapéuticos con una alta selectividad por esas dianas moleculares. Y la tercera, seleccionar, mediante un ensayo, los grupos de pacientes con mayores probabilidades de responder a ese tratamiento combinado aditivo o sinérgico.
En la terapia dirigida a dianas moleculares relacionadas directamente con los procesos fisiológicos a modificar (mitosis, síntesis de proteína, replicación, transcripción, etc.) generalmente la vía por la que transcurre la señal fisiológica no influye. Sin embargo, en los medicamentos antitransducción de la señal biológica, sí es importante conocer esas vías y su interacción, ya que esto influye en la farmacodinamia del medicamento y en su efectividad terapéutica.
Las vías de transducción son ramificadas y muy interrelacionadas [20, 21]. Las vías reconocidas en el cáncer pueden ser de tres tipos: las más frecuentes (MAPK, TP53, Rb1 y AKT), las asociadas con las más frecuentes (NFKappaB, PI3K, PKC quinasas, STAT y TGFbeta) y las específicas de algunos cánceres (WNT, NOTCH y SHH) [22]. Las proteínas formadoras de esas vías de señalización en el cáncer son expresadas por genes con variaciones en su secuencia de ADN o por alteraciones epigenéticas. Esas alteraciones genéticas ocurren en dos tipos de genes: oncogenes (promotores del crecimiento) y genes supresores de tumores. Los oncogenes son transmitidos genéticamente con carácter dominante y generan un aumento de la función en la proteína afectada. Los genes supresores son transmitidos con carácter genético recesivo y producen una pérdida de la función o una disminución en la cantidad de la proteína alterada. La combinación de esas alteraciones en diferentes procesos celulares y en sus vías de señalización es el mecanismo que constituye la diferencia entre los cánceres humanos. Se pueden generar fallos en el ciclo celular, en el desarrollo de la apoptosis y en el sistema reparador del ADN genómico. Esto último provocará más mutaciones progresivamente con un aumento del crecimiento tumoral y afectación de otros procesos celulares intrínsecos y extrínsecos, hasta que las células tumorales invasivas y heterogéneas migren y se implanten en otro sitio diferente del foco primario. La neoplasia maligna dejará de ser una enfermedad local para convertirse en una enfermedad sistémica.
Es más probable que los genes mutados o amplificados en el ADN genómico de células tumorales para cada tipo de cáncer sean factores de sobrevivencia, que aquellos sobreexpresados solamente. La identificación de los genes con mutaciones activadoras o con un aumento en el número de copias codificantes de las proteínas formadoras de la vía de transducción de una diana terapéutica o de otra vía relacionada, pudieran formar las bases de diagnosticadores de la respuesta a esa terapia. La respuesta o no al tratamiento con un medicamento anticanceroso, no solamente va estar predicho por el aumento o disminución de la expresión o no de su diana molecular. Por ejemplo, las mutaciones y amplificaciones génicas sobreactivadoras del receptor de factor de crecimiento epidérmico son favorables indicadores de respuesta; sin embargo, las mutaciones activadoras de los genes KRAS y RAF (codifican para proteínas de esa misma vía de señalización), la amplificación del gen HER2 y la sobreexpresión del gen ILGF-1 son desfavorables indicadores de respuesta antiproliferativa de los medicamentos antirreceptor del factor de crecimiento en células de cáncer de colon [15]. Estos dos últimos genes codifican para proteínas de otras vías de señalización relacionadas con la del receptor del factor de crecimiento epidérmico. Lo anterior sugiere la relación que debe existir al estudiar la expresión de genes con otras modificaciones genéticas del ADN y orienta cómo pudiera ser la búsqueda de diagnosticadores para esta enfermedad.
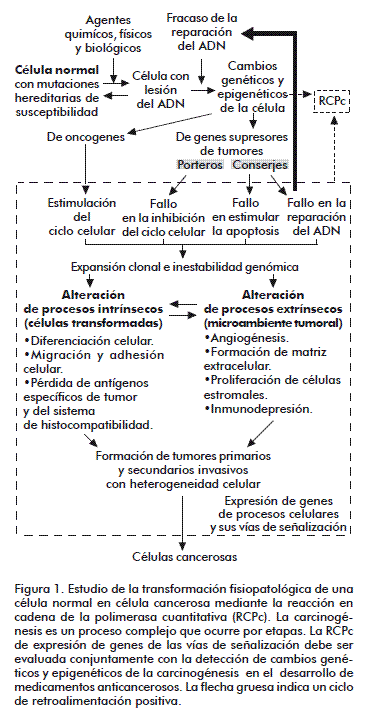
La RCPc ofrece posibilidades para detectar esas variaciones genéticas en las células tumorales y dilucidar qué mecanismo tumoral está influyendo más en un paciente que en otro y orientar qué terapéutica pudiera ser mejor indicada en cada caso (Figura 1).
LA RCPc PERMITE DETERMINAR CON ALTA SENSIBILIDAD Y ESPECIFICIDAD LA EXPRESIÓN RELATIVA DE GENES
]]> La RCPc, en la que se logra la cuantificación del producto amplificado durante su formación [23] y también conocida como RCP cinética o cuantitativa en tiempo real, se usa ampliamente en biología, durante el proceso de desarrollo de medicamentos (PDM) y en la oncología [24]. Es una técnica importante en la detección de modificaciones del ADN genómico en enfermedades tumorales malignas, y para determinar los niveles relativos del ARN mensajero (ARNm) de oncogenes o genes supresores de tumores [23] y de genes de citoquinas y quimoquinas a nivel tumoral y a nivel sistémico [7]. También se emplea en la verificación de datos de microarreglos [9]; en la validación de experimentos de silenciamiento genético con ARN simple de interferencia [25]; para determinar la carga viral [26, 27], la expresión relativa de ARN regulatorio o microARN [28]; para estudiar las mutaciones y los polimorfismos de las células tumorales [29]; en la cuantificación de las dosis de genes o aberraciones cromosomales [30]; y en la determinación de hipo e hipermetilación de ADN [31]. Algunas de esas alteraciones pueden estar en el ADN libre circulante en el torrente sanguíneo [32], y se pueden estudiar junto con el ARN regulatorio sin que estén purificados [33]. La detección de esas alteraciones permite el diagnóstico del síndrome de predisposición a cáncer familiar. También facilita el pronóstico de la respuesta al tratamiento, o la posible evolución satisfactoria de la enfermedad, y la curación de la enfermedad mínima residual o su persistencia [34].
DESCRIPCIÓN DE LA RCPc
La RCPc es un ensayo de reacciones enzimáticas cíclicas de amplificación y detección simultánea de secuencias de ácidos nucleicos para determinar su cantidad inicial. En esa cuantificación se usa la polimerasa y los marcadores directos o indirectos de fluorescencia. El aumento de la fluorescencia es proporcional a la cantidad de ácido nucleico producido durante cada ciclo de RCP, lo que permite la cuantificación exacta de las moléculas diana (Figura 2). El ciclo de RCP en el cual la fluorescencia se eleva por encima de un valor definido se denomina ciclo de cuantificación (Cc). Mientras más ADN o ARNm haya en el material de partida menor es el Cc. Existen varios pasos para un estudio de expresión génica mediante la RCPc: el diseño experimental, la recogida y el almacenamiento de muestras, la purificación del ácido nucleico y su almacenamiento, la optimización de la reacción de la reverso transcriptasa y de la ADN polimerasa, el método de detección del producto génico, el control de la calidad y el análisis e interpretación de los resultados (Figura 3). En ocasiones se tiene muy poco volumen de muestras biológicas de enfermos de gran interés clínico y científico, por lo que se requieren procesos estandarizados en la recogida de las muestras, su transportación, almacenamiento y extracción del ácido nucleico.
En el diseño experimental se intenta disminuir la variabilidad biológica y técnica cuando se comparan dos grupos de muestras, de manera de que sean lo más similares posible, excepto en el fenotipo de investigación (enfermos o sanos, tratados o no tratados, antes o después del tratamiento). En cada paso se controla esa variabilidad mediante la identificación de genes dianas y genes de referencia, en la calibración de las muestras biológicas en estudio y en la selección de los controles positivos y negativos adecuados para el estudio de ARN y en el diseño de los oligonucleótidos cebadores para ARNm [35]. Los genes dianas se pueden identificar por dos métodos. Uno es mediante hipótesis o método cerrado, en el que se estudia un grupo de genes y sus variantes transcripcionales de corte y empalme, relacionados con un proceso fisiológico o patológico determinado [36]. En este se debe conocer el proceso a estudiar desde el punto de vista empírico-teórico y bioinformático, para la selección de los genes que ayudarán a responder la pregunta formulada por el investigador. El otro método es de descubrimiento o abierto, en el que se estudian genes de todo el genoma, sin un conocimiento previo completo de los genes que se van a estudiar.
Para aplicar la técnica, se seleccionan aquellos genes de una gran parte o de todo el genoma que modifican significativamente su expresión en técnicas genómicas de alto flujo (los bioarreglos de expresión de genes y la secuenciación nucleotídica de alto flujo). Generalmente, se detectan entre 20 y 50 genes [37, 38], y con la RCPc se pueden estudiar cuantitativamente mejor esos genes y su influencia en un proceso biológico o fisiopatológico terapéutico (validación analítica).
La calibración del ensayo de expresión del ARNm se realiza a partir de genes de referencia internos y la comparación de cada muestra con calibradores experimentales. Los genes de referencia no se deben alterar por las condiciones experimentales establecidas y vincularse a diferentes procesos celulares [10, 39]. Estos genes corrigen las diferencias entre las muestras por la cantidad y calidad de ácido nucleico inicial, las variaciones en la síntesis de ADN complementario (ADNc), la presencia de inhibidores de la RCPc, y las variaciones o errores en la manipulación. Los calibradores experimentales pueden ser una línea celular no tratada, una muestra biológica antes de que el sujeto haya recibido un tratamiento (tiempo cero) o una célula o tejido normal. El calibrador corrige las diferencias entre los genes que se van a estudiar y los genes de referencia, entre cada corrida experimental y entre lotes de muestras, durante estudios de larga duración. Un diseño de estudio de muestras poblacionales pareadas o el aumento del tamaño de esas muestras que se van a estudiar, y la valoración del tipo de muestras biológicas a escoger o el mejor modo de extracción de estas, contribuyen a disminuir la variabilidad biológica y técnica como la calibración del ensayo [40].
]]>
RECOLECCIÓN Y CUANTIFICACIÓN DE LA MUESTRA
En la recolección y transporte de las muestras biológicas para los estudios de expresión de genes en la RCPc, actualmente se utilizan como soluciones estabilizantes para sangre: Paxgene™ (Preanalytix Gmbh, Feldbachstrasse, Suiza) o RNAlater® (Ambion, Inc., Texas, Estados Unidos de América), y para líneas celulares y tejidos de organismos: RNAlater®, que garantiza la estabilidad del ARN a 25 °C durante varios días, y Trireagent® (Sigma-Aldrich, St. Louis, EE.UU.) mediante congelación. En el proceso de recolección y conservación de las muestras sanguíneas para estudios de expresión de genes se deben evitar los cambios de temperatura, la demora en la manipulación de las muestras, y ejecutar el aislamiento celular lo más rápido posible para evitar los genes inducidos ex vivo como respuesta al estrés [41].
En la extracción de ARN mediante los estuches comerciales actuales se elimina la contaminación de ADN genómico. Durante ese procedimiento, se debe evitar la degradación del ARN por la acción de ribonucleasas, y se debe conservar a - 70 o - 80 °C en altas concentraciones, en alícuotas para usar una vez, y en viales de plásticos certificados como libres de nucleasas. En la calidad del ARN extraído de la muestra se evalúa la concentración, la pureza (con ausencia de inhibidores de la polimerasa o de la fluorescencia) [6, 42] y su integridad [43]. La concentración y la pureza se determinan mediante espectrofotometría por la densidad óptica a 260 nm y las relaciones de densidad óptica a 260/280 nm y 260/230 nm, respectivamente. La absorbancia a 280 nm indica la contaminación de proteínas y la absorbancia a 230 nm, de fenoles o urea. La integridad de esas moléculas puede determinarse por electroforesis en gel de agarosa o de capilar mediante el uso del bioanalizador, donde se da un resultado global del estado del ARN total [44].
REACCIONES ENZIMÁTICAS
En la optimización de las reacciones enzimáticas de la transcriptasa inversa y de la ADN polimerasa se debe tener en cuenta si la reacción es en uno o dos pasos, y los reactivos de cada una de ellas, así como las tres etapas en que se divide la RCPc: la desnaturalización, la hibridación y la extensión, que son muy similares a la RCP de punto final. El perfil de expresión de genes a partir del análisis de ARN codificante en esta técnica se realiza en dos pasos: 1) la reacción de conversión del ARN hacia ADNc dependiente de la transcriptasa inversa, 2) y la reacción de amplificación del ADNc por la acción de la ADN polimerasa, que permite la cuantificación de los productos. Si estos dos pasos ocurren sin interrupción en un vial, la RCPc se clasifica como de un paso. Los componentes de las reacciones de obtención del ADNc y de amplificación del gen diana son asequibles comercialmente como mezclas, y muchas veces la optimización es mínima.
En la detección del producto génico se aplican dos métodos: directo e indirecto. En el método directo, el marcador fluorescente se une a cualquier sitio de la doble cadena de ADN. Puede hacerlo de dos formas: en condiciones no saturantes del ADN (por ejemplo: el marcador Sybrgreen™) en las que se detecta la señal de fluorescencia al final de cada fase de extensión, y en condiciones saturantes del ADN (por ejemplo: los marcadores LCGreen®, EvaGreen y el Resolight®) en las que se detecta la fluorescencia una vez terminado el último ciclo de la RCP. En el método directo, el marcador fluorescente es covalentemente conjugado a una sonda nucleotídica que se une a una secuencia génica determinada. En este método se emplean las sondas de hibridación (Hybprobe™) y las de hidrólisis (Taqman®), que se añaden en la misma mezcla de los oligonucleótidos cebadores. En las sondas de hibridación se emplea dos sondas nucleotídicas: una conjugada al fluoróforo aceptor-emisor y la otra, al fluoróforo donador. Cuando se unen al ADN desnaturalizado, la sonda aceptora emite la energía transferida por la sonda donadora. En las sondas de hidrólisis se emplea una sonda nucleotídica marcada con dos fluoróforos (uno es apagador y otro emisor) y la detección de la máxima fluorescencia se logra cuando dicha sonda es hidrolizada por la actividad exonucleásica de la ADN polimerasa y el fluoróforo emisor desprende la luz al ser separado del fluoróforo apagador.
La RCPc puede detectar un gen (variante simple) o dos o más genes (variante múltiple) en un solo vial [35]. En la variante múltiple de RCPc, los genes de referencias y los genes en estudio son coamplificados en la misma reacción, por lo que disminuye la variabilidad de pozo a pozo y garantiza una precisa cuantificación relativa de genes, la automatización y la generación de gran cantidad de datos, la disminución de los costos y la preservación de muestras de interés médico-científico. En esta metodología, además de una adecuada combinación de fluoróforos donadores y apagadores, el equipo de RCPc debe ser capaz de hacer la lectura a las longitudes de onda de emisión de esos fluoróforos.
]]>
ANÁLISIS DE DATOS Y CONTROL DE LA CALIDAD DE LA RCPc
En el análisis de datos y control de la calidad del ensayo de la RCPc se evalúan cuatro parámetros: la especificidad, la sensibilidad, la reproducibilidad y la eficiencia.
Especificidad
La especificidad depende del diseño de los oligonucleótidos cebadores y de las condiciones de reacción. Se debe evitar la formación de dímeros de cebadores oligonucleotídicos. Este elemento se verifica mediante el análisis de la curva de fusión o disociación, la electroforesis de gel de agarosa y los controles negativos y positivos. La temperatura de fusión es la temperatura en la cual la mitad de los productos de dos cadenas enrolladas de ADN se desnaturaliza a una simple cadena.
En el método de fusión se va aumentando la temperatura para disminuir la fluorescencia, las dos hebras de ADN se van separando y el fluoróforo se va liberando, y una vez que se despegan las dos hebras, la fluorescencia cae bruscamente. Ese estudio se realiza con un marcador fluorescente de unión a las moléculas de ADN, para diferenciar la señal de los productos específicos expresados de aquella de los dímeros de oligonucleótidos cebadores, pues estos tienen una temperatura de fusión menor que los productos del gen de interés.
Sensibilidad
La sensibilidad o el límite de detección es la mínima cantidad de ácido nucleico inicial que produce una señal de fluorescencia por encima del Cc. Este valor umbral se puede determinar por el método de fijar el punto, el método máximo de la segunda derivada, o a partir de 10 veces la desviación estándar de la línea base [29].
Reproducibilidad
]]> En la reproducibilidad se trata de minimizar las fuentes de variabilidad entre los análisis en el Cc y en la intensidad de fluorescencia independiente de la heterogeneidad del ácido nucleico en estudio, mediante el empleo de métodos adecuados de normalización [45, 46], la preparación de curvas estándares de 4 a 5 diluciones seriadas con un factor de dilución de 1/10 y dos o tres réplicas para cada dilución como mínimo. Se ha reportado una variabilidad interensayo en la RCPc entre 3 y 10 % del promedio de la concentración de las réplicas técnicas, cuando dos alícuotas de ARN fueron procesadas en paralelo desde el inicio de la síntesis de ADNc [13].Eficiencia
La eficiencia da una buena estimación de la amplificación del producto de RCP en cada ciclo. Hay dos métodos para analizar la eficiencia de la cuantificación relativa de genes, uno es mediante la curva de calibración y la otra mediante estudios dinámicos de datos [47]. La eficiencia por el método de la curva de calibración se obtiene de la interpolación del logaritmo (en base 2 o 10) de las concentraciones iniciales de los patrones de ácido nucleico en el eje x, frente a los Cc en el eje y. Se considera una eficiencia aceptable cuando la pendiente de la curva de calibración oscila entre -3.8 a -3.3. El método de la doble variación del ciclo umbral es un caso particular de este método, cuando la eficiencia es aproximadamente de 100 %. Cuando no es así, aparecen tres escenarios: uno en el que la eficiencia es la misma para todos los genes en todas las muestras; otro, donde la eficiencia es igual para cada gen en todas las muestras, y el tercero, en el que la eficiencia es diferente para los genes y las muestras. En el primer y segundo escenario se realiza la corrección de la fórmula de la variación del Cc con la eficiencia calculada. En el tercer escenario se necesita una optimización de las condiciones bioquímicas de la RCPc.
Este método requiere la realización de curvas de calibración para todas las muestras y los genes (al menos tres concentraciones y dos réplicas técnicas por cada muestra), lo cual puede encarecer el estudio y hacer difícil la aplicación de la RCPc en el modo de alto flujo o de análisis de gran número de muestras y genes por ensayo, y el consiguiente aumento en la generación de datos y resultados.
En el método de estudios dinámicos de los datos, la eficiencia se estima mediante el empleo de un modelo sigmoidal matemático a partir de los parámetros cinéticos, obtenido de la mejor curva de regresión de Cc, frente al número de ciclos o mediante parámetros estimados a partir de la mejor curva de regresión de Cc frente al rendimiento de productos [47]. En este método, la RCPc puede ser aplicada más fácilmente en su modalidad de alto flujo. Después se realiza el análisis estadístico por métodos paramétricos o no, para rechazar la hipótesis nula de si existe igualdad de expresión de genes entre los dos grupos de muestras estudiadas, de acuerdo con un tamaño de muestra poblacional estimado con una buena potencia y nivel de significación estadística.
Existe una guía para disminuir la fuente de variabilidad técnica y biológica de este ensayo en constante revisión, que aporta la información mínima para la publicación de experimentos de RCPc (Minimum Information for Publication of Quantitative Real-Time PCR Experiments, MIQE) [48]. Orienta a los autores acerca de los detalles de las muestras, la plataforma instrumental y los protocolos que se deben recoger y cómo los datos primarios de expresión de genes deben estar disponibles. Esta guía ayuda a una mayor transparencia experimental, consistencia de los datos cuantitativos [34], y a un aumento de la integridad y la coherencia de la literatura científica para la confección de estudios de metaanálisis.
DIAGNOSTICADORES GENÓMICOS BASADOS EN LA RCPc
Un diagnosticador es un parámetro objetivamente cuantificable y evaluable que sea indicador de un proceso biológico, patogénico o de una respuesta farmacológica a una intervención terapéutica.
El desarrollo de diagnosticadores transita por varias fases: descubrimiento, verificación y desarrollo. En la fase de descubrimiento se identifican aquellos posibles diagnosticadores (denominados diagnosticadores propuestos o de tipo III) a partir de las muestras analizadas, el conocimiento científico y de los resultados, y se validan mediante una técnica independiente a como fueron descubiertos. En la fase de verificación de diagnosticadores se realiza la validación preclínica o clínica de las pruebas seleccionadas, mediante los estudios retrospectivos y prospectivos (denominados diagnosticadores válidos probables o de tipo II).
]]> Se han descrito cinco etapas en la validación preclínica de un diagnosticador probable para cualquier enfermedad [13]. En esta fase se prefiere la búsqueda de un conjunto de genes con mayores magnitudes de cambios en la RCPc, más específicos al determinar la eficacia y la optimización de las dosis, la formulación y las vías de administración de muchos candidatos terapéuticos, desde los tamizajes iniciales hasta el tránsito exitoso a la fase clínica. En la fase de desarrollo, los diagnosticadores (denominados diagnosticadores válidos existentes o de tipo I) se emplean en la estratificación de pacientes en los hospitales e instituciones de salud [49, 50]. Por ejemplo, en un ensayo clínico fase III multicéntrico, la RCPc fue usada para cuantificar la expresión del transcripto BCR/ABL en pacientes con leucemia mieloide crónica con una respuesta citogenética completa al Imatinib [51]. Se demostró que los pacientes que disminuyeron esos transcriptos en al menos 3 log durante un año de terapia, tuvieron un riesgo bajo de progresión de la enfermedad en los 12 meses siguientes. Ese criterio de respuesta molecular mediante la RCPc ha sido progresivamente usado para el monitoreo de esta enfermedad. Actualmente, el monitoreo de las concentraciones del transcripto de fusión BCR-ABL1 en sangre o en médula ósea mediante la RCPc, está aceptado para la valoración clínica de los pacientes con leucemia mieloide crónica tratados con Imatinib [52]. En la validación de los diagnosticadores para cáncer, se describen una serie de evidencias y recomendaciones estadísticas que se deben tener en cuenta [50].Los diagnosticadores genómicos se evalúan mediante las moléculas de ADN y ARN. Los diagnosticadores proteómicos se miden a través de las proteínas celulares. Ambos conceptos han aparecidos debido al desarrollo de las tecnologías de la automatización y la informática, generadoras de gran cantidad de datos por experimentos. Los diagnosticadores genómicos generalmente pueden detectar una enfermedad o condición específica heredable, y los diagnosticadores proteómicos, en algunos casos. Cuando eso sucede, se refiere a diagnosticadores genéticos. Los diagnosticadores genómicos no pueden determinar los cambios definitivos que están ocurriendo a nivel celular, como sí lo hacen los proteómicos [13]. Esa determinación indirecta del funcionamiento celular (subrogada) puede ser compensada por las ventajas siguientes: los diagnosticadores genómicos determinados por la RCPc pueden ser más específicos que aquellos determinados a nivel proteico en el cáncer de origen epitelial. Sus mediciones pueden ser de muy alta sensibilidad, pueden determinarse de una manera de alto flujo más barata que los diagnosticadores proteómicos, y requieren menos cantidad de tejidos o muestra inicial. Los métodos de análisis de ARN emplean reactivos de investigación disponibles y listos para uso y más fácil de generar a partir de la secuencia nucleotídica reportada de los genes que se han de cuantificar. Para ser examinados en un bioarreglo, los diagnosticadores proteómicos necesitan la generación de un panel grande de anticuerpos, y en la espectrometría de masas, requieren un panel de patrones de péptidos.
Ambos métodos, los genómicos y los proteómicos, tienen su fuente de error; existe una alta correlación en los resultados entre ellos cuando se estudian proteínas estructurales; y es baja cuando se analizan proteínas no estructurales [53]. A mayor identificación de los diagnosticadores terapéuticos o toxicológicos a nivel genético, proteico y metabólico, mayor será la capacidad de predicción de los modelos.
La complementación en la información cuantitativa obtenida por la RCPc en la expresión relativa de genes con las alteraciones del ADN (mutaciones, polimorfismos, aumento en el número de copias de genes) y cambios epigenéticos (hipermetilación del ADN o acetilación de histonas) (Figura 1), la información adicional de las cantidades y actividades de proteínas u otras macromoléculas (lípidos, glúcidos), de metabolitos (radicales libres) y otros datos clínicos de interés facilitarán el desarrollo de la biología de sistema (Figura 4) [10, 54]. Este enfoque sistémico favorecerá la elaboración de modelos que permitan una mejor predicción de la respuesta al tratamiento y la generación de medicamentos más efectivos, ajustados a las características de cada enfermo, y un mayor conocimiento de esta enfermedad [16, 55].
En la medicina molecular, las decisiones clínicas se basarán cada vez más en una alta confiabilidad de los perfiles moleculares de tumores y de diversas muestras clínicas (sangre, lágrima, saliva, líquido cefalorraquídeo, orina, heces fecales, semen, biopsias de tumores heterogéneos embebidos en parafina y fijada en formalina, etcétera), y predominará la obtención no invasiva sobre la invasiva, en varios períodos de la enfermedad, sobre todo en el diagnóstico temprano. Lo anterior repercute en el empleo de nuevas terapéuticas medicamentosas, quirúrgicas o radiológicas. Este aspecto debe ser tenido en cuenta también en el PDM, ya que puede permitir una mejor selección de los diagnosticadores genómicos (independientes o en combinación con los diagnosticadores proteómicos o metabolómicos) bien definidos, para mejorar los diseños de los estudios, y que se puedan comprobar mejor las hipótesis. La determinación de qué grupos de genes en la RCPc se debe incorporar al desarrollo de medicamentos, dependerá del grado de certeza del pronóstico obtenido, con una favorable relación costo-beneficio en el PDM en comparación con otros tipos de diagnosticadores (proteómicos o metabolómicos) y las tecnologías utilizadas. La tecnología de la RCPc ha llegado a ser introducida en los países en desarrollo para la detección de enfermedades infecciosas [56]. La extensión de la RCPc para el diagnóstico de cáncer en estos países dependerá de sus índices de morbilidad y mortalidad por esta enfermedad crónica no transmisible, y de cómo y cuánto esta tecnología se haya introducido en la medicina clínica y en el PDM globalmente.
APLICACIONES DE LA RCPc EN LAS FASES PRECLÍNICAS Y CLÍNICAS DEL PDM ANTICANCEROSOS
El desarrollo de las pruebas genómicas mediante la RCPc como técnica complementaria o independiente, se ha enfocado en las aplicaciones siguientes: 1) pruebas para el diagnóstico precoz o predisposición al cáncer, 2) pruebas para la eficacia de candidatos a fármacos, 3) pruebas de toxicidad de candidatos terapéuticos, 4) pruebas para la selección de pacientes y diseño de ensayos clínicos (Figura 4).
Pruebas de diagnóstico o predisposición al cáncer
]]> Las primeras pruebas de diagnóstico y predisposición tienen una relación indirecta con el tratamiento, porque mientras más temprano se diagnostiquen esas alteraciones, más rápidamente se pueden tratar los pacientes y mejorar su pronóstico. La expresión de cinco genes seleccionados en un estudio de bioarreglo de un grupo de pacientes con carcinoma hepatocelular de concentraciones bajas de alfafetoproteína se comparó con otros de cifras elevadas de ese diagnosticador. Mediante la RCPc se confirmaron los genes GPC3, PEG10, MDK, SERPIN1 y QP-C, y ayudaron al diagnóstico precoz del carcinoma hepatocelular en pacientes con alfafetoproteína normal y tumores muy pequeños [30]. Ese panel de cinco genes representa diferentes vías y respuestas celulares, permite una lectura más abarcadora del cambio patológico y aumenta la exactitud diagnóstica en esta enfermedad.Pruebas de eficacia
En la predicción de eficacia a medicamentos, la tecnología de la RCPc identificó 54 genes expresados diferencialmente entre líneas celulares de mama (MDA-MB-231) y sublíneas derivadas de esas células con actividad metastásica pulmonar. Ese perfil de genes no solo estaba presente en ratones sino también en seres humanos [57]. Ello sugiere la relevancia de esos genes con la metástasis. Esas sublíneas celulares podrían servir como modelo a nivel celular y a nivel de organismo de esa complicación del cáncer mamario, en caso de xenotransplante, y precisar in vitro e in vivo si la indicación de un compuesto con actividad biológica es antitumoral primario o antimetastásico.
La RCPc puede aportar señales a la valoración de la eficacia de un candidato terapéutico mediante el estudio de los genes asociados con la homeostasis del sistema inmune. La determinación del perfil de expresión de genes de citoquinas y quemoquinas en la RCPc se ha usado como un método directo para valorar el estado funcional de la respuesta inmune sistémica (linfocitos circulantes) y periférica (microambiente tumoral) de pacientes con cáncer vacunados con péptidos, proteínas completas o células tumorales [7].
La respuesta inmune sistémica de pacientes con melanoma vacunados con péptidos se evaluó funcionalmente mediante la RCPc de la expresión del ARNm del interferón gamma en células mononucleares de sangre periférica, expuestas in vitro a esos péptidos durante 2 h. Este ensayo sin manipulaciones prolongadas in vitro y con un ahorro de tiempo, presentó una elevada correlación con el método tradicional de sensibilización in vitro durante 10 días de esos linfocitos T citotóxicos específicos contra péptidos de melanoma [58].
La única desventaja de la RCPc es no tener la sensibilidad del método tradicional de sensibilización in vitro por 10 días para detectar respondedores con muy bajas cantidades de células T citotóxicas específicas precursoras, con solo 2 h de sensibilización ex vivo. Sin embargo, el método tradicional no brinda información directa de los procesos fisiológicos que ocurren in vivo. Se quisiera encontrar un parámetro biológico, ya sea el número de células T citotóxicas específicas o las concentraciones mínimas necesarias de ARNm u otras moléculas de células inmunes específicas, que pronostique cuándo una respuesta inmunológica es significativamente efectiva en los pacientes enfermos vacunados [59-61].
En el microambiente tumoral se han monitoreado las interacciones de las células tumorales con la respuesta inmune periférica mediante la cuantificación de la expresión de genes de interferón gamma, interleucina 10, factor de crecimiento transformante beta 1 y beta 2 en la RCPc, a partir de muestras de tejido en aguja fina. Los pacientes buenos respondedores presentaron una sobreexpresión de interleucina 10 (citoquina inmunosupresora) antes de la vacunación, lo cual se pudiera explicar por la acción mediadora de esta citoquina entre la respuesta inmune innata y la adaptativa [7]. En estos estudios, la RCPc no necesitó grandes cantidades de material biológico (bastó con el material extraído mediante aspiración con una aguja fina y la posibilidad de que el ácido nucleico de 10 a 100 células fuese amplificado linealmente), a diferencia de otras técnicas como la inmunohistoquímica o la citofluorescencia. Además, la RCPc permitió el seguimiento de los cambios dinámicos en la expresión de antígenos asociados a tumor, la expresión de citoquinas y marcadores específicos de células inmunes durante la inmunización o el tratamiento con una generación más fácil de nuevos reactivos. Por ejemplo, la generación de los anticuerpos policlonales o monoclonales para la inmunohistoquímica o citofluorescencia es más compleja y consume más tiempo que la síntesis de los oligonucleótidos cebadores de la RCPc.
Pruebas de toxicidad de candidatos terapéuticos
En las pruebas de toxicidad de candidatos terapéuticos se ha demostrado que las sustancias con mecanismos similares de toxicidad inducen la expresión de genes similares. Los grupos de genes específicos de toxicidad descubiertos en el bioarreglo se pudieran confirmar y evaluar sistemáticamente en la RCPc. Los nuevos diagnosticadores genómicos de toxicidad que se identifiquen deben ser más sensibles, específicos, reproducibles y con mayor valor de predicción que los actualmente aceptados. Deben dar una respuesta entre 1 a 3 días, antes de los 14 días en que se obtienen los resultados histopatológicos actuales [14]. Si esas pruebas fueran evaluadas entre múltiples especies biológicas (ratas, ratones, monos) en los ensayos de seguridad preclínica de candidatos terapéuticos, brindaran un mayor beneficio. Por ejemplo, los niveles de expresión urinarios de los genes clusterin y KIM-1 determinado en la RCPc se correlacionan con la necrosis tubular renal en el tejido de riñón de ratas y monos.
La expresión del gen KIM-1 correlaciona con los niveles de la proteína KIM-1 en orina de esos animales [24]. La medición del gen KIM-1 es también una prueba de toxicidad renal tubular proximal en seres humanos. El diseño de los cebadores oligonucleotídicos de la RCPc a partir de regiones génicas conservadas entre especies biológicas ayudaría con ese objetivo y en la validación de esos ensayos.
]]> La RCPc facilitará el estudio del metabolismo de los medicamentos a través de la expresión de los genes del complejo citocromo P450 (CYP), donde se ha visto que algunos de ellos inducen la expresión de las isoformas más frecuentes de ese complejo (CYP1A2, CYP2C9, CYP2C19, CYP2D6 y CYP3A4). Esas isoformas influyen en el metabolismo del 90 % de los medicamentos disponibles en el mercado. En un modelo in vivo de rata se administró un inductor de los genes CYP1A, CYP2B, CYP3A y CYP4A durante 8 días, se midieron cinéticamente los niveles de ARNm en la RCPc y se compararon con la determinación de esas enzimas por Western Blot y actividad enzimática. Se demostró un aumento de la sensibilidad y la especificidad de la RCPc en la detección de cambios en la inducción de los genes CYP relacionados con medicamentos y sus estudios toxicológicos, con respecto a las dos técnicas de análisis de proteína [28].Pruebas para la selección de pacientes y diseño de ensayos clínicos
En la estrategia de desarrollo clínico de medicamentos anticancerosos, se debe tener un plan a priori para el estudio de los diagnosticadores, con un método simple bien probado, que permita la adecuada selección de los pacientes. De lo contrario, aumentaría el número de falsos positivos (enfermos que recibirán un tratamiento no efectivo) y negativos (enfermos que no accederán a una terapia efectiva) de ese ensayo diagnóstico; un aumento en el riesgo de fallo en el desarrollo clínico de los fármacos anticancerosos y, por último, se alteraría la relación costo-beneficio y efectividad de esos candidatos terapéuticos [18, 48].
Los factores genéticos determinados durante el PDM pueden usarse en los ensayos clínicos específicos como elementos de diseño. Se describen tres tipos de diseños de estudio para diagnosticadores genómicos durante los ensayos clínicos [12]: dos de tipo prospectivo: el tamizado y el selectivo; y uno de tipo retrospectivo: el estratificado. En el diseño tamizado, el factor genético es un criterio de exclusión de la población que no responderá a un medicamento seguro o eficaz para ella, y disminuye el riesgo de fallo en estudios más grandes y costosos. En el diseño selectivo, el factor genético es un criterio de inclusión que permite estudiar su efecto entre diferentes grupos y optimizar las dosis de los medicamentos. En el diseño estratificado, el factor genético es analizado después del ensayo clínico, para ganar elementos de cómo será la indicación de la prueba farmacogenómica en un estudio prospectivo, y en la prescripción del medicamento personalizado. Esta área de diseño de ensayos clínicos está evolucionando rápidamente: se emplean diagnosticadores genómicos y no genómicos para lograr ahorro de tiempo y recursos en el desarrollo de medicamentos anticancerosos con menos índices de fallos [62].
En la selección de pacientes para recibir determinado candidato terapéutico, no se trata de identificar un perfil de expresión de genes para cada constitución genética, sino de identificar haplotipos o combinaciones de genes específicos que hagan una predicción del aumento en la eficacia y una disminución en la toxicidad de los medicamentos en una amplia población o grupo de pacientes [4, 17, 23]. La determinación de la expresión de genes con la RCPc y la amplificación génica mediante la hibridación con fluorescencia in situ, usadas de manera independiente, mostraron una alta correlación en un estudio del gen del receptor HER2/neu en muestras de cáncer de tejido mamario [6]. El primer ensayo ha brindado una valoración funcional de ese gen y de eventos importantes desencadenados en esa vía de señalización. Revela aspectos de la biología que permiten la subclasificación de este cáncer y seleccionar los pacientes probablemente más respondedores a la terapia antiHER-2/neu (trastuzumab) [6]. Se plantea que el conocimiento del perfil genético de la vía de señalización de ese medicamento en algún otro tipo de cáncer (no mamario) pudiera ser indicativo con una alta certeza de una buena respuesta terapéutica y debe ser tenido en cuenta en los futuros ensayos clínicos [17].
CONCLUSIONES
La RCPc es una técnica que puede ser utilizada independiente o de manera complementaria con tecnologías genómicas de mayor flujo para la determinación del perfil de expresión de ARNm. Las ventajas aportadas por el uso de la RCPc en el PDM del cáncer son: la elevada sensibilidad y especificidad analítica; el rango dinámico amplio entre 4 a 10 órdenes de magnitud; la cuantificación exacta de genes expresados en forma relativa o absoluta durante las fases de hibridación o de amplificación; el potencial para ser usada en alto flujo; la necesidad de muy poca cantidad de muestra, que puede ser obtenida de manera no invasiva; la posibilidad de seguimiento de los cambios dinámicos en la expresión de genes de antígenos tumorales y de células inmunes, durante la inmunización o el tratamiento; y su realización con reactivos más fáciles de generar.
La variación biológica y técnica de este ensayo son las desventajas señaladas debido a no seguir ciertas normas y cuidados en su ejecución y en la publicación de los resultados. En una enfermedad compleja y multifactorial como el cáncer, la RCPc se ha comparado con los procedimientos establecidos en el PDM y en la práctica clínica, con una adecuada relación costo-beneficio que pueda influir en su aplicación en las etapas más tempranas de sus fases preclínica y clínica. Con esto se busca favorecer la decisión estratégica y científica de la aprobación o el rechazo de los candidatos terapéuticos o la entrada de otro nuevo para mejorar la eficiencia de ese proceso y, sobre todo, está ayudando a incrementar el conocimiento de esta enfermedad. Al final, la información brindada por la RCPc de expresión de genes, de conjunto con la obtenida de la expresión de microARN, la detección de otras alteraciones genéticas, epigenéticas, proteómicas, glicómicas y metabolómicas de esta enfermedad, buscan una incorporación más rápida y efectiva de los candidatos en estudio al arsenal terapéutico, que salven y aumenten la calidad de vida de los pacientes.
]]>
AGRADECIMIENTOS
Este trabajo forma parte de los proyectos de investigación financiados por el CIGB. El autor agradece por la revisión del manuscrito y las sugerencias al Dr. Carlos Duarte Cano, del CIGB.
REFERENCIAS
]]>
1. Globetech Media. Los diagnósticos acompañantes favorecen la medicina personalizada. LabMedica. 2008 [cited 2013 Nov 27];25:4. Available from: http://mydigitalpublication.com/display_article.php?id=46132.
2. Ministerio de Salud Pública. Anuario Estadístico de Salud, Cuba, 2012 [Internet]. Habana: Dirección Nacional de Registros Médicos y Estadísticas de Salud, Minsap; 2013 [cited 2013 Oct 17]. Available from: http://files.sld.cu/dne/files/2013/04/anuario_2012.pdf.
3. Pearce HL, Blanchard KL, Slapak CA. Failure modes in anticancer drug discovery and development. In: Neidle S, editor. Cancer Drug Design and Discovery. London: Elsevier Inc; 2008. p. 424-35.
4. Wang J, Urban L. The impact of early ADME profiling on drug discovery and development strategy. Drug Discovery World. 2004;5:73-86.
5. Furones-Mourelle JA. Bases científicas para el desarrollo y la utilización de medicamentos. En: Morón-Rodríguez FJ, editor. Farmacología General. La Habana: Editorial Ciencias Médicas; 2002. p. 9-21.
6. Ross JS, Schenkein DP, Kashala O, Linette GP, Stec J, Symmans WF, et al. Pharmacogenomics. Adv Anat Pathol. 2004;11(4):211-20.
7. Mocellin S, Rossi CR, Pilati P, Nitti D, Marincola FM. Quantitative real-time PCR: a powerful ally in cancer research. Trends Mol Med. 2003;9(5):189-95.
8. Workman P, Collins I. Modern cancer drug discovery: integrating targets, te¬chnologies and treatments. In: Neidle S, editor. Cancer Drug Design and Discovery. London: Elsevier Inc; 2008. p. 3-38.
9. Jia HL, Ye QH, Qin LX, Budhu A, Forgues M, Chen Y, et al. Gene expression profiling reveals potential biomarkers of human hepatocellular carcinoma. Clin Cancer Res. 2007;13(4):1133-9.
10. Preziosi P. Science, pharmacoeconomics and ethics in drug R&D: a sustainable future scenario? Nat Rev Drug Discov. 2004;3(6):521-6.
]]>11. Dix R. Experimental medicine: Developing biomarkers in early discovery to bridge preclinical and clinical development. Drug Discovery World. 2004;5:56-60.
12. Katz DA. Overview of Pharmacogenetics. In: Enna SJ, Williams M, Frechette R, Kenakin T, McGonigle P, Ruggeri B, editors. Curr Protoc Pharmacol. New Jersey: John Wiley & Sons, Inc.; 2007. p. 6.10.1-6.10.24.
13. Freeman WM, Bixler GV, Brucklacher RM, Lin CM, Patel KM, VanGuilder HD, et al. A multistep validation process of biomarkers for preclinical drug development. Pharmacogenomics J. 2010;10(5):385-95.
14. DeCristofaro M, Daniels KK. Toxicogenomics in Biomarker Discovery. In: Mendrick DL, Mattes WB, editors. Methods in Molecular Biology, vol. 460: Essential Concepts in Toxicogenomics. Totowa: Humana Press; 2008. p. 185-95.
15. Schulz WA. An introduction to human cancers. In: Schulz WA, editor. Molecular Biology of Human Cancers: An advanced Student’s Textbook. Dordrecht: Springer Science + Business Media, Inc; 2005. p. 1-23.
16. Levitzki A, Klein S. Signal transduction therapy of cancer. Mol Aspects Med. 2010;31(4):287-329.
17. Ocak S, Sos ML, Thomas RK, Massion PP. High-throughput molecular analysis in lung cancer: insights into biology and potential clinical applications. Eur Respir J. 2009;34(2):489-506.
18. Petak I, Schwab R, Orfi L, Kopper L, Keri G. Integrating molecular diagnostics into anticancer drug discovery. Nat Rev Drug Discov. 2010;9(7):523-35.
19. Kamb A, Wee S, Lengauer C. Why is cancer drug discovery so difficult? Nat Rev Drug Discov. 2007;6(2):115-20.
20. Krauss G. Structure and Function of Signal Pathways. In: Krauss G, editor. Biochemistry of Signal Transduction and Regulation. 3rd ed. Weinheim: Wiley -VCH Verlag GmbH & Co; 2003. p. 115-130.
21. Granner DK. Hormone Action and Signal Transduction. In: Rodwell VW, Murray RK, Davis JC, Mayes PA, editors. Harper’s Illustrated Biochemistry. 26th ed. New York: Lange Medical Books/McGraw-Hill; 2003. p. 456-73.
22. Schulz WA. Cancer pathways. In: Schulz WA, editor. Molecular Biology of Human Cancers: An advanced Student’s Textbook. Dordrech: Springer Science+Business Media, Inc; 2005. p. 113-144.
23. Joyce C. Quantitative RT-PCR: A Review of Current Methodologies. In: O'Connell J, editor. Methods in Molecular Biology, vol. 193: RT-PCR Protocols. New Jersey: Humana Press Inc; 2002. p. 83-91.
24. Goodsaid F. Quantitative Real Time Polymerase Chain Reaction in Drug Development Research. Drug Development Res. 2004;62(2):151-8.
25. Malek A, Tchernitsa O. Evaluation of targets for ovarian cancer gene silencing therapy: In vitro and in vivo approaches. In: Min WP, Ichim T, editors. RNA Interference, Methods in Molecular Biology, vol. 623. Dordhrecht: Springer Science+Business Media; 2010. p. 423-37.
26. Schlecht NF, Kulaga S, Robitaille J, Ferreira S, Santos M, Miyamura RA, et al. Persistent human papillomavirus infection as a predictor of cervical intraepithelial neoplasia. JAMA. 2001;286(24):3106-14.
27. Soto Y, Kourí V, Martínez PA, Correa C, Torres G, Goicolea A, et al. Normalización de un sistema de reacción en cadena de la polimerasa en tiempo real para la cuantificación de papilomavirus humano de alto riesgo oncogénico. VacciMonitor. 2012;21(1):30-37.
28. Smith SM, Murray DW. An Overview of MicroRNA Methods: Expression Profiling and Target Identification. In: Espina V, Liotta LA, editors. Molecular Profiling: Methods and Protocols, Methods in Molecular Biology, vol. 823. Dordrecht: Springer Science + Business Media; 2012. p. 119-39.
29. Taylor CF. Mutation scanning using high-resolution melting. Biochem Soc Trans. 2009;37(Pt 2):433-7.
30. Ginzinger DG, Godfrey TE, Nigro J, Moore DH, 2nd, Suzuki S, Pallavicini MG, et al. Measurement of DNA copy number at microsatellite loci using quantitative PCR analysis. Cancer Res. 2000;60(19):5405-9.
31. Esteller M, Corn PG, Baylin SB, Herman JG. A gene hypermethylation profile of human cancer. Cancer Res. 2001;61(8):3225-9.
32. Schwarzenbach H, Hoon DS, Pantel K. Cell-free nucleic acids as biomarkers in cancer patients. Nat Rev Cancer. 2011;11(6):426-37.
33. Balcells I, Cirera S, Busk PK. Specific and sensitive quantitative RT-PCR of miRNAs with DNA primers. BMC Biotechnology. 2011;11:70.
34. Day PJ. Miniaturized PCR systems for cancer diagnosis. Biochem Soc Trans. 2009;37(Pt 2):424-6.
35. Qiagen kit handbooks and user manuals. Critical Factors for Successful Real-Time PCR. 2010 [cited 2013 Nov 27]. Available from: http://www.gene-quantification.de/qiagen-qpcr-sample-assay-tech-guide-2010.pdf.
36. Fathman CG, Soares L, Chan SM, Utz PJ. An array of possibilities for the study of autoimmunity. Nature. 2005;435(7042):605-11.
]]>37. Kubista M, Andrade JM, Bengtsson M, Forootan A, Jonak J, Lind K, et al. The real-time polymerase chain reaction. Mol Aspects Med. 2006;27(2-3):95-125.
38. Xi L, Nicastri DG, El-Hefnawy T, Hug¬hes SJ, Luketich JD, Godfrey TE. Optimal markers for real-time quantitative reverse transcription PCR detection of circulating tumor cells from melanoma, breast, colon, esophageal, head and neck, and lung cancers. Clin Chem. 2007;53(7):1206-15.
39. Heckmann LH, Sorensen PB, Krogh PH, Sorensen JG. NORMA-Gene: a simple and robust method for qPCR normalization based on target gene data. BMC Bioinformatics. 2011;12:250.
40. Sims AH. Bioinformatics and breast cancer: what can high-throughput genomic approaches actually tell us? J Clin Pathol. 2009;62(10):879-85.
41. Debey S, Schoenbeck U, Hellmich M, Gathof BS, Pillai R, Zander T, et al. Compa¬rison of different isolation techniques prior gene expression profiling of blood derived cells: impact on physiological responses, on overall expression and the role of different cell types. Pharmacogenomics J. 2004;4(3):193-207.
]]>42. Nolan T, Hands RE, Bustin SA. Quantification of mRNA using real-time RT-PCR. Nat Protoc. 2006;1(3):1559-82.
43. Life Technologies Inc. Ambion´s Technical Bulletin #159. Working with RNA. 2010 [cited 2013 Nov 27]. Available from: http://www.invitrogen.com/site/us/en/ home/References/Ambion-Tech-Support/nuclease-enzymes/general-articles/working-with-rna.html.
44. Ho-Pun-Cheung A, Bascoul-Mollevi C, Assenat E, Boissiere-Michot F, Bibeau F, Cellier D, et al. Reverse transcription-quantitative polymerase chain reaction: description of a RIN-based algorithm for accurate data normalization. BMC Mol Biol. 2009;10:31.
45. Huggett J, Dheda K, Bustin S, Zumla A. Real-time RT-PCR normalisation; stra¬tegies and considerations. Genes Immun. 2005;6(4):279-84.
46. Murphy J, Bustin SA. Reliability of real-time reverse-transcription PCR in clinical diagnostics: gold standard or substandard? Expert Rev Mol Diagn. 2009;9(2):187-97.
]]>47. Yuan JS, Reed A, Chen F, Stewart CN, Jr. Statistical analysis of real-time PCR data. BMC Bioinformatics. 2006;7:85.
48. Bustin SA, Benes V, Garson JA, He¬llemans J, Huggett J, Kubista M, et al. The MIQE guidelines: minimum information for publication of quantitative real-time PCR experiments. Clin Chem. 2009;55(4):611-22.
49. Wang Y, Barbacioru C, Keys D, Brzoska P, Chen C, Li K, et al. Real-Time polymerase chain reaction gene expression assays in biomarker discovery and validation. In: Wang F, editor. Methods in Pharmacology and Toxicology: Biomarker Methods in Drug Discovery and Development. Totowa: Humana Press; 2010. p. 63-86.
50. Dignam J, Bregant J, Paik S. Statistical Considerations in Assessing Molecular Markers for Cancer Prognosis and Treatment Efficacy. In: Looney SW, editor. Methods in Molecular Biology: Bioestatistical Methods. New Jersey: Humana Press; 2002. p.169-89.
51. Sarker D, Workman P. Pharmacodynamic biomarkers for molecular cancer therapeutics. Adv Cancer Res. 2007;96:213-68.
52. Wang L, McLeod HL, Weinshilboum RM. Genomics and drug response. N Engl J Med. 2011;364(12):1144-53.
]]>53. Nishizuka S, Charboneau L, Young L, Major S, Reinhold WC, Waltham M, et al. Proteomic profiling of the NCI-60 cancer cell lines using new high-density reverse-phase lysate microarrays. Proc Natl Acad Sci USA. 2003;100(24):14229-34.
54. Kitano H. Perspectives on Systems Biology. New Generation Computing 2000;18:199-216.
55. Lopez-Lazaro M. A new view of carcinogenesis and an alternative approach to cancer therapy. Mol Med. 2010;16(3-4):144-53.
56. Huggett J, Green C, Zumla A. Nucleic acid detection and quantification in the developing world. Biochem Soc Trans. 2009;37(Pt 2):419-23.
57. Wang H, Huang S, Shou J, Su EW, Onyia JE, Liao B, et al. Comparative analysis and integrative classification of NCI60 cell lines and primary tumors using gene expression profiling data. BMC Genomics. 2006;7:166.
58. Kammula US, Marincola FM, Rosenberg SA. Real-time quantitative polymerase chain reaction assessment of immune reactivity in melanoma patients after tumor peptide vaccination. J Natl Cancer Inst. 2000;92(16):1336-44.
59. Panelli MC, Wang E, Monsurro V, Marincola FM. The role of quantitative PCR for the immune monitoring of cancer patients. Expert Opin Biol Ther. 2002;2(5):557-64.
60. Zitvogel L, Kepp O, Kroemer G. Immune parameters affecting the efficacy of chemotherapeutic regimens. Nat Rev Clin Oncol. 2011;8(3):151-60.
61. Whiteside TL. Immune responses to cancer: are they potential biomarkers of prognosis? Front Oncol. 2013;3:107.
62. Borad M J, Von Hoff DD. Chapter 3: Clinical trial designs for more rapid proof-of-principle and approval. In: Neidle S, ed. Cancer Drug Design and Discovery. London: Elsevier Inc. 2008, p. 53-87.
]]>
Recibido en diciembre de 2013.
Aprobado en mayo de 2014.
Damián Mainet-González. Departamento de Farmacogenómica, Subdirección de Investigaciones Biomédicas, Centro de Ingeniería Genética y Biotecnología, CIGB. Ave. 31 e/ 158 y 190, Cubanacán, Playa, CP 11600, La Habana, Cuba. E-mail: damian.mainet@cigb.edu.cu.
]]>