Lic. Yanier Núñez Figueredo,1 DraC. Juana Tillán Capó,2 Téc. Carmen Carrillo Domínguez,3 Lic. Marta Guerra Ordóñez 4 y Lic. Reinaldo Rivero Martínez 5
Se evaluó el extracto acuoso liofilizado de Boerhavia erecta L. sobre la transmisión colinérgica e histaminérgica, se emplearon cobayos Hartley para la extracción de porciones de íleon que fueron estimulados con histamina y acetilcolina con y sin la presencia del extracto, también se provocó un previo bloqueo de los receptores histaminérgicos y colinérgicos presentes en el órgano para después estimular el mismo con el extracto de B. erecta. En todos los casos se determinó la amplitud de las contracciones del órgano; los registros se realizaron mediante un transductor isotónico acoplado a un polígrafo Nihon Kodhen. El extracto acuoso liofilizado de B. erecta a concentraciones entre 0,1 mg/mL y 1 mg/mL no presentó actividad antimuscarínica y si mostró efecto antihistamínico in vitro. El extracto de B. erecta a concentraciones entre 1 y 10 mg/mL administrada de forma conjunta con acetilcolina 3x10-3 M provocó una contracción mayor que las inducidas por la B. erecta administrada de forma independiente y menor que la provocada por la acetilcolina, un comportamiento similar se obtuvo tras la administración conjunta de B. erecta e histamina 10-5 M. Cuando los receptores muscarínicos e histamínicos fueron bloqueados con atropina y difenhidramina respectivamente y posteriormente se añadió B. erecta, las contracciones provocadas por esta última fueron menores que las provocadas por el extracto sin previo bloqueo de los receptores. Estos resultados indicaron que el extracto acuoso de B. erecta. tiene tanto efecto agonista como antagonista para la histamina en dependencia de la concentración a la que se utilice y no presenta actividad antimuscarínica.
Palabras clave: Boerhavia erecta L., extracto acuoso liofilizado, íleon, asma, acetilcolina, histamina.
Boerhavia erecta L. es una planta perteneciente a la familia Nictagináceas muy común en terrenos yermos, campos cultivados, orilla de los ríos y aún en las calles. Se encuentra en las Antillas Mayores, Islas Vírgenes, La Florida desde México a través de la América continental hasta la parte norte de Sudamérica y en el Africa tropical.
Hierba perenne, ascendente, ramificada de 3 a 12 cm de alto, a menudo pubescente, al menos en la parte baja, las ramas son lampiñas o puberulentas. Hojas opuestas de rómbico-aobadas a oblongas a casi orbiculares de 2 a 6 cm de largo y de 0,8 a 5 cm de ancho, redondeadas, obtusas y ocasionalmente agudas en el apéndice, troncadas, redondeadas o subacorazonada en la base con el peciolo delgado, enteras u onduladas. Flores perfectas, en panículas delgadas, a menudo de 3 cm de largo, subtendidas por brácteos diminutos; sus ramas casi filiformes, lampiñas o puberulentas. Las flores son rojizas de cáliz campanulado. Estambres de 1 a 5 filamentos delgados, soldados en la base, ovario estopitado, estilo filiforme, estigma peltado.
La raíz de esta planta es algo aromática y se considera antiespasmódica, útil en los accidentes epilépticos. También es utilizada contra el histerismo, la corea y algunas enfermedades nerviosas. En decocción tiene propiedades emetocatárticas y es empleada contra la disentería y como diurética. En cocimiento es estimulante sobre la secreción biliar y se utiliza para contener hemorragias, contra la fiebre biliosa, el paludismo, la ictericia, la hidropesía, insuficiencia renal, la albuminuria y las congestiones del hígado y el bazo. El jugo amargo de la raíz es utilizado en las congestiones hepáticas. Los tallos foliáceos son utilizados como diurético y el polvo de la planta en general es usada como expectorante, contra el asma y depurativa.1
El Centro de Investigación y Desarrollo de Medicamentos (CIDEM) se realiza la investigación de B. erecta extracto acuoso liofilizado para el tratamiento del asma bronquial, por lo que se deció evaluar el efecto del mismo sobre la musculatura lisa y en especial sobre la transmisión colinérgica e histaminérgica, ya que como es conocido cuando la acetilcolina (Ach) interactúa con sus receptores M1 y M3 y la histamina con sus receptores H1 presentes en el músculo liso provoca contracción del mismo y por lo tanto incide de manera negativa en los cuadros asmáticos.2
Extracto acuoso liofilizado a partir del follaje de B. erecta; número de herbario 4642 de la estación experimental de plantas medicinales "Dr. Juan Tomas Roig", lote 9/10/01.
Reactivos
Animales de experimentación
Se utilizaron cobayos machos, de la raza Hartley, de 200 a 250 g de masa corporal procedentes del Centro Nacional para la Producción de Animales de Laboratorios (CENPALAB).
Condiciones ambientales y de laboratorio
Para la determinación del efecto de B. erecta extracto acuoso liofilizado sobre la musculatura lisa se realizaron los siguientes ensayos:
Transmisión colinérgica5,9,10
Transmisión histaminérgica5-9, 11-13
En todos los casos se determinó la amplitud de las contracciones de las porciones de órganos aislados, los registros se realizaron con la ayuda de un transductor isotónico acoplado a un polígrafo Nihon Kodhen con una velocidad del papel 10 mm/min y una sensibilidad igual a 1.
Los resultados obtenidos, en los diferentes ensayos, se expresaron a través de la media ± desviación estándar. Los mismos se procesaron mediante un análisis de varianza de una vía y posteriormente se realizó la prueba de Duncan con un nivel de significación de p<0,05.14
A concentraciones menores a 1 mg /mL no se observó contracción de la musculatura lisa. ]]>
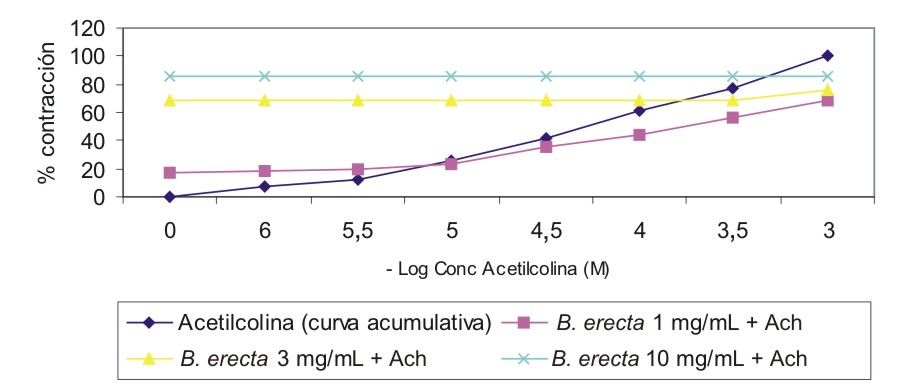
A concentraciones de 0,1; 0,3 y 1 mg/mL de B. erecta extracto acuoso liofilizado no se observó efecto antimuscarínico in vitro.En la figura 1 se observa que a concentraciones de la muestra de 3 y 10 mg/mL se produce una contracción tal que no se modifica cuando se añade de forma acumulativa la acetilcolina. Después de adicionar 1 mg/mL de B. erecta se produjo una contracción sobre el íleon que comenzó a aumentar tras añadir concentraciones de Ach mayores a 3 x 10-5 M, pero esta no superó la contracción provocada por la Ach de manera independiente.
Fig.1. Contracción provocada por la administración conjunta de B erecta extracto acuoso liofilizado 1, 3 y 10 mg/mL y Ach 10-6 - 10-3 M.
En la figura 2 se puede observar como la atropina 3´10-12 M provoca inhibición de la respuesta contráctil inducida por B. erecta extracto acuoso liofilizado y Ach 10-3 M.
En la figura 3, se puede observar que a concentraciones de histamina mayores a 3 ´10-7 M todas las contracciones difieren significativamente entre sí para p<0,01, apreciándose una disminución dosis dependiente del porcentaje de contracción provocada por dicho agonista.
A la concentración de 10-7 M de histamina todas las contraciones presentaron diferencias significativas con respecto al tratamiento control para p<0,05.
A concentraciones del agonista inferiores a 10-7 M no se observaron diferencias significativas entre ninguna de las concentraciones.
En la figura 4 se puede apreciar que cuando la B. erecta 1,3 y 10 mg/mL fue administrada de manera conjunta con histamina a la concentraciones de 10-8 - 10-5 M, esta presentó un comportamiento semejante al mostrado tras la administración conjunta de B. erecta y Ach.
Fig. 4. Contracción provocada con la administración conjunta de B. erecta extracto acuoso liofilizado 1,3;10 mg/mL e histamina 10-8 - 10-5 M.
En la figura 5 se representan los resultados de la contracción provocada por la B. erecta una vez bloqueados los receptores H1 con 2 ´10-5 M de difenhidramina, observándose también un efecto similar al mostrado cuando se bloquearon los receptores muscarínicos.
Fig. 5. Resultado de la contracción provocada por la B. erecta extracto acuoso liofilizado 1,3 y 10 mg/mL sobre el ileón aislado de cobayos después de un previo bloqueo de los receptores histaminérgicos con difenhidramina 2 ´ 10-5 M
** difieren para p <0,01. ]]>
Boerhavia erecta L. extracto acuoso liofilizado a concentraciones superiores a 1mg/mL produce una contracción de la musculatura lisa intestinal, probablemente mediado por un efecto directo sobre los receptores muscarínicos e histaminérgicos, específicamente los M1, M3 y H12 ya que estos al ser estimulados con sus agonistas correspondientes provocan contracción de la musculatura lisa.
Cuando se realizó la estimulación del órgano conjuntamente con B. erecta y acetilcolina, se pudo observar que las concentraciones de 3 y 10 mg/mL del extracto produjeron una contracción tal que no fue modificado por la Ach.
Solamente cuando la B. erecta fue administrada a la concentración de 1 mg/mL se produjo un aumento de la contracción provocada por la acción de la Ach a concentraciones superiores a 3 ´10-5 M y no se superó la máxima contracción provocada por dicho agonista de manera independiente.
De manera similar, cuando se realizó la estimulación del órgano conjuntamente con B. erecta e histamina se pudo observar que las concentraciones de 3 y 10 mg/mL provocaron una contracción tal por parte de B. erecta extracto acuoso liofilizado que no fue modificado por la histamina. Cuando la Boerhavia fue administrada a la concentración de 1 mg/mL se produjo un aumento de la contracción provocada por la histamina a concentraciones superiores a 3 ´10-6 M y no se superó la máxima contracción provocada por el agonista de manera independiente.
Los resultados obtenidos pueden deberse a que B. erecta extracto acuoso liofilizado presenta una composición química heterogénea a predominio de flavonoides, triterpenos, taninos, aminas, azucares reductores, aminoácidos, entre otros17 lo que le confiere la propiedad de presentar diversos efectos biológicos.
Finalmente se puede concluir que Boerhavia erecta L. extracto acuoso liofilizado a concentraciones menores a 1 mg/mL no provocó contracción de la musculatura lisa, a concentraciones entre 0,1 y 1 mg/mL presentó buena actividad antihistamínica in vitro y no mostró actividad anticolinérgica, a concentraciones superiores a 1 mg/mL provocó contracción del íleon aislado de cobayos, probablemente mediado por un agonismo de los receptores de la histamina y la Ach.
The aqueous frozen-dried extract of Boerhavia erecta L. was evaluated as regards the cholinergic and histaminergic transmission. Hartley Guinea pigs were used to extract ileum portions that were estimulated with histamine and cetylcholine with or without the presence of the extract. A previous block of the histaminergic and cholinergic receptors present in the organ was provoked to further estimulate it with the B. erecta extract. The amplitude of the organ's contractions was determined in every case. Registers were made by an isotonic transductor coupled to a Nihon Kodhen polygrapher. The aqueous frozen-dried extract of B. erecta at concentrations between 0,1 mg/mL and 1 mg/mL did not present antimuscarine activity, but it did show in vitro antihistamine effect. The B. erecta extract at concentrations from 1 to 10 mg/mL administered together with acetylcholine 3x10-3 M caused a higher contraction than the induced by B. erecta administered in an independent way and lower than the produced by acetylcholine. A similar behavior was observed after the joint administration of B. erecta and histamine 10-5 M. When the muscarine and histamine receptors were blocked with atropine and diphenhydramine, respectively, and B. erecta was added later, the contractions provoked by the latter were lower than the caused by the extract without previous block of the receptors. These results showed that the aqueous extract of B. erecta L. has both agonist and antagonist effect for histamine, depending on the concentration at which it is used, and that it has no antimuscarine activity
Key words: Boerhavia erecta L., aqueous frozen-dried extract, ileum, asthma, acetylcholine, histamine.
Recibido: 29 de abril de 2004. Aprobado: 12 de mayo de 2004.
Lic. Yanier Núñez Figueredo. Centro de Investigación y Desarrollo de Medicamentos. Calle 17 No. 6208 e/ 62 y 64 Playa. La Habana, Cuba.
E-mail: cidem.cb@infomed.sld.cu
cinfa@infomed.sld.cu
Fax: (537) 33 5556
1 Licenciado en Ciencias Farmacéuticas. Aspirante a investigador.
2 Doctora en Ciencias Veterinarias. Investigadora Auxiliar.
3 Técnica Medio en Farmacia.
4 Máster en Ciencias. Licenciada en Microbiología. Investigadora Auxiliar
5 Licenciado en Ciencias Farmacéuticas. Aspirante a investigador.