Facultad de Ciencias Médicas "Dr. Salvador Allende"
Laboratorio Central de Farmacología
Dr. Francisco J. Morón Rodríguez1 y Dra. Déborah Morón Pinedo2
Antecedentes: Morinda citrifolia L. es una planta medicinal tradicional, a la cual le atribuyen diversas propiedades; sin embargo, existen pocos trabajos publicados que validan científicamente su uso.
Objetivo: revisar y actualizar la información científica que puede avalar el uso médico de la especie, particularmente del fruto. Métodos: se emplearon las palabras claves Morinda citrifolia, Morinda litoralis o Morinda bracteata para realizar una revisión en las bases de datos disponibles (PubMed, COCHRANE, ESBCO, SCIELO, LILACS, CUMED, MEDNAT, RECU). A partir de los resultados, se buscaron los artículos originales y se analizó la información para relacionar cada uso etnomédico con las investigaciones científicas que pudieran validar su acción farmacológica y la seguridad toxicológica.
Resultados: se encontraron un total de 47 referencias en las bases consultadas. Sólo 5 avalaron, en modelos preclínicos mayoritariamente in vitro, las actividades farmacológicas del jugo del fruto para los usos etnomédicos relacionados con el cáncer e inmunoestimulación, así como con el dolor y la inflamación. La seguridad del empleo estuvo sustentada solamente por 1 trabajo sobre toxicidad aguda oral realizado con extracto etanólico de fruto y 1 artículo informaba sobre un paciente con insuficiencia renal crónica y los problemas de salud observados con la ingestión del jugo. Las hojas y raíces de la planta están menos investigadas que el fruto.
Conclusiones: la información científica disponible, no permite validar los usos y la seguridad del empleo tradicional de Morinda citrifolia, porque está limitada a estudios ]]>
Palabras clave: Morinda citrifolia, fitoterapia, plantas medicinales, medicina complementaria, etnomedicina, toxicidad.
Existe un creciente interés y uso popular del fruto de Morinda citrifolia L. (sin., Morinda bracteata Roxb. y Morinda litoralis Blanco), de la familia Rubiaceae, que ha sido promovido por diversas publicaciones populares, incluida la prensa, que informan o, más bien desinforman, a la población sobre supuestas propiedades comprobadas científicamente que posee esa especie; algunos llegan a afirmar que alcanzan la cifra de más de 120 problemas de salud los que pueden ser tratados, y hasta curados, con la planta y sus extractos.Noni, uno de sus nombres populares, es una de las plantas medicinales tradicionales más importantes en Polinesia, donde las indicaciones se centraban primariamente en la aplicación tópica de las hojas, las raíces, la corteza y el fruto verde. Sin embargo, se reporta que ha cambiado este patrón de uso hacia el empleo del jugo del fruto, maduro o en estado de putrefacción, en Hawai durante los años mas recientes. Algunas publicaciones atribuyen al investigador Ralph M. Heinicke, basado en los usos polinesios tradicionales, haber sido un promotor del empleo de noni en diversas indicaciones, que incluyen el tratamiento del cáncer a partir de resultados incipientes de investigaciones.1
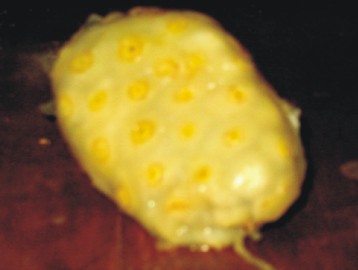
Fig. Fruto maduro de M. citrifolia. Foto: F. Morón.
El empleo tradicional de noni por los polinesios le atribuye efectos relacionados con actividad antibacteriana, antiviral, antifúngica, antitumoral, antihelmíntica, analgésica, antiinflamatoria, hipotensora e inmunoestimulante; se dice que es usado desde hace más de 2 000 años.2
El problema no puede ser visto de una manera simple; no se trata de la frase to be or not to be del ilustre escritor inglés Shakespeare y tampoco es una cuestión de "creer o no creer" como si se abordara un problema filosófico de manera dogmática en la cual se decide aceptar un mito o refutarlo a priori.
La medicina es una ciencia y las decisiones tienen que ser respaldadas por investigaciones. Cada día se avanza en el método de la medicina basada en hechos o resultados, como elementos para tomar la mejor decisión al elegir una conducta, terapéutica o diagnóstica, ante un problema de salud.
Las publicaciones disponibles, sobre el tema que se trata, están dispersas y muchas corresponden a especialidades que no son asequibles para los médicos dedicados a la práctica clínica.
El uso irracional, tanto de medicamentos como de plantas medicinales u otros procedimientos, es a juicio de los autores un problema de salud universalizado. La Organización Mundial de la Salud ha publicado recientemente un documento que aborda esta situación para las medicinas tradicionales y las complementarias.3
Las razones antes referidas, motivaron a los autores a realizar una búsqueda de los trabajos científicos publicados, con el objetivo de revisar, actualizar y comentar la información que pudiera avalar el uso médico de la especie.
Se emplearon las palabras claves Morinda citrifolia, Morinda bracteata y Morinda litoralis; así como, los nombres de autores que en textos pseudo-científicos que circulan se les atribuye participación importante en la investigación o uso de la especie (Ralph M. Heinicke, Walter Lübeck, Hendrik Hannes y Charles Garnier), para buscar en las bases de datos disponibles, que fueron:
La investigación en las bases se realizó el día 25 de junio de 2004.
A partir de las referencias encontradas, se buscaron los artículos originales y se analizó la información para relacionar cada uso etnomédico con los trabajos científicos que pudieran validar su acción farmacológica y la seguridad toxicológica.
Las búsquedas, sobre Morinda citrifolia y sus sinonimias, efectuadas en las bases de datos bibliográficas sólo tuvieron resultados positivos en PubMed y EBSCO; en las restantes no se encontró ninguna referencia. En PubMed se encontraron 44 referencias desde el 1955 hasta al 2004 y en EBSCO se obtuvieron sólo 3 que correspondían al período 1998-2004.
De los trabajos científicos publicados por R.M. Heinicke se encontraron en PubMed 7 artículos en los años 1953-1972; sin embargo, ninguno era referente a la especie medicinal que fue objeto de esta revisión.
La búsqueda de los autores Walter Lübeck y Hendrik Hannes en PubMed no dio ningún resultado del primero y del segundo sólo 3 artículos en el período 1967-1968, pero ninguno de ellos era sobre la M. citrifolia. ]]>
Charles Garnier, otro investigador mencionado, es autor de artículos científicos, pero ninguno es sobre la especie de interés.
Vale comentar que la inexistencia de esos autores o sus publicaciones sobre M. citrifolia no permite negar la realidad de tales artículos, pero si se puede decir que no han sido publicados en revistas internacionales indexadas en varias bases de datos. Sin embargo, es sorprendente que investigadores de países desarrollados no hayan publicado sus resultados en revistas científicas de amplia difusión.
La información encontrada, en las bases de datos, se dividió según las partes usadas de la planta y por acciones farmacológicas para facilitar el análisis.
El jugo del fruto, en concentraciones de 5 % v/v o superior, inhibió significativamente, en comparación con los controles de volúmenes equivalentes de solución salina 0,9 %, la iniciación de nuevos brotes vasculares en explantes de vena placentaria humana. Estas concentraciones del jugo también redujeron la velocidad de crecimiento y la proliferación de brotes capilares de nuevo desarrollo. La concentración del 10 % de jugo en el medio de cultivo, indujo degeneración vascular y apoptosis en los pozos con células capilares establecidas a los pocos días de haber sido aplicado. ]]>
Los autores también encontraron que el jugo, a concentración del 10 % en el medio de cultivo, inhibió la iniciación capilar en explantes de tumores mamarios humanos y en explantes tumorales, con brotes capilares, los vasos degeneraron rápidamente.
Los modelos, antes mencionados, de matriz de coagulo de fibrina tridimensional con explantes de vena placentaria y de tumor de mama humanos, son modelos para evaluar el desarrollo angiogénico vascular.4
Un estudio realizado con jugos de noni tahitiano, comercializados como suplementos dietéticos, administrados al 10 % en el agua de beber durante 1 semana, previno la formación de un adducto de 7-12 dimetilbenzo[a]antraceno (DMBA)-DNA. Las concentraciones de DMBA-DNA fueron reducidas en el corazón (30 %), los pulmones (41 %), el hígado (42 %) y los riñones (80 %) en ratas Sprague-Dowley hembras. Sin embargo, el efecto fue mucho mayor en ratones C57BL-6 machos, los cuales redujeron el DMBA-DNA en el corazón (60 %), el hígado (70 %) y los riñones (90 %). El jugo tuvo efecto antioxidante in vitro que fue comparable con el producido por vitamina C, polvo de semilla de uva y picnogenol en dosis equivalentes a las diarias recomendadas en los Estados Unidos. Estos resultados hicieron que los autores sugirieran que pudiera contribuir a prevenir el cáncer.5
Una fracción enriquecida de polisacárido del jugo tuvo efectos profilácticos y terapéuticos potenciales contra el modelo de Sarcoma 180 sensible a inmunomoduladores. La actividad antitumoral de ese extracto produjo una curación del 25 al 45 % en ratones alogénicos y el efecto fue abolido completamente por la administración simultánea de inhibidores específicos de macrófagos (2-cloro adenosina), de células T (ciclosporina) o de células asesinas naturales (anticuerpo GM1 antiasialo). La fracción produjo efectos sinérgicos beneficiosos cuando se combinó con fármacos antineoplásicos como cisplatino, adriamicina, mitomicina C, bleomicina, etopósido, 5-fluoruracilo, vincristina o camtotecina. No fue favorable cuando se asoció con paclitaxel, arabinósido de citosina o fármacos anticancerosos inmunosupresores como ciclofosfamida, metrotexato o 6-tioguanina. También fue favorable la administración conjunta con citocina Th1 e interferón gamma, pero la actividad fue abolida cuando se combinó con citocina Th2, interleucina-4 o interleucina-10; lo que sugiere que la fracción induce, in vivo, un estado inmune dominante Th1. La asociación de la fracción con imexón, un inmunomodulador sintético, también fue beneficiosa; pero resultó desfavorable la combinación con el copolímero MVE-2, un inmunomodulador de alto peso molecular, interleucina-2 o interleucina-126.
Una fracción rica en polisacáridos del jugo del fruto, con actividad antitumoral en el modelo de carcinomatosis peritoneal de pulmón de Lewis (LLC), incrementó significativamente la supervivencia de ratones portadores de tumor LLC isogénico. No tuvo efecto citotóxico significativo en el cultivo de células de LLC, LLC1; pero pudo activar exudado de células peritoneales (PEC) para trasmitir toxicidad cuando se cultivó conjuntamente con las células tumorales. Eso sugiere que la fracción suprimió el crecimiento tumoral mediante la estimulación del sistema inmune del huésped. El tratamiento conjunto con el agente inmunosupresor 2-cloroadenosina (C1-Ade) o con ciclosporina A (cys-A) disminuyó el efecto de la fracción del jugo, sustentando un mecanismo inmunomodulador. Además, la fracción liberó varios mediadores de células efectoras murinas, como: factor alfa de necrosis tumoral (TNF-alfa), interleucina-1beta (IL-1beta), IL-10, IL-12 p70, interferón-gamma (IFN-gamma) y óxido nítrico (NO); pero no tuvo actividad sobre IL-2 y suprimió la liberación de IL-4. El incremento del tiempo de supervivencia y la curación ocurrieron al combinar dosis sub-óptimas de quimioterápicos como: adriamicina, cisplatino, 5-fluorouracilo y vincristina; lo que sugiere la aplicación clínica de la fracción polisacárida del jugo como complemento en el tratamiento del cáncer.6,7
El jugo del fruto tiene 2 glucósidos, 6-O-(beta-D-glucopiranosil)-1-O-octanoil-beta-D-glucopiranosa y ácido asperulosídico. Estos compuestos suprimieron la transformación celular inducida por 12-O-tetradecanoilphorbol-13-acetato (TPA) o por factor de crecimiento epidérmico (EFG) y la actividad AP-1 asociada en células epiteliales JB6 de ratón. La fosforilación de c-Jun inducida por TPA o EGF, pero no las cinasas reguladas por señal extracelular o p38 cinasas, fue bloqueada por los compuestos del noni antes descritos; lo anterior indicó que las cinasas N-terminales c-Jun fueron críticas en la mediación de la actividad AP-1 inducida por TPA o EGF y la subsiguiente transformación celular en células JB6.8
Otros compuestos han sido encontrados en el jugo del fruto. Se han identificado 3 glucósidos: 6-O-(beta-D-glucopiranosil)-1-O-octanoil-beta-D-glucopiranosa, 6-O-(beta-D-glucopiranosil)-1-O-hexanoil-beta-D-glucopiranosa y 3-metilbut-3-enil 6-O-beta-D-glucopiranosil-beta-D-glucopiranósido.9 Además, en la fracción del fruto soluble en n-butanol fueron identificados los glucósidos, rutina y ácido asperulosídico; así como, un éster ácido graso trisacárido identificado como 2,6-di-O-(beta-D-glucopiranosil)-1-O-octanoil-beta-D-glucopiranosa.10
El extracto etanólico del fruto pulverizado inhibió, in vitro, la ciclooxigenasa-1 (COX-1) y tuvo una concentración inhibitoria media (CI50) igual a 163 µg/mL, mientras que los controles con aspirina o indometacina inhibieron la COX-1 con CI50 iguales a 241 y 1,2 µg/mL respectivamente.11 Sin embargo, la administración de jugo del fruto maduro (50 % en agua peso a peso), administrado en dosis de 20 g de material vegetal fresco/kg, por vía oral, no tuvo efecto analgésico en el modelo de contorsiones inducidas por ácido acético 0,75 % intraperitoneal (0,1 mL/10 g) en ratones OF-1 (F. Morón y otros. Laboratorio Central de Farmacología, resultado no publicado).
Existe el reporte de que el jugo causó hiperpotasemia en un paciente con insuficiencia renal crónica que llevaba una dieta baja en potasio. La concentración de potasio en varias muestras de jugo fue de 56,3 mEq/L, parecida a la que se encuentra en los jugos de naranja y de tomate.12 ]]>
Un extracto hidroalcohólico 50 % de fruto seco, administrado en dosis de 10 g de material vegetal seco/kg, por vía oral o subcutánea, no causó toxicidad general en ratones.13
Las hojas contienen un dímero iridoide formado por 2 unidades de iridoides unidos por un extraño grupo éter que inhibieron significativamente al activador de proteína-1 (AP-1) inducido por radiación ultravioleta B (UVB) en cultivo celular.14
En la hoja se identificaron 1 glucósido iridoide y 5 glucósidos flavonoles. El irinoide existe como mezcla epimérica en solución. Todos estos compuestos tuvieron actividad secuestradora de radicales libres, efecto antioxidante in vitro, en concentraciones de 30 µM.15
El irinoide, citrifolinosida, inhibió el activador de proteína-1 (AP-1) inducido por UVB en cultivo celular.16 ]]>
Otros estudios informan que la hoja contiene el glucósido irinoide, citrifolinosida A, y los irinoides asperulosida y ácido asperulosídico.17 Además, las hojas tienen un benzofurano (5-benzofurano ácido carboxílico-6-formil metil éster) y un bis-nor-isoprenoide (4-(3'(R)-hidroxibutil)-3,5,5, trimetil-ciclohex-2-en-1-ona).18El extracto alcohólico de hojas tiernas mostró actividad antihelmíntica in vitro contra Ascaris lumbricoides humano.19
Los extractos clorofórmico, hexánico y metanólico de la hoja desecada en frío, aplicados respectivamente en dosis de <2 mg/placa, > 1mg/placa y <1 mg/placa, tuvieron actividad antimutagénica, contra mutágenos indirectos, en el modelo in vitro de Salmonella typhimurium TA100. Sin embargo, no tuvieron efecto contra mutágenos directos en dosis hasta 10 mg/placa.20
El extracto acuoso liofilizado de raíz sin corteza, administrado en dosis de 800 mg/kg, por vía intraperitoneal, tuvo actividad analgésica significativa y en los modelos de plato caliente y de contorsiones en ratones. El efecto del extracto fue antagonizado por naloxona, lo que indica un efecto central tipo morfínico, y no mostró toxicidad en los ratones. Además, el extracto administrado en dosis de 1,6 g/kg, intraperitoneal, disminuyó todos los parámetros conductuales en los modelos de 2 compartimentos, de selección de luz/oscuridad y de la escalera; conjuntamente con el tiempo de sueño inducido. Estos resultados sugieren que el extracto tuvo efecto sedante.22
En esta revisión, se encontraron relativamente pocas referencias, en total 47, en las bases consultadas.
Sólo 5 avalaron, en modelos preclínicos mayoritariamente in vitro, la actividad farmacológica del jugo para los usos etnomédicos, que se pudieran agrupar como, relacionados con cáncer e inmunoestimulación,4-8 así como dolor e inflamación.11 Este último se efectuó en el modelo de ciclooxigenasa 1 (COX-1) in vitro. Esa enzima, si bien es inhibida por los fármacos antiinflamatorios no esteroideos inespecíficos (AINE) como la aspirina, es la llamada ciclooxigenasa constitutiva que se considera relacionada principalmente con los efectos adversos, a diferencia de la COX-2 que está relacionada con las acciones farmacológicas de interés terapéutico.
La ausencia de efecto analgésico del jugo que se encontró, no contradice que puede ser capaz de inhibir la COX-1, como publicaron anteriormente otros autores;11 pero sugiere que el jugo de noni no tiene efecto sobre la COX-2 y por tanto carece de efecto analgésico de tipo periférico como los AINE. No se espera que tenga actividad en los modelos in vivo para estudiar efecto central, tipo morfina, porque los fármacos de este grupo son activos en los modelos experimentales para el dolor tanto periférico como central. ]]>
Los artículos sobre actividades del jugo o el fruto relacionadas con el cáncer se caracterizan porque sólo en 2, uno in vitro4 y otro in vivo5, evaluaron el jugo; 2 estudiaron fracciones de polisacáridos in vivo6,7 y otro un compuesto químico aislado a partir del fruto.8
La experiencia, sobre validación de extractos de plantas medicinales, en el Laboratorio Central de Farmacología de la Facultad de Ciencias Médicas "Doctor. Salvador Allende de La Habana, Cuba, desde 1988, ha llevado a considerar que los estudios in vitro suelen, con bastante frecuencia, dar resultados falsos positivos o negativos. Esto se debe a que los extractos, que más se asemejan al preparado de uso tradicional, suelen ser mezclas acuosas muy complejas, con contenidos iónicos, osmolaridad, pH y otras características, capaces de producir respuestas en los modelos experimentales, que hagan falsamente pensar en la existencia de principios activos, cuando en realidad se está observando un efecto causado por otros factores de la composición del extracto que no se pueden controlar.
Otro aspecto muy importante a considerar, es la respuesta a principios activos puros extraídos de la parte de la planta en estudio; la demostración de un efecto biológico, de un compuesto o fracción activa, no permite asegurar que el extracto crudo produzca la misma actividad por las múltiples interacciones de sus numerosos componentes.
La seguridad del empleo en humanos, está sustentada solamente por 1 trabajo sobre toxicidad aguda de un extracto hidroalcohólico del fruto;13 mientras que 1 artículo explica en pacientes con insuficiencia renal la posibilidad de efectos adversos, por su rico contenido en K+. Muchos de los usos que se proponen para el jugo requieren administraciones durante períodos de tiempo prolongados, lo que requiere ser evaluado, al menos, en modelos de toxicidad subcrónica y estudiar la genotoxicidad. Los efectos adversos pueden escapar a la sabiduría popular y pasar inadvertidos cuando el uso prolongado hace más difícil la asociación de causalidad con el remedio que consume. De manera anecdótica, personas que lo consumen o lo consumieron han comentado a los autores que bajaron de peso, lo anterior puede verse por algunos como otro efecto beneficioso, pero vale preguntarse: ¿no será un efecto tóxico? De hecho, la pérdida o no ganancia de peso es uno de los signos posibles de toxicidad cuando se hace un estudio subcrónico preclínico en animales.
Las hojas14-20 y raíces21-22 de la planta están menos investigadas que el jugo. ]]>
Por lo antes expuesto, se puede concluir que la información científica disponible no permite validar los usos y la seguridad del empleo de Morinda citrifolia porque está limitada a estudios preclínicos farmacológicos y carece de un mínimo de investigaciones toxicológicas que respalden la seguridad. Esto es particularmente relevante en tratamientos para problemas de salud de complejidad como el cáncer.
El uso popular y la información científica interesante, aunque limitada, conducen a recomendar que se profundicen los estudios farmacológicos preclínicos y que se realicen las investigaciones toxicológicas, en extractos estandarizados, que permitan hacer un ensayo clínico en pacientes en un futuro cercano con el objetivo de establecer realmente la eficacia y finalmente la efectividad.
Antecedents: Morinda citrifolia L. is a traditional medicinal plant, which has been attributed diverse properties; however, a few papers have been published scientifically validating its use.
Objective: To review and update the scientific information supporting the medical use of this species, particularly of its fruit.
Methods: The key words Morinda citrifolia, Morinda litoralis or Morinda bracteata were used to make a review in the available databases (Pubmed, COCHRANE, ESBCO, SCIELO, LILACS, CUMED, MEDNAT, RECU). Starting from these results, the original articles were searched and information was analyzed to relate each etnomedical use to the scientific papers that could validate their pharmacological action and the toxicological safety.
Results: 47 references were found in the consulted databases. Only 5 supported, in preclinical models mostly in vitro, the pharmacological activities of the fruit juice for etnomedical uses connected with cancer and immunostimulation, pain and inflammation. The safety of its use was only supported by one paper on acute oral toxicity carried out with ethanolic extract from fruit and one article reported a patient that showed the potentiality of adverse effects in those with renal failure. The leaves and roots of the plant are less investigated than the fruit.
Conclusions: The available scientific information does not allow to validate the uses and safety of the traditional utilization of Morinda citrifolia, since it is limited to preclinical pharmacological studies and the toxicological investigations supporting its safety are insufficient.
1. McClatchey W. From Polynesian healers to health food stores: changing perspectives of Morinda citrifolia (Rubiaceae). Integr Cancer Ther. 2002;1(2):110-20.
2. Wang MY, West BJ, Jensen CJ, Nowicki D, Su C, Palu AK, et al. Morinda citrifolia (Noni): a literature review and recent advances in noni research. Acta Pharmacol Sin. 2002;23(12):1127-41.
3. World Health Organization. WHO guidelines on developing consumer information on proper use of traditional, complementary and alternative medicine. Geneva: World Health Organization; 2004.
4. Hornick CA, Myers A, Sadowska-Krowicka H, Anthony CT, Woltering EA. Inhibition of angiogenic initiation and disruption of newly established human vascular networks by juice from Morinda citrifolia (noni). Angiogenesis. 2003;6(2):143-9.
5. Wang MY, Su C. Cancer preventive effect of Morinda citrifolia (noni). Ann NY Acad Sci. 2001;952:161-8.
6. Furusawa E, Hirazumi A, Story S, Jensen J. Antitumour potential of a polysaccharide-rich substance from the fruit juice of Morinda citrifolia (noni) on sarcoma 180 ascites tumour in mice. Phytother Res. 2003;17(10):1158-64.
7. Hirazumi A, Furusawa E. An immunomodulatory polysaccharide-rich substance from the fruit juice of Morinda citrifolia (noni) with antitumour activity. Phytother Res. 1999;13(5):380-7.
8. Liu G, Bode A, Ma WY, Sang S, Ho CT, Dong Z. Two novel glycosides from the fruits of Morinda citrifolia (noni) inhibit AP-1 transactivation and cell transformation in the mouse epidermal JB6 cell line. Cancer Res. 2001;61(15):5749-56.
9. Wang M, Kikuzaki H, Jin Y, Nakatani N, Zhu N, Csiszar K,et al. Novel glycosides from noni (Morinda citrifolia). J Nat Prod. 2000;63(8):1182-3.
10. Wang M, Kikuzaki H, Csiszar K, Boyd CD, Maunakea A, Fong SF, et al. Novel trisaccharide fatty acid ester identified from the fruits of Morinda citrifolia (noni). J Agric Food Chem. 1999;47(12):4880-2.
11. Li RW, Myers SP, Leach DN, Lin GD, Leach G. A cross-cultural study: anti-inflammatory activity of australian and chinese plants. J Ethnopharmacol. 2003;85(1):25-32.
12. Mueller BA, Scott MK, Sowinski KM, Prag KA. Noni juice (Morinda citrifolia): hidden potential for hyperkalemia? Am J Kidney Dis. 2000;35(2):310-2.
13. Mokkhasmit M, Swatdimongkol K, Satrawaha P. Study on toxicity of Thai medicinal plants. Bull Dept Med Sci. 1971;12(2/4):36-65.
14. Sang S, Liu G, He K, Zhu N, Dong Z, Zheng Q, et al. New unusual iridoids from the leaves of noni (Morinda citrifolia L.) show inhibitory effect on ultraviolet B-induced transcriptional activator protein-1 (AP-1) activity. Bioorg Med Chem. 2003;11(12):2499-502.
15. Sang S, Cheng X, Zhu N, Stark RE, Badmaev V, Ghai G, et al. Flavonol glycosides and novel iridoid glycoside from the leaves of Morinda citrifolia. J Agric Food Chem. 2001;49(9):4478-81.
16. Sang S, He K, Liu G, Zhu N, Cheng X, Wang M, et al. A new unusual iridoid with inhibition of activator protein-1 (AP-1) from the leaves of Morinda citrifolia L. Org Lett. 2001;3(9):1307-9.
17. Sang S, Cheng X, Zhu N, Wang M, Jhoo JW, Stark RE, et al. Iridoid glycosides from the leaves of Morinda citrifolia. J Nat Prod. 2001;64(6):799-800.
18. Siddiqui BS, Ismail FA, Gulzar T, Begum S. Isolation and structure determination of a benzofuran and a bis-nor-isoprenoid from Aspergillus niger grown on the water soluble fraction of Morinda citrifolia Linn. leaves. Nat Prod Res. 2003;17(5):355-60.
19. Raj RK. Screening of indigenous plants for anthelmintic action against human Ascaris lumbricoides: Part--II. Indian J Physiol Pharmacol. 1975;19(1):47-9.
20. Kusamran WR, Tepsuwan A, Kupradinun P. Antimutagenic and anticarcinogenic potentials of some Thai vegetables. Mutat Res. 1998;402(1/2):247-58.
21. Hiwasa T, Arase Y, Chen Z, Kita K, Umezawa K, Ito H, et al. Stimulation of ultraviolet-induced apoptosis of human fibroblast UVr-1 cells by tyrosine kinase inhibitors. FEBS Lett. 1999;444(2-3):173-6.
22. Younos C, Rolland A, Fleurentin J, Lanhers MC, Misslin R, Mortier F. Analgesic and behavioral effects of Morinda citrifolia. Plant Med. 1990;56(5):430-4.
Recibido : 1 de noviembre de 2004. Aprobado: 2 de noviembre de 2004.
DrC. Francisco J. Morón Rodríguez. Facultad de Ciencias Médicas "Dr. Salvador Allende".Laboratorio Central de Farmacología. Carvajal e/ Agua Dulce y A, Cerro. La Habana,Cuba. CP 12000
Telf. (53-7) 406571 al 73 Ext. 1048 ó 1034. e-mail: moron@infomed.sld.cu
1 Doctor en Ciencias Médicas. Especialista de II Grado en Farmacología. Profesor Titular.
2 Doctora en Medicina.