ARTÍCULO ORIGINAL
Estabilidad del polvo de Parthenium hysterophorus L. (escoba amarga) basado en el contenido de partenina mediante cromatografía líquida de alta eficacia
Parthenium hysterophorus L. (escoba amarga) powder stability on the basis of parthenin contents by using high-performance liquid chromatography
]]>
Yanelis Saucedo HernándezI; Bassam Mohamad SafaII; Mirtha Mayra González BediaIII; Hilda M. González San MiguelIV; Luis Ramón Bravo SánchezV; Elisa Jorge RodríguezVI; Adalberto QuintanaVII; Miguel Ángel Alba de ArmasVIII; Reinaldo Quiñones RamosIX; Ana Hernández MonzónX
I Licenciada en Ciencias Farmacéuticas. Máster en Química Farmacéutica. Profesora Asistente. Departamento Farmacia. Facultad de Química Farmacia, Universidad Central de Las Villas (UCLV). Villa Clara, Cuba.
II Licenciado en Ciencias Farmacéuticas. Departamento de Farmacia, UCLV. Villa Clara, Cuba.
III Licenciada en Ciencias Farmacéuticas. Máster en Tecnología y Control de Medicamentos. Profesora Titular. Departamento de Farmacia, UCLV. Villa Clara, Cuba.
IV Doctora en Ciencias. Profesora Auxiliar. Departamento de Farmacia. Instituto de Farmacia y Alimentos. Universidad de La Habana (UH). Ciudad de La Habana, Cuba.
V Doctor en Ciencias Químicas. Licenciado en Química. Máster en Tecnología y Control de Medicamentos. Profesor Titular. Departamento de Farmacia, UCLV. Villa Clara, Cuba.
VI Doctora en Ciencias Farmacéuticas. Licenciada en Ciencias Farmacéuticas. Máster en Tecnología y Control de Medicamentos. Profesora Titular. Departamento de Farmacia, UCLV. Villa Clara, Cuba
VII Técnico en Química. Departamento de Farmacia, UCLV. Villa Clara, Cuba.
VIII Licenciado en Ciencias Farmacéuticas. Máster en Tecnología y Control de Medicamentos. Profesor Auxiliar. Departamento de Farmacia, UCLV. Villa Clara, Cuba. ]]>
IX Máster en Ciencias. Profesor Titular. Departamento de Agronomía, Facultad de Ciencias Agropecuarias. UCLV, Villa Clara, Cuba.
X Técnico en Química. Departamento de Farmacia, UCLV. Villa Clara, Cuba.
INTRODUCCIÓN: Parthenium hysterophorus L. (escoba amarga) es una planta de reconocida acción antiparasitaria, carece de investigaciones analíticas y tecnológicas que permitan dar seguimiento a la estabilidad intrínseca del sólido en polvo de la planta, para la futura obtención de una forma farmacéutica de utilidad antiparasitaria científicamente fundamentada.
OBJETIVO: establecer la estabilidad integral del polvo obtenido de follaje de P. hysterophorus en condiciones reales de almacenamiento basado en partenina.
MÉTODOS: se desarrolló un estudio de la estabilidad intrínseca del sólido en polvo de P. hysterophorus frente a factores externos (humedad, temperatura y luz).
RESULTADOS: la cromatografía líquida de alta eficacia (CLAE) para la cuantificación de partenina en el sólido en polvo del P. hysterophorus es específica y puede emplearse en los estudios de estabilidad. Se demostró que la humedad y la luz son factores que influyen negativamente en la estabilidad química de la partenina.
CONCLUSIONES: la estabilidad química del sólido en polvo, conservado en frascos de vidrio ámbar cubiertos con papel de aluminio y tapón de goma, evaluada según las normativas ICH (2005), es insuficiente para su comercialización como materia prima para la elaboración de formas de dosificación. ]]>
Palabras clave: Parthenium hysterophorus, partenina, estabilidad.
INTRODUCTION: Parthenium hysterophorus (escoba amarga) is a well-known antiparasitic plant, but the lack of analytical and technological research studies does not allow following-up the intrinsic stability of the plant solid powder for obtaining a scientifically-proved pharmaceutical form with antiparasitic action.
OBJECTIVE: to ascertain the integral stability of the powder from P. hysterophorus foliage under actual storage conditions, taking the parthenin content as a basis.
METHODS: the intrinsic P. hysterophorus solid powder stability was determined against external factors such as humidity, temperature and light.
RESULTS: the high-performance liquid chromatography is a specific technique to quantify the parthenin contents in P. hysterophorus powder and may be used in the stability studies. It was proved that humidity and light had a negative impact on the chemical stability of the parthenin.
CONCLUSIONS: the chemical stability of the solid powder, preserved in amber glass flasks covered with aluminium paper and rubber cap and evaluated according to ICH standards (2005), is not adequate for this substance to be marketed as raw material for dosage form preparations.
Key words: Parthenium hysterophorus, parthenin, stability.
INTRODUCCIÓN
El uso universal de la cromatografía líquida de alta eficacia (CLAE) en el análisis de los sesquiterpenos presentes en Parthenium hysterophorus L., se expone en diversas publicaciones, se describe el empleo de columnas ODS y fase móvil de acetonitrilo: agua, al separar las lactonas de las especies de Parthenium en una columna del ultrasphere-ODS por elución con un gradiente de acetonitrilo-agua a 215 nm.1,2 Otro ejemplo de separaciones analíticas de sesquiterpenos mediante CLAE es el estudio de extractos de Solanum tuberosum L., con el empleo de columnas de µBondapaK C (10 µm) (30 cm x 4,6 mm) a una longitud de onda de 225 nm. En el caso de la separación de hidrocarburos sesquiterpenos mediante el empleo de columnas Nucleosil 5 (7 µm), LiChrosorb RP18 (10 µm) y una longitud de onda de 220 nm.3 Por otra parte, no existen técnicas analíticas ni estudios de preformulación, descritos en la bibliografía, que garanticen el control de calidad y la estabilidad del material de partida y finales a partir de la planta.
Por ello, se plantea, con vistas a su futura estandarización como ingrediente farmacéutico activo herbario, desarrollar el estudio de estabilidad química inicial del polvo de follaje de Parthenium hysterophorus L.
]]>
MÉTODOS
Obtención del material vegetal
Las partes aéreas de la planta (follaje) se colectaron de un entorno localizado (Reparto Universitario) donde predominaba un suelo con características pardo con carbonato y se identificaron en el Jardín Botánico de la Universidad Central de las Villas por el doctor Cristóbal Ríos Albuerne con número de voucher 08133.
Estudio de estabilidad inicial del estado sólido
]]>
Procedimiento: se realizó siguiendo la metodología descrita.4,5 El muestreo se hizo cada 15 d, se valoraron las características organolépticas y se realizó la determinación cuantitativa del metabolito de interés (partenina), para lo cual se utilizó cromatografía líquida de alta eficacia (CLAE) y cromatografía en capa delgada (CCD) con las condiciones cromatográficas siguientes:
- Cromatografía en capa delgada (CCD): fase estacionaria: sílica gel GF 60, dimensiones (8,1 x 4,5 cm) y 0,2 mm de espesor. Fase móvil: cloroformo:acetona (6:2). Revelador: luz ultravioleta a una longitud de onda (l) de 254 nm y posterior aspersión con disolución de vainillina 1 %.
- Cromatografía líquida de alta eficacia (CLAE): fase estacionaria: LiChrospher - 100 RP- 18, fase móvil: acetonitrilo:agua (40:60), gradiente de elución: 10 min (40:60), 15 min (100 % acetonitrilo), 20 min (40:60), flujo: 1,0 mL/min, detector: longitud de onda variable; l= 210 nm, volumen de inyección: 10 µL.3
Procedimiento experimental: se pesó 0,1 g del sólido en polvo (3 réplicas), se colocaron en frascos ámbar y protegidos de la luz, y se mantuvieron durante 3 meses en las condiciones siguientes: a) estudio de estabilidad acelerada: 40 ± 2 °C/75 ± 5 % HR, condición del envase: frasco ámbar con tapón de goma protegido de la luz.2 b) estabilidad a largo plazo: 30 ± 2 °C/65 ± 5 % HR2, envase: frasco ámbar con tapón de goma protegido de la luz. Se observó el comportamiento organoléptico de los sólidos en polvo a tiempo inicial y a los 3 meses. Se aplicó la técnica de determinación cuantitativa de partenina en los sólidos de P. hysterophorus mediante CLAE tiempo inicial y a los 3 meses.
Estudio de estabilidad. Condiciones de estrés de humedad
]]>
Procedimiento experimental: se pesaron 3 réplicas correspondientes a 0,1 g del sólido en polvo, se colocaron en frascos ámbar y protegidos de la luz, y se mantuvieron durante 3, 6 y 12 meses en la condición siguiente: ensayo de estrés de humedad 25 ± 2 °C/80 ± 5 % HR.2 Envase: frasco destapado protegido de la luz. Se aplicó la técnica de determinación cuantitativa de partenina en los sólidos en polvo de P. hysterophorus mediante CLAE, para determinar el contenido de su principal ingrediente activo, la partenina, a tiempo inicial y a los 3, 6 y 12 meses.
Técnica de cuantificación (CLAE)3
Preparación de la muestra: se pesaron con exactitud 0,5 g de material vegetal y se realizó una extracción con 40 mL de metanol, se agitó en baño ultrasónico durante 10 min. El extracto fue filtrado y lavado con 15 mL de metanol. Luego se repitió la extracción partiendo de los 0,5 g de material vegetal, se reunieron los filtrados concentrándolos a vacío en rotoevaporador y se redisolvió en 20 mL de metanol. Se tomó una alícuota de 1 mL, se disolvió en 10 mL y se enrasó con acetonitrilo:agua.
Estabilidad acelerada y de vida en estante1,2
]]>
Procedimiento experimental: se pesaron 3 réplicas correspondientes a 0,1 g del sólido en polvo, se colocaron en frascos ámbar y protegidos de la luz, se mantuvieron durante 3 meses en las condiciones siguientes:
- Estudio de estabilidad acelerada: 40 ± 2 °C/75 ± 5 % HR. Condición del envase: frasco ámbar con tapón de goma protegido de la luz (ICH, 2005).
- Estabilidad a largo plazo: 30 ± 2 °C/65 ± 5 % HR.2 Envase: frasco ámbar con tapón de goma protegido de la luz. Se observó el comportamiento organoléptico, teniendo en cuenta el olor, color, sabor y aspecto de los sólidos pulverulentos a tiempo inicial y a los 3, 6 y 12 meses. Se aplicó la técnica de determinación cuantitativa de partenina en los sólidos en polvo de P. hysterophorus mediante CLAE descrita anteriormente, para determinar el contenido de su principal ingrediente activo a tiempo inicial y a los 3, 6 y 12 meses.
RESULTADOS
Estudio de estabilidad inicial del estado sólido ]]>
La observación de las características organolépticas del polvo permitió comprobar que no sufrió alteraciones visuales, mantuvo su color y apariencia con respecto a la muestra que no fue sometida a las condiciones señaladas.
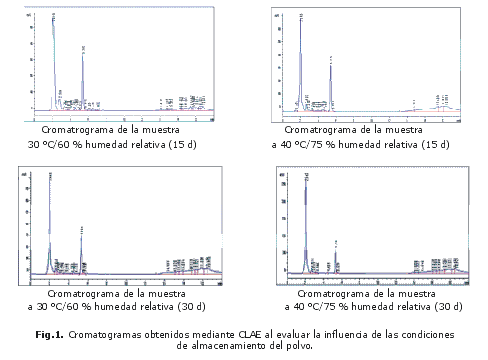
Al realizar la comparación de ambas condiciones evaluadas a los 15 d, se apreció una reducción significativa de la concentración de ingrediente activo en las muestras sometidas a 75 % de humedad relativa y 40 ºC. La concentración de ingrediente activo experimentó una marcada disminución al desarrollarse la evaluación a los 90 d de almacenamiento bajo ambas situaciones experimentales, con una mayor incidencia de la segunda variante ensayada (tabla 1) (Fig. 1).

Se apreciaron diferencias significativas entre las condiciones evaluadas (30 ºC/60 % HR y 40 ºC/75 % HR) comparadas con la concentración del ingrediente activo a tiempo cero y entre ambas variantes, lo cual demuestra la incidencia más marcada de la segunda condición en la estabilidad química del principal componente presente en el polvo de la planta, donde se emplea una temperatura de 40 ºC a una humedad relativa de 75 %. El procesamiento estadístico de los resultados mediante la prueba estadística Anova mostró los resultados siguientes: Variance Check, Cochran's C test: 0,726552 p= 0,0117475 Levene's test: 5,31078 p= 0,0135981.
Estudio de estabilidad. Condición de estrés de humedad
El sólido almacenado en frascos protegidos de la luz, sin tapa y expuestos a una temperatura de 25 °C y 80 % HR, muestra una disminución marcada en la altura del pico correspondiente a la partenina, lo que evidencia la existencia de diferencias significativas en relación con la concentración de este ingrediente activo en el material vegetal (tabla 2) (Fig. 2). ]]>
Estabilidad acelerada y vida estante
Atendiendo a la incidencia de factores como la temperatura, humedad y luz en la estabilidad química del sólido en polvo analizado en los estudios de estabilidad en fase sólida inicial, se evaluó el polvo sometido a estrés de humedad. Con el objetivo de tener criterios acerca de la estabilidad química de la partenina, se desarrolló un estudio de estabilidad acelerada y de vida de estante según se describe en las ICH (2005) a muestras conservadas en envases, las cuales controlan la incidencia de factores que aceleran su degradación (frascos de vidrio de color ámbar con tapón de goma protegidos de la luz con papel de aluminio). Durante el tiempo de estudio transcurrido en cada una de las condiciones de almacenamiento, no se observó ningún cambio significativo en el color, olor y el aspecto de los sólidos.
Al cabo de 6 meses de mantener al sólido en condiciones de envejecimiento natural y acelerada la concentración de partenina, muestra una disminución significativa en ambas condiciones, que alcanza valores de degradación que rebasan 5 % para la condición de 30 °C y 60 % de HR en vida de estante y en la condición acelerada de almacenamiento (tablas 3 y 4) (Figs. 3 y 4). Existen diferencias significativas entre las variantes analizadas en comparación con la concentración de partenina en la muestra inicial, además se evidenciaron diferencias significativas al comparar las condiciones analizadas entre sí (tabla 4).
DISCUSIÓN
]]>
La utilización de CLAE en extractos y el polvo de la planta solo ha sido descrita en la literatura especializada para el control de la calidad de P. hysterophorus,1-3 no es reflejada su aplicación en los estudios de estabilidad de extractos de la planta. Se destaca de igual forma en la literatura especializada el empleo de columnas ODS RP18 y como fases móviles la utilización de acetonitrilo: agua y metanol: agua y la detección a 215 nm.Resulta por ello de particular interés el estudio de estabilidad química preliminar del polvo de la planta, como aspecto novedoso a destacar utilizando como herramienta analítica la CLAE. Los resultados obtenidos evidencian que la humedad es un factor que afecta la estabilidad del componente principal al controlar otros factores como la temperatura y la luz, caracterizada por una degradación que supera 10 % a los 6 meses de almacenamiento. El hecho de que las lactonas sesquiterpénicas sufren reacciones de hidrólisis, podría explicar los resultados obtenidos. Es necesario destacar que la mayor degradación se observó al comparar la concentración del componente a (t0) en relación con la concentración a los 15 d, independientemente de la HR, lo cual indica que la degradación de la partenina se produce sobre todo por el contenido de humedad residual de la muestra de partida y no por la humedad relativa.
La temperatura de almacenamiento es uno de los factores que más acelera la degradación química de la partenina. Se evidencia la inestabilidad química de la partenina en el sólido de P. hysterophorus, en las condiciones de almacenamiento empleadas en este estudio y la necesidad de evaluar alternativas que incluyan la vías para disminuir el porcentaje de humedad del sólido y condiciones de almacenamiento que favorezcan la estabilización. Se recomienda utilizar un sistema envase-cierre que proteja de ambos factores para conservar al sólido pulverulento, así como a las formulaciones que lo contengan. Un aspecto a destacar es que el sistema envase cierre empleado en el estudio de estabilidad acelerada y vida estante permitió una mayor protección del sólido pulverulento de la contaminación microbiana, en relación con las condiciones de almacenamiento utilizadas en el estudio de su estabilidad intrínseca durante 3 meses. El almacenamiento del sólido pulverulento en frascos ámbar con tapón de goma, garantizó que el valor de ufc/g se mantuviera por debajo del límite permisible.
REFERENCIAS BIBLIOGRÁFICAS
1. Marchand B, Rodríguez E. Application of High-Performance Liquid chromatography of analysis and isolation of sesquiterpene lactones. J Chromatography. 1983;265:97-104.
2. Harborne JB. Preparative chromatography techniques. Application in natural product isolation. 2da. ed. Berlin-New York: Springer-Verlag; 1998. p. 244.
3. Merfort I. Review of the analytical techniques for sesquiterpenes and sesquiterpene lactones. J Chromatography. 2002;967(1):15-30.
4. ICH. Harmonised Tripartite Guideline. Guidance for industry. Stability testing of new drug substances and products, Q1A. Geneva: ICH; 2005. p. 1-13.
5. Steele G. Preformulation as an aid to product design in early drug development. En: Pharmaceutical preformulation and formulation. UK: Interpharm, Florida; 2004. p. 21-89; 175-96.
Recibido: 2 de abril de 2008.
Aprobado: 5 de marzo de 2009.
MSc. Yanelis Saucedo Hernández. Departamento Farmacia. Facultad de Química Farmacia. Universidad Central de Las Villas (UCLV). Villa Clara, Cuba. Correo electrónico: ysaucedo@uclv.edu.cu ]]>