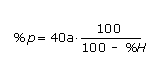
Especificidad de la cromatografía líquida de alta eficacia para evaluar estabilidad química basada en partenina del follaje seco pulverizado de Parthenium hysterophorus L. (escoba amarga)
Specificity of HPLC to assess the chemical stability based on partenine from Parthenium hysterophorus L. powdered dry foliage (escoba amarga) ]]>
Yanelis Saucedo HernándezI; Bassam Mohamad SafaII; Mirtha Mayra González BediaIII; Hilda M. González San MiguelIV; Luis Ramón Bravo SánchezV; Elisa Jorge RodríguezVI; Adalberto QuintanaVII; Ricardo Quiñones RamosVIII; Ana Hernández MonzónIX
ILicenciada en Ciencias Farmacéuticas. Máster en Química Farmacéutica. Asistente. Departamento de Farmacia. Facultad de Química Farmacia. Universidad Central de Las Villas (UCLV). Villa Clara, Cuba.
IILicenciado en Ciencias Farmacéuticas. Departamento de Farmacia. UCLV. Villa Clara, Cuba.
IIILicenciada en Ciencias Farmacéuticas. Máster en Tecnología y Control de Medicamentos. Doctora en Ciencias. Profesora Titular. Departamento de Farmacia. UCLV. Villa Clara, Cuba
IVDoctora en Ciencias. Profesora Auxiliar. Departamento de Farmacia. Instituto de Farmacia y Alimentos (IFAL). Universidad de la Habana (UH). Villa Clara, Cuba.
VLicenciado en Química. Máster en Tecnología y Control de Medicamentos. Doctor en Ciencias Químicas. Profesor Titular. Departamento de Farmacia. UCLV. Villa Clara, Cuba. ]]>
VILicenciada en Ciencias Farmacéuticas. Máster en Tecnología y Control de Medicamentos. Doctora en Ciencias Farmacéuticas. Profesora Titular. Departamento de Farmacia. UCLV. Villa Clara, Cuba.
VIITécnico en Química. Departamento de Farmacia. UCLV. Villa Clara, Cuba.
VIIILicenciado en Ciencias Farmacéuticas. Máster en Ciencias. Profesor Titular. Departamento de Agronomía, Facultad de Agropecuaria. UCLV. Villa Clara, Cuba.
IXTécnica en Farmacia. Departamento de Farmacia. UCLV. Villa Clara, Cuba.
RESUMEN
INTRODUCCIÓN: se requiere una técnica de análisis específica que permita dar seguimiento al estudio de la estabilidad intrínseca del follaje seco pulverizado de Parthenium hysterophorus L. (escoba amarga), para la obtención de una forma farmacéutica de utilidad antiparasitaria con los requisitos de calidad, seguridad y eficacia exigidos.
OBJETIVO: demostrar la especificidad de la técnica analítica de cromatografía líquida de alta eficacia para la cuantificación de partenina en el polvo de P. hysterophorus para su aplicación en estudios de estabilidad. ]]>
MÉTODOS: se aplicó cromatografía líquida de alta eficacia a muestras degradadas de P. hysterophorus, bajo condiciones degradativas en medio ácido, básico y oxidativo. Se evaluó la especificidad de la técnica de análisis para detectar el componente de interés sin interferencias de sus productos de degradación y su posible utilidad en estudios de estabilidad del polvo de la planta.
RESULTADOS: la cromatografía líquida de alta eficacia para cuantificar partenina en el polvo de P. hysterophorus resultó específica en las condiciones de trabajo establecidas y puede emplearse en estudios de estabilidad del sólido en el polvo de la planta.
CONCLUSIONES: la técnica de cromatografía líquida de alta eficacia propuesta es específica y se recomienda su utilización en los estudios de estabilidad del sólido en polvo de la planta.
Palabras clave: Parthenium hysterophorus, partenina, cromatografía líquida de alta eficacia, especificidad, estabilidad.
INTRODUCTION: it is required a specific analysis technique allowing the follow-up to stability study intrinsic of Parthenium hysterophorus L. (escoba amarga) powdered dry foliage to achieve in a pharmaceutical way a antiparasitic usefulness with the quality, safety and effectiveness demanded requirements.
OBJECTIVE: to demonstrate the specificity of analytical technique of high-performance liquid chromatography for quantization of partenine in the powder of P. hysterophorus for its application in stability studies.
METHODS: high performance liquid chromatography was applied to P. hysterophorus degraded samples under degradation conditions in an oxidative, basic and acid medium.The analysis technique specificity was assessed to detect the interest component without interferences of its degradation products and its possible usefulness in studies on solid stability in the plant powder.
RESULTS: high-performance liquid chromatography to quantify the presence of partenine in the P. hysterophorus powder was specific in established work conditions and may be used in solid stability studies of plant powder.
CONCLUSIONS: the high-performance proposed is specific and it is recommended in solid stability studies of solids in plant powder. ]]>
INTRODUCCIÓN
La cromatografía líquida de alta eficacia (CLAE) constituye una herramienta analítica de elección en la literatura internacional para la determinación cuantitativa de lactonas sesquiterpénicas, metabolitos mayoritarios en la planta.1-3 No obstante no ha sido descrita por los autores que abordan la temática, la aplicación de una técnica de análisis cuantitativo en estudios de estabilidad de extractos de Parthenium hysterophorus L. Se requiere como requisito indiscutible en la realización de los estudios de estabilidad del sólido en polvo de la planta, de una técnica analítica específica que permita detectar y cuantificar el ingrediente activo de interés (partenina) y dar seguimiento a los productos de degradación como interferencias potenciales en la matriz analizada. Demostrar la especificidad de esta técnica es el objetivo de este trabajo.4-7
]]>
MÉTODOS
Las partes aéreas de la planta (follaje) se colectaron en el Reparto Universitario de Santa Clara, donde predomina el suelo con características pardo con carbonato, y se identificó en el Jardín Botánico de la Universidad Central de Las Villas por el doctor Cristóbal Ríos Albuerne con número de voucher 08133.
Especificidad de la técnica analítica mediante cromatografía líquida de alta eficacia para la estabilidad8-10
Preparación de la disolución de referencia (150 mg/L)
]]>
Se preparó una disolución de patrón de trabajo de partenina de concentración 2,5 mg/mL. A partir de esta disolución se tomó una alícuota de 120 µL, se transfirió a un matraz aforado de 2 mL y se completó el volumen con acetonitrilo:agua (40:60) (150 mg/L).
Preparación de la disolución de la muestra sin degradar
Se pesaron 0,5 g (con error de ± 0,1 mg) del sólido en polvo de la planta y se realizó una extracción con 40 mL de metanol, se agitó en baño ultrasónico durante 10 min. El extracto se filtró y se lavó con 15 mL de metanol. Luego se repitió la extracción, se reunieron los filtrados, se concentraron a vacío en rotoevaporador y se redisolvieron en 20 mL de metanol. Se tomó una alícuota de 1 mL, se disolvió en acetonitrilo: agua (40:60) y se enrasó en 10 mL. La disolución se filtró por miliporo de 0,45 µm y se inyectó en el instrumento 20 µL de esta disolución.
]]>
Preparación de las disoluciones de las muestras degradadas
Medio oxidante, ácido y básico: Se realizó la extracción del sólido en polvo de la planta, según el procedimiento descrito con anterioridad para la preparación de la disolución de la muestra sin degradar, hasta que se reunieron los filtrados. Se adicionó el agente degradante a cada filtrado: 10 gotas de peróxido de hidrógeno (H2O2) 3 % (medio oxidante), 10 mL de HCl 1 mol/L (medio ácido) y 10 mL de NaOH 1 mol/L (medio básico) y se reflujó en los últimos 2 casos. La muestra sometida a medio oxidante se protegió de la luz y se calentó en baño de María a 50 ºC. Se determinó el contenido de partenina mediante CLAE a los 10 min Para ello, cada muestra se concentró a vacío, se redisolvió en 20 mL de metanol, se tomó 1 mL, se ajustó el pH entre 7 y 8 con disoluciones de HCl o NaOH a 0,5 mol/L, según el caso, y se enrasó a 10 mL con la fase móvil acetonitrilo:agua (40:60) en un matraz aforado.
Luz natural y artificial: se colocaron en una placa petri, de forma extendida, 0,5 g del sólido en polvo de la planta y se mantuvieron bajo el efecto de la luz solar (no directa) y de la luz artificial durante 72 h. En el caso de la luz artificial las muestras se mantuvieron a una distancia de 20 cm de una lámpara de luz UV (254 nm). En ambos casos se obtuvo la disolución de la muestra degradada, para el análisis, según la metodología de preparación de la muestra sin degradar descrita con anterioridad.
Perfiles de CLAE: las condiciones cromatográficas fueron las siguientes: FE: LiChrospher-100 RP-18, FM: acetonitrilo (A): agua (B) (40:60), gradiente de elución: 40 % A (0-10 min), 40-100 % A (10-15 min) y 100-40 % A (15-20 min), flujo: 1,0 mL/min, detector: longitud de onda (l) variable; l= 210 nm. Se inyectaron 10 µL de cada muestra, previamente filtrada por filtro miliporo de 0,45 µm, en el instrumento de CLAE. Además, las muestras se inyectaron bajo las mismas condiciones cromatográficas en un instrumento de CLAE con los detectores multiespectral y de espectrometría de masas (CLAE-EM), para demostrar la homogeneidad del pico correspondiente a la partenina. La expresión de cálculo para determinar el porcentaje de partenina en base seca en el sólido en polvo de la planta (muestra sin degradar y muestras degradadas) mediante la técnica por CLAE es la siguiente:
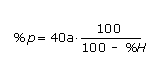
Donde:
]]>
% p: porcentaje de partenina en base seca (%).
Cromatografía en capa delgada cualitativa (CCD)
Fase estacionaria: gel de sílice 60 GF 254, dimensiones (4 x 8 cm) y 0,2 mm de espesor. Fase móvil: cloroformo: acetona (6:2). Se emplearon como reveladores la luz UV a 254 nm y el asperjado con disolución de vainillina (0,5 g de vainillina, 10 mL de etanol, 3 gotas de ácido acético y 0,5 mL de ácido sulfúrico concentrado).
Se realizó un seguimiento cualitativo mediante la CCD a las muestras sometidas a las diferentes condiciones degradativas (estrés), en comparación con el comportamiento cromatográfico de la disolución de referencia. Se aplicaron 20 mL de cada variante analizada y del patrón de referencia; se emplearon las condiciones cromatográficas descritas anteriormente. Se calculó la razón de flujo (Rf) de las manchas obtenidas en los cromatogramas en comparación con la disolución de referencia. ]]>
Espectrofotometría ultravioleta
Muestra sin degradar: se pesaron con exactitud 250 mg del sólido en polvo y se realizó una extracción con 10 mL de metanol, se agitaron en zaranda durante 10 min y se filtró. Se tomó 20 µL de la solución anterior y se enrasó a un volumen de 2 mL con metanol en matraz aforado. Se efectuó un barrido de exploración en el intervalo de 200 a 300 nm. Se realizaron las mediciones con metanol como blanco.
Muestras degradadas (medios ácido, básico, oxidante, luz UV y solar): las muestras de ensayo concentradas a sequedad se redisolvieron en metanol, se enrasaron en matraces aforados de 2 mL. Se obtuvo la absorbancia en el intervalo de 200 a 300 nm, con el empleo como blanco del metanol.
RESULTADOS
]]>
Especificidad de la técnica analítica mediante cromatografía líquida de alta eficacia para la estabilidad
Se evalúo la especificidad de la técnica analítica CLAE con vistas a su aplicación en estudios de estabilidad del polvo y se valoró la posible interferencia de productos de degradación en relación con la respuesta cromatográfica del ingrediente activo principal. Se valoró el perfil cromatográfico de cada condición analizada, al ser sometidas las muestras de ensayo a degradaciones en diferentes condiciones extremas, que propicien una degradación del ingrediente activo que no supere 20 %, según se establece.5,11,12 Para ello, se evaluaron las respuestas cromatográficas a cada condición analizada, al ser sometidas las muestras de ensayo a degradaciones en diferentes condiciones de estrés como: medio ácido (HCl 1 mol/L), medio básico (NaOH 1 mol/L), oxidación (H2O2 3 %), luz solar y ultravioleta.
El cromatograma obtenido mediante CLAE de la sustancia de referencia (Fig. 1) y de la muestra sin degradar (Fig. 2), evidencian un pico cromatográfico bien definido y resuelto a un tiempo de retención de 5,3 min, correspondiente al metabolito de interés.
Medio básico: en esta condición se obtuvo una reducción significativa de la concentración de partenina (%) en relación con la que se obtuvo en la muestra sin degradar. Además, se detectaron nuevos picos cromatográficos que pueden corresponder a posibles productos de degradación, dentro de los cuales se destaca, por su mayor área, el que aparece a tiempo de retención de 7,5 min, que sugiere la presencia de un producto de menor polaridad en relación con el metabolito activo (partenina) (tablas 1 y 2) (Fig. 3).
Medio ácido: se apreció un comportamiento similar al obtenido en medio básico, caracterizado por una reducción significativa de la concentración de partenina (%) en relación con la muestra sin degradar (tablas 1 y 2) (Fig. 4) y la aparición de nuevos picos cromatográficos. De ellos el de mayor área, que aparece a un tiempo de retención de 7,9 min, podría brindar un criterio de la presencia de un producto de degradación de menor polaridad en relación con el metabolito activo (partenina).
Medio oxidante: se apreció un comportamiento similar al obtenido en medio ácido y básico (tablas 1 y 2) (Fig. 5). Se destaca un nuevo pico cromatográfico a un tiempo de retención de 7,3 min.
Luz solar y ultravioleta (UV): en esta condición se obtuvo una reducción menos marcada de la concentración de partenina (%) en relación con la que se obtuvo en la muestra sin degradar. En el caso de la luz UV se destaca un pico en el cromatograma CLAE a un tiempo de retención de 7,71 min, lo cual sugiere la formación de un posible producto de degradación de una menor polaridad en relación con la partenina (tablas 1 y 2) (Figs. 6 y 7).
Como se observa en todas las condiciones, se obtuvo un pico estrecho correspondiente al componente principal (partenina), bien resuelto, sin colas, ni solapamientos (la ausencia de solapamientos está demostrada por la información dada por los espectros de masa y UV en cada una de las regiones del pico de partenina y con una adecuada separación de los nuevos picos tras la degradación). Los resultados espectrales se muestran en la figura 8 y confirmaron la elución del pico a un tiempo de retención de 5,3 min corresponde a una única sustancia, por causa de la aparición de un pico de m/z 280,2 aducto [M+ NH4]+ en correspondencia con la masa molar (262,3 g/mol). Por tanto, se demostró que la técnica analítica de CLAE desarrollada, es específica frente a los productos de degradación de la matriz analizada.
]]>
Cromatografía en capa delgada cualitativa (CCD)
La determinación de las razones de flujo (Rf) de cada una de las muestras analizadas, sometidas a las diferentes condiciones degradativas, en comparación con la solución de referencia, evidenció los resultados siguientes:
Medio básico: se observó la aparición de una mancha fluorescente a la luz ultravioleta a un valor de Rf de 0,67. Se evidenció la presencia a la luz ultravioleta de una segunda mancha fluorescente a un valor de Rf de 0,98, no siendo detectada al revelado con vainillina.
Medio ácido: se observó la aparición de una mancha fluorescente a la luz ultravioleta y de color carmelita al revelado con vainillina a un valor de Rf de 0,125. Se evidenció la presencia de una segunda mancha fluorescente a la luz ultravioleta y de color verde al revelado con vainillina a un valor de Rf de 0,93.
Medio oxidante: se observó la aparición de una mancha fluorescente a la luz ultravioleta y de color carmelita al revelado con vainillina, presentó un valor de Rf de 0,26. Se evidenció la presencia de una segunda mancha fluorescente a la luz ultravioleta, no siendo detectada al revelado con vainillina a un valor de Rf de 0,98.
Se evidencia atendiendo a los resultados anteriores, la presencia de posibles productos de degradación en cada medio analizado; se detectaron 2 nuevas sustancias en cada condición, en comparación con la sustancia de referencia (fluorescente a la luz ultravioleta y de coloración azul violácea al asperjado con vainillina, con un valor de Rf de 0,5).
]]>
Espectrofotometría ultravioleta directa
Muestra sin degradar
El espectro UV del polvo en metanol en el intervalo de 200 a 300 nm evidenció la presencia de un máximo de absorción a una longitud de onda de 215 nm, correspondiente a una transición (p-p*), característico de las enonas (Fig. 9).
Medio ácido y básico. Caracterización espectrofotométrica cualitativa
El espectro UV de la muestra objeto de análisis sometida a la degradación en medio ácido mostró la presencia un máximo de absorción a una longitud de onda de 206 nm (Fig. 10). ]]>
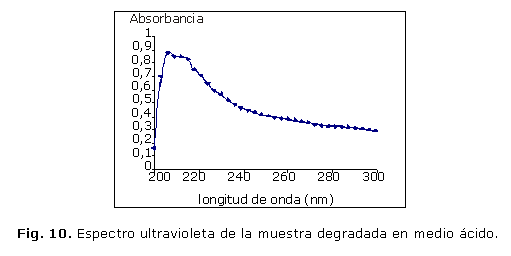
El espectro UV de la muestra sometida a la degradación en medio alcalino evidenció la presencia de un máximo alrededor de 212 nm (Fig. 11).
Medio oxidante. Caracterización espectrofotométrica cualitativa
El espectro UV de la muestra sometida a la degradación oxidativa con peróxido de hidrógeno 3 %, evidenció la presencia de un máximo de absorción a una longitud de onda de 221 nm, correspondiente a una transición (p-p*), lo cual corroboró el pico característico de las enonas entre 215 y 250 nm (Fig. 12).
]]>
DISCUSIÓN
Atendiendo a los resultados obtenidos, se evidencia la mayor incidencia de la condición degradativa en medio ácido en la concentración de partenina, seguida del medio básico y medio oxidante, con una degradación inferior a 16 %; finalmente, se muestra que la menor afectación de la concentración del ingrediente activo principal se obtiene bajo el efecto de la luz artificial y luz solar. Los espectros UV obtenidos como resultado de la evaluación de las muestras sometidas en cada medio de degradación (ácido, básico, oxidativo) mostraron máximos de absorción, característicos de la banda de transición (p-p*) de las enonas, lo cual infiere la presencia de posibles productos de degradación de estructura química similar a la partenina, además, confirma que este método analítico no es recomendable en la realización de estudios de estabilidad del sólido en polvo.
El análisis comparativo de los cromatogramas obtenidos para la sustancia de referencia, muestra sin degradar y las muestras sometidas a las condiciones de degradación drásticas, demuestra la especificidad del método analítico CLAE, al no evidenciarse interferencias, ni solapamientos respecto al pico con una elución a un tiempo de retención de 5,3 min, correspondiente al ingrediente activo principal.
REFERENCIAS BIBLIOGRÁFICAS
1. Merfort I. Review of the analytical techniques for sesquiterpenes and sesquiterpene lactones. J Chromatogr A. 2002;967(1):115-30.
2. Harborne JB. Preparative chromatography techniques. Application in natural product isolation. 2nd ed. New York: Ed. Alan R. Liss; 1998. pp. 261-302.
3. Marchand B, Rodríguez E. Application of high-performance liquid chromatography of analysis and isolation of sesquiterpene lactones. J Chromatography. 1983;265:97-104.
4. EURACHEM Guide. The Fitness for Purpose of Analytical Methods. A Laboratory Guide to Method Validation and Related Topics. Reino Unido: Guidelines 25; 1998. p. 12-20.
5. ICH. Harmonised Tripartite Guideline. Guidance for industry. Stability testing of new drug substances and products, Q1A. Geneva; 2005. p. 1-13.
6. Thompson M, Wood R. Harmonised guidelines for internal quality control in analytical chemistry laboratories. Pure Appl Chem. 1995;67:49-56.
7. Thompson M, Ellison, SL, Fajgelj Ales, Willetts P, Wood R. Harmonized guidelines for the use of recovery information in analytical measurement (Technical Report). Pure Appl Chem. 1999;71(2):337-348.
8. Dehesa M. Contribución al estudio químico farmacéutico de las hojas de la especie Tamarindus indica L. [Tesis Doctoral]. Ciudad de La Habana: Universidad de La Habana; 2005.
9. Jin P, Madieh S, Augsburger LL. The solution and solid state stability and excipient compatibility of parthenolide in feverfew. AAPS PharmSciTech; 2008.
10. Jin P, Madieh S, Augsburger LL. Selected physical and chemical properties of feverfew (Tanacetum parthenium) Extracts important for formulated product quality and performance. AAPS PharmSciTech. 2008;9(1):22-30.
11. CECMED. Validación de métodos analíticos. Regulación No. 41. La Habana. 2007.
12. Klick S, Muijselaar G, Waterval J, Eichinger T, Christian K, Thijs K, et al. Toward a generic approach for stress testing of drug substances and drug products. Pharm Technol. 2005;2(1):48-66.
Recibido: 2 de abril de 2008.
Aprobado: 30 de enero de 2010.
MSc. Yanelis Saucedo Hernández. Departamento de Farmacia. Facultad de Química Farmacia. Universidad Central de Las Villas (UCLV). Villa Clara, Cuba. Correo electrónico: ysaucedo@uclv.edu.cu ]]>