
ARTÍCULO ORIGINAL
Composición química volátil del aceite esencial de Eryngium foetidum L. colombiano y determinación de su actividad antioxidante
Volatile chemical composition of the essential oil from colombian Eryngium foetidum L. and determination of its antioxidant activity
Beatriz E. Jaramillo,I Edisson Duarte,II Irina MarteloIII ]]>
I Doctora en Química. Grupo de Investigaciones Agroquímicas, Programa de Química, Facultad de Ciencias Exactas y Naturales. Universidad de Cartagena. Campus de Zaragocilla. Cartagena, Colombia.
Introducción: el culantro (Eryngium foetidum L., Apiaceae) es una hierba nativa de América tropical y las Antillas. Es usada en diferentes recetas de comida típicas del Caribe, Latinoamérica y el lejano oriente. Estudios indican que esta planta es rica en calcio, hierro, caroteno, y riboflavina; sus hojas son utilizadas como saborizantes y condimentos de algunos alimentos. Su aplicación medicinal incluye su uso como té para la gripe, diabetes, el estreñimiento y la fiebre. Se usa comúnmente en salsas como estimulante del apetito. Especies de E. foetidum de varios países han mostrado una composición variable de su aceite esencial, sobre todo, en sus hojas.
Objetivo: establecer la composición química volátil del aceite esencial obtenido de hojas y tallos frescos de E. foetidum y evaluar su actividad antioxidante.
Métodos: el aceite esencial fue aislado usando la técnica de hidrodestilación. La composición química volátil se determinó mediante cromatografía de gases acoplada a detectores de ionización en llama (GC-FID) y espectrometría de masas (GC-MS). La actividad antioxidante fue determinada mediante el ensayo de decoloración del radical DPPH. (2,2-difenil-1-picril hidracilo).
Resultados: el aceite esencial de las hojas de E. foetidum presentó un alto porcentaje de aldehídos alifáticos (E-2-dodecenal, 5-dodeceno, tetradecanal, tetradecenal) y aromáticos (2,4,6-trimetilbenzaldehído, 3,4,5-trimetilfenol). La actividad antioxidante se expresó como porcentaje de inhibición del radical DPPH. (89,39 %).
Conclusiones: en el aceite esencial de E. foetidum colombiano predominaron compuestos aldehídos alifáticos y aromáticos. El resultado del ensayo de DPPH. mostró que el aceite esencial posee una capacidad antioxidante alta, esto lo hace una fuente importante de antioxidantes naturales.
Introduction: culantro (Eryngium foetidum L., Apiaceae) is a herb native to Tropical America and the West Indies. Although widely used in dishes throughout the Caribbean, Latin America, and the Far East. The herb is reportedly rich in calcium, iron, carotene, and riboflavin and its harvested leaves are widely used as a food flavoring and seasoning herb for meat and many other foods. Their medicinal values include its use as a tea for flu, diabetes, constipation, and fevers. One of its most popular uses is in chutneys as an appetite stimulant. Species of E. foetidum from several countries have shown a variable composition of its essential oil, particularly, in their leaves.
Objective: to establish the volatile chemical composition of the essential oil obtained from fresh leaves and stems of E. foetidum and to evaluate its antioxidant activity.
Methods: the essential oil was isolated by hydrodistillation. The volatile chemical composition was analyzed by Gas Chromatography coupled to flame ionization detector (GC-FID) and Mass Spectrometry (GC-MS). The antioxidant activity was determined using the test radical DPPH decoloration. (2,2-diphenyl-1-picryl hidrazyl).
Results: the essential oil from E. foetidum showed a high percentage of aliphatic aldehydes (E-2-dodecenal, 5-dodecene, tetradecanal, tetradecenal) and aromatic (2,3,5-trimethylbenzaldehyde, trimethylphenol). The antioxidant activity was expressed as percentage inhibition of DPPH. radical (89.39 %).
Conclusions: in the essential oil from Colombian E. foetidum predominant aliphatic aldehydes and aromatic compounds. The DPPH test showed that AE has antioxidant capacity, this makes it an important source of natural antioxidants.
Key words: Eryngium foetidum L., essential oils, Apiaceae, gas, chromatography, natural antioxidant.
INTRODUCCIÓN ]]>
Eryngium foetidum L, conocida popularmente como culantro, coriander, chicoria, culantro de coyote, culantrón, culantro de sabana, cilantrón y cimarrón, pertenece a la familia Apiaceae; es una hierba perenne, fuertemente aromática de hasta 60 cm de altura. La planta es empleada como febrífugo, emenagogo, aperitivo, antiescorbútico, antirreumático, antiséptico, antiemético, carminativo y en el tratamiento de la gripe, dolor de cabeza, hemorragias, dolor de estómago, convulsiones, diarreas, malaria, tos y espasmos.1-3Diversas investigaciones realizadas con esta hierba, indican que el extracto acuoso presenta actividad antipirética, efecto anticonvulsionante y actividad anticonceptiva en ratas y ratones,3 la decocción de las hojas, administrada por vía oral, presentó actividad antiinflamatoria en ratas, el extracto metanólico presentó actividad antioxidante in vitro y presenta actividad antihelmíntica frente a S. stercoralis.4-6
En los sistemas vivos existen múltiples reacciones de óxido-reducción indispensables para la vida, sin embargo, la oxidación puede ser también una fuente de enfermedades, cuando se pierde el equilibrio entre los oxidantes y antioxidantes, lo cual se conoce como estrés oxidativo, que puede causar daños a biomoléculas como los lípidos, las proteínas, el ADN, entre otras.7-11 El descubrimiento de ciertas sustancias antioxidantes en especies vegetales en las cuales se ignoraba su presencia, incrementaría su valor y podría convertirlos en fuentes viables para obtener estos compuestos.12-14 Entre las sustancias químicas presentes en las plantas con amplia aplicación, figuran los aceites esenciales (AEs), constituidos por una mezcla compleja de metabolitos secundarios volátiles con propiedades medicinales, como, actividad antimicrobiana, antigenotóxica y de inhibición del crecimiento celular tumoral.15-18 Los aceites esenciales son de gran utilidad en diversas ramas de la industria de las cuales se mencionan: fragancias, aromas y sabores, como biorreguladores en agroquímica, pinturas, textiles, empaques plásticos y en la farmacología, entre otras.12,19,20
Estudios realizados han señalado que muchos de los AEs tienen marcada actividad antioxidante,21-24 por lo que muchas ramas de la industria, que usan antioxidantes en sus procesos, se han interesado en ellos; pero no todos los compuestos presentes en los aceites esenciales son responsables de esta actividad, ni necesariamente son compuestos mayoritarios, por lo que se hace necesario detectar e identificar los minoritarios, aun si se encuentran en concentraciones muy bajas, la técnica analítica más usada para este fin es la cromatografía de gases acoplada a un espectrómetro de masas (GC MS).25,26
En el presente trabajo, se obtuvo el aceite esencial de la planta aromática de culantro (Eryngium foetidum L.), recolectada en el municipio de María La Baja del Departamento de Bolívar, Colombia y se estudió su composición química volátil y su actividad antioxidante.
MÉTODOS
Material vegetal
Las plantas de E. foetidum fueron recolectadas en el área rural del municipio de María la Baja, Bolívar (Colombia). Solo se usaron hojas y tallos frescos en las extracciones. La identificación taxonómica de las plantas se llevó a cabo en el Instituto de de Biología de la Facultad de Ciencias Exactas y Naturales, de la Universidad de Antioquia (Medellín-Colombia). Los pliegos testigo de cada planta quedaron depositados como muestra permanente en el Herbario Universidad de Antioquia (HUA) (No HUA 167357), clasificada por el Dr. Francisco J. Roldán Palacios. ]]>
Extracciones
La extracción del AE de culantro (Eryngium foetidum L.), se llevó a cabo empleando un equipo de destilación tipo clevenger con reservorio de destilación Dean Stark, según el procedimiento descrito por Stashenko y otros.23,25 Las hojas y tallos de E. foetidum se cortaron finamente, 500 g del material vegetal se sumergieron en agua en un balón de 3 L y se sometieron a ebullición; la duración de la hidrodestilación fue de 3 h, luego el aceite esencial se separó del agua por decantación y fue secado con Na2SO4. Una alícuota del aceite (30 µL) se diluyó en 1 mL de diclorometano para el análisis cromatográfico.23,25,26
Proceso cromatográfico.
Los aceites esenciales se analizaron en un cromatógrafo Agilent Technologies 7890ª Network GC acoplado a un detector selectivo de masas (MSD) Agilent Technologies 5975 inert GC MS system, equipado con un puerto de inyección split/splitless (230 ºC, relación de split 20:1).
Para la separación de las mezclas se utilizó una columna capilar HP 5MS de 30 m x 0,25 mm d.i. x 0,25 µm df, con fase estacionaria de 5 % fenil-poli (metilsiloxano). La temperatura inicial del horno fue de 50 ºC por 2 min y luego siguió a una rata de 5 ºC/min hasta 250 ºC y 5 min a esa temperatura, el tiempo de la corrida fue de 47 min. El gas de arrastre utilizado fue el helio, con una presión de entrada en la cabeza de la columna de 12,667 psi a una velocidad de 1,172 mL/min. Para la identificación de los compuestos se usaron algunos terpenos estándar, analizados bajo las mismas condiciones instrumentales que las muestras, espectros de masas e índices de retención de Kováts de componentes, que se compararon con los reportados en la literatura.27-29
Determinación de la actividad antioxidante in vitro.
Para determinar la capacidad antioxidante del aceite esencial de E. foetidum a través del ensayo de decoloración del radical estable DPPH• (1,1-difenil-2-picril-hidracilo) descrito por Scherer,30 fue evaluado el rango de concentraciones de DPPH• a utilizar, se realizaron ensayos preliminares utilizando como sustancia patrón el ácido ascórbico. ]]>
Se tomaron alícuotas (0,71; 0,57; 0,43; 0,28 y 0,14 mL) de una solución metanólica de DPPH. 1,37 mM a las cuales se adicionó metanol, para obtener concentraciones de 0,25; 0,20; 0,15, 0,10 y 0,05 mM, respectivamente. La reacción se realizó empleando 3,9 mL de estas soluciones de DPPH• y adicionando 0,1 mL de aceite esencial, los cuales se sometieron a un período de incubación en la oscuridad durante 90 min, luego se leyó la absorbancia a 517 nm en un espectrofotómetro UV-VIS. La actividad antioxidante se expresó como porcentaje de inhibición, la cual corresponde a la cantidad de radical DPPH• neutralizado por el aceite esencial, de acuerdo con la ecuación siguiente:30,31
Del mismo modo, se calculó el porcentaje de DPPH• remanente:
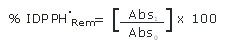
Donde: Abs0 es la absorbancia del blanco (solución metanólica de DPPH•) y Abs1 es la absorbancia de la muestra. La medida de la actividad antioxidante se realizó por triplicado.
]]>
RESULTADOSEl rendimiento de aceite esencial obtenido de las hojas frescas de E. foetidum fue de 0,2 %. En la figura 1 se muestra el perfil cromatográfico típico de los metabolitos secundarios volátiles presentes en el aceite esencial de E. foetidum.
En la tabla se muestran los compuestos mayoritarios encontrados en el AE de E. foetidum, estos fueron el 2-dodecen-1-al (43,96 %), 5-dodeceno (30,15 %), tetradecanal (5,28 %), tetradecenal (5,41 %), 3,4,5-trimetilfenol (3,08 %) y 2,4,6-trimetilbenzaldehído (2,24 %).
Si bien es cierto que existen diversos métodos para evaluar la actividad antioxidante, sea in vivo o in Vitro, el método de decoloración del radical DPPH• permite tener una idea aproximada de lo que ocurre en situaciones complejas in vivo. En la figura 2 se muestra la actividad antioxidante del ácido ascórbico (sustancia antioxidante utilizada como referencia) vs. la actividad antioxidante del aceite esencial de E. foetidum cuyo porcentaje de inhibición frente al radical DPPH• resultó de 96,4 y 80,39 %, respectivamente.
DISCUSIÓN
Se identificaron 17 componentes en concentraciones relativas superiores a 0,2 % en el aceite esencial de E. foetidum colombiano. Este se caracterizó por los altos porcentajes de aldehídos aromáticos y lineales: 2,4,6-trimetilbenzaldehído, nonanal, decanal, decenal, undecanal, dodecanal, tridecenal, tetradecenal. La comparación con los aceites de otras localidades muestran que la composición varía según el origen geográfico de la planta. Por ejemplo, el 2-dodecenal, el principal componente (43,96 %) del AE de E. foetidum colombiano, ya se ha informado como principal constituyente de los aceites procedentes de Vietnam (45,5 %),32 Malasia (59,7 %),33 Venezuela (27,5 %)34 y Perú (61,8 %).35 Pero solo como componente menor en los aceites obtenidos en Cuba36 y Taiwán.37 Mientras el 2,3,6-trimetilbenzaldehído ha sido reportado como componente mayoritario en el AE de E. foetidum obtenido en S. Tomé,6 Por el contrario, su isómero de posición, el 2,4,5trimetilbenzaldehído estuvo presente como constituyente mayoritario (20,5 %) en el aceite obtenido en Cuba.36 El aceite esencial de las hojas de E. foetidum presentó, en general, buena capacidad antioxidante, los resultados dan un soporte acorde con el uso de E. foetidum en la medicina y cocina tradicional de Colombia y de otros países latinoamericanos; esto permitirá proponerla como una fuente natural con un alto uso potencial en la industria farmacéutica y de alimentos, además porque se han encontrado reportes de que posee también propiedades antiinflamatorias.38 Si bien los metabolitos antioxidantes en plantas son estudiados principalmente sobre la base de sus estructuras polifenólicas, existe literatura en la cual se refiere que también se halla actividad antioxidante en los aceites esenciales cuyos componentes principalmente son terpenos y terpenoides.39-42 ]]>
AGRADECIMIENTOS
A la Universidad de Cartagena por la financiación de este proyecto. A Maritza Villalobos B, QF, por su valiosa colaboración en el desarrollo de esta investigación.
REFERENCIAS BIBLIOGRÁFICAS
1. Robert A, De Filipps S, Maina L, Crepin J. Medicinal Plants of the Guianas. Washington DC: Smithsonian Institution; 1994. p.384.
2. Gupta MP. Doscientas setenta plantas medicinales iberoamericanas. Bógota, Colombia: Talleres de Editorial Presencia; 1995. p. 320-1.
3. Simon OR. Singh N. Demonstration of anticonvulsant properties of an aqueous extract of Spirit Weed (Eryngium foetidum L.). West Indian Med. 1986;35(2):121-5.
4. Quignard ELJ. Screening of plants found in Amazonas state for lethality towards brine shrimp. Acta Amazónica. 2003;33(1):93-104.
5. Cavin A, Dyatmyko W, Hostettmann K. Screening of Indonesian plants for antifungal and free radical scavenging activities. Pharmaceutical Biol. 1999;37:260-8.
6. Martins AP. Essential oil composition of Eryngium foetidum from S. Tome e Principe. J Essent Oil Res. 2003;15:93-5.
7. Halliwell B. Free radicals, proteins and DNA: oxidative damage versus redox regulation. Biochemical Society Transactions. 1996;24:1023-7.
8. Halliwell B, Gutteridge JM. The definition and measurement of antioxidants in biological systems. Free Radic Biol Med. 1995;18:125-6.
9. Halliwell B, Gutteridge JM. Free Radicals in Biology and Medicine. Oxford: Clarendon Press; 1989. p. 543.
10. Perkins MJ. Radical Chemistry. New York: Ellis Horwood; 1994. p.182.
11. Ahmad S. Oxidative stress and antioxidant defenses in biology. New York: Chapman & Hall; 1995. p. 511.
12. Bandoni A. Los Recursos Vegetales Aromáticos en Latinoamérica. CYTED. La Plata (Argentina): Editorial de la Universidad de La Plata; 2000. p. 410.
13. Antonio J, Meléndez-Martínez PD, Fraser PM. Accumulation of health promoting phytochemicals in wild relatives of tomato and their contribution to in vitro antioxidant activity. Phytochemistry. 2010;71:1104-14.
14. Dini I, Tenore GC, Dini A. Antioxidant compound contents and antioxidant activity before and after cooking in sweet and bitter Chenopodium quinoa seeds. LWT Food Science and Technology. 2010;43(3):447-51.
15. Vila R, Santana AI, Pérez-Rosés R. Composition and biological activity of the essential oil from leaves of Plinia cerrocampanensis, a new source of ábisabolol. Bioresource Technology. 2010;101(7):2510-4.
16. Yang FL. Diatomaceous earth enhances the toxicity of garlic, Allium sativum, essential oil against stored-product pests. J Stored Products Research. 2010;46(2):118-23.
17. Ahmadi F, Sadeghi S, Modarresi M, Abiri R, Mikaeli A. Chemical composition, in vitro anti-microbial, antifungal and antioxidant activities of the essential oil and methanolic extract of Hymenocrater longiflorus Benth., of Iran. Food Chemical Toxicology. 2010;48(5):1137-44.
18. Bakkali F, Averbeck S, Averbeck D, Idaomar M. Biological effects of essential oilsA review. Food Chemical Toxicology. 2008;46(2):446-75.
19. Varona S, Martín A, Cocero MJ. Formulation of a natural biocide based on lavandin essential oil by emulsification using modified starches. Chemical Engineering and Processing: Process Intensification. 2009;48(6):1121-8.
20. Gamal MS. Environmentally friendly pesticides: Essential oil-based w/o/w multiple emulsions for anti-fungal formulations. Industrial Crops Products. 2010;31(1):99-106.
21.Guimarães R, Sousa MJ, Ferreira I. Contribution of essential oils and phenolics to the antioxidant properties of aromatic plants. Industrial Crops Products. 2010;32(2):152-6.
22. Puertas MA, Hillebrand S, Stashenko E, Winterhalter P. In vitro radical scavenging activity of essential oils from Columbian plants and fractions from oregano (Origanum vulgare L.) essential oil. Flavour Fragr J. 2002;17:380-4.
23.Stashenko E, Jaramillo B, Martínez J. Comparison of different extraction methods for the analysis of volatile secondary metabolites of Lippia alba (Mill.) N. E. Brown, grown in Colombia, and evaluation of its in vitro antioxidant activity. J Chromatogr A. 2004;1025:93-103.
24. Tiziana M, Damien HJ, Deans SG, Fiquereido AC, Barroso JG, Ruberto G. Antimicrobial and antioxidant properties of some commercial essential oils. Flavour Fragr J. 1998;13:235-44.
25. Stashenko EE, Jaramillo BE, Martínez JR. Analysis of volatile secondary metabolites from Colombian Xylopia aromatica (Lamarck) by different extractive and headspace methods and gas chromatography. J Chromatogr A. 2004;1025:105-13.
26. Mehdi Jalali-Heravi, Hadi Parastar, Hassan Sereshti. Towards obtaining more information from gas chromatographymass spectrometric data of essential oils: An overview of mean field independent component analysis. J Chromatogr A. 2010;1217(29):4850-61.
27. Davies NW. Gas chromatography retention indices of monoterpenos and sesquiterpenes on methyl silicone and carbowax 20M phases. J Chromatogr A. 1990;503:1-24.
28. Adams RP. Identification of essential oil components by gas chromatography/mass spectrometry. Carol Stream (Illinois): Allured Publishing Corporation; 1995. p. 469
29. Joulain D, König W. The atlas of spectral data of sesquiterpene hydrocarbons. Hamburg: E.B.-Verlag; 1998. p. 658.
30. Scherer R, Teixeira H. Antioxidant activity index (AAI) by the 2,2-diphenyl-1picrylhydrazyl method. Food Chemistry. 2008;112:654-8.
31. Molyneux, P. The use of the stable free radical diphenylpicrilhydracyl (DPPH) for estimating antioxidant activity. J Science Technol. 2004;26(2):211-9.
32. Leclercq PA. Composition of the essential oil of Eryngium foetidum L. from Vietnam. J Essential Oil Research. 1992;4:423-4.
33. Wong KC, Feng MC, Sam TW, Tan GL. Composition of the essential oil of Eryngium foetidum L. leaves and roots. J Essent Oil Res. 1994;6:369-74.
34. Cardozo E, Rubio M, Rojas LB, Usubillaga A. Composition of the essential oil from the leaves of Eryngium foetidum L. from the Venezuelan Andes. J Essent Oil Res. 2004;16(1):33-4.
35. Banout, J. Effect of solar drying on the composition of essential oil of sacha culantro (Eryngium foetidum l.) grown in the peruvian Amazon. J Food Process Engineering. 2010;33(1):83-103.
36. Pino JA, Rosado A, Fuentes V. Composition of the leaf oil of Eryngium foetidum L. from Cuba. J Essential Oil Research. 1997;9:467-8.
37. Yeh PH. Essential oils. XVI. Oil of Eryngium foetidum. J Chin Chem Soc. (Taipei) 1974;21:139-147.
38. Garcia Gimenez MD. Topical antiinflammatory activity of phytosterols isolated from Eryngium foetidum on chronic and acute inflammation models. Phitotherapy Research. 1999;13(1):78-80.
39. Chanwitheesuk A, Teerawutgulrag A, Rakariyatham N. Screening of antioxidant activity and antioxidant compounds of some edible plants of Thailand. Food Chemistry. 2005;92:491-7.
40. Sarikurkcu C, Arisoy K, Tepe B, Cakir A, Abali G, Mete E. Studies on the antioxidant activity of essential oil and different solvent extracts of Vitex agnus castus L. fruits from Turkey. Food Chem Toxicol. 2009;47(10):2479-83.
41. Foti M, Ingold KU. Mechanism of inhibition of lipid peroxidation by ã-terpinene, an unusual and potentially useful hydrocarbon antioxidant. J Agric Food Chem. 2003;51:2758-65.
42. Choi HS, Song HS, Ukeda H, Sawamura M. Radical-scavenging activities of citrus essential oils and their components: detection using 1,1-diphenyl-2picrylhydrazyl. J Agric Food Chem. 2000;48:4156-61.
]]>
Recibido: 5 de septiembre de 2010.
Aprobado: 10 de enero de 2011.
Beatriz E. Jaramillo. Programa de Química, Campus de Zaragocilla, Universidad de Cartagena. Colombia. Telefax: 57-5-6698180. Correo electrónico: beatrizjaramilloc@yahoo.com ]]>