 ]]>
]]>
ARTÍCULO DE REVISIÓN
Farmacognosia y farmacobotánica de especies pertenecientes a los géneros Esenbeckia y Raputia (Rutaceae)
Pharmacognosy and pharmacobotany of species of genera Esenbeckia and Raputia (Rutaceae)
]]>
Dr. C. Carlos Andrés Coy Barrera,I Dr. C. Luis Enrique Cuca Suárez,II Ing. Carolina Quintero LondoñoII Universidad Militar Nueva Granada. Cundinamarca, Colombia.
II Universidad Nacional de Colombia. Bogotá D.C., Colombia.
Introducción: Esenbeckia y Raputia son géneros que pertenecen a la familia Rutaceae, que tienen información etnobotánica relevante, la cual deriva en estudios fitoquímicos que demuestran la cantidad de metabolitos secundarios que producen y su variabilidad molecular, lo cual muestra la importancia de estudios posteriores a estos géneros, que están distribuidos en Centroamérica y Suramérica, con el fín de tener información importante en la búsqueda de nuevos agentes terapéuticos para combatir enfermedades del tipo microbiano y afines.
Objetivos: reunir y analizar información científica actualizada referente a los géneros Esenbeckia y Raputia como fuente natural de compuestos biológicamente activos, los cuales pueden llegar a ser utilizados en la medicina natural por su potencial farmacológico.
Métodos: se incluyeron en el análisis artículos científicos y libros relacionados con los temas de composición química, usos tradicionales y evaluaciones farmacológicas, así como otros elementos de interés en la investigación de plantas medicinales.
Resultados: la información analizada puede servir de base para el desarrollo de nuevas investigaciones que avalen el empleo en la terapéutica de productos fitoterápicos con elevada eficacia, seguridad y calidad. La revisión de los resultados en otros grupos de investigación permite establecer estrategias racionales de investigación científica, que contribuyan al uso de los recursos que se encuentran en universidades y centros de investigación y salud.
Conclusiones: los elementos encontrados en la bibliografía consultada permiten asegurar que las especies pertenecientes a los géneros Esenbeckia y Raputia, pueden ser potencialmente empleadas en usos fitoterapéuticos, debido, entre otras cosas, al importante número de metabolitos secundarios identificados que poseen actividad farmacológica demostrada. ]]>
Palabras clave: Rutaceae, Esenbeckia, Raputia, alcaloides, cumarinas, limonoides.
Introduction: Esenbeckia and Raputia are genera of the family Rutaceae about which relevant ethnobotanical information has been reported. Such data have been obtained from phytochemical studies showing the number of secondary metabolites they produce and their molecular variability. Hence the importance of later studies about these genera, which are distributed in Central and South America, with the purpose of obtaining important information useful in the search for new therapeutic agents against microbial and other related diseases.
Objectives: collect and analyze updated scientific information about the genera Esenbeckia and Raputia as natural sources of biologically active compounds which may be used in natural medicine due to their pharmacological potential.
Methods: the analysis included scientific papers and books dealing with the chemical composition, traditional uses and pharmacological evaluation of medicinal plants, as well as other topics of interest to natural medicine research.
Results: the information analyzed may be the starting point for new research demonstrating the effectiveness, safety and quality of phytotherapy. Review of the results obtained by other research teams makes it possible to establish rational scientific research strategies, thus contributing to the use of resources from universities, research centers and health institutions.
Conclusions: according to the information found in the literature consulted, species of genera Esenbeckia and Raputia may be used for phytotherapeutic purposes, due, among other reasons, to the considerable number of identified secondary metabolites with proven pharmacological activity.
Key words: Rutaceae, Esenbeckia, Raputia, alkaloids, coumarins, limonoids.
]]>
INTRODUCCIÓN
La familia Rutaceae comprende un amplio número de plantas con alto potencial químico y farmacológico. Muchas de estas especies han sido importantes por la aplicabilidad que poseen dentro de la medicina folclórica tradicional; que va desde el tratamiento de enfermedades en la piel, de tipo alérgico como la curación de ulceraciones y heridas superficiales, hasta la atención de enfermedades gastrointestinales,2 como diarrea, disentería. También se usa como febrífugo,1 estimulante, para afecciones paralíticas, diurético, analgésico,2 tónico, de antídoto contra mordedura de serpiente, hemorragias, cataratas3 y reumatismo.4 En general las especies de la familia Rutaceae se caracterizan porque de ellas se ha aislado un significativo número de metabolitos secundarios, principalmente alcaloides,5-10 cumarinas6-13 y algunos tipos de lignanos,7 que se caracterizan por poseer una lista interesante de actividades biológicas.8-10 Si a lo anterior se suma que las sociedades humanas han logrado avances científicos en diversos campos, se hace necesario incrementar las investigaciones en búsqueda de estructuras «lead» o «plantilla» para fármacos eficientes contra la inflamación, las enfermedades cardiovasculares y afecciones endocrinológicas, así como para enfermedades mucho más graves como el cáncer, que constituye más de 12 % de la mortalidad mundial de acuerdo a la Organización Mundial de la Salud, o las enfermedades infecciosas ocasionadas por patógenos bacterianos, fúngicos y virales y las enfermedades tropicales causadas por parásitos protozoarios (malaria, amibiasis, toxoplasmosis, tripanosomiasis y leishmaniosis), que afectan aproximadamente a 25 % de la población mundial.9-25
Familia Rutaceae
Descripción botánica y taxonómica
]]>
La familia Rutaceae abarca unas 1 600 especies de arbustos y árboles, raramente se encuentran plantas herbáceas, predominan en los países cálidos del antiguo y del nuevo mundo.10 Por su taxonomía se caracterizan porque tienen las hojas simples, a veces divididas en segmentos muy numerosos o compuestas, en las cuales suelen hallarse bolsitas de esencia, que vistas las hojas a contraluz, aparecen como puntos claros y semejan estar perforadas. Las flores tienen el cáliz y la corola de 4 o 5 piezas y los estambres están comúnmente en un número doble, es decir, 8 o 10, a veces en mayor número y con los filamentos soldados en grupos, como en el género de los naranjos y los limoneros. El pistilo se asienta sobre una especie de disco basal más o menos grueso y el fruto forma de 4 a 5 cavidades, o hasta 10 en los limones y naranjas; puede ser seco y abridero, como en las Rudas y Dictamos, o carnoso e indehiscente como en el género Citrus. Otra de las características de las especies de esta familia es que poseen aceites esenciales en diferentes órganos, en la corteza del tallo, en las hojas, en las flores y en los frutos.11-26 La utilidad en diferentes campos de especies de esta familia es numerosa, por ejemplo en la industria alimenticia se encuentra el género Citrus al que corresponden los cítricos como la naranja, mandarina etc., en la industria farmacológica el género Haplophyllum, rico en alcaloides, y en la industria ornamental el género Hortia que posee flores vistosas.Los estudios de clasificación taxonómica muestran que la familia Rutaceae pertenece a la clase angiosperma, a la subclase Archiclamydeae, orden Sapindales, suborden Rutales, este suborden está conformado por 5 familias: Rutaceae, Georaceae, Burseraceae, Simaroubaceae, Meliaceae.12 La familia Rutaceae consta de 6 subfamilias: Rutoidea (5 tribus y 15 subtribus), Dyctiolomatoidea, Flindersioidea, Spatheloidea, Toddaloidea, (1 tribu y 5 subtribus). Los géneros más abundantes son: Fagara, Zanthoxylum, Haplophyllum, Phebalium, Esenbeckia, Cusparia, Galipea, Diosmia, Citrus, Skinmia, Ruta, Dictamnus, Casimiroa, Amyris, Murraya y Hortia.
Origen y distribución geográfica
Las especies de esta familia se encuentran ubicadas en regiones tropicales y subtropicales, y algunas especies se encuentran más distribuidas en las zonas templadas del planeta.27 La familia Rutaceae es la más ampliamente distribuida en Colombia, sobre todo en la cordillera central.13 Se han identificado 19 géneros (tabla 1), cuyos ejemplares se encuentran clasificados en los diferentes herbarios del país.
Géneros de la familia Rutaceae encontrados en Colombia:
1. Amyris.
2. Angostura. ]]>
3. Casimiroa.
4. Citrus.
5. Coleonema.
6. Cusparia.
7. Erythrochiton.
8. Esenbeckia.
9. Galipea.
10. Hortia.
11. Monnieria.
12. Murraya. ]]>
13. Peltostigma.
14. Pilocarpus.
15. Pitavia.
16. Raputia.
17. Ruta.
18. Ticorea.
19. Zanthoxylum.
]]>
Fitoquímica y farmacología
En la familia Rutaceae se ha encontrado gran variedad de metabolitos, entre los cuales, vale la pena mencionar: alcaloides,14 cumarinas,15,16 cromanos, flavonoides,17,18 lignanos, limonoides, terpenos, aceites esenciales,19-35 y otros metabolitos de menor importancia para la familia, debido a los escasos reportes que se tienen estos, como son ácido benzoico y sus derivados, cinámico, etc., y arilcetonas.20-22,27
Género Esenbeckia
]]>
Descripción morfológica del género Esenbeckia
Comprende principalmente árboles, plantas leñosas, arbustos y en muy pocas ocasiones hierbas. Sus especies tienen, hojas esparcidas u opuestas, simples o compuestas, glabras y con puntos translúcidos, porque poseen glándulas oleíferas. Las flores son actinomorfas, de cáliz y corola tetrámeros o pentámeros, tienen 4 estambres o más; a menudo sus filamentos son ensanchados en la base, poseen tálamo desarrollado, generalmente en forma de discos entre los estambres o por encima de estos.
Distribución
Esenbeckia es un género al cual pertenecen unas 30 especies ubicadas principalmente en América, desde el sur de los EE. UU., el sur de México hasta Chile, Argentina y Brasil; los principales centros de diversidad son el sudeste de Brasil y una parte del sur de México, esta especie predomina en la región tropical.23,24 En Colombia, la especie Esenbeckia alata se encuentra en los departamentos del Valle y Sucre, Esenbeckia amazonia koastra en Boyacá, Esenbeckia panamensis en el Chocó, Esenbeckia litoralis en Bolivar y Esenbeckia pentaphylla en el Magdalena. En el mundo, especies como Esenbeckia yaxhoob y Esenbeckia leiocarpa, poseen una interesante etnobotánica y son comúnmente utilizadas para curación de dolencias estomacales, para intoxicaciones y en algunos casos como antibacteriano.25-41
Fitoquímica y farmacología
]]>
Los principales tipos de metabolitos aislados del género Esenbeckia son los alcaloides quinolínicos, quinolónicos, acridónicos, cumarinas lineales, furocumarinas, terpenos, floroglucinoles, chalconas y en menor proporción se encuentran derivados del ácido cinámico y lignanos; a continuación se muestran los metabolitos aislados de este género de acuerdo a la revisión bibliográfica.
Triterpenos y terpenos
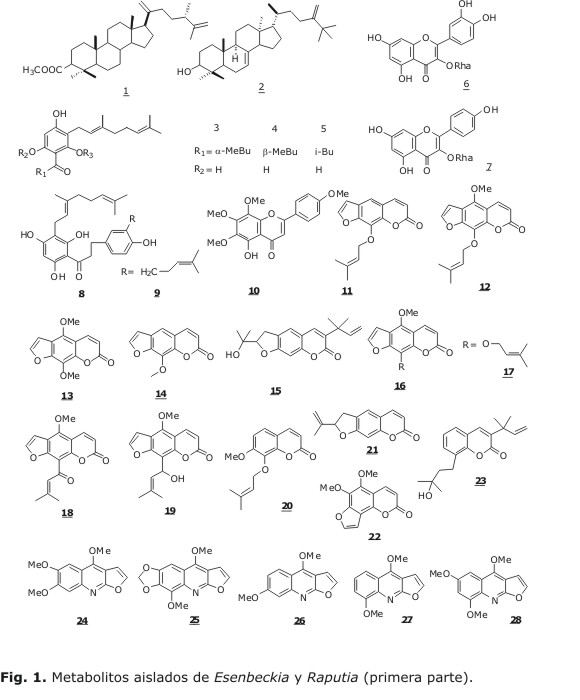
Aunque uno de los triterpenos más comunes aislados en estudios fitoquímicos de especies del género Esenbeckia es el lupeol,26 de las hojas de E. yaxhoob se aisló acetato de (24S)-24-metildammarano-20,25-dien-3-b-ilo, 1 del extracto de hojas de la especie E. stephani, se aisló el triterpeno llamado 24-metilen-25-metiltirucal- (8)-en-3-ol, de nombre común wallenol. 227 Se ha estudiado el aceite esencial de las hojas de E. almawillia, el cual contiene monoterpenos como a-pineno, mirceno, phellandreno, safrol, -humuleno, nerolidol, entre otros.28
Acilfloroglucinoles
De estudios realizados al extracto en acetona a la especie E. nesiótica, se obtuvieron mezclas de floroglucinoles (3, 4, 5), los cuales presentaron una moderada actividad citotóxica frente al ensayo de Artemia salina.29
]]>
Flavonoides
Se han aislado de las hojas de E. grandiflora dos flavonoles glicosidados, quercetina-3-O-rhamnósido 6, kaempferol-3-O-rhamnósido 7, dos dihidrochalconas, 2',4',6',4-tetrahidroxi-3'-geranil-3-prenil-dihidrochalcona 8, 2',4',6',4-tetrahidroxi-3'-geranil-dihidrochalcona 9,30 del extracto etanólico de la madera, en un trabajo del año 2001 realizado a la especie E. litoralis, y otro realizado a E. almawillia en 2007, se obtuvo la flavona denominada gardenina B 10.31,48
Cumarinas
En la familia Rutaceae las cumarinas han sido uno de los metabolitos más representativos en casi todas sus especies. Estudios realizados al género esenbeckia han demostrado una marcada producción de diferentes tipos de núcleos de cumarina con patrones de oxigenación distintos, lo cual resulta interesante, debido a sus propiedades y actividad biológica.32
Las furocumarinas han sido catalogadas como marcadores taxonómicos del género Esenbeckia, porque han sido encontradas en varias de sus especies.33
Furanocumarinas lineales ]]>
En el estudio fitoquímico del extracto etanólico de un árbol conocido como "Takans-ché" (E. Yaxhoob), muy utilizado en la medicina tradicional en México, se aisló la furanocumarina lineal llamada imperatorina 11, con alta actividad citotóxica, en las raíces de la especie E. grandiflora, se han podido aislar, swietenocumarina B 12, Isopimpinelina 13, xantotoxina 14, con una importante actividad larvicida contra Aedes aegypti, un mosquito muy común en Suramérica y occidente de África, el cual se caracteriza por ser uno de los vectores del dengue hemorrágico.34
En 1995, se obtuvo de la corteza de la especie E. almawillia la chalepina 15, antes aislada de otras especies de la familia Rutaceae.42 De los frutos de E. berlandieri se aisló bergapteno 16, muy utilizado en la industria farmacéutica para el tratamiento del vitíligo, enfermedad en la piel que causa despigmentación por el déficit de producción de melanina, responsable de la coloración normal. En el extracto etanólico de la madera de E. litoralis y en las hojas de E. ovata, hay reportes de phellopterina 17.43,35
Del extracto de raíces y hojas de E. grandiflora, se aisló 5-senecioil-xantotoxina 18.50 Por otro lado, un estudio realizado a la misma especie en 2005, permitió aislar una nueva cumarina con actividad larvicida llamada, 5(-1'-hidroxi-isopentenil)-bergapteno 19, de esta misma especie se aisló la cumarina simple con actividad citotóxica llamada daphnetin-7-metil-8(-3-3-dimetilalil-eter) 20.54
En un estudio anterior realizado a la especie E. alata en nuestro grupo, se aisló la leptophyllidina 21, la cual posee una moderada actividad antimicrobiana.36
Furanocumarinas angulares
Es muy común el aislamiento e identificación de furanocumarinas angulares, como es el caso de la especie E. grandiflora, donde se ha encontrado pimpinelina 22, con actividad larvicida.54 Investigaciones hechas a las especies E. almawillia y E. grandiflora han demostrado la presencia de 3(-1'-1'-dimetilalil)-columbianetina 23.54
]]>
Alcaloides
Al igual que las cumarinas, los alcaloides son muy comunes en este género. Existen reportes principalmente de tres tipos de alcaloides como son: quinolínicos, entre los que se encuentran los furoquinolínicos, alcaloides acridónicos y quinolónicos (especialmente los 2-alquil-quinolónicos). Estos metabolitos en la actualidad son considerados también marcadores quimiotaxonómicos del género Esenbeckia.42
Alcaloides furanoquinolínicos
Se han realizado investigaciones fitoquímicas a los extractos obtenidos de las hojas de E. belizencis y se han encontrado alcaloides furoquinolínicos con actividad citotóxica, kokusaginina 24 y flindersiamina 25.37 De E. pentaphylla, E. litoralis y E. flava, se ha aislado evolitrina 26,55 en las hojas de E. pentaphylla y E. grandiflora se obtuvo g- fagarina 27.50,38 En 2002, estudios hechos en México para la especie E. conspecta, dieron como resultado el aislamiento de maculosidina 28 y dictamnina 29.53 De la especie E. litoralis, se ha aislado skinmianina 30.39
Alcaloides quinolónicos
]]>
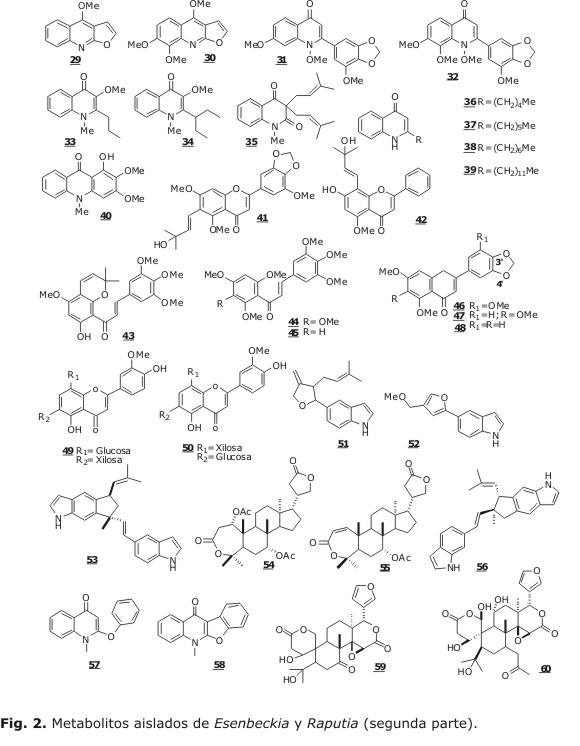
Estudios a E. almawillia y E. grandiflora en 1995 condujeron al aislamiento e identificación de dos alcaloides tipo 2-alquil-quinolin-4-ona, 7-metoxi-(3´-metoxi-4´,5´-metilenodioxifenil)-1-metil-quinolin -4-ona 31 y 7,8-dimetoxi-2(-3'-metoxi-4´,5´-metilenodioxifenil)-1-metilquinolin-4-ona 32.42Del extracto clorofórmico de las hojas de E. leiocarpa, fueron aislados dos alcaloides quinolónicos con actividad antialimentaria contra Pectinophora gossypiella, 3-metoxi-1-metil-2-propil-4-quinolona, leiokinina A 33 y 2(-1'-etilpropil)-1-metil-4-quinolona, leiokinina B 34. Estos alcaloides fueron sintetizados, con el fín de confirmar sus estructuras.40
Del extracto de hojas del género E. almawillia, muy utilizado en Brasil para el tratamiento de enfermedades gastrointestinales y cuyo nombre común es "laranjinha-branca", se aisló el alcaloide 3,3-diisopentenil-N-metil-2,4-quinoldiona 35.35
Otras investigaciones realizadas a la especie E. almawillia, revelan la presencia de metabolitos con actividad citotóxica y fungicida. De allí se aislaron: 8-metoxi-1-metil-2-pentil-4-quinolona 36, 8-metoxi-1-metil-2-hexill-4-quinolona 37 y 8-metoxi-1-metil-2-heptil-4-quinolona 38. De la especie E. leiocarpa se aisló el alcaloide quinolónico con la cadena lateral más larga, llamado 1,4-dihidro-5-metoxi-1-metil-2-tridecilquinolin-4-ona 39.41
Alcaloides acridónicos
Aunque no hay muchos reportes acerca de la presencia de este tipo de alcaloides, se ha encontrado en E. litoralis un alcaloide denominado arborinina 40.55 Para observar todas las estructuras ver figuras 1 y 2.
Usos en la medicina folclórica tradicional del género Esenbeckia
Existen algunos reportes de los usos del género Esenbeckia en la medicina tradicional, principalmente México y Brasil, aunque estos varían según el lugar de origen resulta importante resaltar el uso de estas especies para enfermedades gastrointestinales, dolores de muela y dolor de cabeza (tabla 1).
Actividad biológica de algunos metabolitos aislados del género Esenbeckia
Algunos compuestos aislados de este género presentan reportes de actividad citotóxica y antibacteriana, como es el caso de algunos alcaloides aislados de tipo furoquinolínico; además, algunos alcaloides quinolónicos presentan actividad antialimentaria (tabla 2).42,43 ]]>
Género Raputia
Morfología del género Raputia
Este género comprende árboles que miden entre 6 y 14 m de altura, su corteza es lisa y de un color amarillo claro, tiene hojas compuestas y alternas, las flores son actinomorfas, por lo general, presenta inflorescencias y el fruto es esquizocárpico, generalmente se encuentra en zonas húmedas sobre todo entre 900 y 2 600 m sobre el nivel del mar.44
En algunas especies, las inflorescencias son bastante elongadas (en R. amazonica, 84 cm), mientras que en R. brevipedunculata y R. hirsuta, estas miden 1,2 cm, la corola es simpétala, zigomórfica e imbricada, los filamentos de los estambres son fértiles, las anteras son asimétricas y adyacentes, los frutos son mericárpicos, glabros y redondos.45 ]]>
Distribución y origen del género Raputia
El género Raputia está distribuido principálmente en Costa Rica, Brasil, Colombia, Perú y Ecuador.46 En Colombia se ha encontrado en dos departamentos, Cundinamarca y Valle del Cauca. El género Raputia posee 22 especies que son; R. alba, R. amazonica, R. aromatica, R. brevipedunculata, R. conchocarpus, R. heptaphylla, R. heterophylla, R. hirsuta, R. larensis, R. magnifica, R. maroana, R. megalantha, R. neblinensis, R. ossana, R. paraensis, R. praetermissa, R. sigmatanthus, R. simulans, R. subsigmoidea, R. szczerbanii, R. trifoliata, R. ulei.
Fitoquímica y farmacología
El género Raputia fue determinado en 1775 por Aublet, quien se basó en las características morfológicas de R. aromatica Aubl.45 Sin embargo, en un estudio posterior, Emmerich, en 1975 observó diferencias morfológicas entre las especies que hasta entonces constituían el género en cuestión. Esta investigación tuvo en cuenta como patrón de comparación una especie de R. aromatica Aubl., el estudio de las flores de las especies se adoptó como carácter morfológico fundamental para la organización del «complejo Raputia», esto condujo a una nueva clasificación de las especies de dicho complejo, reunidas en 4 nuevos géneros: Raputia, Neoraputia, Raputiarana y Stigmathantus.47 Las investigaciones fitoquímicas realizadas al género Neoraputia (este último género según Emmerich pertenece a la tribu Cuspariae, tribu a la que el género Raputia también pertenece),65 revelan la presencia de metabolitos tipo flavona, con sustituyentes prenilados como 5,7,5'-trimetoxi-6-(30-hidroxi,30-metil-trans-but-10-enil)-3', 4'-metilenodioxi-flavona 41 y trans-tefrostaquina 42 los cuales se caracterizan por estar polimetoxilados.48
Se han realizado diversos estudios a especies del género Neoraputia. Para el caso del extracto hexánico de la corteza de Neoraputia magnifica se aislaron flavonoides polimetoxilados49 de tipo chalcona, como son; 2'-hidroxi-3,4,4',5-tetrametoxi-5',6'-(2",2"-dimetilpirano)chalcona 43, 5,7,3',4',5'-pentametoxiflavanona 44 y 5,6,7,3',4',5'-hexametoxiflavona 45. Del fruto de Neoraputia magnifica se han aislado flavonoides polioxigenados con actividad promisoria frente a Tripanosoma cruzi,50 causante de la enfermedad de Chagas, como son: 3',4'-Metilenodioxi-5',5,6,7-tetrametoxiflavona 46, 3',4'-metilenodioxi-5,6,7-trimetoxiflavona 47 y 3',4'-metilenodioxi-5,7-dimetoxiflavona 48; en este caso se observaron sustituyentes metilenodioxi en posición 3', 4'. No obstante, es claro que se necesitan más investigaciones fitoquímicas detalladas del género Neoraputia para una mejor comprensión de su clasificación taxonómica en la familia Rutaceae; hasta el momento se puede decir que este tipo de núcleos es característico para este género. Para el caso del género Raputia existen algunos reportes, uno de ellos fue realizado en 1991, en el cual se aislaron dos flavonoides glicosidados de la corteza del tallo de R. paraensis: 6-C-b-D-glucosil-8-C-b-D-xilosilcrisoeriol 48 y 6-C-b-D-xilosil-8-C-b-D-glucosilcrisoeriol 49.51 En Brasil, un estudio efectuado a una especie del género Raputia en 2004, reveló la presencia de alcaloides indólicos como el 5-[(3'-dimetilalil-4'-metilideno)-2'-tetrahidrofur-2'-il]-indol 51, 5-[(4'-metoxi-metil)-2'-furil]-indol 52 y 5',6'-[5-metil-5(7-indol-5''-il-eteno-6,7-diil)-3(metilprop-2-en-2-il)]-ciclopentano -5',6'-diil-indol 53,52 los cuales han sido aislados en otros géneros de la misma familia (Merrilia y Citrus); además, se aislaron también limonoides con la particularidad de tener el esqueleto A y D modificados, lo cual es común en la familia Rutaceae como son kiadalactona 54 y 1-deacetoxi-1,2-dehidrokiadalactona 55.52 En la figura 2 se pueden observar todas las estructuras. En 2010, en estudios realizados a la especie R. simulans en Grecia,53 se lograron aislar compuestos del tipo alcaloide bisindólico denominados raputindoles, un ejemplo es el caso del rapuntindol A 56, este tipo de metabolitos se caracteriza porque posee un anillo ciclopentilo unido a un anillo bencénico, el cual forma parte de un anillo indólico prenilado, además son compuestos que no han sido reportados previamente y que no se han aislado en otras especies. Esto puede llegar a ser importante para utilizar la quimiotaxonomía como herramienta en la clasificación de las especies pertenecientes al género raputia. En 2011 se aislaron también los alcaloides heptaphyllona A 57 y heptaphyllona B 58 , los cuales resultaron ser alcaloides quinolónicos con estructura novedosa y los seco-limonoides Ichangina 59 y raputiólido 60 aislados de la especie R. heptaphylla.54 especie recolectada en Colombia; resulta importante que el limonoide 60, ha mostrado actividad leishmanicida promisoria frente a L. (V) panamensis, agente parasitario causante de leishmaniosis cutánea en zonas tropicales del país.
]]>
CONCLUSIONES
Los géneros Esenbeckia y Raputia, producen un número importante de compuestos con una gran variabilidad molecular, y un amplio rango de actividades biológicas; muchos de ellos con actividad antimicrobiana establecida y soportada por información documentada obtenida por varias investigaciones del tipo fitoquímico y farmacológico, lo cual convierte estos dos géneros en potenciales fuentes de compuestos importantes en la búsqueda de nuevos fármacos de interés terapéutico.
Por otra parte, para el caso del género esenbeckia, los metabolitos secundarios con más alto porcentaje de producción son las cumarinas y los alcaloides, lo que resulta común para muchos de los géneros de la familia Rutaceae al cual pertenece, además, estos compuestos se consideran marcadores quimiotaxonómicos.
En Raputia los metabolitos secundarios más comunes son los alcaloides y los limonoides siendo los alcaloides de tipo indólico y furanoquinolínico los más representativos, en el caso de los limonoides esos son del tipo seco-limonoide, los cuales se encuentran distribuidos principalmente en las familias Rutaceae y Meliaceae.
Por lo anterior, los estudios fitoquímicos y farmacológicos encaminados en la búsqueda de nuevas fuentes de metabolitos con acciones terapéuticas frente a microorganismos, deben estar centrados en especies que posean una amplia variabilidad molecular en cuanto a metabolitos secundarios se refiere, por tal motivo, Esenbeckia y Raputia, dos de los géneros que aún no poseen muchos estudios en el campo de productos naturales se convierten en una importante fuente. este trabajo en un aporte investigativo importante para estudios posteriores en el campo de la medicina y los compuestos bioactivos.
]]>
REFERENCIAS BIBLIOGRÁFICAS
1. Heneka B, Rimpler H, Ankli A, Sticher O, Gibbons S, Heinrich M. A furanocoumarin and polymethoxylated flavonoids from the Yucatec Mayan plant Casimiroa tetrameria; Phytochemistry. 2005;66(6):649-52.
2. Anaya AL, Macias-Rubalcava M, Cruz-Ortega R, Garcia-Santana C, Sanchez-Monterrubio PN, Hernandez-Bautista BE, et al. Allelochemicals from Stauranthus perforatus, a Rutaceous tree of the yucatan península. Phytochemistry. 2005;66(4):487-94.
3. Rana VS, Juyal JP, Blazquez MA. Chemical constituents of the volatile oil of Murraya koenigii leaves. Int J Aromather. 2004;14(1):23-5.
4. Wang S, Ju X, Chen X, De Hu Z. Separation and determination of coumarins in the root bark of tree citrus plants by micellar electrokinetic capillary chromatrography. Planta Med. 2003;69(5):483-6. ]]>
5. Kuzovkina I, Al´terman I, Schneider B. Specific accumulation and revised structures of acridone alkaloid glucosides in the tips of transformed roots of Ruta graveolens. Phytochemistry. 2004;65(8):1095-100.
6. Chlouchi A, Muyard F, Girard C, Girard C, Waterman P, Bévalot F. Coumarins from the twigs of Diplolaena mollis P.G Wilson (Rutaceae). Biochem Syst Ecol. 2005;33(9):967-9.
7. Gozler B, Rentsch D, Gozler T, Unver N, Hesse M. Lignans, alkaloids and coumarins from Haplophyllum volcanicum. Phytochemistry. 1996;42(3):695-9.
8. Adams M, Ettl S, Kunert O, Wube AA, Haslinger E, Bucar F, et al. Antimycobacterial activity of geranylated furocoumarins from Tetradium danielii. Planta Med. 2006;72(12):1132-5.
9. Newman J, Cragg G, Snader K. Natural products as sources of new drugs over the period 1981-2002. J Nat Prod. 2003;66(7):1022-37. ]]>
10. Pio Font Quer. Plantas Medicinales, El Dioscórides Renovado. Barcelona: Ediciones Península; 2001. p. 20-35.
11. Patiño O. Estudio fitoquímico parcial de Zanthoxylum quinduensis (Rutaceae) [Tesis de Grado]. Bogotá: Departamento de Química, Universidad Nacional de Colombia; 2004.
12. Waterman PG, Grundon MF. Chemistry and chemical taxonomy of the rutales. En: Structural diversity and distribution of alkaloids in the Rutales. London: Academic Press; 1983. p. 10-28.
13. Base de Datos SPICA. Herbario Nacional de Colombia. Santa Fe de Bogotá: Instituto Nacional de Ciencias Naturales, Universidad Nacional de Colombia; 2008. [citado Feb 2013]. Disponible en: http://www. unal.edu.co/ICN
14. Mester I. The occurrence of the alkaloids in Rutaceae. Fitoterapia. 1973;44(2):123-52.
15. Wang S, Ju X, Chen X, De Hu Z. Separation and determination of coumarins in the root bark of tree citrus plants by micellar electrokinetic capillary chromatrography. Planta Med. 2003;69(5):483-6.
16. Murray R, Mendez J, Brown S. The natural coumarins, occurrence, chemistry and biochemistry. USA: John Wiley & Sons Ltd; 1982. p. 52-99.
17. Kuo PC, Hsu MY, Damu AG, Su CR, Li CY, Sun HD, et al. Flavonoids and coumarins from leaves of Phellodendron chinense. Planta Med. 2004;70(2):183-5.
18. Sohrab M, Chowdhury R, Hasan Ch, Rashid M. Chemotaxonomic significance of polyoxygenated flavonoids from the leaves of Micromelum minutun. Biochem Syst Ecol. 2004;32(9):829-31.
19. Barros Filho BA, Nunes FM, Oliveira MCF de, Mafezoli J, Andrade M, Silveira ER, et al. Volatile constituents from Esenbeckia almawillia (Rutaceae). Biochem Syst Ecol. 2004;32(9):817-21.
20. Dewick MP. Medicinal Natural Products A Biosynthetic Approach. 2nd. ed. USA: John Wiley & Sons Ltd; 2002. p. 14-120.
21. Angulo AA. Estudio fitoquímico de Zanthoxylum setulosum (Rutaceae) [Tesis de Magíster]. Bogotá: Departamento de Química, Universidad Nacional de Colombia; 2001.
22. Fernandez Da Silva MFG, Gottlieb OR, Ehrendorfer F. Chemosystematics of the Rutaceae: suggestions for a more natural taxonomy and evolutionary interpretation of the family. Plant Syst Evol. 1988;161(3-4):97-134.
23. Guilhon G, Baeta A, Maia J, Conserva L. 2-alkil-4-quinolone alkaloids and cinnamic acid derivatives from Esenbeckia almawillia. Phytochemistry. 1994;37(4):1193-5.
24. Oliveira P, Santana A, Conserva L, Maia J, Guilhon G. Alkaloids and coumarins from Esenbeckia species. Phytochemistry. 1996;41(2):647-99.
25. Torres OL. Estudio fitoquímico y de actividad biológica de los extractos etanólicos de hojas, corteza y madera de Esenbeckia litoralis (Rutaceae) [Tesis de Magíster]. Bogota: Departamento de Química, Universidad Nacional de Colombia; 2001.
26. Mata R, Macias M, Rojas I, Hensen B, Toscano R, Amaya A. Phytotoxic compounds from Esenbeckia yaxhoob. Phytochemistry. 1998;49(2):441-9.
27. Rios M, Aguilar B. Terpenes and new bishomotriterpene from Esenbeckia stephani (Rutaceae). Biochem Syst Ecol. 2002;30(10):1006-8.
28. Barros-Filho BA, Nunes FM, de Oliveira MCF, Andrade M, de Mattos MC. Metabólitos secundários de Esenbeckia almawillia Kaastra (Rutaceae). Quim Nova 2007;30(7):1589-91.
29. Rios M, Delgado G. Polyprenols and acylphloroglucinols from Esenbeckia nesiotica. Phytochemistry. 1992;31(10):3491-4.
30. Trani M, Carbonetti A, Delle Monache G, Delle Monache F. Dihydrochalcones and coumarins of Esenbeckia grandiflora subsp. Brevipetiolata. Fitoterapia. 2004;75(1):99-102.
31. Torres OL. Estudio fitoquímico y de actividad biológica de los extractos etanólicos de hojas, corteza y madera de Esenbeckia litoralis (Rutaceae) [Tesis de Magíster]. Bogotá: Departamento de Química, Universidad Nacional de Colombia; 2001.
32. Kostova I. Synthetic and natural coumarins as cytotoxic agents. Curr Med Chem. 2005;5(1):29-46.
33. Rios M, Delgado G. Furocoumarins, terpenes, and sterols from Esenbeckia kunth (Rutaceae); Biochem Syst Ecol. 2002;30(7):697-9.
34. Oliveira P, Conserva L, Brito A, Lemos R. Coumarin derivatives from Esenbeckia grandiflora and its larvicidal activity against Aedes aegypti. Pharm Biol. 2005;43(1):53-7.
35. Rios M, Aguilar-Guadarrama B. Furoquinoline alkaloids, furocoumarins and terpenes from Esenbeckia litoralis (Rutaceae). Biochem Syst Ecol. 2002;30(10):977-9.
36. García O, Cuca LE. Constituyentes no polares de la Corteza de Esenbeckia alata y Actividad Antimicrobiana. Rev Colombiana Quím. 2003;32(1):23-8.
37. Rios M, Delgado G. Terpenoids and alkaloids from Esenbeckia belizencis spontaneous oxidation of furoquinoline alkaloids. J Nat Prod. 1992;55(9):1307-9.
38. Simpson D, Jacobs H. Alkaloids and coumarins from Esenbeckia pentaphylla (Rutaceae). Biochemical Systematics Ecology. 2005;33(8):841-4.
39. Dreyer DL. Alkaloids, limonoids and furocoumarins from three Mexican species. Phytochemistry. 1980;19(5):941-4.
40. Nakatsu T, Johns T, Kubo I. Isolation, structure and synthesis of novel 4-quinoline alkaloids from Esenbeckia leiocarpa. J Nat Prod. 1990;53(6):1508-13.
41. Delle Monache F, De Moraez M, Sandor P. Esenbeckia leiocarpa: IIa. further components. Gazz Chim Ital. 1990;120(2):387-9.
42. Aguilar-Guadarrama B, Rios M. N-dymethylallylanthranilate, a new compound from Esenbeckia yaaxhokob. Planta Med. 2003;70(14):85-6.
43. Zografos A, Christos A, Markopolous O. One Step synthesis for the preparation of quinoline alkaloids analogues. Org Lett. 1999;1(12):1953-5.
44. Puentes L. Estudio químico de algunos de los metabolitos presentes en el extracto etanólico de Raputia heptaphylla (Rutaceae) [Tesis de grado]. Bogotá: Departamento de Química, Universidad Nacional de Colombia; 2005.
45. Kallunki J. An emended description of and new combinations in Raputia (Cuspariinae, Rutaceae). Brittonia. 1990;42(3):175-7.
46. Kallunki J, Morthon C. Pollen morphology of the subtribe Cuspariinae (Rutaceae). Brittonia. 1993;45(4):286-314.
47. Kallunki J. Revision of Raputia Aubl. (Cuspariinae, Rutaceae). Brittonia. 1994;46(4):279-95.
48. de Souza J, Arruda A, Muñoz G, Arruda M, Muller A. Prenylated flavones from Neoraputia paraensis. Phytochemistry. 1999;52(8):1705-9.
49. Passador E, Fatima Das GM, Da Silva F, Rodrigues E, Fernandes J, Vieira P, et al. A Pyranochalcone and a flavanone from Neoraputia magnifica. Phytochemistry. 1996;45(7):1533-7.
50. Tomazela D, Pupo M, Passador M, da Silva M, Vieira P, Fernandes J, et al. Pyrano chalcones and a flavone from Neoraputia magnifica and their Trypanosoma cruzi glycosomal glyceraldehyde-3-phosphate dehydrogenase-inhibitory activities. Phytochemistry. 2000;55(6):643-51.
51. Bakhtiar A, Gleye J, Moulios C, Foraste I. C-Glycosyl flavones from Raputia paraensis. Phytochemistry. 1991;30(11):3840-1.
52. Vieira LV, Moura T, das GFMF, Fernandes JB, Vieira PC, Oliva G, et al. Novo alcalóide bisindol de Raputia prateermissa Emmerich (Rutaceae) e sua importancia quimiossitemática; XXIV Reuniäo anual sobre Evolucao, Sistemática e ecologia micromoleculares. Instituto de Química, Universidade Federale de Fluminense; 2004. p. 21.
53. Vougogiannopoulou K, Fokialakis N, Aligiannis N, Cantrell C, Skaltsounis A. The raputindoles: Novel cyclopentyl bisindole alkaloids from Raputia simulans. Org Lett. 2010;12(9):1908-11.
54.Coy Barrera CA, Coy Barrera ED, Granados Falla DS, Delgado Murcia G, Cuca Suarez LE. Seco-limonoids and quinoline alkaloids from Raputia heptaphylla and their antileishmanial activity. Chem Pharm Bull. 2011;59(7):855-9.
]]>
Recibido: 24 de enero de 2013.
Aprobado: 28 de junio de 2013.
Carlos Andrés Coy Barrera. Facultad de Ciencias Básicas y aplicadas. Universidad Militar Nueva Granada, Campus Universitario Rio Grande. Cundinamarca, Colombia. Correo electrónico: carlos.coy@unimilitar.edu.co ]]>