Enfoque de la Autoridad Reguladora Cubana sobre la reglamentación para la Medicina Natural y Tradicional
Approach of the Cuban regulatory authority to natural and traditional medicine regulations
DraC. Celeste Sánchez-González, MSc.Francisco Debesa-García, MSc. Raúl Yañez-Vega, Lic. Anaira López-Romo
Grupo de Políticas y Asuntos Reguladores. Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CEDMED). La Habana, Cuba.
]]>
RESUMEN
Introducción: la medicina natural y tradicional (MNT) ocupa un espacio renovado en la salud y la sociedad cubana.
Objetivos: caracterizar la reglamentación para la MNT y contribuir a su desarrollo mediante la recuperación de disposiciones nacionales que pautan los estándares para medicamentos y dispositivos médicos relacionados con la misma.
Métodos: se realizó un estudio descriptivo, transversal y retrospectivo; la base reglamentaria se recuperó mediante revisión de las publicaciones de artículos científicos entre 1989 y 2012, así como de sesiones de trabajo con funcionarios clave y entrevistas a expertos.
Resultados: el número de disposiciones compiladas ascendió a 22. El Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CECMED) se identificó entre los 6 principales reguladores en esta esfera y las instituciones reguladas fueron 5.
Conclusiones: se mostró por primera vez un panorama general de la evolución de la reglamentación sobre la MNT, sus hitos, estructuras y necesidades de desarrollo. Se evidenció que el CECMED ha dado respuesta al mandato del Consejo de Ministros sobre el control en este campo, e investiga estrategias para cumplir las direcciones trazadas para la transformación del modelo económico y social del país con la perspectiva de la garantía sanitaria de medicamentos a utilizar en las modalidades de la MNT y dispositivos médicos con calidad, seguridad, eficacia y efectividad, en favor de preservar el derecho a la salud de los cubanos.
Palabras clave: regulación, medicina natural y tradicional.
ABSTRACT
Introduction: Natural and traditional medicine (NTM) has gained space in Cuban health and society.
Objectives: characterize NTM regulations and contribute to their development by means of the retrieval of national regulations about standards for NTM drugs and medical devices.
Methods: a descriptive cross-sectional retrospective study was conducted. The regulatory bases were retrieved from a review of scientific papers published between 1989 and 2012, as well as work sessions with key officials and interviews with experts.
Results: a total 22 regulations were collected. The Center for State Control of the Quality of Drugs and Medical Equipment (CECMED) was identified as among the 6 main regulators in this field, with 5 institutions regulated.
Conclusions: for the first time a general overview was provided of the evolution of NTM regulations, their milestones, structures and development needs. It was shown that CECMED has accomplished the mandate of the Council of Ministers about regulation in this field, and that it investigates strategies aimed at fulfilling the directives received in relation to the transformation of the Cuban economic and social development model ensuring the quality, safety, efficacy and efficiency of NTM drugs and medical devices to preserve the right of Cubans to health care.
INTRODUCCIÓN
El desarrollo de la Medicina Natural y Tradicional (MNT) es una voluntad política del gobierno cubano que cuenta ya con más de tres décadas. Sus inicios se remontan a finales de la década de los años 80 y fue revitalizado en los 90 por las Fuerzas Armadas Revolucionarias (FAR). Su alcance a varios ministerios y a todo el país supera ya los 10 años.
El Lineamiento 158 de la política del Estado y del gobierno1 para el redimensionamiento del modelo económico del país promulgado en abril de 2011 en el seno del VI Congreso del Partido Comunista de Cuba, refiere: “Prestar la máxima atención al desarrollo de la medicina natural y tradicional”. Desde el año 2011 el Ministerio de Salud Pública (MINSAP) ha incluido anualmente el tema en sus objetivos de trabajo priorizados, en función de la creación e implementación del marco regulador para la MNT en el Sistema Nacional de Salud (SNS). Consecuentemente, el actual Centro para el Control de Medicamentos, Equipos y Dispositivos Médicos (CECMED), también los contempla entre sus objetivos anuales y ha desarrollado múltiples tareas al respecto.
Por la relevancia del tema, esta investigación se trazó los siguientes objetivos:
· Caracterizar y dotar de visibilidad la reglamentación vigente sobre los medicamentos y dispositivos médicos relacionados con la MNT,
· Identificar la estrategia a ser adoptada por le CECMED en su condición de Autoridad Reguladora Nacional para su desarrollo y perfeccionamiento,
· Recuperar las regulaciones y disposiciones que en el país marcan pautas y orientan los estándares para productos y procesos involucrados en la MNT,
]]> · Organizar y poner a disposición de los especialistas que laboran en esta materia la base reglamentaria recuperada,· Realizar el diagnóstico de la base, en particular, el nivel de cobertura alcanzado y sus posibilidades de mejora de acuerdo con las responsabilidades reglamentarias asignadas al CECMED y,
· Proponer estrategias que permitan su desarrollo y sirvan para diseñar el trabajo futuro en esta Autoridad Nacional Reguladora de Medicamentos.
MÉTODOS
Se realizó un estudio descriptivo, transversal y retrospectivo. La base reglamentaria se recuperó mediante revisión de las disposiciones técnicas y jurídicas publicadas en el país y disponibles en los archivos legales del MINSAP, del extinto Buró Regulatorio para la Salud y del CECMED entre 1989 y 2013, de artículos científicos de revistas nacionales y extranjeras, sesiones de trabajo con funcionarios involucrados y entrevistas a expertos.
Se seleccionaron los ejes del diagnóstico considerando:
· Las estructuras reguladoras y de los principales actores,
La información compilada fue organizada teniendo en cuenta el tipo de documento y la fecha de emisión.
Las insuficiencias y posibilidades de mejora se identificaron en análisis de grupo con técnicas de tormenta de ideas y fueron organizadas mediante matriz DAFO, a partir de la cual se propusieron estrategias para su perfeccionamiento.
RESULTADOS
Recuperación, organización y publicación de regulaciones que pautan y orientan en el país los estándares para productos y procesos involucrados en la MNT
Las bases técnicas y jurídicas con las disposiciones de respaldo para esta actividad a nivel nacional se encontraban dispersas y varias de ellas no publicadas, por lo que antes de realizar este trabajo era prácticamente imposible disponer de una imagen panorámica de las mismas. Su búsqueda y recuperación fue más compleja porque muchas publicaciones carecían de citas de las fuentes originales que respaldaran con exactitud la cronología en la regulación, siendo frecuentes las contradicciones entre las fechas de diferentes documentos.
La reglamentación básica para el país que fue compilada tanto en sus versiones digitales como impresas consta de 22 disposiciones en total, como se muestra cronológicamente en la tabla.
Sus niveles de emisión fueron como sigue: 1 por el Ministro de las FAR, 1 por el Comité Ejecutivo del Consejo de Ministros, 9 por el MINSAP, 1 por el Buró Regulatorio de Protección de la Salud (BRPS) y 10 por el CECMED. La base recuperada se instaló en la intranet del CECMED a fin de que pudiera ser consultada por todos los especialistas del Centro.
]]> Principales actores identificados:a) Reguladores.
b) Regulados.
]]> Han estado representados por la agricultura, responsable de los cultivos, siembra y recolección de la droga cruda, la apicultura a cargo de la obtención de miel y jalea real, la industria farmacéutica procesadora de las drogas crudas para la obtención de los diferentes extractos y medicamentos homeopáticos, las unidades de producción local elaboradoras de formas terminadas (en la actualidad en número aproximado de 114) y los dispensarios de las farmacias encargados de la fabricación a menor escala de un grupo específico de productos terminados, los que ascienden a 678. Otras entidades que pueden fabricar este tipo de preparaciones pertenecen al Ministerio de Educación, al de las Fuerzas Armadas y al Ministerio del Interior.Diagnóstico de la base reglamentaria específica para la MNT
El primer documento que formalizó el desarrollo de la MNT y dio origen a la evolución de la reglamentación en esta materia fue la Directiva 26/95 del segundo secretario del Comité Central del PCC y Ministro de las FAR, del 18 de enero de 1995. Esta directiva creó una Comisión Nacional encargada de la dirección y coordinación de todas las actividades relacionadas con la estrategia y desarrollo del Programa Nacional de Plantas Medicinales y otras medidas de la Medicina Tradicional, presidida por el Ministro de Salud e integrada por los Ministros de la Agricultura y el de Ciencia, Tecnología y Medio Ambiente.
El segundo documento en importancia y alcance, sustituyó a la Directiva 26/95 y fue promulgado por el Comité Ejecutivo del Consejo de Ministros el 7 de enero de 2002, como su Acuerdo 4282, para consolidar la estrategia y desarrollo de la MNT. Brindó continuidad al trabajo y tuvo idéntico enfoque que el de su predecesor.
Para la formación de capital humano existen dos (2) promulgadas por el MINSAP:
Sobre las estructuras nacionales a nivel del MINSAP se recopilaron seis (6) instrumentos jurídicos para la creación de organizaciones:
Otros documentos técnicos complementarios de la base recuperada fueron:
El Manual de Normas y Procedimientos de Farmacias Comunitarias y Hospitalarias de la Dirección de Farmacia, emitido en 2009 y vigente, se aplica en toda la red de farmacias del país. No es específico para las preparaciones de productos naturales, pero constituye un complemento a mencionar por su destacado rol en la normalización de las prácticas de elaboración.
Base reglamentaria del CECMED de MNT para los productos y procesos bajo su actual alcance.
La política farmacéutica nacional relacionada con el control estatal de la calidad de los medicamentos4 fue el primer y único documento programático del CECMED que incluyó los productos de origen natural y sus perspectivas, abordados en los “Fundamentos y los principales roles del CECMED, y en el Programa Nacional referido a la actualización y desarrollo de regulaciones, control analítico y licencias sanitarias.
El papel del CECMED en el marco del Programa Nacional de la MNT fue distinguido con perfil propio en el Decreto 4282 del Consejo de Ministros del 2002 en su acuerdo tercero, ya mencionado. En respuesta a este mandato, el CECMED creó dos estructuras en el año 2002, al establecer un departamento de productos naturales y homeopáticos para la atención de la actividad (Resolución 04/2002 del 16 de enero de 2002) y un comité de calidad de los medicamentos de origen natural para apoyar el trabajo (Resolución 21/2002 del 07 de mayo de 2002). El departamento fue disuelto en febrero del 2005, fecha en la que se convirtió en el Grupo de productos naturales y homeopáticos.
Hasta el año 2002 no existieron disposiciones específicas para el registro de los productos de origen natural. Los medicamentos industriales fueron evaluados siguiendo los requisitos generales vigentes (Resolución MINSAP No. 168/2000, Requisitos para el registro de medicamentos de uso humano, del 4 de octubre de 2000), con las adecuaciones procedentes. Con fundamento en el Acuerdo 4282, en mayo de 2002 el CECMED promulgó los requisitos específicos para registrarlos,5 y para los de fabricación local y dispensarial no susceptibles del registro, se pusieron en vigor en 2003, los requisitos para autorizar su uso.6
El CECMED emitió las buenas prácticas de fabricación de medicamentos herbarios,7 como el Anexo No. 3 de las Buenas Prácticas para la Fabricación de Productos Farmacéuticos (BPFPF) del año 2000, con vigencia ratificada en la lista de anexos que fueron actualizados en 2012.
Como documentos de apoyo fueron emitidas las directrices sobre la calidad de los medicamentos en farmacias comunitarias y hospitalarias en 2004 aprobadas mediante la Resolución No. 43-2004 del CECMED, aunque no se llegó a alcanzar completamente su implementación.
La segunda etapa reguladora del CECMED sobre los productos y procesos relacionados con la MNT data de 2011 y 2012 y a la misma corresponden las normativas de fabricación y el registro de productos homeopáticos8, 9 conforme el desarrollo de la fabricación nacional industrial de los medicamentos homeopáticos por el Instituto Finlay.
]]> El reglamento para el comité de expertos asesor del CECMED en MNT10 se aprobó en 2011, basado en uno general para la selección y manejo de especialistas, vigente desde 2008.También se implementaron por el CECMED seis (6) procedimientos para garantizar la consistencia en la evaluación de registro, para la información administrativa y de calidad de productos de origen natural y homeopático, y no clínica y clínica de homeopáticos.
Para los dispositivos médicos usados en la MNT, no existen disposiciones específicas, son generales y han sido emitidas por el antiguo Centro de Control Estatal de Equipos Médicos. Se aplican en agujas para acupuntura, catgut para implantación y equipos para estimulación sobre los puntos acupunturales con luz, ultrasonido, electroacupuntura y ozonoterapia.
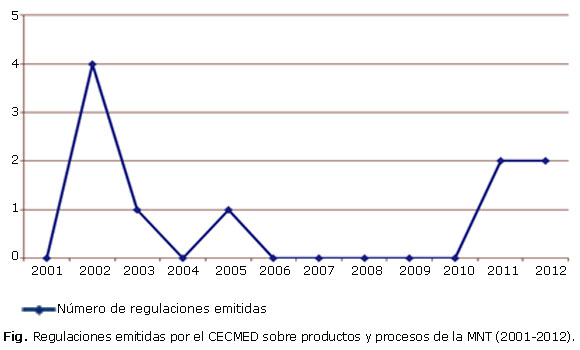
En la figura se muestra la emisión en el tiempo de estas regulaciones por el CECMED.
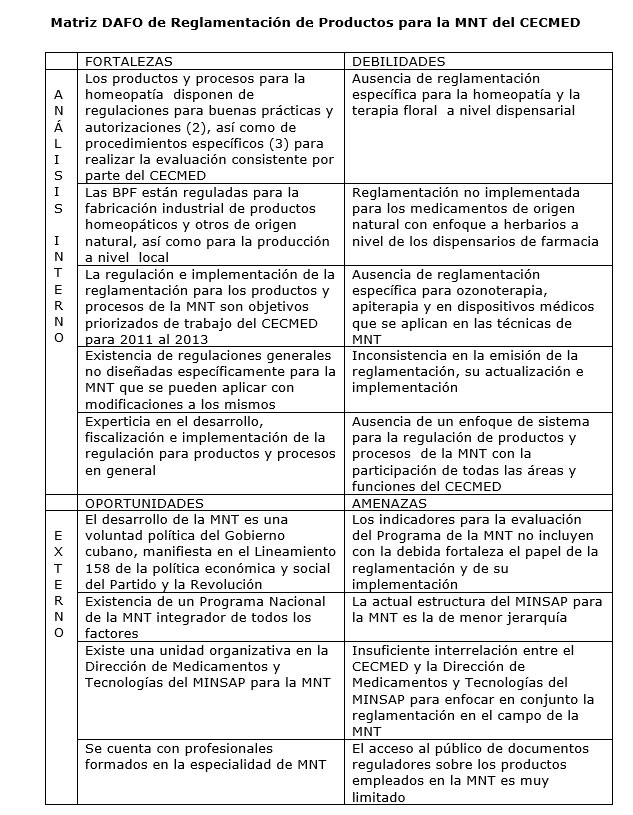
Los resultados del análisis permitieron identificar las principales fortalezas y debilidades del trabajo del CECMED con las oportunidades y amenazas externas. Puede resumirse que la caracterización realizada puso de manifiesto un conjunto de debilidades y fortalezas, oportunidades y amenazas que se presentan en la matriz DAFO del cuadro presentado más adelante, a partir de cuyo análisis fueron confeccionadas las siguientes propuestas de estrategias para el desarrollo del CECMED en la esfera de productos y procesos de la MNT:
a) Actualizar las disposiciones para medicamentos y dispositivos médicos empleados en la MNT necesarias y elaborar las que se requieran.
b) Continuar fortaleciendo la consulta de las disposiciones que elabora el CECMED sobre la MNT con los factores del PNM, universidades, los departamentos de Atención Farmacéutica y de la MNT de la Dirección de Medicamentos y Tecnologías, entre otros.
c) Desarrollar un trabajo conjunto entre el CECMED y la Dirección de Medicamentos y Tecnologías del MINSAP para fortalecer la reglamentación de medicamentos y dispositivos médicos empleados en la MNT y la evaluación de su implementación en las áreas de convergencia.
]]>
DISCUSIÓN
En la evaluación del diagnóstico resalta la diversidad de actores en materia de regulación, lo que evidencia el enfoque multidisciplinario del programa seguido en el país y constituye un rasgo positivo. Al analizar las estructuras involucradas con la MNT del MINSAP y del CECMED, a través del tiempo, se observa que las mismas han ido disminuyendo su amplitud y jerarquía. El primero ha establecido 4 estructuras para la atención a la MNT, 2 de ellas inexistentes a la fecha y el segundo estableció 3, de las cuales 1 solamente mantiene su vigencia. Esto resulta contradictorio con la prioridad actual de la MNT.
En la base recuperada, es predominante la reglamentación promulgada por el MINSAP y sus dependencias (CECMED y BRPS), lo que resulta lógico, teniendo en cuenta el papel rector conferido a este organismo por las altas esferas de dirección del país, por ambas partes, y que esta investigación está dirigida a productos de uso en humanos, correspondientes a la jurisdicción del mismo. No obstante, los motores históricos del trabajo lo constituyeron la directiva de las FAR 26/95 y el Acuerdo 4282 del Comité Ejecutivo del Consejo de Ministros. Para el CECMED, este último constituye un hito regulador, ya que en su acuerdo tercero, enunció el mandato de “encargar al CECMED… el establecimiento de las regulaciones referentes a las Buenas Prácticas de Fabricación (BPF), así como a los requerimientos para la producción local, el registro sanitario de medicamentos naturales, la autorización y control de los ensayos clínicos y todas aquellas medidas reguladoras relacionadas con los medicamentos de origen natural, debiendo hacerse énfasis en los estudios de estabilidad de los mismos”. Puede notarse que fue abundante en detalles al pautar la labor de este centro, permitiendo evaluar su cumplimiento sin ambigüedades.
En correspondencia con el Acuerdo 4282, la emisión en el tiempo de las regulaciones por el CECMED, pone de manifiesto que el período de mayor emisión corresponde al año 2002, es decir, que la respuesta reguladora de esta entidad fue inmediata publicando 4 regulaciones, dos de ellas referidas a los requisitos de autorización y uso para estos productos elaborados a nivel dispensarial y local, y otra para el registro de los fabricados a escala industrial, los que incluyen los estudios de estabilidad y los ensayos clínicos. En 2003 se elaboraron las BPF específicas y en 2011 se reglamentó la fabricación industrial de la homeopatía con buenas prácticas y requisitos de registro.
Al evaluar los campos de cobertura de la reglamentación observamos que para los productos homeopáticos, si bien el registro y las BPF cubren los productos y procesos para esta modalidad de la MNT, no se han emitido ni se han oficializado las normas para las preparaciones en los dispensarios de las farmacias, donde se emplean documentos técnicos adquiridos en los cursos de formación de estos especialistas, tal como el Manual de Normas Técnicas de Farmacias Homeopáticas del Instituto Finlay, La Habana, 1997.
Es ostensible que los fitofármacos y apifármacos son los que mayor tradición reguladora presentan, porque se han emitido regulaciones para la fabricación a escala industrial nacional, media o local y dispensarial, mientras que también cuentan con requisitos para el registro y autorización de fabricación a los dos primeros niveles. No obstante se constató que las disposiciones deben actualizarse. La composición y especificaciones para estas preparaciones en los dispensarios están normadas en el Formulario Nacional de fitofármacos y apifármacos 2013.
Las esencias florales se fabrican solamente a nivel dispensarial y se controlan como preparaciones extemporáneas según las indicaciones de la prescripción.
El ozono de la ozonoterapia es un producto complejo. Cuando se presenta con formas farmacéuticas convencionales, se aplican los requisitos vigentes, pero se requiere reglamentar la aplicación directa desde los sistemas que lo generan.
]]> La reglamentación nacional y del CECMED recuperada y organizada permite mostrar por primera vez un panorama general de la evolución de la reglamentación sobre la MNT, sus hitos, estructuras y necesidades de desarrollo.El CECMED ha dado respuesta al mandato del Consejo de Ministros para la reglamentación en este campo, lo mantiene priorizado como muestra este estudio, e investiga estrategias para cumplir las direcciones trazadas para la transformación del modelo económico y social del país bajo la perspectiva de la garantía sanitaria de medicamentos y dispositivos médicos a utilizar en las modalidades de la MNT con calidad, seguridad, eficacia y efectividad, en favor de preservar el derecho a la salud de los cubanos.
REFERENCIAS BIBLIOGRÁFICAS
1. PCC. Lineamentos de la Política Económica y Social del Partido y la Revolución. [Monografía en Internet]. [citado 20 de junio de 2013]. Disponible en: http://www.granma.cubaweb.cu/secciones/6to-congreso-pcc/Folleto%20 Lineamientos%20VI%20Cong.pdf
2. MINSAP. Guía Terapéutica y Dispensarial de Fitofármacos y Apifármacos. La Habana (Cuba); 1992.
3. MINSAP. Formulario Nacional de Fitofármacos y Apifármacos. La Habana (Cuba). Editorial de Ciencias Médicas; 2010.
4. MINSAP. Resolución 170/2000. Política Farmacéutica Nacional Relacionada con el Control Estatal de la Calidad de los Medicamentos y Diagnosticadores. [Monografía en Internet]. [citado 20 de agosto de 2013]. Disponible en: http://www.cecmed.cu/ Docs/RegFarm/DRA/DispGen/Res/Res_MINSAP-170-00.pdf
5. CECMED. Resolución 28-2002. Requisitos para las solicitudes de Inscripción, Renovación y Modificación de Medicamentos de Origen Natural de Uso Humano. [Monografía en Internet].[citado 20 de junio de 2013]. Disponible en: http://www.cecmed.cu/ Docs/RegFarm/DRA/LicProd/2001-2002/Res/Res_CECMED-28-02.pdf
6. CECMED. Resolución 29-2002. Requisitos para las solicitudes de Autorización de Uso de Medicamentos de Origen Natural de Uso Humano de producciones locales y dispensariales. [Monografía en Internet].[citado 20 de junio de 2013]. Disponible en: http://www.cecmed.cu/Docs/RegFarm/DRA/LicProd/2001-2002/Res/Res_CECMED-29-02.pdf
7. CECMED. Resolución 58-2003. Buenas Prácticas de Fabricación de Medicamentos Herbarios. [Monografía en Internet]. [citado 20 de junio de 2013]. Disponible en: http://www.cecmed.cu/Docs/RegFarm/DRA/BPPF/ 2003-2008/Res/Res_CECMED-58-03.pdf
8. CECMED. Resolución 97-2011. Regulación No. 58. Buenas Prácticas de Fabricación de Medicamentos Homeopáticos. [Monografía en Internet]. [citado 20 de agosto de 2013]. Disponible en: http://www.cecmed.cu/Docs/RegFarm/DRA/BPPF/2010-2012/Res/Res_CECMED-97-11.pdf
9. CECMED. Resolución 36-2011. Reg. No. 53. Requisitos para el Registro de Medicamentos Homeopáticos. [Monografía en Internet].[citado 20 de agosto de 2013]. Disponible en: http://www.cecmed.sld.cu/Docs/RegFarm/DRA/LicProd/2010-2012/Reg/Reg_53-11.pdf
10. CECMED. Resolución 117-2011. Reglamento interno del Comité de Expertos de la Medicina Natural y Tradicional. [Monografía en Internet]. [citado 20 de agosto de 2013]. Disponible en: http://www.cecmed.cu/Pages/Reg_DispGen.html
Recibido: 16 de octubre de 2013.
Aprobado: 10 de diciembre de 2013.
Celeste Sánchez-González . Avenida 1ra entre 168 y 170. Edif. D-1. Apto. 13 Reparto Flores. Playa, La Habana. Teléfono: 271 2892 Correo electrónico: evareg@cecmed.sld.cu
]]>