ARTÍCULO ORIGINAL
Respuesta clínica e inmunogénica del tratamiento con Heberón en pacientes con carcinoma basal, Policlínico Mario Gutiérrez Ardaya
Clinical and immunogenic response of Heberón treatment in patients with basal cell carcinoma, Mario Gutiérrez Ardaya Polyclinic
Ernesto Pérez Leyva 1, Mildred Yaniela Brizuela Noguera 2, Juana Madeleyne Ortíz Leyva 3
1. Especialista de Primer Grado en Medicina General Integral y Farmacología. Investigador Agregado. Asistente. Facultad de Ciencias Médicas Mariana Grajales Coello. Holguín. Cuba.
2. Especialista de Primer Grado en Medicina General Integral y Farmacología. Asistente. Facultad de Ciencias Médicas Mariana Grajales Coello. Holguín. Cuba.
3. Licenciada en Ciencias Farmacéuticas, Contabilidad y Finanzas. Policlínico Universitario Jimmy Hirzelt. Granma. Cuba.
RESUMEN
Introducción: el carcinoma basocelular es la neoplasia de piel más frecuente en pacientes de la raza blanca; el interferón alfa 2b recombinante humano es un fármaco modificador de la respuesta biológica empleado actualmente en el tratamiento de esta enfermedad.
Objetivo: determinar la respuesta clínica e inmunogénica del Heberón en el carcinoma basocelular.
Métodos: se realizó un ensayo de uso terapéutico que incluyó 18 pacientes con el diagnóstico histológico de basotelioma, la intervención consistió en la aplicación perilesional de nueve dosis del medicamento Heberón por un período de tres semanas, luego se realizó biopsia por ponche, evolutiva, a la 13 semana de concluido el tratamiento.
Resultados: al concluir la terapéutica el 84,61% de los pacientes logró la desaparición total de la lesión, según se observó basado en los criterios clínicos, dermatoscópicos e histológicos. El 15,38% alcanzó una respuesta parcial, la calidad de la cicatrización fue buena y al año de seguimiento los pacientes curados no mostraron recidivas de la lesión tumoral. Una ventaja de esta modalidad de tratamiento fue la evolución clínica favorable de lesiones neoplásicas y preneoplásicas a distancia. Los eventos adversos más frecuentes observados con el empleo del Heberón fueron: fiebre, escalofríos, edema y eritema, mialgias, artralgias, dolor en el sitio de inyección y malestar general en el 72,22%; 55,55%; 50,00%; 44,44%; 33,33% y 27,77%, respectivamente, clasificados como leves y moderados según su severidad, así como, de muy probables según su causalidad. Solo el 29,41% de los pacientes presentaron anticuerpos anti-interferón.
Conclusiones: el Heberón es un medicamento eficaz, seguro para el tratamiento del carcinoma basocelular; con el uso de esta terapia puede aparecer inmunogenicidad.
Palabras clave: carcinoma basocelulares, interferones, terapéutica.
ABSTRACT
Introduction: Basal cell carcinoma is the most frequent skin neoplasm in white patients; Human recombinant interferon alpha 2b is a drug modifying the biological response currently used in the treatment of this disease.
Objective: To determine the clinical and immunogenic response of the Heberon in basal cell carcinoma.
Method: A therapeutic use trial involving 18 patients with the histological diagnosis of basothelioma was performed. The intervention consisted of the perilesional application of nine doses of the drug Heberón for a period of three weeks, followed by a biopsy for evolutionary puncture At 13 weeks after the treatment.
Results: At the conclusion of the treatment, 84.61% of the patients achieved the total disappearance of the lesion by clinical, dermatoscopic and histological criteria; 15.38% achieved a partial response, the quality of the healing was good and at one year of follow up the patients cured showed no recurrence of the tumor lesion. An advantage of this modality of treatment was the favorable clinical evolution of neoplastic and preneoplastic lesions at a distance. The most frequent adverse events observed with Heberón's use were fever 72.22%, chills 55.55%, edema and erythema 50.00%, myalgias 44.44%, arthralgia, pain at the injection site 33.33% And malaise 27,77% classified as mild and moderate according to their severity, as well as very probable according to their causality. Only 29.41% of the patients had anti-interferon antibodies.
Conclusions: Heberón is an effective, safe drug for the treatment of basal cell carcinoma with the use of this therapy may appear immunogenicity.
Key words: basal cell carcinoma, interferons, therapeutics.
]]> INTRODUCCIÓN
El cáncer de piel no melanocítico (CCNM) incluye el carcinoma basocelular (CBC) y el de células escamosas (CEC), el carcinoma basocelular (CBC) es la neoplasia de piel más frecuente en el ser humano, representa aproximadamente entre el 70% y el 80% de los cánceres cutáneos no melanoma en la población de piel blanca. Su tasa de incidencia se incrementa en el 20% en las últimas dos décadas e involucra a grupos etarios cada vez más jóvenes, representa mundialmente un serio problema, tanto en términos de salud, como económico; en los Estados Unidos el costo anual del tratamiento es de aproximadamente 500 millones de dólares. Anualmente se diagnostican entre dos y tres millones de nuevos casos con CBC y CEC, por lo que el número de pacientes supera a los afectados por cáncer de pulmón, mama, colon, recto, próstata, vejiga y todos los tipos de linfomas 1.
En los últimos 50 años, los países de América Latina y el Caribe, experimentan cambios demográficos y epidemiológicos, que favorecen el aumento absoluto de las personas que padecen la enfermedad 2. Cuba se sitúa actualmente, dentro de los países de América Latina 3-5y el tercer mundo con mayor incidencia del cáncer de piel no melanoma. Según los datos que aparecen reflejados en el Registro Nacional 6 del Cáncer del año 2012, esta neoplasia cutánea maligna se ubica en el primer lugar de la tabla general por cáncer para ambos sexos reportándose 5 291casos en el sexo masculino y 4 494 casos en el sexo femenino, se exhibe una tasa de 93,9 y 80 por cada 100 000 habitantes respectivamente; a pesar que aún existen dificultades en el reporte de la enfermedad al comparar estas cifras con años anteriores se evidencia un incremento considerable en el número de los casos.
Los CBC son tumores epiteliales malignos de localización cutánea, descritos por Jacob en 1807, que surgen de células pluripotenciales de la zona basal de la epidermis y de la vaina radicular externa del pelo a nivel del istmo inferior y de la protuberancia. Estas se relacionan con las radiaciones ultravioletas 7 y en menor frecuencia con otras causas. Están involucradas mutaciones de distintos genes, entre las que se destaca la del gen supresor de tumor Patched en el cromosoma 9q 22 8. El aspecto clínico-patológico y el comportamiento biológico de los CBC, dependen de la interacción entre el epitelio y el estroma que lo rodea 9.
Comienza con un nódulo perlado refringente, que puede seguir diversos patrones de crecimiento o desarrollo que le dan individualidades propias y constituyen las formas clínicas de la enfermedad: nodular perlada, ulcus rodens, plano cicatrizal, infiltrante y terebrante. Entre estos tipos clínicos el nodular es el más frecuente, pero en la práctica es difícil observar lesiones puras, pues estos patrones tienden a mezclarse para constituir las llamadas formas mixtas y cualquiera de ellas puede o no estar pigmentada.
Histológicamente pueden clasificarse según criterios de Lever en: diferenciados e indiferenciados sólidos; semejante histológicamente a estructuras anexas epidérmicas que pueden ser capilares, glandulares o adenoideas y mixtos, que le dan o no, origen al tumor 10. Son de crecimiento lento y una vez instituido el tratamiento adecuado, el pronóstico es favorable. Excepcionalmente producen metástasis 11.
Actualmente los CBC no son considerados una amenaza para la vida de los pacientes, pero representan gran impacto económico en los servicios de salud y días laborables perdidos. También hay una afectación psicológica, se ve involucrada la autoestima del paciente, ya que estos al destruir la piel y los tejidos circundantes, provocan una desfiguración estética significativa, especialmente en la cara 12, localización más frecuente del CBC, aunque, se describen en otras localizaciones.
El arsenal terapéutico para el tratamiento de los CBC es muy amplio, utilizándose diferentes métodos. Aunque apenas existen estudios que comparan la eficacia de los diferentes tratamientos, la cirugía y la radioterapia parecen ser los métodos más efectivos, es el tratamiento quirúrgico el procedimiento con la tasa más baja de recurrencia 13. El tratamiento tiene como objetivo principal la eliminación completa de la lesión tumoral, con resultados cosméticos aceptables.
Se encuentran disponibles modalidades terapéuticas quirúrgicas y no quirúrgicas. Las quirúrgicas contienen métodos excisionales como la cirugía convencional; en esta técnica el incumplimiento del margen de seguridad oncológico recomendado determina la aparición de las recidivas tumorales; para establecer el margen oncológico se tienen en cuenta el tamaño del tumor, su localización y la variedad histológica 14.
La cirugía micrográfica de Mohs es el tratamiento de elección propuesto en la actualidad para tumores recurrentes, pobremente delimitados y que presentan un patrón histológico agresivo. También está indicado en tumores con topografía sugerente de alto índice de recurrencia, como es el área periorbitaria y centrofacial; ya que al realizar cortes de congelación horizontal y un mapeo estricto, permite el control de todos los márgenes de la lesión. Con este método se logran las cifras más altas de curación (97,5%) 15. También se utilizan procedimientos destructivos que incluyen la electrodesecación, curetaje, criocirugía y láser de dióxido de carbono.
]]> En el grupo de los procedimientos no quirúrgicos se emplea la radioterapia, terapia fotodinámica, quimioterapia, 5-fluoruracilo tópico o intralesional, el uso de interferones y más recientemente el imiquimod, el empleo de medicamentos que inhiben la vía Hedgehog como el Vismogenib y también el extracto de nuez de anacardo 16.La elección del procedimiento terapéutico dependerá de los recursos disponibles, la habilidad en el manejo de una u otra técnica por parte de quien haga el tratamiento, la localización anatómica de la lesión, su tamaño y las características individuales del paciente. Ninguno de estos tratamientos es totalmente efectivo y todos son susceptibles de fallar en algunos casos. Por estas razones, resulta conveniente disponer de nuevas alternativas de tratamiento que tengan ventajas específicas sobre otras técnicas y que pueden ser más convenientes para algunos casos, incluso los que tienen recidivas o no responden completamente a otros tratamientos.
Los interferones (INFs) son descubiertos por Isaac y Lindenmann en 1957 en Londres 17. Los INFs son tipos de citoquinas que se encuentran normalmente en el cuerpo, son las primeras citoquinas producidas en el laboratorio para el uso como modificadores de respuesta biológica. Los INFs son moléculas proteicas reguladoras del crecimiento celular 18. Basados en sus propiedades antigénicas específicas, los INFs pueden ser divididos en alfa, beta y gamma.
En la actualidad se conocen más de 20 subtipos de INFs. Todos los INFs poseen actividad inmunorreguladora, antiproliferativa y antiviral. Su efecto inmunomodulador incluye la estimulación de la actividad lítica de las células natural killer (NK), células T citotóxicas específicas y de macrófagos sobre células tumorales, la modificación de producción de anticuerpos (Ac) por linfocitos B, la regulación de antígenos de histocompatibilidad (HLA) en las membranas celulares y la estimulación de la producción de INF-alfa 19-21. La acción directa antitumoral incluye efectos antiproliferativos, tóxicos y la unión de antígenos de superficies sobre la célula tumoral, mientras que la acción indirecta, activación del macrófago, células T, células NK y modulación de la producción de anticuerpos.
Debido a estas propiedades, los IFNs tienen un gran uso en la terapéutica, por lo que constituyen uno de los principales materiales biotecnológicos que se producen en el ámbito mundial (Borden y col. 1997) 22. En números anteriores de la Revista Correo Científico Médico, Pérez Leyva expone las propiedades de estas citoquinas 23.
A finales de la década del 80 se inician los estudios de este fármaco como terapia en el CBC, un incremento de las investigaciones sobre ese campo se produce en los años 90 donde se desarrollan estudios clínicos que evidencian la eficacia y seguridad de los interferones en el tratamiento del CBC, varias combinaciones de interferones alfa y beta se comparan para buscar mejores efectos, así como, preparados de liberación prolongada que permiten disminuir la frecuencia de la administración del fármaco y que la terapia resulte más cómoda para el paciente.
Sin embargo, todos estos intentos no muestran mayor eficacia cuando se compara con el interferón alfa 2b recombinante solo; el surgimiento de nuevos tratamiento con una eficacia superior conlleva a que la investigación y desarrollo de medicamentos en esta enfermedad se dirija hacia otras dianas farmacológicas olvidándose del interferón por unos cuantos años 24-29, muestra fehaciente de este hecho son los escasos trabajos publicados en el ámbito internacional. Hasta el año 2009 Anasagasti30 despierta especial interés en Cuba al evaluar por primera vez la combinación de INFs alfa y gamma (HeberPAG) perilesionalmente en CBC agresivos, extensos, recurrentes y resistentes a otros tratamientos (cirugía, radioterapia, quimioterapia), al utilizar la pauta de tres veces a la semana durante tres semanas y realización de biopsia cutánea a las 13 semanas de finalizar el tratamiento. Se incluyen 12 pacientes con CBC, de los cuales 47% presentan eliminación completa del tumor; en 40% de los casos se obtiene una reducción del 30% y 13% permanecen estables a los 38 meses de seguimiento.
La principal ventaja terapéutica de la nueva combinación al parecer consiste en la prolongada respuesta clínica observada en los pacientes con TPNM avanzados tratados con HeberPAG; sin embargo, resulta necesario contrastar los resultados de este estudio, así como, desarrollar nuevos ensayos clínicos donde se comparen el nuevo producto con el interferón alfa 2 b recombinante humano, (hasta el momento la “good standarts” de este tipo de tratamiento), pues a pesar que en Cuba se desarrolla desde hace muchos años el Heberón, existen escasas publicaciones del uso de este medicamento en el basotelioma que permitan determinar la efectividad del fármaco en la práctica médica habitual; por consiguiente la presente investigación se realizó con el objetivo determinar la efectividad seguridad e inmunogenicidad del tratamiento con Interferón alfa 2 b recombinante humano en pacientes con carcinoma basocelular.
MÉTODOS
]]> Se realizó un ensayo de uso terapéutico. El universo estuvo representado por el total de pacientes con diagnóstico histológico de cualquier variedad de carcinoma basocelular, que acudieron al Servicio de Dermatología del Policlínico Mario Gutiérrez Ardaya, durante el período septiembre 2013- a septiembre 2014. La muestra estuvo conformada por 18 pacientes, tributarios del tratamiento.Criterios de inclusión:
Consentimiento de participar en el estudio.
Pacientes con confirmación histológica de carcinoma basocelular.
Edad mayor de 18 años.
Criterios de exclusión
Pacientes embarazadas.
Pacientes que manifiesten hipersensibilidad a los Interferones o alguno de los componentes del producto.
Pacientes con trastornos en la coagulación, trastornos inmunitarios, colagenosis, enfermedades metabólicas, antecedentes de enfermedades cerebrovasculares, enfermedades cardiovasculares descompensadas, retinopatías, hepatopatías y leucosis.
Paciente con enfermedades mentales que incapaciten para cooperar en el interrogatorio y en general con el estudio.
Pacientes que no cumplan con el esquema completo de tratamiento por abandono, fallecimiento, pacientes que presenten reacciones adversas clasificadas como graves.
Los datos se obtuvieron a partir de la revisión del cuaderno de recogida de datos y las historias clínicas
Se procedió primeramente a realizar una caracterización general de la muestra en la que se tuvo en cuenta la edad, sexo, fototipo de piel y enfermedades asociadas; los elementos antes mencionados pueden influir en las respuestas del paciente al tratamiento por lo que resultó indispensable tener el control y descripción de estas variables de confusión.
]]> La intervención consistió en la administración por vía intradérmica, perilesional de los interferones alfa 2b recombinante humano (Heberón) producido en el Centro de Ingeniería Genética y Biotecnología (CIGB) de la Habana Cuba; comercializado por Heber Biotec SA, con una frecuencia de tres veces por semana durante tres semanas, pudiéndose repetir el ciclo durante dos ocasiones más en caso de que los resultados del tratamiento no fueran satisfactorios con un primer ciclo.La dosis total a administrar dependió del tamaño de la lesión y varió desde tres millones de unidades del producto en tumores de 1 cm2 a 10 cm2 y la dosis de 10 millones de unidades en tumores que superaron los 10 cm2; otro criterio para seleccionar la dosis fue la variedad clínica e histológica del tumor. La formulación farmacéutica empleada fue el liofilizado que se reconstituyó en 1 ml de agua para inyección, administrándose inmediatamente luego de su preparación. La evaluación final se realizó a la semana 16 de haber iniciado el tratamiento y al año del mismo. Durante las consultas de seguimiento (semanas 2, 4, 16) se realizaron exámenes complementarios.
Las variables principales de respuesta en relación con la efectividad de tratamiento fueron: el tamaño y la evolución de la lesión tumoral; se tomó como referencia los criterios RECIST 31 para calificar a los pacientes con respuesta completa, parcial, enfermedad estable o progresiva, luego se calculó la proporción de paciente con respuesta completa y parcial lo que representó la respuesta objetiva. Para considerar el tratamiento eficaz la proporción de pacientes con respuesta objetiva debió ser superior al 60%.
Otras variables secundarias de respuesta observadas en el estudio fueron: la calidad en la cicatrización, las recidivas tumorales al año de la terapia y la localización y evolución de lesiones preneoplásicas. En relación con la seguridad del tratamiento se identificaron el tipo de reacción adverso, luego se clasificaron según su severidad utilizando los criterios de gradación de eventos adversos clínicos y de laboratorio del Programa de Evaluación de la Terapia del Cáncer 32. Para determinar la relación de causalidad se utilizó el algoritmo de la Food and Drug Administration (FDA) 33 y para considerar segura la terapia la proporción de pacientes que presentó eventos adversos graves debió ser inferior al 40%. Los anticuerpos anti-interferón alfa fue un indicador que se determinó antes de la terapia y en la semana 16.
Para el análisis estadístico de las variables cualitativas se utilizó análisis de frecuencia simple y estadísticos descriptivos. Para las variables cuantitativas se aplicaron las medidas de tendencia central y de variabilidad absoluta, fundamentalmente. Se utilizó el paquete estadístico SPSS (Statistical Package for Social Sciences). La investigación cumplió con los principios de la Declaración de Helsinki. Todos los pacientes dieron su consentimiento informado para esta intervención. El Comité de Ética de la investigación y Consejo Científico de la institución aprobaron la ejecución del protocolo de la investigación. Los autores de este trabajo no refieren conflictos de intereses.
RESULTADOS
En las características demográficas de los pacientes (tabla I) predominaron ligeramente los pacientes del sexo femenino (66,66%). La totalidad de los pacientes presentaban la piel blanca (100%). El fototipo II y III fue el mayor encontrado para el 50,00% y el 38,88%, respectivamente. La edad promedio de los pacientes fue de 64,1 años y osciló entre 47 y 87 años. Trece pacientes (72,22%) presentaron alguna enfermedad asociada; y prevaleció la hipertensión arterial (33,33%).
Tabla I. Características demográficas de los pacientes
| Variables | ]]> N | (%) | |
| 18 | (100,00) | ||
| Género | Masculino | 6 | (33,33) |
| Femenino | 12 | ]]> (66,66) | |
| Raza | Blanca | 18 | (100,00) |
| Fototipos de piel | Tipo I (Siempre se quema, nunca se broncea) | 1 | (5,55) |
| Tipo II (Siempre se quema, luego se broncea ligeramente) | ]]> 9 | (50.00) | |
| Tipo III (A veces se quema, siempre se broncea) | 7 | (38,88) | |
| Tipo IV (Nunca se quema siempre se broncea) | 1 | (5,55) | |
| Edad | Media± DS | ]]> 64,16± 12,4 | |
| Mediana | 61 | ||
| (Min; Max) | (47; 87) | ||
| Enfermedades asociadas | 13 | (72,22) | |
| Hipertensión arterial | 6 | ]]> (33,33) | |
| Diabetes mellitus | 1 | (5,55) | |
| Cardiopatía isquémica | 1 | (5,55) | |
| Asma Bronquial | 1 | (5,55) | |
| ]]> Alcoholismo | 1 | (5,55) | |
| Glaucoma | 1 | (5,55) | |
| Insuficiencia venosa periférica | 1 | (5,55) | |
| Neurosis ansiosa depresiva | ]]> 1 | (5,55) | |
| Hiperplasia prostática benigna | 1 | (5,55) | |
| Migraña | 1 | (5,55) | |
Fuente: historias clínicas individuales
En la evaluación inicial de la lesión tratada, a todos los pacientes se les realizó dermatoscopía inicial (tabla II). La media de la suma de los diámetros (menor y mayor) fue de 19,88 mm con una variación entre 9 y 75 mm. La mayoría de las lesiones se localizaron en la nariz (44,44%) y en la cara (27,77%). Como subtipo clínico de lesión predominaron el nodular y el pigmentado para el 72,22% y el 16,66%, respectivamente. Según el subtipo histológico prevalecieron las lesiones nodular o sólido (55,55%).
]]> Tabla II. Evaluación inicial de la lesión tratada| Suma de Diámetros(mm) | Media± DS | 19,88 ± 19,90 |
| Mediana | 10,5 | |
| (Min; Max) | (9; 75) | |
| Localización | Nariz | ]]> 8 (44,44) |
| Cara | 5 (27,77) | |
| Pabellón auricular | 1 (5,55) | |
| Cuero cabelludo | 1 (5,55) | |
| Frente | 1 (5,55) | |
| Cuello | ]]> 1 (5,55) | |
| Tórax | 1 (5,55) | |
| Subtipo clínico | Nodular | 13 (72,22) |
| Pigmentado | 3 (16,66) | |
| Nódulo ulcerativo | 2 (11,11) | |
| ]]> Subtipo histológico | Nodular o sólido | 10 (55,55) |
| Adenoideoquístico | 3 (16,66) | |
| Superficial | 1 (5,55) | |
| Baso-escamoso | 1 (5,55) | |
| Queratótico | ]]> 1 (5,55) | |
| Esclerodermiforme | 1 (5,55) | |
| No especificado | 1 (5,55) |
Fuente: Historias clínicas individuales.
Se evaluaron 17 pacientes (uno abandonó tempranamente la terapia) y solo se pudo administrar una dosis al realizar la evaluación final de la lesión tratada (tabla III). En esta evaluación final se tuvo en cuenta la respuesta clínica dermatoscópica e histológica, en la cual 12 pacientes (70,58%) tuvieron respuesta completa, 5 (29,41%) manifestaron respuesta parcial a los cuales se le propuso iniciar con un segundo ciclo de tratamiento, pero con Heberpag. No hubo pacientes con enfermedad estable, ni progresión de la enfermedad.
Tabla III. Respuesta clínica de los pacientes según evolución de la lesión
neoplásica, resultados estéticos y recidivas al año del tratamiento
| Variables | n | ]]> % |
| Evolución de la lesión | ||
| Curado | 12 | 70,59 |
| Parcial | 5 | 29,41 |
| Resultados estéticos | ||
| Buenos | ]]> 11 | 91,66 |
| Regular | 1 | 8,33 |
| Recidivas al año | ||
| Sin recidivas | 12 | 100,00 |
Fuente: historias clínicas individuales
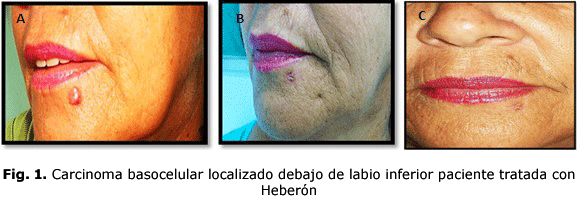
]]> Teniendo en cuenta que el 100% de los pacientes presentaron una respuesta objetiva se consideró que la terapia con Heberón resultó ser efectiva para el tratamiento del carcinoma basocelular en la muestra de pacientes del estudio. Por la evaluación estética final de la lesión tratada según el color, predominó la normocromía. Por la textura la mayoría de los pacientes presentaron elasticidad normal o ligera disminución. En relación con el volumen prevalecieron las lesiones planas.La mayoría de los pacientes presentaron sensibilidad normal, el 100% de los pacientes incluidos en el estudio no tenían queloides. La mayoría de los pacientes (91,66%) tuvieron una buena calidad de la cicatrización. Al evaluar la presencia de recidivas tumorales al año de la intervención en consulta de seguimiento fue significativo que el 100% de los pacientes clasificados como curados (12) se mantuvieron sin lesiones recidivantes, lo cual muestra que hasta ese momento la respuesta objetiva es sostenida en el tiempo (fig. 1). En A se observa la lesión antes del tratamiento. B nótese la evolución clínica favorable después del tratamiento (semana 16) así como resultados estéticos satisfactorios. C la misma paciente luego del tratamiento en una vista frontal.
Es frecuente que los pacientes presenten más de una lesión neoplásica y también que coexistan lesiones preneoplásicas. En el presente estudio cuatro pacientes (23,53%), presentaban este tipo de lesiones, luego del tratamiento en dos pacientes (11,76%) uno que presentaba un cuerno cutáneo alejado de la lesión neoplásica tratada (la cual desaparece totalmente) y otro caso que presentaba múltiples lesiones localizadas cerca y a distancia de la lesión tratada al evaluarlas se modificaron sustancialmente. El producto puede beneficiar en algunos casos a los pacientes que presenten más de una lesión (fig. 2). la lesión tratada se localizaba en la punta de la nariz, además, presentaba lesión preneoplasica cuerno cutáneo en antebrazo derecho. En A se muestra cuerno cutáneo localizado en el antebrazo derecho lesión preneoplásica a distancia de la lesión tratada. B respuesta favorable de lesiones a distancia nótese desaparición del cuerno cutáneo después del tratamiento. C vista ampliada del cuerno cutáneo. D vista ampliada antebrazo derecho en la que no hay evidencia del cuerno cutáneo después del tratamiento.
En la (fig. 3), A nótese las múltiples deformidades que presenta en el rostro como consecuencia de las cirugías convencionales anteriormente realizadas, obsérvese las cicatrices e injertos que presenta, también presenta lesiones de Herpes Zóster oftálmico. B vista ampliada de la pirámide nasal lesión tratada. C evolución clínica satisfactoria de la paciente. D a la 13 semana de haber concluido el tratamiento, nótese la desaparición clínica de la lesión y los resultados estéticos favorables E, F, G otras lesiones neoplásicas que presentaba la paciente anterior localizada en el antebrazo derecho; estas tumoraciones se encontraban distantes de la lesión tratada nótese como se modifica de forma satisfatoria estas lesiones.
Todos los pacientes presentaron eventos adversos (tabla IV). Los más frecuentes reportados (≥10%) fueron: fiebre, escalofríos, edema y eritema, mialgias, artralgias dolor en el sitio de inyección, malestar general, astenia y los dolores óseos. La mayoría de los eventos adversos fueron leves (88,73%) y moderados (11,27%), solo se interrumpió el tratamiento en un paciente que presentó un absceso perilesional, al cual se le pudo administrar cuatro dosis del medicamento, es significativo señalar que este pacientes en la evaluación final tuvo una respuesta completa, de forma general se garantizó el cumplimiento del tratamiento. El 87,32% de los eventos adversos se clasificaron como muy probables, lo cual evidenció la imputabilidad del Heberón en su aparición.
Tabla IV. Tipo de reacción adversa presentada, clasificación según severidad
y causalidad
| ]]> Variables | n | % |
| Reacción adversa | ||
| Fiebre | 13 | 72,22 |
| Escalofríos | 10 | 55,55 |
| ]]> Edema y eritema | 9 | 50,00 |
| Mialgias | 8 | 44,44 |
| Artralgias | 6 | 33,33 |
| Dolor en el sitio de inyección | ]]> 6 | 33,33 |
| Malestar general | 5 | 27,77 |
| Astenia | 2 | 11,11 |
| Dolores óseos | 2 | ]]> 11,11 |
| Náuseas | 1 | 5,55 |
| Hiperglucemia | 1 | 5,55 |
| Sensación de desmayo | 1 | 5,55 |
| ]]> Cefalea | 1 | 5,55 |
| Lipotimia | 1 | 5,55 |
| Prurito perilesional | 1 | 5,55 |
| Disuria | ]]> 1 | 5,55 |
| Absceso perilesional | 1 | 5,55 |
| Diarreas | 1 | 5,55 |
| Severidad | ||
| Leve | ]]> 63 | 88,73 |
| Moderada | 8 | 11,27 |
| Causalidad | ||
| Muy probable | 62 | 87,32 |
| Probable | ]]> 4 | 5,63 |
| Posible | 5 | 7,04 |
Fuente: historias clínicas individuales n=18
Evaluar la inmunogenicidad de las nuevas terapias biológicas es un aspecto esencial en la investigación científica actual que contribuye a identificar como influye este fenómeno en la respuesta al tratamiento, a estandarizar la técnica y a individualizar las terapias. En el presente estudio (tabla V) se obtuvo un total de cinco muestras positivas a la presencia de anticuerpos, que reconocen la molécula de IFN-alfa humano recombinante, que corresponde al 29,41% del total de los pacientes del estudio. No hubo pacientes con autoanticuerpos, por tanto, se consideraron anticuerpos inducidos por la terapia, pues los cinco pacientes cuya muestra inicial resultó tener niveles más bajos de anticuerpos; luego se incrementaron de forma notable.
Tabla V. Presencia de anticuerpos anti interferones antes y después del tratamiento
| Anticuerpos anti interferones | Antes del tratamiento | ]]> Después del tratamiento | ||
| No | % | No | % | |
| Sí |
|
| 5 | 29,41 |
| ]]> No | 17 | 100,00 | 12 | 70,59 |
| Total | 17 | 100,00 | 17 | 100,00 |
DISCUSIÓN
Dentro de los factores predisponentes para padecer de CBC existe la raza blanca. El 90% de los pacientes afectados son de raza blanca. A menor fototipo de piel según Fitzpatrick, existe mayor riesgo de padecer de CBC. En la actualidad se estima, que tres de cada diez personas de raza blanca, tienen la posibilidad de desarrollar un CBC; es mayor aún el riesgo, en aquellas personas que tienen poca o ninguna capacidad de broncearse y con antecedentes de quemaduras solares antes de los 20 años. En los pacientes albinos, los CBC son de tipos histológicos más agresivos 1-3.
El paciente de sexo masculino es más propenso a padecer de CBC. Los autores consideran que el cáncer de piel es más frecuente en el sexo masculino que en el femenino, teniendo en cuenta que estos son los que más se exponen al sol, debido a sus ocupaciones y obligaciones, por un problema de machismo entre los hombres sobre todos cubanos, hay mayor descuido y falta de percepción de riesgo sobre el efecto de la exposición prolongada a los rayos ultravioletas, los cuales van causando daños acumulativos a lo largo de su vida.
En los últimos años en los medios de difusión masiva se entrevistan a profesionales de salud que advierten sobre los potenciales perjuicios de la exposición sin protección de la piel a la luz ultravioleta, lo que considero ha influenciado en que la población, sobre todo hace que los jóvenes tomen conciencia de la necesidad de usar medios de protección; otra arista que influye de manera negativa en la fotoprotección, a pesar de los esfuerzos de la industria farmacéutica cubana en ampliar cada año el números de medicamentos en su cuadro básico y tener una mayor autonomía, no ha logrado hasta el momento proveer de bloqueadores solares, es poca su disponibilidad y altos precios, que no siempre son accesibles a la mayoría de la población y en muchas ocasiones no se garantiza la estabilidad del producto en el mercado.
Al comparar los resultados con otros estudios se encontró que con respecto al tamaño de la lesión, no todos los estudios en los que se utilizan los interferones en el tratamiento del carcinoma basocelular, ofrecen el tamaño de la lesión en un Primer Ensayo (Cornell 1990) 26.
La media de la zona de la lesión fue de 83 mm2 en el grupo de tratamiento y de 75 mm2 en el grupo de placebo. En el segundo ensayo (n = 35) de interferón beta recombinante, se administró un millón de unidades tres veces a la semana, durante tres semanas y se comparó con placebo (Rogozinski 1997) 27. No se proporcionó el tamaño y la ubicación del CCB.
En el tercer ensayo (Alpsoy 1996) 45 pacientes son asignados al azar para recibir 15 o 30 millones de unidades de interferón alfa-2a, 2b o 2a y 2b 28. El objetivo del estudio fue evaluar la efectividad del IFN alfa-2a y 2b y averiguar si este efecto puede aumentar mediante su combinación. El tamaño de la lesión varía de 0,5 a 8,9 cm2.
En un cuarto ensayo (Edwards 1990) de 65 pacientes, se compara una dosis única de diez millones UI de interferón alfa-2b quelato de protamina-cinc (una preparación de liberación sostenida) con la misma dosis semanal durante tres semanas 29. Sólo se incluyeron las lesiones que variaban en tamaño de 0,5 a 1,5 cm para los CCB nodulares o de 2 cm para los CCB superficiales (diámetro más grande).
]]> Los CBC se localizan generalmente en áreas expuestas a la luz solar; su ubicación en la cara y el cuello representan el 80% de todas las lesiones, seguido de áreas como los hombros, pecho y espalda con el 15% y el resto se distribuyen en otras áreas del cuerpo. Discriminando la región de cabeza y cuello, las áreas más frecuentemente afectadas son la región nasal, frontal, periorbitaria y la auricular. Esta distribución por regiones anatómicas tiene algunas variantes en los distintos trabajos reportados.En el estudio de Raasch y otros autores, realizado en Australia, se reporta un predominio de lesiones en cara y cuello, al subtipo clínico el CBC nodular (también llamado nódulo-ulcerativo) representa entre el 50% y 54% de los CBC y el subtipo histológico el patrón sólido, nodular o de nido grande es el tipo histológico más frecuente (representa el 70% de todos los casos) 3; resultados que coinciden con los encontrados en este estudio.
Anasagasti en su estudio evalúa por primera vez la combinación de INFs alfa y gamma intra y perilesionalmente en CBC agresivos, extensos, recurrentes y resistentes a otros tratamientos (cirugía, radioterapia, quimioterapia) utilizando la pauta de tres veces a la semana durante tres semanas y realización de biopsia cutánea a las 13 semanas de finalizar el tratamiento. Se incluyen 12 pacientes con CBC, de los cuales 47% presentan eliminación completa del tumor, en el 40% de los casos se obtiene una reducción del 30% del tumor y 13% permanecen estables 30.
La metodología utilizada en el anterior estudio es la que más coincide con el nuestro, solo se evidencia una mayor cantidad de pacientes con respuestas objetivas. En otros estudios se muestran resultados inferiores a esta investigación, aunque también tienen el inconveniente que el diseño, análisis e interpretación de los resultados son muy diferentes, algunos tienen más de 20 años de publicación, tal es el caso de Cornell 26. En relación con la eficacia (comparación 09/01) existe significativamente menos fracasos iniciales del tratamiento en el grupo de interferón comparado con el placebo, RR 0,02 (IC del 95%: 0,12 a 0,32).
Rogozinski (comparación 10/01) concluye que existe significativamente menos fracasos tempranos del tratamiento en el grupo de placebo comparado con el grupo de interferón beta, (RR 0,53, IC del 95%: 0,33 a 0,86) 27. Alpsoy plantea que el fracaso temprano del tratamiento es para el IFN alfa-2a y el IFN alfa-2b de 33,3% y para el IFN alfa-2a + 2b (26,6%) 28.
Por último, en el estudio de Edwards 29 se refleja significativamente menos fracasos tempranos del tratamiento a favor de tres inyecciones semanales en comparación con una dosis única. Mientras Cornell26 en su estudio no especifica los parámetros que tiene en cuenta para evaluar los resultados estéticos después de un año del tratamiento donde encuentra que el 83% de los pacientes y el 61% de los médicos, calificaron la apariencia estética como excelente en los pacientes tratados con interferón.
Edwards 29 por su parte solo evalúa los resultados cosméticos según la percepción de los pacientes, los participantes que presentan erradicación del tumor, califican su resultado estético como excelente en el 51%, muy bueno en el 22%, bueno en el 14%, satisfactorio en el 10% y deficiente en el 3%.
Aunque en la presente investigación no se tuvo en cuenta el criterio de los pacientes con la satisfacción del resultado final, ofrece a los investigadores una metodología que garantiza una mayor objetividad para valorar la calidad de la cicatrización.
Con la utilización de los interferones en el tratamiento del carcinoma basocelular solo el estudio Seguimiento a largo plazo del carcinoma basocelular tratados con interferón alfa 2b perilesional en monoterapia de Tucker SB evalúa la aparición de recidivas tumorales en un período mayor de 5 años; en el cual se concluye, que las curas clínicas son notadas en 95 de 98 bccs (51 nodulares y 44 superficiales) con un período de seguimiento término medio de 10,5 años (9 meses a 18,5 años). De estos, 35 de los 50 pacientes, que incluye 68 de los 98 tumores, son seguidos por un período mínimo de diez años, con un seguimiento promedio de 13,5 años 34. De los 68 tumores seguidos, las tasas de la cura son de 96%. El análisis global de datos usando estimaciones de Kaplan-Meier demuestra una tasa de éxito del 98% en los años quinto y décimo; y una tasa de éxito de 96% en el año 15.
Por su parte Anasagasti 2009 30 refiere que a los 38 meses de seguimiento los pacientes permanecen sin presentar recidivas tumorales. Según Cornell también hubo una diferencia significativa en las tasas de recidiva a las 52 semanas que indican una mejor respuesta para el grupo de tratamiento comparado con el grupo vehículo 26.
]]> Teniendo en cuenta los resultados anteriores es necesario establecer diseños de estudios que evalúen las recidivas tumorales en un tiempo mayor que el estudiado, con el que se podría determinar a largo plazo la efectividad de la nueva combinación.Al consultar las investigaciones internacionales y nacionales no se encontraron estudios que describieran simultáneamente el resultado de lesiones preneoplásicas y carcinoma basocelular en pacientes tratados con interferón. Sin embargo, Edwards L (1986) 35 en su estudio titulado Efecto del interferón alfa 2B intralesional en la Queratosis actínica señala que las inyecciones de IFN-α2b intralesional tres veces a la semana por dos o tres semanas, comparado con placebo demuestra que el interferón es efectivo para el tratamiento de las queratosis actínica. Las limitaciones del uso clínico de intralesional IFN están relacionadas con respecto a la comodidad del tratamiento, son estas las inyecciones múltiples y muchas visitas al médico.
Otro estudio de ese mismo investigador en el año 1990 evalúa la aplicación de una formulación de gel de IFN- α2b 30 millones de IU, aplicándolo cuatro veces por cuatro semanas y comparado con placebo en el que se concluye que la respuesta clínica es poco significativa con la nueva forma farmacéutica 36.
En relación con los eventos adversos al comparar los resultados con los reportados en las investigaciones se encontró en una primera investigación a (Cornell 1990) 26 quien refiere que los eventos adversos se presentan en el grupo tratado con interferón y con más frecuencia los síntomas similares a la gripe que el grupo vehículo.
Rogozinski (1997) por su parte reporta como eventos adversos solo inflamación en el sitio de la inyección, en 11 de 16 pacientes en el grupo de tratamiento, y en 4 de 18 de los que reciben placebo 27. En el ensayo de Alpsoy (1996) se destaca dolor en el sitio de la inyección y todos los pacientes tuvieron síntomas similares a la gripe (fiebre, escalofríos, cefaleas, fatiga, mialgia) especialmente dentro de las dos primeras semanas después del comienzo del tratamiento 28.
En el estudio de Edwards (1990) todos los pacientes presentaron al menos una reacción adversa 29. Los efectos secundarios son similares tanto para el grupo de dosis única, como para el de dosis repetidas y son comunes con el interferón. Las reacciones adversas que se presentan en al menos el 20% de los participantes del estudio son fiebre, rigores, mialgia, cefalea y náuseas. Otros efectos secundarios incluyen artralgia, malestar general, fatiga, diarrea, parestesia, somnolencia, sed, mareos, vómitos, erupciones cutáneas y anorexia. Las reacciones adversas comienzan el día del tratamiento y en general duran de cinco a ocho horas, excepto las cefaleas que persisten cerca de un día.
Varios estudios evalúan la inmunogenicidad en pacientes tratados con interferones, sin embargo, esta variable no se ha estudiado en los pacientes con carcinoma basocelular en un estudio titulado Inmunogenicidad del interferón alfa-2b recombinante (Heberón alfa R®). Detección de anticuerpos mediante un ensayo inmunoenzimático y neutralización de actividad antiviral del autor González-Cabañas encuentra en muestras de individuos sanos y enfermos tratados o no con interferón (IFN) alfa-2b recombinante (Heberón alfa R) o leucocitario natural (Heberón alfa N); se estudia la presencia de anticuerpos anti-IFN mediante un ensayo inmunoenzimático (ELISA) tipo "sandwich" (IFN alfa-2b/muestra/proteína A-peroxidasa) con confirmación de la especificidad en este estudio 37. La técnica descrita es similar a la empleada en nuestra investigación.
Este autor también investiga la neutralización de la actividad antiviral de IFN alfa-2b. Por ELISA no se encuentra anticuerpos anti-IFN en 184 individuos no tratados, mientras que en otras muestras evaluadas por bioensayo hay actividad neutralizante en sujetos con hepatitis viral crónica (8/181; 4,4%) y neoplasias (11/121; 9,1 %) y no en otros 98 con otras enfermedades o sanos. No se detecta anticuerpos anti-IFN en ninguno de los individuos tratados con IFN leucocitario, 27 de ellos evaluados por ELISA y 52 por neutralización de la actividad antiviral 37.
Después del tratamiento con IFN alfa-2b se confirma mediante ELISA la positividad en una niña con linfangioma y en un adulto con papilomatosis laríngea entre 177 pacientes. Los sueros positivos por ELISA tienen títulos neutralizantes de 1:25 y 1:64 000, respectivamente. El tratamiento induce actividad neutralizante en 13,1% (19/145) de los pacientes evaluados por bioensayo. La incidencia total de anticuerpos inducidos por el tratamiento, evaluada por cualquiera de los métodos, es de 6,4% (19/296). Esta cifra es similar a la reportada para el IFN alfa-2b 37.
En otro estudio de la investigadora Torres Rives B titulado Evaluación de la inmunogenicidad del Interferón alfa 2b humano recombinante en pacientes con hepatitis crónica y hemangiomas de la infancia se evaluaron los sueros; de un total de 221 pacientes (130 de hepatitis y 91 de hemangioma) de los cuales 4 (1,8%) presentan autoanticuerpos anti-IFN, antes del inicio de la terapia (naturales) 38. Durante el curso del tratamiento se detecta anticuerpos anti-IFN en 27 pacientes (12,2%) y actividad neutralizante en 13 (5,8%). No se evidencia asociación significativa entre la presencia de anticuerpos anti-IFN de unión, ni su actividad neutralizante con la respuesta al tratamiento. La presencia de anticuerpos se observa con mayor frecuencia en niños menores de un año y con menor frecuencia, en pacientes mayores de 60 años.
]]> Por su parte Soler Arus E en su estudio Interferon alfa-2b recombinante en hepatitis C crónica: Resultados del tratamiento y determinación de anticuerpos anti-interferón, de 22 pacientes con diagnostico serológico (anti-VHC +), bioquímico (alanina-aminotransferasa - ALAT > 2 veces lo normal) e histológico de hepatitis C crónica, dos desarrollan anticuerpos anti-IFN después del tratamiento, con capacidad neutralizante en uno de ellos, posiblemente relacionados con la evolución desfavorable de ese caso 39.Sobre estos estudios se destacó que difieren del que se desarrolló, pues también evalúan la actividad neutralizante de los anticuerpos anti-interferones, limitación importante del nuestro, algunos con un número superior de pacientes, pesquisa además, la presencia de los anticuerpos anti-interferones en individuos sanos y en enfermedades que tienen un esquema, vía de administración y posología diferente al de los carcinoma basocelulares, aspectos que pueden influir en la aparición de los anticuerpos anti-interferones, aunque sobre esta temática existen controversias, hay autores que plantean que al inicio de esta terapia puede aparecer un título elevado de anticuerpos, pero que con la terapia mantenida la presencia de los interferones disminuye de manera sustancial.
CONCLUSIONES
El Heberón es un producto eficaz, seguro que se puede utilizar en la terapéutica del carcinoma basocelular. Con el uso de esta terapia puede aparecer inmunogenicidad. En los pacientes que estén presentes simultáneamente lesiones preneoplásicas y basotelioma puede resultar beneficioso el empleo de esta terapia.
Se recomienda mantener el fármaco-vigilancia del medicamento, para así evaluar la seguridad del tratamiento a largo plazo y también desarrollar estudios analíticos donde se correlacione la actividad neutralizante de interferones alfa, con la respuesta clínica y la aparición de efectos adversos. Se sugiere efectuar protocolos donde se compare la nueva combinación de interferones alfa-gamma (Heberpag) con el interferón alfa (Heberón).
REFERENCIAS BIBLIOGRÁFICAS
1. Sallyann KC, Chen S. Analyzing the Cost of Preventing Nonmelanoma Skin Cancer. J Invest Derm. 2009[citado 21 ene 2017]; 129(12):2745-2746. Disponible en: http://www.sciencedirect.com/science/article/pii/S0022202X15341713?via%3Dihub
2. Lukaszuk BLM, Cidral Muniz E, Leite da Veiga M, Iribas JL. Aspectos epidemiológicos del cáncer no melanoma de piel en un servicio de dermatología de la ciudad de Santa Fe - Argentina 2007. Rev Argent Dermatol. 2008 [citado 8 jun 2017]; 89(1): 30-36. Disponible en: http://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S1851-300X2008000100005&lng=es
3. World Health Organization. From Australia to Brazil: sun worshippers beware. Bull World Health Organ. 2009[citado 8 jun 2017]; 87(8):574–575. Disponible en: www.who.int/entity/bulletin/volumes/87/8/09-030809.pdf
4. Victoria Bárzaga HO. Métodos para la prevención y tratamiento del carcinoma basocelular. AMC. 2011[citado 21 ene 2011]; 15(2):212-213.Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1025-02552011000200001
5. Victoria Bárzaga HO, Lazo Sánchez L. Relación clínico histopatológica de lesiones tumorales de la piel. AMC.2006 [citado 18 ene 2010]; 10(4):219-221. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1025-02552006000400009
6. Cuba. Ministerio de Salud Pública. Anuario Estadístico de Salud. La Habana: MINSAP; 2016. Disponible en: http://files.sld.cu/dne/files/2017/05/Anuario_Estad%C3%ADstico_de_Salud_e_2016_edici%C3%B3n_2017.pdf
7. Madan V, Hoban P, Strange RC, Fryer AA, Lear JT. Genetics and risk factors for basal cell carcinoma. Br J Dermatol. 2006[citado 8 jun 2017]; 154(supl1):5–7.Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2133.2006.07229.x/full
8. Rodust PM, Stockfleth E, Ulrich C, Leverkus M, Eberle J. UV-induced squamous cell carcinoma: a role for antiapoptotic signalling pathways. Brit J Dermatol. 2009[citado 8 jun 2017]; 3(161):107-115. Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2133.2009.09458.x/full
9. Buljan M, Bulat V, Situm M, Mihić LL, Stanić-Duktaj S. Variations in clinical presentation of basal cell carcinoma. Acta Clin Croat. 2008[citado 8 jun 2017]; 47(1):25-30. Disponible en: http://hrcak.srce.hr/25816
10. Kirkham N. Tumors and Cysts of the epidermis. En: Elder DE, Elenitsas R, Johnson B, Jaworsky C. Lever´s histopathlogy of the skin. 9th ed. Philadelphia: Lippincott Wilkins; 2006.p.617-654
11. Lamon T, Gerard S, Meyer N, Losfeld B, van Kan GA, Balardy L, et al. Exceptional bone metastasis of basal cell carcinoma in Gorlin-Goltz syndrome. Dermatology. 2010 [citado 8 jun 2017]; 220(1):57-59. Disponible en: https://www.karger.com/Article/FullText/264669
12. Bin Yap FB. Clinical characteristics of basal cell carcinoma in a tertiary hospital in Sarawak, Malaysia. Int J Dermat. 2010[citado 8 jun 2017]; 49(2):176-179.Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1365-4632.2009.04342.x/epdf
13. Bath Hextall FJ, Perkins W, Bong J, Williams HC. Intervenciones para el carcinoma basocelular de la piel. Cochrane Plus. 2013 [citado 22 ene 2016]; 5.Disponible en:http://www.bibliotecacochrane.com/BCPGetDocumentForPrint.asp?DocumentID=CD003412
14. Aguayo Leiva IR, Ríos Bucetay L, Jaen Olasolo P. Tratamiento quirúrgico vs no quirúrgico en el carcinoma basocelular. Actas Dermo Sifiliogr.2010 [citado 22 ene 2016]; 101(8):683–692. Disponible en: http://www.sciencedirect.com/science/article/pii/S0001731010002796?via%3Dihub
15. Galimberti G, Pontón Montaño A, Ferrario D, Kowalczuk A, Galimberti R. Cirugía micrográfica de Mohs en el tratamiento de carcinoma basocelular. Actas Dermo Sifiliogr. 2010[citado 22 ene 2016]; 101 (10): 853-857. Disponible en:http://www.sciencedirect.com/science/article/pii/S0001731010003352?via%3Dihub
16. Love WE, Bernhard JD, Bordeaux JS. Topical imiquimod or fluorouracil therapy for basal and squamous cell carcinoma: a systematic review. Arch Dermatol. 2009[citado 22 ene 2016]; 145(12):1431-1438. http://jamanetwork.com/journals/jamadermatology/fullarticle/712288
17. Isaacs A, Lindenmann J. Virus Iterference .I. The Interferon. Proc R Soc Lond B Biol Sc.1957 [citado 12 nov 2015]; 147(927):258-263.Disponile en: http://rspb.royalsocietypublishing.org/content/147/927/258
18. Ross C, Tingsgaard P, Jorgensen H, Vejlsgaard GL. Interferon treatment of cutaneous T-cell lymphoma. Eur J Haematol. 1993[citado 12 nov 2015]; 51(2):63-72. http://onlinelibrary.wiley.com/doi/10.1111/j.1600-0609.1993.tb01595.x/full
19. García García I, González Delgado CA, Valenzuela Silva C, Hernández Bernal F, Ferrero-Bibilonia J, Soto Hernández R, et al. Bioequivalence of two recombinant interferon alpha-2b liquid formulations in healthy male volunteers. Drugs RD. 2004[citado 12 nov 2015]; 5(5): 271-280.Disponible en: https://link.springer.com/article/10.2165/00126839-200405050-00003
20. Stewart WE. The interferon system. New York: Springer-Verland Wien; 1980.
]]>21. Darnell JE, Kerr IM, Stark GR. JaK-Stat Pathways and transcriptional activation in response to interferons and other extracellular signaling proteins. Science. 1995[citado 12 nov 2015];264(5164):1415-1421.Disponible en: http://search.proquest.com/openview/e4cca120f2e48ad3d6edeb9971a818fb/1?pq-origsite=gscholar&cbl=1256
22. Ruiz L, Reyes N, Aroche K, Báez R, Aldana R, Hardy E. Some factors affecting the stability of interferon alpha 2b in solution. Biologicals. 2006[citado 12 nov 2015]; 34(1):15-19. Disponible en: http://www.sciencedirect.com/science/article/pii/S1045105605000758?via%3Dihub
23. Pérez E, Batista K, Guerra O, Bello I, Serrano MV. Interferones una opción terapéutica moderna en el tratamiento de los carcinomas basocelulares. CCM. 2016[citado 15 dic 2016]; 20(2). Disponible en: http://scielo.sld.cu/pdf/ccm/v20n2/ccm06216.pdf
24. Buechner S, Wernli M, Bachmann F, Harr T, Erb P. Intralesional interferon in basal cell carcinoma: how does it work? Recent Results Cancer Res. 2002[citado 15 dic 2016]; 160: 246-250. Disponible en: https://link.springer.com/chapter/10.1007/978-3-642-59410-6_29
25. Fenton S, Kennedy S, Moriarty P. The role of interferon alpha 2b as an adjunctive treatment in the management of aggressive basal cell carcinoma of the eyelids. Acta Ophthalmol Scand. 2002[citado 15 dic 2016]; 80(6):674-675. Disponible en: http://onlinelibrary.wiley.com/doi/10.1034/j.1600-0420.2002.800623_3.x/full
26. Cornell RC, Greenway HT, Tucker SB, Edwards L, Ashworth S, Vance JC, et al. Intralesional interferon therapy for basal cell carcinoma. J Am Acad Dermatol. 1990[citado 15 dic 2016]; 23(4 Pt 1):694-700. Disponible en: http://www.sciencedirect.com/science/article/pii/019096229070276N?via%3Dihub
27. Rogozinski TT, Jablonska S, Brzoska J, Michalska I, Wohr C, Gaus W. Intralesional treatment with recombinant interferon beta is an effective alternative for the treatment of basal cell carcinoma. Double-blind, placebo-controlled study. Przeglad Dermatologiczny. 1997; 84(3):259-263.
28. Alpsoy E, Yilmaz E, Basaran E, Yazar S. Comparison of the effects of intralesional interferon alfa-1a, 2b and the combination of 2a and 2b in the treatment of basal cell carcinoma. J Dermatology. 1996[citado 15 dic 2016]; 23(6):394-396.Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1346-8138.1996.tb04040.x/full
29. Edwards L, Tucker SB, Perednia D, Smiles KA, Taylor EL, Tanner DJ, et al. The effects of an intralesional sustained-release formulation of interferon alfa-2b on basal cell carcinoma. Arch Dermatol. 1990; 126(8):1029-1032.
]]>30. Anasagasti Angulo L, Garcia Vega Y, Barcelona Perez S, López Saura P, Bello Rivero I. Treatment of advanced, recurrent, resistant to previous treatments basal and squamous cell skin carcinomas with a synergistic formulation of interferons. Open, prospective study. BMC Cancer. 2009[citado 15 dic 2016]; 9:262. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2724551/
31. Guijo Hernández T, Rodríguez Benítez A, Sánchez de la Orden C, Fernández Rosa S, Rodríguez Cabillas ME. Utilización de los criterios RECIST en el seguimiento de tumores sólidos. (31 Congreso nacional Sociedad española de radiología médica) 25-28 Mayo 2012; Granada.
32. National Cancer Institute. Common Terminology Criteria for Adverse Events (CTCAE). U.S.Department of Health And Human Services.2010 [citado 12 jun 2017].Disponible en: https://searchworks.stanford.edu/view/9100287
33. OMS. Buenas prácticas de fármaco-vigilancia para las américas. Buenas Prácticas de Farmaco-vigilancia para las Américas.2008 [citado 22 Jun 2017].Disponible en:http://www.paho.org/hq/dmdocuments/2008/3_GT_VConfernecia_Farmacovigilancia.pdf
34. Tucker SB, Polasek JW, Perri AI, Goldsmith EA. Long-term follow-up of basal cell carcinomas treated with perilesional interferon alfa 2b as monotherapy. JAAD.2006 [citado 7 mar 2016]; 54(6):1033-1038. Disponible en: http://www.jaad.org/article/S0190-9622%2806%2900551-2/abstract
35. Edwards L, Levine N, Weidner M, Piepkorn M, Smiles K. Effect of intralesional interferon in actinic keratoses. Arch Dermatol.1986 [citado 7 mar 2016]; 122(7):779-782.Disponible en: http://jamanetwork.com/journals/jamadermatology/article-abstract/547332
36. Edwards L, Levine N, Smiles KA. The effect of topical interferon alfa 2b on actinic kerotoses. J Dermatol Surg Oncol. 1990 [citado 7 mar 2016]; 16(5):446-449.Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1524-4725.1990.tb00062.x/abstract
37. González Cabañas R, Ferrero Bibilonia J, Morales Menéndez MG, Aguilera Rodríguez A, López Saura P. Inmunogenicidad del interferón alfa-2b recombinante (Heberón alfa R®). Detección de anticuerpos mediante un ensayo inmunoenzimático y neutralización de actividad antiviral. Biotecnología Aplicada. 1998[citado 7 mar 2016]; 15(2):71-76.Disponible en: http://elfosscientiae.cigb.edu.cu/PDFs/Biotecnol%20Apl/1998/15/2/071-076.pdf
38. Torres Rives B, Miranda Moles A, García García I, Porreo Martín J, Nodarse Cuní H. Evaluación de la Inmunogenicidad del Interferón alfa 2b humano recombinante en pacientes con Hepatitis crónica y Hemangiomas de la infancia. Rev Habanera Cien Méd.2005 [citado 7 mar 2016]; 4(5): Disponible en:http://www.revhabanera.sld.cu/index.php/rhab/article/view/840/658
39. Soler Arus E, Velázquez Infante M, Padrón Guillermo J, Menéndez Morales M G, Oramas Bienvenido G. et. al. Interferón alfa-2b recombinante en hepatitis C crónica: Resultados del tratamiento y determinación de anticuerpos anti-interferón. Biotecnología Aplicada. 1997[citado 7 mar 2016]; 14(4):242-247. Disponible en: http://elfosscientiae.cigb.edu.cu/PDFs/Biotecnol%20Apl/1997/14/4/242-247.pdf
Agradecimientos: Los autores agradecen la colaboración del Centro de Ingeniería Genética y Biotecnología en el desarrollo de este estudio, de forma especial al equipo de trabajo liderado por el Dr.C Iraldo Bello Rivero, promotor de los estudios clínicos del Heberferón.
Recibido: 12 de junio de 2017
Aprobado: 19 de junio de 2017
Dr. Ernesto Pérez Leyva. Facultad de Ciencias Médicas Mariana Grajales Coello. Holguín. Cuba.
Correo electrónico: ernestopl@infomed.sld.cu