Lic. Gema E. García Dafonte,1 Lic. Celeste M. Arranz Calzado,2 Lic. Berta Rodríguez Pendás,2 Lic. Isabel Almeida Zaldívar,3 Dr. Roberto M. González Suárez,4 Lic. Remigio Coto Rodeiro,5 Dr. Sergio Santana Porbén6 y Dr. Armando Lozano Guadarrama7
Se presentaron los resultados de la estandarización de un juego de reactivos (CUALINEN-HCG) para la detección de la gonadotropina coriónica humana (HCG) en muestras de orina de mujeres embarazadas y de su validación diagnóstica en el nivel primario. CUALINEN-HCG es un microELISA de doble captura, que cuenta con un anticuerpo monoclonal específico para la subunidad b de la hCG (AcM-b hCG-IG1) y de conjugados enzimáticos con el sustrato colorimétrico correspondiente, obtenido y purificado en el Instituto Nacional de Endocrinología. Los resultados de la validación analítica del CUALINEN-HCG mostraron que era capaz de distinguir entre muestras de orinas positivas y negativas con una relación positivo/negativo de 10 veces; se obtuvieron coeficientes de variación del 6 % en estudios de precisión (interensayos e intraensayos) realizados para el control positivo. Se procesaron 91 muestras de orina matutina de mujeres con amenorrea de entre 4 y 16 sem a partir de la última fecha de menstruación. En las que el embarazo fue diagnosticado posteriormente. Se logró la validación en el nivel primario del CUALINEN-HCG con una sensibilidad y especificidad diagnóstica de 85 y 95 %, respectivamente y una exactitud diagnóstica del 90 %. Se recomendó su uso como herramienta auxiliar para el diagnóstico del embarazo en nivel primario a partir de la primera semana de ausencia de la menstruación (5 sem de amenorrea).
DeCS: GONADOTROPINAS CORIONICAS; TEST DE ELISA; ANTICUERPOS MONOCLONALES; ORINA; TECNICAS DE DIAGNOSTICO OBSTETRICO Y GINECOLOGICO; EMBARAZO.
La detección de embarazo en estadios iniciales constituye un problema de los servicios de salud primarios en Cuba, por la carencia de métodos inmunoquímicos que puedan ser utilizados por el médico, como proceder diagnóstico antes de las 6 sem de amenorrea, momento en el cual el ultrasonido y el tacto vagino-abdominal resultan ineficientes. Esto no solo es importante en la atención temprana de la maternidad, sino que, es vital para disminuir la mortalidad y las complicaciones asociadas con embarazos ectópicos.1
Los objetivos de este trabajo son demostrar que el juego de reactivo CUALINEN-HCG es una alternativa diagnóstica simple para la detección de embarazo, que excluye el uso de colorímetros o fluorímetros, lo que lo hace accesible a servicios de asistencia médica con menos recursos, manteniendo los niveles de calidad analíticos requeridos, y contribuir de esta forma a la detección de embarazos ectópicos en las primeras 6 sem de gestación disminuyendo los riesgos asociados con esta patología.
El resto de los reactivos empleados en la preparación de soluciones fueron obtenidos de la Merck.
Se diseñó un juego de reactivos (CUALINEN-HCG) que contiene la cantidad de reactivos suficientes para procesar 10 muestras de orina por duplicado con los 2 controles por duplicado:
R1: 2 tiras de polivinilo (PVC), utilizadas como fase sólida recubiertas con 10 µg/mL de AcP-hCG.
R5: Bulbo con conjugado antirratón-peroxidasa, líquido (predilución 1/200). Dilución final de trabajo 1/3 000.
R2: Bulbo con control positivo, liofilizado (100 UI/L).
R3: Bulbo con control negativo, liofilizado (< 5 UI/L).
R4: Bulbo con AcM-bhCG-IG1, liofilizado (10 µg/mL). ]]>
R6: Bulbo con ortofenildiamina, liofilizado.
R7: Bulbo con tampón diluente de R6, líquido (fosfato-citrato-H2O2).
R8: Bulbo con 2 mL de tampón TRIS-Tween concentrado (10X), líquido.
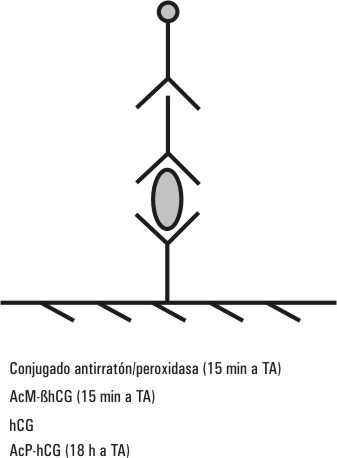
Los reactivos se manipularon según el prospecto del CUALINEN-HCG incluido en cada juego, el diseño general del inmunoensayo (IE) se muestra en la figura 1.

Previamente a la validación clínica se validaron estos reactivos, para lo cual se utilizaron 14 muestras de orina de mujeres embarazadas ya confirmadas con la clínica y otras 9 negativas o de mujeres no embarazadas.
Para establecer por apreciación visual la menor concentración de hCG detectada, se evaluaron patrones con concentraciones de 12,5 - 25 - 50 y 100 UI/L en R8 (tampón TRIS-Tween) conjuntamente con R2 (control positivo) y diluciones 1/2, 1/4 y 1/8 de R2 con R3 (control negativo); posterior a los 15 min de incubación con el sustrato enzimático (R6+R7), se comparó la intensidad del color desarrollado (coloración amarilla) para cada preparación con respecto al R3. La concentración menor que mostró una coloración superior al R3 se clasificó con una cruz (+) y se consideró arbitrariamente como la menor concentración de hCG capaz de diferenciarse del R3 en 15 min. Las muestras con densidad óptica (DO) mayor que R2 se consideraron con 2 cruces (++).
Se comparó la DO a 492 nm obtenida en 14 muestras de orina de mujeres embarazadas con respecto a la obtenida en las 9 de mujeres no embarazadas, con el propósito de registrar las diferencias en DO 492 nm de estas 2 poblaciones.
La precisión intraensayo e interensayo se evaluó determinando el valor de DO 492 nm en un espectrofluorímetro computadorizado SUMA (modelo 121-b, marca registrada, CIE) a R2 y R3, mediante el cálculo de la desviación en las lecturas de DO de 8 réplicas de los controles positivo y negativo procesadas dentro de una misma corrida (intra) y de 2 réplicas para cada control ejecutadas en 15 corridas independientes (inter).
Se analizaron muestras de suero, orina, sin diluir y con diluciones seriadas, desde 1:2 hasta 1:250 en R8 correspondiente a una mujer con 8 sem de embarazo normal.
CUALINEN-HCG se utilizó en un protocolo de validación diagnóstica aplicado en el nivel primario en el que participaron el consultorio del médico de la familia (CMF 80-2), responsable de la colección de la muestra de orina, captación de la embarazada y seguimiento de la misma hasta confirmar o no el embarazo. El hospital materno-infantil de 10 de Octubre, responsable de colectar, conservar y procesar las muestras de orina provenientes del CMF 80-2 y el Instituto Nacional de Endocrinología como autor y productor del juego de reactivos y promotor principal de la validación externa del mismo.
Se procesaron 91 muestras de orina pertenecientes a mujeres en un rango de edad entre 15 y 49 años que refirieron retraso menstrual entre 4 y 10 sem, a partir de la última menstruación.
Para el análisis de los resultados se confeccionaron tablas de contingencia de doble entrada y se evaluaron las características operacionales del juego de reactivos CUALINEN-HCG en términos de su sensibilidad (S), especificidad (E) y exactitud (A) diagnóstica.15 La significación estadística de los resultados se evaluó mediante técnicas estadísticas tradicionales.16
Se realizó un estudio de estabilidad de la HCG en 13 orinas positivas las cuales fueron conservadas a diferentes temperaturas de menos 20 °C, 4 °C, temperatura ambiente (20 °C) y 37 °C. Las muestras se conservaron a estas temperaturas y se procesaron el mismo día de su recolección (considerando este como el tiempo 0), a las 48, 72 y 168 h (1 sem después), para comparar los resultados.
La concentración de 100 UI/L del patrón y del R2 mostró diferencias evidentes (++) con respecto al R3 a los 15 min de incubación con el sustrato; también se detectó visualmente la aparición de un amarillo menos intenso (+), pero diferenciable de R3 para el patrón correspondiente a la concentración de 25 UI/L y dilución 1/4 de R2 estableciendo de manera arbitraria la concentración de 25 UI/L como la mínima detectable.
Las diferencias registradas de los valores de DO obtenidos para las muestras positivas (DO = 1,5 ± 0,72) y las negativas (DO = 0,14 ± 0,06), demuestran que es evidente la diferenciación visual de estas 2 poblaciones. El rango de valores de DO para las muestras positivas, oscila entre 0,78 (X - DE) y 2,2 (X + DE) y son superiores a los registrados para R2 (tabla 1) que oscila entre 0,72 a 0,92 (X ± 2DE) por lo que establecimos 100 UI/L como límite de clasificación de la positividad.
Tabla 1. Estudio de precisión del CUALINEN-HCG
| Controles | ]]> Repetibilidad (n = 8) | Reproducibilidad (n =15) | ||
| (X ± DE) | CV % | (X ±DE) | CV % | |
| Positivo (R2) | 0,70 ± 0,04 | 6,0 | ]]> 0,82 ± 0,05 | 6,0 |
| Negativo (R3) | 0,15 ± 0,03 | 20,0 | 0,11 ± 0,05 | 45,0 |
CUALINEN-HCG presentó valores de CV % intraensayo e interensayo para el control R2 inferiores al 10 %, catalogado como óptimo para este tipo de IE (tabla 2), no ocurrió así con el CV % del R3 por los valores de DO registrados en la zona de imprecisión del equipo.
El resultado de este estudio (fig. 2), en el caso de la orina, reportó valores de densidad óptica proporcionales a la dilución, describió una línea recta, sin embargo, en la muestra de suero sin diluir fueron, menores (0,5) y no alcanzaron el valor máximo hasta una dilución de 1:8 de la muestra, lo que sugiere la no utilización de este tipo de muestra en esta prueba.
]]>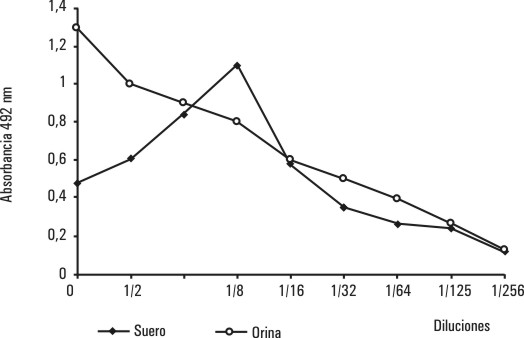
FIG.2. Estudio de la linealidad en muestra de orina de una mujer embarazada.
Los resultados de la validación diagnóstica en el escenario escogido dieron un valor de exactitud diagnóstica del 90 %, para una S y E de 85 y 95 %, respectivamente (tabla 2).
Tabla 2. Estudio de sensibilidad y especificidad diagnóstica del CUALINEN-HCG en la atención primaria
| CUALINEN-HCG | ]]> Criterio de certeza | Total | |
| Positivos | Negativos | ||
| Positivos | 41 | 2 | 43 |
| Negativos | 7 | 41 | 48 |
| Total | ]]> 48 | 43 | 91 |
S = Verdaderos positivos ´ 100 /verdaderos positivos +falsos negativos.
S = 41 ´100 / 41 + 7
S = 85 %
E = Verdaderos negativos ´ 100 / verdaderos negativos + falsos positivos.
E = 41 ´ 100 / 41 + 2
E = 95 %
Tabla 3. Estudio de estabilidad de la HCG en la orina (n=13)
| Temperatura de conservación (°C) | Tiempo 0 Diag + (%) | Tiempo 48h Diag +/- (%) | Tiempo 72h ]]>
Diag +/- (%) | Tiempo168 h Diag +/- ( %) |
| - 20 | 13 (100) | 13/0 (100) | 12/1 (92,3) | 10/3 (76,9) |
| 4 | 13 (100) | ]]> 12/1 (92,3) | 12/1 (92,3) | 9/4 (69,2) |
| 20 | 13 (100) | 12/1 (92,3) | 12/1 (92,3) | 8/5 (61,5) |
| 37 | 13 (100) | ]]> 11/2 (84,6) | 9/4 (69) | 5/8 (38,5) |
El logro principal de este trabajo fue el desarrollo y puesta a punto de un juego de reactivos para la detección de embarazo (CUALINEN-HCG) aplicable en el nivel primario, el cual demostró ser lo suficientemente robusto para funcionar adecuadamente bajo las condiciones de trabajo de un laboratorio de rutina.
Los resultados de la validación analítica y diagnóstica en el nivel primario corroboran lo anterior en opinión de los propios evaluadores;17 la S y E diagnóstica fue del 85 y 95 %, respectivamente, para una exactitud diagnóstica del 90 % utilizando 100 UI/L como límite de clasificación de la positividad.
Se demostró que el límite de clasificación de la positividad en 100 UI/L no resultó conveniente en el escenario ensayado, por cuanto 15 mujeres de cada 100 tendrán un diagnóstico de embarazo negativo aún en presencia de este; por otra parte, los estimados de la S fueron inferiores a los referidos en la literatura,18 donde se plantean que la S y E diagnósticas deben ser superiores al 90 %.
No obstante, otras variables relacionadas con la forma de colección de la muestra y su conservación, merecen ser analizadas para evaluar la magnitud de su influencia sobre los resultados y evitar errores en estudios posteriores. Se conoce que la colección de la primera orina de la mañana garantiza los niveles de hCG requeridos para detectar la concentración real de la hormona21 por lo que recomendamos, al inicio de este estudio, la colección de la primera orina matutina, y posteriormente, se aceptó el procesamiento de la segunda, para incrementar las muestras del estudio. El tiempo de almacenamiento de las orinas entre 8 y 15 °C, antes de ser procesadas, no fue controlado, si se conoce que en muchos casos fue más de 8 d hasta lograr completar las muestras suficiente para las tiras, por lo que el análisis retrospectivo de los resultados falsos negativos y la estabilidad de hCG en esas muestras de orina no pudo realizarse.
Experiencias anteriores de nuestro grupo de trabajo en condiciones controladas de laboratorio donde se colectó la segunda orina matutina de embarazadas con tiempos de amenorrea menores de 6 sem procesadas el mismo día de su colección dieron resultados positivos verdaderos por lo que pensamos que la S = 85 % está más relacionada con la estabilidad de la hormona en la muestra de orina que con la sensibilidad del CUALINEN-HCG.
Se ha reportado que la estabilidad de la hormona disminuye al aumentar la temperatura de almacenamiento, pasa a sus formas melladas y libres22,23 y que las formas melladas, conservadas en refrigeración por más de 2 sem, se disocian a sus subunidades libres y alteran los resultados en la cuantificación de hCG.24,25 Estos procesos de disociación son mucho más importantes en matrices con bajo contenido proteico como la orina, donde los procesos de disociación de la hCG se aceleran.26 Las muestras en trabajos anteriores fueron procesadas, por lo general, el mismo día, pero se demostró además que para los anticuerpos y estándares utilizados la estabilidad se mantuvo al menos en 6 meses en que se realizaron los estudios de estabilidad en condiciones de conservación de congelación a -20 °C, y conservación de liofilización para los controles.27,28
Estimamos que estos 2 factores, colección de la segunda orina matutina y condiciones de preservación de las muestras, influyeron de manera decisiva en la S = 85 %.
La estabilidad de la molécula de hCG depende del tiempo y la temperatura de conservación por lo que las muestras no congeladas disminuyeron su porcentaje de positividad en todos los casos de temperatura de conservación excepto a -20 °C durante 48 h y que fue muy significativo la disminución de la positividad por debajo del 70 % cuando fueron almacenadas por períodos de 168 h o sea 1 sem. Por tales motivos recomendamos procesar las orinas frescas y de lo contrario conservarlas en congelación (-20 °C) no más de 48 h, para asegurar así la estabilidad de esta hormona.
La linealidad del método fue demostrada para las muestras de orina, no así para el suero, por lo que se recomienda no utilizar este para la detección del embarazo.
La utilización de este kit diagnóstico representa un ahorro por concepto de divisas ya que si tenemos en cuenta que una tira reactiva para una sola prueba de embarazo cuesta alrededor de 50 centavos dólar, y en este caso los reactivos producidos en el INEN tienen un bajo costo, solo se compararía con el costo de la placa de ELISA que es de alrededor de un dólar, pero con la cual se pueden realizar 40 muestras, vemos que además del ahorro, esto representa un impacto social pues en el país no se ofrece este servicio en otros hospitales.
Subject headings: GONADOTROPINS; CHORIONIC; ENZYME-LINKED IMMUNOSORBENT ASSAY; ANTIBODIES, MONOCLONAL; URINE; DIAGNOSTIC TECNIQUES, OBSTETRICAL AND GYNECOLOGICAL; PREGNANCY.
Recibido: 4 de noviembre de 2002. Aprobado: 19 de diciembre de 2002.
Lic. Gema E. García Dafonte. Instituto Nacional de Endocrinología, Zapata y D, El Vedado, Ciudad de La Habana, Cuba.
1 Licenciada en Bioquímica. Máster en Ciencias Biológicas. Investigadora Agregada. Laboratorio Bioquímica Clínica. Instituto de Medicina del Deporte, Ciudad de La Habana.
2 Licenciada en Bioquímica. Investigadora Auxiliar. Laboratorio de Diabetes. Instituto Nacional de Endocrinología, Ciudad de La Habana.
3 Licenciada en Laboratorio Clínico. Laboratorio Bioquímica Clínica. Hospital Militar "Carlos J. Finlay", Ciudad de La Habana. ]]>
4 Especialista de II Grado en Bioquímica Clínica. Investigador y Profesor Titular. Instituto Nacional de Endocrinología, Ciudad de La Habana.
5 Licenciado en Bioquímica. Laboratorio Bioquímica Clínica. Hospital Materno-Infantil "10 de Octubre", Ciudad de La Habana.
6 Especialista de II Grado en Bioquímica Clínica. Laboratorio Clínico. Hospital "Hermanos Ameijeiras", Ciudad de La Habana.
7 Especialista de I Grado en Medicina General Integral. Hospital General Docente "Enrique Cabrera". Ciudad de La Habana.