 ]]>
]]>
ARTÍCULO ORIGINAL
Influencia de factores perinatales en la pesquisa neonatal de hiperplasia adrenal congénita en Ciudad de La Habana y La Habana
Influence of perinatal factors on the neonatal screening of congenital adrenal hyperplasia in Ciudad de La Habana
MSc. Dra. Tania Mayvel Espinosa Reyes,I Dra. Milaydis Hernández Benítez,I Dr. Francisco Carvajal Martínez,I Dr. C. Ernesto González Reyes,II Dra. Emma Domínguez AlonsoI
]]>
IInstituto Nacional de Endocrinología. La Habana, Cuba.
RESUMEN
Introducción: los costos económicos y psicosociales asociados con los resultados falsos positivos de la pesquisa neonatal de hiperplasia adrenal congénita son altos. ]]>
Objetivos: identificar los factores perinatales que intervienen en la elevación y en el tiempo de normalización de los valores de 17 hidroxiprogesterona (17OHP), en pacientes no afectados por hiperplasia adrenal congénita.
Métodos: se realizó un estudio descriptivo longitudinal retrospectivo en 1 114 pacientes procedentes de Ciudad de La Habana y La Habana, con resultados falsos positivos en la pesquisa, desde enero/2007 hasta junio/2010. Se identificaron las diferencias en la frecuencia de los factores perinatales reconocidos en este grupo con una muestra de población general, y otra integrada por enfermos de hiperplasia adrenal congénita.
Resultados: de los pacientes falsos positivos, el 50,7 % pertenecía al sexo masculino y 49,3 % al femenino. El 54,7 % nació por cesárea, y el 82 % no presentó sufrimiento fetal agudo, aquellos con menor edad gestacional y peso al nacer más bajo presentaron niveles medios de 17OHP más elevados. El 68,1 % normalizó la 17OHP al cumplir un mes de vida, independientemente del tipo de parto y de la presencia de sufrimiento fetal agudo; pero la edad gestacional y el peso al nacer tuvieron correlación inversa con la persistencia de su elevación. Predominó el parto eutócico en los neonatos enfermos y normales, y la cesárea en los falsos positivos. La media de la edad gestacional y del peso al nacer fue significativamente menor en los casos en el primer grupo, comparada con la de los grupos restantes.
Conclusiones: la prematuridad y el bajo peso al nacer tuvieron una influencia significativa sobre la elevación y la persistencia de los valores de 17OHP, no así el tipo de parto y el sufrimiento fetal agudo.
Palabras clave: hiperplasia adrenal congénita, prematuridad, bajo peso, falsos positivos.
ABSTRACT
Introduction: the psychosocial and economic costs associated with the false-positive results of the neonatal screening of congenital adrenal hyperplasia are high.
Objectives: to identify the perinatal factors to get involved in the rise and in the normalization time of values of 17 hydroprogesterone (17OHP) in patients not involved by a congenital adrenal hyperplasia. ]]>
Methods: a retrospective, longitudinal and descriptive study was conducted in 1 114 patients from Ciudad de La Habana and La Habana with false-positive results according to screening from January, 2007 to June, 2010. Authors identified the differences in frequency of perinatal factors recognized in this group with a sample of general population, and other including congenital adrenal hyperplasia patients.
Results: from the false-positive patients, the 50.7 % was of male sex and the 49.3 % to the female one. The 54.7 % was born by cesarean section and the 82 % has not acute fetal suffering, those small for the gestational age and lower birth weight had mean levels of 17OHP higher. The 68.1 % normalized the OHP at one month of life, independently the type of labor and of the presence of acute fetal suffering but the gestational age and the birth weight had an inverse correlation with the persistence of its rise. There was predominance of eutocia labor in the sick and normal neonates and the cesarean section in the false-positive ones. The mean of gestational age and of the birth weight was significantly minor in the cases of the first group, compared with the remaining groups.
Conclusions: the prematurity and the low birth weight had a significant influence on the rise and the persistence of values of 17OHP, but not the type of labor and the acute fetal suffering.
Key words: congenital adrenal hyperplasia, prematurity, low weight, false-positives.
INTRODUCCIÓN
La hiperplasia adrenal congénita (HAC) define un grupo de enfermedades autosómicas recesivas, en las cuales se produce un trastorno de la esteroidogénesis suprarrenal, debido a mutaciones genéticas que afectan las enzimas que intervienen en la biosíntesis del cortisol. Es el desorden adrenal más común en la infancia, y la causa más frecuente de ambigüedad sexual. Los niños y las niñas son afectados por igual. La frecuencia es variable, según las formas clínicas descritas, y las formas clásicas se presentan en 1:12 000-25 000 nacidos vivos, y las no clásicas en 1:8 000.1-8 ]]>
El déficit de 21 hidroxilasa es su forma más común, y constituye del 90 al 95 % de todos los pacientes con HAC; también es la más frecuente de las enfermedades metabólicas hereditarias. Se produce por mutaciones en el gen CYP21A2 que codifica la enzima P450c21 (21 hidroxilasa), el cual está ubicado en el brazo corto del cromosoma 6.
En el déficit de 21 hidroxilasa se describe una forma clásica de presentación neonatal y otra no clásica de expresión tardía. La forma clásica representa los casos más severos de este déficit, y se asocia aproximadamente en un 75 % a pérdida de sal. El diagnóstico clínico de la forma clásica es particularmente difícil en varones, en quienes la virilización puede ser poco evidente en el período neonatal, con riesgo de muerte por una crisis suprarrenal entre la 2ª y 3ª semana de vida. Por otra parte, en los recién nacidos (RN) del sexo femenino que presenten grados severos de virilización, se corre el riesgo de una asignación errónea del sexo, con todos los problemas médicos, familiares, sociales y legales que esta situación conlleva.1,4,6-10
En la actualidad, la determinación de los niveles de 17OHP en muestras de sangre seca es mundialmente aceptada para la pesquisa neonatal de la HAC causada por la deficiencia de 21 hidroxilasa, cuyos objetivos fundamentales son: la detección precoz de los casos más graves con fenotipo perdedor de sal y virilizante simple, la prevención de crisis adrenal con pérdida salina en un varón afectado, y además, evitar la asignación de sexo masculino a una mujer 46 XX afectada.1,11-16
La factibilidad de cada programa de pesquisa está basada en la evaluación de falsos positivos (especificidad) y falsos negativos (sensibilidad). Existe un compromiso entre estos 2 parámetros, y el nivel de corte debe establecerse en el nivel más bajo que asegure una adecuada sensibilidad sin pérdida importante de la especificidad.15,17 Sin embargo, los ensayos aún presentan problemas de especificidad y sensibilidad.
- Falsos positivos (FP): prematuros, bajo peso y enfermedades graves como trastornos respiratorios (especialmente la enfermedad de membrana hialina), la pobre función renal o hepática, el estrés quirúrgico, metabólico o traumático (debido a una inmadurez de la actividad enzimática adrenal, y reserva inadecuada en respuesta al estrés).4,8,11-13,15 Otros factores que contribuyen a la obtención de valores elevados de 17OHP, son la toma de muestra antes de las 48 h de vida,4,8,11,15 así como la baja especificidad de algunos antisueros utilizados en los inmunoensayos, sobre todo, por la reactividad cruzada de estos con la 17OH pregnenolona o su esteroide sulfato, en ambos casos superior al 8 %. Estos compuestos tienden a estar elevados en los RN, por de la posible inhibición de la 3ß-hidroxiesteroide deshidrogenasa por los estrógenos maternos.8,18,19
]]> - Problemas de sensibilidad que dan lugar a falsos negativos: neonatos que recibieron tratamiento esteroideo prenatal o neonatal.13,15,20-22
En Cuba han sido estudiados 548 838 neonatos a través del programa de pesquisa neonatal en el período comprendido desde Enero 2005 a Junio 2010. De ellos, 10 028 han presentado resultados elevados en la pesquisa, y 35 han sido diagnosticados como casos de HAC, para una frecuencia de 1:15 245.23
Los costos económicos y psicosociales, asociados con los resultados FP de los programas de pesquisa neonatal de la HAC, son altos, pues obliga a la repetición de exámenes, evaluación por el endocrinólogo, y genera, además, ansiedad en los padres frente a una eventual enfermedad del RN. Se plantea, que solo los costos de laboratorio relacionados con resultados FP son 10 veces superiores a los de una muestra con resultado normal, por tanto, se recomienda ajustar los valores de referencia teniendo en cuenta la edad gestacional (EG), el peso al nacer (PN) y la edad al momento de la toma de la muestra.16,18
El presente trabajo se propuso determinar la influencia de los factores perinatales en la aparición de un elevado número de pacientes con resultados falsos positivos en el programa cubano de pesquisa neonatal de HAC, lo cual permitirá trazar nuevas estrategias para la confirmación y seguimiento de estos pacientes. El objetivo general fue identificar los factores perinatales que intervienen en la elevación de la 17OHP en pacientes no afectados de HAC; y más específicamente determinar la influencia del tipo de parto, la EG, el PN y el sufrimiento fetal agudo, sobre la elevación de los valores de 17OHP en pacientes no afectados de HAC; determinar la edad al momento de la normalización y su relación con los factores perinatales estudiados; e identificar posibles diferencias en la frecuencia de los factores perinatales reconocidos en el grupo estudiado con una muestra tomada de población general, y una muestra integrada por los pacientes enfermos de HAC.
MÉTODOS
Se realizó un estudio descriptivo longitudinal retrospectivo. El universo estuvo constituido por los RN de La Habana y Ciudad de La Habana estudiados por el programa de pesquisa neonatal de HAC, en el período comprendido desde enero/2007 hasta junio/2010, cuyos resultados de 17OHP en la muestra tomada por punción en el talón fueron elevados. Se incluyeron los 1 114 recién nacidos de La Habana y Ciudad de La Habana pesquisados por el programa neonatal de HAC que asistieron a la consulta de endocrinología pediátrica del Instituto Nacional de Endocrinología (INEN) para su reevaluación, y que no fueron confirmados como casos positivos de HAC, distribuidos de la manera siguiente:
Los pacientes del primer grupo fueron atendidos en la consulta del programa de diagnóstico neonatal de HAC del INEN, y evaluados con una frecuencia mensual hasta la normalización de sus valores. Se revisaron todas sus historias clínicas con el objetivo de identificar los factores perinatales que intervinieron en la cuantía, y la persistencia de la elevación de la 17OHP.
El análisis de los datos de los grupos 2 y 3 estuvo encaminado a identificar las posibles diferencias en la frecuencia de los factores perinatales reconocidos en el primer grupo de estudio. No se incluyó la etapa del inicio del programa (2005-2006) porque durante ese período se utilizó un antisuero diferente, por lo que los resultados no podían considerarse comparables. La información fue recogida en un modelo creado con este propósito, que incluye los acápites de interés.
El UMELISA 17OH Progesterona Neonatal fue desarrollado por el Centro de Inmunoensayo, es un ensayo inmunoenzimático competitivo para la determinación cuantitativa de 17OHP, diseñado para la pesquisa neonatal de la HAC en muestras de sangre seca sobre papel de filtro.18,21,23 El UMELISA 17OHP Suero, es también un ensayo inmunoenzimático competitivo, que utiliza calibradores y muestras de suero humano, y se emplea para la confirmación y seguimiento de los pacientes con sospecha y los casos positivos de HAC (González EC, Marrero N, Pérez PL, Frómeta A, Zulueta O, Herrera D, et al. UMELISA 17OHP Suero: ensayo para la determinación de 17-hidroxiprogesterona en muestras de suero humano. Trabajo presentado en 1er. Congreso Cubano de Endocrinología Pediátrica y de la Adolescencia; 2003. La Habana, Cuba).
Los datos fueron procesados mediante el software estadístico SPSS 10,0. Para su análisis se utilizó distribución de frecuencia, media, porcentajes y odds ratio, con un intervalo de confianza del 95 % y nivel de significación de p< 0,05. Se exploró la asociación de los valores de 17OHP con la EG y el peso natal utilizando el coeficiente de correlación de Pearson. Se compararon los valores promedio de 17OHP entre categorías: tipo de parto y presencia de sufrimiento fetal agudo (SFA) a través de la prueba chi cuadrado para muestras independientes. Se utilizó la regresión lineal múltiple para cuantificar la magnitud de los cambios de la 17OHP por cada unidad de cambio de EG y PN. La presentación de los resultados se realizó en tablas de contingencia en números absolutos y porcentajes. Los investigadores involucrados aseguran confidencialidad en relación con los datos obtenidos de las historias clínicas como fuente de información utilizada y la identidad de los pacientes estudiados. ]]>
RESULTADOS
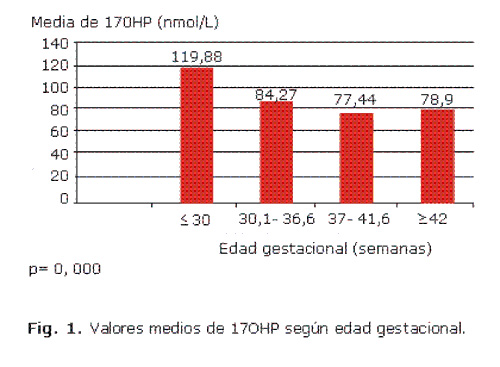
De los 1 114 pacientes con resultados FP de 17OHP en la pesquisa de HAC, 565 (50,7 %) pertenecían al sexo masculino y 549 (49,3 %) al sexo femenino. Se detectó que los valores medios de 17OHP de los varones fueron ligeramente superiores (80,6 nmol/L) con respecto a las determinaciones de las hembras (78,1 nmol/L), diferencias que no fueron significativas. Predominó el parto por cesárea en los casos con resultados FP de 17OHP en la pesquisa: 609 pacientes (54,7 %), el 43,3 % fue producto de un parto normal, y solo el 2 % nació a través de un parto instrumentado (p= 0,984). La media de los valores de 17OHP se comportó de forma similar en los nacidos por parto normal, por cesárea e instrumentado, con cifras de 79,33 nmol/L, 79,46 nmol/L y 80,27 nmol/L respectivamente, lo cual no resultó estadísticamente significativo. En las figuras 1 y 2 se observa que aquellos neonatos con menor EG y PN más bajo presentaron niveles medios de 17OHP más elevados en la pesquisa.
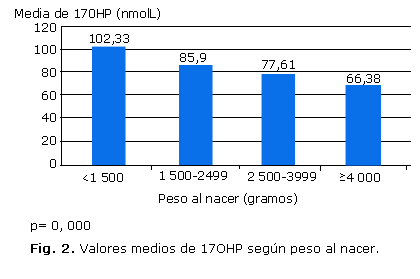
Al aplicar el coeficiente de correlación de Pearson se comprueba que existe una correlación inversa entre la EG y el PN con los valores de 17OHP, en ambos casos con significación estadística (p= 0,000). Cuando se utiliza un modelo de regresión se obtiene que por cada semana de gestación alcanzada, disminuye en 1,36 nmol/L el valor de 17OHP (p= 0,005). Por otra parte, por cada 1 000 g menos de PN, se incrementa el valor de 17OHP en 4 nmol/L (p= 0,031).
Del total de pacientes con 17OHP elevada, no confirmados de HAC, 914 (82 %) no presentaron SFA. En este grupo, la media de los valores en la pesquisa fue de 78,71 nmol/L, y en los que tuvieron eventos perinatales desfavorables (200 para un 18 %) fue de 82,68 nmol/L. Aunque en este último grupo fueron ligeramente más elevados, no se encontraron diferencias con significación estadística (p= 0,054).
En la mayoría de los pacientes estudiados (68,1 %) normalizaron los valores de 17OHP al cumplir un mes de vida, independientemente del tipo de parto. El tiempo medio de normalización fue de 1,35 meses para los nacidos por cesárea, de 1,27 y 1,23 meses para los nacidos por parto normal e instrumentado, respectivamente. Aunque no se encontró correlación significativa entre el tipo de parto y el tiempo de normalización de los niveles hormonales, de los 320 lactantes (28,7 %) que mantuvieron cifras elevadas durante 2 meses o más, 193 pertenecían al grupo de los nacidos por cesárea, lo que se correspondió con el 60,3 % de estos casos. ]]>
Predominó la normalización de las cifras de 17OHP al cumplir un mes de nacido, tanto en los RN pretérmino como los que nacieron a término y postérmino (50, 74 y 77 % respectivamente). El porcentaje de neonatos que demoró más de un mes en alcanzar niveles hormonales adecuados, fue mayor en los nacidos antes de las 37 semanas (49 %), a diferencia de los nacidos a término (22 %) y los postérmino (15 %), lo cual tuvo significación estadística (p= 0,000).
En la figura 3 se evidencia que la EG media fue menor en los RN que requirieron mayor tiempo para la normalización de los niveles plasmáticos de 17OHP, y se encontró una asociación con significación estadística. En los neonatos que presentaron cifras normales a los 15 días (0,5 mes) y al cumplir el primer mes de vida, la EG media fue de 38,6 y 38,3 sem respectivamente, mientras que quienes tardaron 2 y 3 meses, tuvieron una EG media de 36,6 y de 36,1 sem respectivamente, ambas correspondientes con la categoría de pretérmino. Solo 7 casos, con EG media de 37,2 sem (cercana al rango de prematuridad), mantuvieron la 17OHP elevada durante 4 meses.
Los pacientes con muy bajo PN no comenzaron a normalizar los niveles séricos de 17OHP hasta los 2 meses de vida, y en esa etapa lo hizo el 75 %. En los RN con bajo peso se encontró que aproximadamente la mitad de los casos (52 %) se normalizó al cumplir un mes de nacido, mientras que más del 70 % (72 y 83 %) de aquellos con peso normal o alto, ya presentaron cifras normales en este período, lo cual tuvo significación estadística (p= 0,000). ]]>
En la figura 4 se evidencia que aquellos neonatos que demoraron más tiempo en alcanzar cifras normales de 17OHP, presentaron PN medio menores, y se constataron diferencias estadísticamente significativas entre los grupos estudiados. Los 7 neonatos que tardaron 4 meses en normalizar la 17OHP, tuvieron un PN medio adecuado, pero presentaron otras enfermedades posnatales asociadas que no constituyeron objetivo de este estudio. Al aplicar una prueba de correlación de Pearson se demuestra que existe una correlación inversa de la EG y el PN, con el tiempo de normalización de la 17OHP (p= 0,000). Cuando se emplea la regresión lineal se comprueba que por cada semana de EG no ganada, se incrementa el tiempo de normalización en un día, lo cual es estadísticamente significativo (p= 0,000). Sin embargo, el incremento de hasta 1 000 g de PN, no produjo modificaciones significativas desde el punto de vista estadístico en el momento de la normalización.
Predominó la normalización de la 17OHP al cumplir un mes de vida en ambos grupos, 118 casos (59 %) con SFA y 641 (70,1 %). En cada uno de los períodos analizados, la distribución de casos fue equitativa. Al compararlos, no se obtuvieron diferencias estadísticamente significativas, aunque el tiempo medio de normalización de la 17OHP fue de 1,4 meses para quienes tuvieron SFA, y de 1,2 meses para los que no lo tuvieron.
Al determinar el valor medio de 17OHP, se encontró que en el grupo con resultados FP fue de 79,42 nmol/L, el 42,4 % tuvo cifras por encima de 75 nmol/L, y solo el 0,98 % presentó determinaciones mayores de 200 nmol/L en la pesquisa. En los enfermos no pudo establecerse un valor promedio de la hormona en estudio, porque los informes no reportan valores exactos, pero sí es llamativo que el 78,26 % tuvo valores superiores a 75 nmol/L y el 43,47 % exhibió cifras que superaron el último punto de la distribución, establecido en 200 nmol/L.
]]>
El tipo de parto que predominó en los neonatos con resultados FP en la pesquisa de HAC fue la cesárea (54,7 %), mientras que el 72,8 % de los RN con valores normales, nació por parto normal. Al comparar ambos grupos, se obtuvieron diferencias estadísticamente significativas. En los enfermos predominó también el parto normal (57,1 %), pero no hubo diferencias significativas con el grupo de estudio (figura 5).
La media de la EG en los neonatos con resultados FP de 17OHP fue de 37,6 sem, con un tiempo de gestación mínimo de 27 sem y máximo de 42,2. Quienes presentaron resultados normales nacieron a las 39,1 sem de gestación como promedio (intervalo de 26-43 sem), y los enfermos de HAC tuvieron una EG media de 39,2 sem (EG mínima 35,6-máxima 41,5 sem), con diferencias estadísticamente significativas, lo cual queda expuesto en la figura 6.
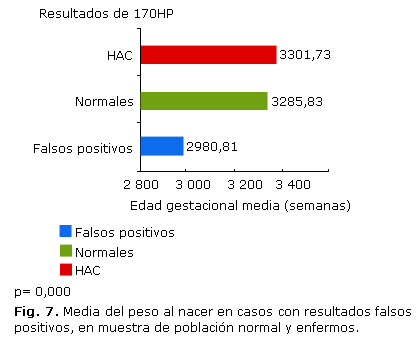
En la figura 7 se observa que el PN fue significativamente menor en los casos con resultados FP, comparados con los RN enfermos y aquellos con resultados normales de 17OHP. El grupo de los pacientes con HAC tuvo un PN medio de 3 301,73 g (intervalo 2 200 g-4 050 g), los que tuvieron valores normales de 17OHP mostraron una media de 3 285,83 g (mínimo 1040 g-máximo 5 260 g), mientras que los RN con FP presentaron peso medio de 2 980,81 g (intervalo 976 g-5 050 g).
]]>
DISCUSIÓN
Los programas de pesquisa neonatal están dirigidos a la identificación presintomática de determinados estados genéticos, metabólicos o endocrinos mediante el uso de pruebas que pueden ser aplicadas a toda la población de RN.24 En el caso de la HAC, a diferencia de otras enfermedades diagnosticadas mediante detección neonatal, se dispone de menos tiempo para prevenir sus consecuencias, pues la crisis suprarrenal se presenta habitualmente entre la 2ª y 3ª semana de vida.4,6,8,15,18,20,21,25
En Cuba, se decidió emplear 55 nmol/L como nivel de corte y asumir un 2 % de resultados FP. Se diseñó, además, un protocolo específico para el seguimiento de los casos con resultados elevados de 17OHP, lo cual asegura la evaluación sistemática desde el punto de vista clínico, bioquímico y psicológico, de los casos confirmados de HAC y la discriminación de aquellos con resultados falsos positivos.18 A pesar de la alta precisión de las pruebas de pesquisa y de la baja prevalencia de la HAC, solo aproximadamente 1-2 de cada 100 RN con resultados positivos tendrá la enfermedad, pues existen numerosas causas que influyen en los valores de 17OHP en el período neonatal.26
Algunos autores han encontrado niveles medios de 17OHP ligeramente superiores en los varones, comparado con los de las hembras,15,18,27 lo cual se corresponde con los resultados obtenidos en esta investigación. Se presume que existen diferencias según el sexo, probablemente los varones sanos tienen niveles más altos de 17OHP. Esto se ha propuesto como explicación de la preponderancia del sexo masculino entre quienes requieren repetir la toma de muestra (proporción M:F, 2,2:1), así como de la discreta disminución de la sensibilidad de la pesquisa neonatal en las niñas. No obstante, en la literatura revisada no se encontraron estudios previos que hayan identificado al sexo como factor de riesgo en las tasas de FP.15,27 Sin embargo, debido a que la HAC es un trastorno autosómico recesivo, el número de casos con deficiencia de 21 hidroxilasa diagnosticados a través del tamizaje neonatal, no exhibe diferencias en cuanto al sexo. En ausencia de pesquisa, se detectan mayor cantidad de niñas, lo que hace suponer la existencia de una mortalidad por HAC no reconocida entre los varones.15,28 En Cuba han sido diagnosticados 17 hembras y 18 varones desde el inicio del programa, con una proporción mantenida de 1:1.23 ]]>
En relación con el tipo de parto, no se encontraron diferencias significativas en cuanto a los valores medios de 17OHP en esta investigación. No obstante, predominó el nacimiento por cesárea entre los casos con resultados FP en la pesquisa, con un comportamiento similar a lo reportado por González y otros,18 quienes señalan que los nacidos por partos distócicos presentaron niveles de 17OHP ligeramente superiores a los de parto eutócico, con un incremento al doble del porcentaje de muestras elevadas. Consideramos que esto pudiera estar en relación con los eventos perinatales desfavorables, que se asocian con frecuencia a las distocias del parto. Estos resultados discrepan con los obtenidos por Metz,29 quien no encontró influencia negativa del modo de parto en los valores de 17OHP, aunque estudió una serie pequeña de solo 88 niños.
Uno de los principales problemas que se afrontan en los programas de pesquisa, es que los niveles de 17OHP pueden encontrarse elevados en prematuros (especialmente en aquellos con menos de 31 sem de gestación), o con bajo peso al nacer, sin que presenten ningún error congénito en la biosíntesis de esteroides. En ellos existe una disminución de la actividad de la 3-beta-hidroxiesteroide-deshidrogenasa, y cuando son menores de 30 sem de EG, aparece una disminución de la actividad de la 11-beta-deshidrogenasa o un retraso en la expresión de esta enzima, lo cual justifica la elevación de dicho metabolito.8,30
El perfil esteroideo en pretérminos sugiere una deficiencia funcional de varias enzimas esteroidogénicas, con un nadir en la función a las 29 sem de gestación.15 La alta incidencia de FP en prematuros, probablemente se relaciona, además, con una degradación de 17OHP disminuida por inmadurez de la función hepática, a lo que se suma una producción aumentada de la hormona a causa del estrés al que están sometidos estos neonatos.4,31 El pretérmino severamente enfermo muestra unos niveles elevados de 17OHP, sobre todo, hacia el quinto día, que junto con la elevación concomitante de cortisol, hacen suponer que se encuentra en una situación de estrés importante.1,30 Todo esto hace difícil definir un valor de corte único para todos los recién nacidos, ya que los prematuros aumentan significativamente la tasa de falsos positivos.4,15,26,32 En la muestra estudiada, así como en otras investigaciones realizadas (González EC, Frómeta A, García CM, Díaz A, Hernández J, Socorro C, et al. Niveles de 17a-hidroxiprogesterona en recién nacidos con resultados elevados en el pesquisaje neonatal de hiperplasia suprarrenal congénita. Trabajo presentado en 2do. Congreso cubano de Endocrinología Pediátrica y de la Adolescencia; 2006 nov 29-dic 1. La Habana, Cuba) (González EC. Factores que influyen en los resultados del tamiz neonatal de la HAC: la experiencia cubana. Trabajo presentado en 7mo. Congreso Internacional y Latinoamericano de Errores Innatos del Metabolismo y Tamiz Neonatal; 2009. México),15,18,28,29,31-34 la prematuridad se ha correlacionado significativamente con el aumento de la 17OHP en sangre, incluso se ha planteado que la EG es el mejor predictor de las concentraciones plasmáticas de este metabolito, y se estima que puede ser más específico que el peso al nacer, a pesar de que su determinación es menos fidedigna. Una explicación pudiera ser que la EG se relaciona más con el desarrollo de la glándula suprarrenal en el feto que el PN.
No obstante, el retardo del crecimiento fetal también se relaciona positivamente con los niveles de hormona liberadora de corticotropina (CRH), ACTH y cortisol; y negativamente, con las cantidades de dehidroepiandrosterona sulfato (DHEA-S). En los embarazos con insuficiencia útero-placentaria y con afectación del medio ambiente uterino, la CRH parece regular el eje adrenal y aumentar la secreción del cortisol fetal.35
Adicionalmente, los RN hipotróficos presentan diferentes trastornos metabólicos, de los cuales la hipoglucemia es el más frecuente. En general, existe un control inadecuado de la glucemia, y es probable que estos neonatos secreten hormonas hiperglucemiantes (hormona de crecimiento, adrenalina, cortisol, glucagón, y tal vez, hormonas tiroideas) para mantener sus niveles de glucemia compatibles con la vida.36
Respecto a la influencia del peso al nacer, muchos autores (González EC. Factores que influyen en los resultados del tamiz neonatal de la HAC: la experiencia cubana. Trabajo presentado en 7mo. Congreso Internacional y Latinoamericano de Errores Innatos del Metabolismo y Tamiz Neonatal; 2009. México)1,4,18,26,27,32-34 coinciden en que los valores de 17OHP en los neonatos con peso menor de 2 500 g, son significativamente superiores a los obtenidos en los normopeso, diferencias que son aún más ostensibles al compararlos con las cifras de aquellos con muy bajo peso al nacer (<1 500 g). González18 ha informado que el porcentaje de muestras que se encuentran por encima del nivel de corte en los bajo peso es superior al obtenido en el grupo de neonatos eutróficos (10,6 % en menores de 2 500 g, frente a 1,2 % en los de más de 2 500 g). Un comportamiento similar se apreció en la población estudiada, en la que se incrementó la frecuencia de resultados elevados de 17OHP con la disminución del PN, lo cual conllevó a la repetición de la prueba, pues no se han establecido puntos de corte basados en este parámetro. Aunque no está universalmente aceptado, el parámetro más útil para la estratificación de los resultados de la pesquisa de HAC, se ha propuesto que la especificidad puede mejorar utilizando niveles de corte ajustados preferiblemente a la EG, más que al peso natal.26,34
El estrés intrauterino parece estimular la síntesis de esteroides fetales a través de la activación del eje hipotálamo-hipófisis-adrenal.26 Se conoce que los diferentes tipos de estrés aumentan la secreción de ACTH, a través de acciones centrales mediadas por la CRH y la arginina vasopresina (AVP). Es posible que la CRH placentaria, al igual que la hipotalámica, se estimulen en condiciones de estrés crónico, y modulen el eje adrenal fetal en los embarazos con alto riesgo.35
La secreción de cortisol también aumenta en respuesta a la fiebre, la cirugía, la hipoglucemia, la hipotensión, el esfuerzo y otras situaciones, en las cuales este fenómeno se considera una respuesta contrarreguladora normal a la agresión. De modo crónico (en 24 a 26 h de exposición), la ACTH actúa para aumentar todas las enzimas CYP esteroidogénicas (CYP11A1, CYP17, CYP21A2, CYP11B1), además de la adrenodoxina, efectos que ejerce a nivel transcripcional.9 ]]>
En niños sometidos a estrés fetal prolongado, se han hallado niveles medios de 17OHP mayores comparados con los de quienes presentan estrés relativamente breve (85,7 nmol/L frente a 54,6 nmol/L, p< 0,001), y la elevación ha sido mayor en aquellos con crecimiento intrauterino retardado sobreañadido (99,8 nmol/L).37Probablemente la hipoxia fetal sea la noxa más común de la vida intrauterina, la disminución del 40 % en la presión de oxígeno arterial fetal provoca un aumento importante de la concentración plasmática fetal de ACTH y cortisol.38 Niveles elevados de este glucocorticoide son característicos de los recién nacidos pretérminos, debido a infecciones amnióticas o preeclampsia. Por estas razones, se ha propuesto que la 17OHP, precursora del cortisol, podría ser utilizada como un marcador de la severidad del estrés intrauterino de duración relativamente larga.37 Varios estudios han demostrado que el estrés neonatal, ciertamente, causa elevaciones de la 17OHP en recién nacidos no enfermos.8,10,15,22,26,28,31,37 Otros reportes29 no han encontrado relación entre el estrés perinatal y estas determinaciones hormonales, con lo que coinciden nuestros resultados, en los que predominaron los pacientes que no tuvieron sufrimiento fetal agudo. Tampoco se observaron diferencias significativas en cuanto a los valores medio de 17OHP en la pesquisa, al comparar los neonatos con sufrimiento fetal y sin él. Esto podría explicarse, pues solo se contó con datos vinculados con estrés agudo, ya que en las historias clínicas no se encontraron referencias de sufrimiento fetal crónico, lo cual impidió el análisis de su influencia en la elevación de esta hormona.
Normalmente, existe un aumento de la CRH relacionado con el inicio del parto, lo que provoca una estimulación de la esteroidogénesis adrenal fetal para satisfacer las altas demandas de dehidroepiandrosterona (DHEA: principal fuente de estradiol placentario). De este modo, aumenta también la síntesis de cortisol, hormona que determina la maduración de los órganos fetales, aumenta la producción de surfactante pulmonar, así como el almacenamiento de glucógeno en el hígado, los músculos y el corazón fetal, todo lo cual prepara al feto para resistir la hipoxia durante el parto y para mantener la glucemia en las primeras horas de vida extrauterina.35 Por estas razones, los niveles de 17OHP son elevados al nacer, lo que se considera un alza fisiológica en respuesta al estrés propio del parto, pero disminuyen con rapidez, aproximadamente 5 veces, al segundo día de vida. En el prematuro estas cifras pueden ser 2 o 3 veces más elevadas, y permanecer altas durante algunas semanas.1,7,8,12,25,39
Se conoce que en algunos lactantes los niveles séricos de 17OHP se normalizan lentamente, por lo que deben ser evaluados hasta la obtención de los valores reglamentados. Es muy importante conocer el comportamiento habitual en cada caso, pues permite definir el tiempo de confirmación y seguimiento en los RN con resultados elevados en la pesquisa (González EC, Frómeta A, García CM, Díaz A, Hernández J, Socorro C, et al. Niveles de 17a-hidroxiprogesterona en recién nacidos con resultados elevados en el pesquisaje neonatal de hiperplasia suprarrenal congénita. Trabajo presentado en el 2do. Congreso Cubano de Endocrinología Pediátrica y de la Adolescencia; 2006 nov 29-dic 1. La Habana, Cuba) (González EC. Factores que influyen en los resultados del tamiz neonatal de la HAC: la experiencia cubana. Trabajo presentado en el 7mo. Congreso Internacional y Latinoamericano de Errores Innatos del Metabolismo y Tamiz Neonatal; 2009. México).
Linder y otros40 reportaron que en los prematuros, los valores medio de 17OHP se mantuvieron elevados a los 7 días de vida, con disminución brusca en la segunda sem, después de lo cual experimentaron un descenso gradual, para alcanzar niveles normales a los 90 días de vida. Sin embargo, en los nacidos a término, la media de 17OHP se normalizó a los 3 días. Estos valores fueron independientes de la presencia y severidad del distrés respiratorio y del uso prenatal de esteroides. González también encontró que los niveles de 17OHP se normalizaron lentamente (tiempo medio de 36 días), y se observó que los RN a término tardaron 28 días, mientras que los prematuros o bajo peso, demoraron 45 días como promedio. En otra serie, el mismo autor obtuvo que el 80 % de los neonatos normalizó las cifras de 17OHP antes del mes de nacido, pero en un prematuro fue necesario realizar el seguimiento hasta los 80 días de vida; las diferencias encontradas estuvieron marcadamente influidas por la EG y el PN (González EC, Frómeta A, García CM, Díaz A, Hernández J, Socorro C, et al. Niveles de 17a-hidroxiprogesterona en recién nacidos con resultados elevados en el pesquisaje neonatal de hiperplasia suprarrenal congénita. Trabajo presentado en el 2do Congreso Cubano de Endocrinología Pediátrica y de la Adolescencia; 2006 nov 29-dic 1. La Habana, Cuba).
Los resultados de nuestro estudio fueron similares a los de estas investigaciones, pues la mayoría de los pacientes normalizó los valores de 17OHP al cumplir el primer mes de vida. No se halló correlación significativa entre el tipo de parto y el tiempo de permanencia de la elevación de esta hormona, pero se evidenció la influencia significativa de la EG y el PN, sobre el tiempo requerido para la normalización de los niveles plasmáticos de 17OHP, el cual fue mayor en los neonatos con menor EG y en aquellos con menor PN, con tendencia evidente a aumentar este período, conforme disminuyeron dichos parámetros. El grupo que requirió de un tiempo mayor (4 meses) presentó una EG media cercana al rango de prematuridad, sin embargo, exhibió un PN medio adecuado, lo que nos hace pensar que, probablemente, la EG tiene mayor influencia en la duración de la elevación hormonal.
Se ha considerado que el sufrimiento fetal también contribuye a las elevaciones persistentes de la hormona, tanto en los recién nacidos pretérmino como a término, no obstante se señala que los valores raramente exceden a 2 mg/dL (66 nmol/L).3 En esta investigación no se demostró la influencia del estrés agudo sobre el tiempo requerido para la normalización de los niveles de este metabolito; y en la búsqueda realizada se encontró escasa bibliografía que hiciera referencia al tiempo de normalización, lo cual pudiera estar en relación con varios aspectos, uno de ellos es la existencia de puntos de corte ajustados a la EG y el PN, de gran utilidad para mejorar la especificidad diagnóstica, y una reducción en la tasa de recitados.1,4,8,15,18,30 Otros protocolos incluyen la determinación de metabolitos con menor variabilidad, según eventos perinatales, como el 11 desoxicortisol (producido por 11ß-hidroxilación de 17OHP), el cual no es normalmente secretado en grandes cantidades, incluso en pretérminos, por lo que los niveles elevados de este esteroide se consideran altamente específicos de la deficiencia de 21 hidroxilasa.15
El período de seguimiento puede reducirse también, con un segundo nivel de tamizaje más específico, basado en la detección de las mutaciones conocidas del CYP21A2, que pueden ser detectadas, incluso, en el ADN extraído de la misma muestra de sangre seca usada para la pesquisa.1,12,15,26,35,41,42 Existen laboratorios que incorporan la cromatografía líquida seguida de la espectrometría de masa para perfil esteroideo, con el objetivo de mejorar la especificidad del test de HAC.15,18,26,27,34,42 Todo esto permite confirmar el diagnóstico presuntivo desde etapas muy tempranas, y evita además la necesidad de controles periódicos y de estudios hormonales de confirmación, así como la prolongación del tiempo de seguimiento para descartar los falsos positivos,10,12,15,20 aunque la mayoría de los autores coincide en lo costoso de la implementación de estos estudios.15,18,26,27,34,42
]]>
Al comparar los valores de 17OHP en la pesquisa, se observó que los RN con diagnóstico de HAC mostraron en un mayor por ciento, cifras por encima del último punto de la curva de distribución, lo cual no ocurrió en los falsos positivos. Esto nos hace pensar que los valores por encima de 200 nmol/L corresponden con mayor probabilidad a un neonato enfermo. A pesar de emplearse diferentes ensayos en los programas de detección temprana de HAC (RIA, ELISA, DELFIA), lo cual no hace comparable los valores hormonales, los autores coinciden en que en niños no enfermos, las cifras de 17OHP usualmente decrecen con la edad, mientras que en niños con HAC aumentan progresivamente, siendo más elevadas en aquellos con formas clásicas de la enfermedad respecto a las no clásicas.6,7,17,26,33,42,43En cuanto al comportamiento de los factores perinatales estudiados, se encontró que predominó el parto por cesárea en los pacientes con resultados falsos positivos de 17OHP, mientras que la mayoría de los RN con valores normales y los enfermos nacieron por parto normal.
Tanto la media de la EG, como la del PN, fueron significativamente menores en los RN con FP en la pesquisa, comparados con los casos con determinaciones normales y los enfermos. Estos aspectos pueden ayudar a establecer un diagnóstico diferencial en aquellos neonatos que presenten valores elevados de 17OHP, pues estos resultados son similares a los de otros estudios en los que predominan los pacientes nacidos a término y normopeso, entre los casos confirmados de HAC.8,43 De hecho, se ha reportado que la duración de la gestación en pacientes con esta enfermedad, se encuentra dentro de los límites normales, mientras que los datos acerca del PN no han sido concluyentes, aunque se ha asumido que tanto el PN como la EG de los enfermos, son similares a los de la población de RN sanos.34 Todo esto corrobora nuestra hipótesis de la relación inversa entre el PN y la EG, con la elevación de este metabolito en neonatos no afectados de HAC. Cuando se analiza el intervalo de ambos parámetros en los grupos, se observa mayor similitud entre los falsos positivos y los normales, con respecto a los pacientes con diagnóstico de HAC.
Estos son elementos que deben tenerse en cuenta cuando se presente un neonato bajo peso o pretérmino con resultados elevados en la pesquisa, lo cual puede orientar hacia la probabilidad de un resultado FP. Además, podrá ser un punto de partida para la implementación de un algoritmo de trabajo en los RN con estas peculiaridades, lo que disminuirá, en gran medida, el estrés familiar relacionado con la incertidumbre del diagnóstico, y a su vez, contribuirá a la reducción de los costos de la pesquisa.
Se concluye señalando que la prematuridad y el bajo peso al nacer tuvieron una influencia significativa sobre la elevación de los valores de 17OHP. El tipo de parto y SFA no se relacionaron con los resultados de la pesquisa. Predominó la normalización de los valores de 17OHP al cumplir 1 mes de vida. El tipo de parto y el SFA no se relacionaron con la persistencia de la elevación de la hormona. Los neonatos con menor EG y bajo PN, requirieron mayor tiempo para la normalización de la 17OHP.
La media de la EG y del PN en los recién nacidos con resultados FP fue menor que la de los neonatos con resultados normales y los enfermos, y el tipo de parto que predominó fue la cesárea en el primer grupo, y el parto normal en los grupos restantes. Con estos resultados se plantea la necesidad de ajustar los valores de corte atendiendo a la EG y el PN, por ser los factores que influyen más significativamente en los resultados de 17OHP en la pesquisa neonatal; además, utilizar otros marcadores, junto a la determinación de los niveles de 17OHP en suero, podrían ayudar a una confirmación más rápida y efectiva de la HAC. Tanto para la pesquisa como para el confirmatorio, se sugiere aumentar la dilución para obtener un valor más exacto que permita evaluar la evolución bioquímica del paciente, así como la respuesta al tratamiento, y finalmente implementar una nueva estrategia de trabajo, evaluación y seguimiento de los pacientes con resultados elevados en la pesquisa, tomando en consideración la presencia de los factores perinatales que influyen significativamente en la elevación transitoria de estos valores.
REFERENCIAS BIBLIOGRÁFICAS ]]>
1. Rodríguez-Arnao MD, Rodríguez A, Badillo K, Velasco A, Dulín E, Ezquieta B. Déficit de 21- hidroxilasa: aspectos actuales. Rev Endocrinol Nutr. 2006;53(2):124-36.
2. Bouvattier C, Chatelain P. Congenital adrenal hyperplasia Rev Prat. 2008;58(9):990-4.
3. Sepúlveda AJ. Hiperplasia adrenal congénita. Rev Chil Obstet Ginecol. 2003;68(1):28-31.
4. Cattani OA, Reyes GM, Azócar PM, Soto MJ, Romeo OE, Valdivia VL, et al. Medición de 17OH progesterona sanguínea en recién nacidos chilenos: antecedentes para implementar un programa de detección neonatal de hiperplasia suprarrenal congénita. Rev Méd Chile. 2000;128(10):1113-8.
5. Navaroli FF. Hormonas. Algunas consideraciones teórico-prácticas. Métodos de determinación. Interpretación de los resultados. INEN, 2005. (Comunicación personal). ]]>
6. Soriano GL, Velázquez de Cuéllar PM. Hiperplasia suprarrenal congénita. Rev Pediatr Integral. 2007;11(7):601-10.
7. Forest MG, Castro Feijó L. Hiperplasia suprarrenal congénita. En: Pombo M. Tratado de endocrinología pediátrica. 3ra ed. Madrid: McGraw-Hill Interamericana; 2002. p. 970-1005.
8. Gebara E, Fernández MA, Rojas E, Amina A, López MR. Hiperplasia suprarrenal congénita perdedora de sal en varones durante el período neonatal ¿Es posible adelantarse a la emergencia metabólica? Arch Argent Pediatr. 2009;107(4):369-73.
9. Stewart PM. La corteza suprarrenal. En: Kronenberg HM, Shlomo M, Polonsky KS, Reed Larsen P. Williams Tratado de Endocrinología. 11na ed. USA: Saunders Elsevier Inc; 2008. p. 495-8.
10. Mustafa R, Hashmi HA, Ullah S. Congenital adrenal hyperplasia causing clitoromegaly. J Coll Physicians Surg Pak. 2008;18(6):378-9. ]]>
11. Sahai I, Marsden D. Newborn screening. Critical Reviews in Clinical Laboratory Sciences. 2009;46(2):55-82.
12. Labarta JI, Bello E, Ruiz-Echarri M, Rueda C, Martul P, Mayayo E, et al. Estado en la edad adulta y propuesta de optimización terapéutica de la hiperplasia suprarrenal congénita. An Pediatr Barc. 2003;58(2):12-34.
13. Warman M, Rivarola MA, Belgorosky A. Hiperplasia Suprarrenal Congénita. Déficit de la enzima 21-Hidroxilasa. Revista de Endocrinología Ginecológica y Reproductiva [serie en internet]. 2008 [citado 3 de septiembre de 2010];3(1). Disponible en: http://ttvps.com/saegre/revista/numeros/2008/n1/3_hiperplasia.pdf
14. Votava F, Török D, Kovack S, Möslinger D, Baumgartner-Parzer SM, Sólyom J, et al. Estimation of false negative rate in newborn screening for congenital adrenal hyperplasia. Eur J Endocrinol. 2005;152(6):869-74.
15. White PC. Neonatal screening for congenital adrenal hyperplasia. Nature Reviews Endocrinology. 2009;5(9):490-8.
16. Yoo B, Grosse S. The cost effectiveness of screening newborns for congenital adrenal hyperplasia. Public Health Genomics. 2009;12(2):67-72.
17. Chaler E, Domené H, Muñoz L, Ruibal G. El laboratorio en la patología endocrinopediátrica. Rev argent endocrinol metab. 2007;44(3):95-8.
18. González RE. Desarrollo de ultramicroensayos para el diagnóstico de la deficiencia de biotinidasa y la HAC en el programa cubano de pesquisa neonatal [tesis doctoral]. Centro de Inmunoensayo. La Habana; 2009.
19. Nordenström A, Wedell A, Hagenfeldt L, Marcus C, Larsson A. Neonatal screening for congenital adrenal hyperplasia: 17-hydroxyprogesterone levels and CYP21 genotypes in preterm infants. Pediatrics. 2001;108(4):1-8.
20. Speiser P. Prenatal and neonatal diagnosis and treatment of congenital adrenal hyperplasia. Hormone Research. 2007;68 Suppl:590-2.
21. González EC, Marrero N, Pérez PL, Frómeta A, Zulueta O, Herrera D, et al. An enzyme inmunoassay for determining 17 hydroxyprogesterone in dried blood spots on filter paper using an ultramicroanalytical system. Clin Chem. 2008;acta 394:63-6.
22. White PC, Speiser PW. Congenital adrenal hyperplasia due to 21-hydroxilase deficiency. Endocrine Reviews. 2000;21(3):245-91.
23. Tecnosuma. Informe anual de programas. 2010. (Comunicación personal).
24. González-Lamuño D. Screening metabólico neonatal expandido. Bol Pediatr. 2008;48:329-31.
25. Al Saedi S, Dean H, Dent W, Stockl E, Cronin C. Screening for congenital adrenal hyperplasia: the Delfia screening test overestimates serum 17-hydroxyprogesterone in preterm infants. Pediatrics. 1996;97:100-02.
26. Speiser PW, Azziz R, Baskin LS, Ghizzoni L, Hensle TW, Merke DP, et al. Congenital Adrenal Hyperplasia Due to Steroid 21-Hydroxylase Deficiency: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2010;95(9):4133-60.
27. Gleeson H, Wiley V, Wilcken B, Elliott E, Cowell C, Ambler G, et al. Two-year pilot study of newborn screening for congenital adrenal hyperplasia in New South Wales compared with nationwide case surveillance in Australia. Journal of Paediatrics and Child Health. 2008;44(10):554-9.
28. Scott D, Van Vliet G. How Many Deaths can be prevented by Newborn Screening for Congenital Adrenal Hyperplasia? Hormone Research. 2007;67:284-91.
29. Metz C, Morvan CH. Prematuridad y despistaje neonatal de la hiperplasia congénita de las suprarrenales por déficit de 21-hidroxilasa. Journal D'endocrinologie Pediatrique [serie en internet]. 2001 [citado 21 de noviembre de 2010];2(3). Disponible en: http://pediatrics.aappublications.org
30. Licourt D, Pérez M. Déficit de 21-hidroxilasa: aspectos actuales. Rev Ciencias Médicas. Pinar del Río [serie en internet]. 2009 [citado 21 de noviembre de 2010];13(1). Disponible en: http://scielo.sld.cu/scielo.php?pid=S1561-31942009000100014&script=sci_arttext
31. Ochetti M, Sobrero G, Silvano L, Nieva V, Dipoi M, Tkalenko N, et al. Pesquisa neonatal de Hiperplasia Adrenal Congénita: niveles de corte de 17OH progesterona en una población de Córdoba, Argentina 2010 [monografía en internet] [citado 21 de noviembre de 2010]. Disponible en: http://www.cobico.com.ar/wp-content/archivos/Trabajo-Dra-Ochetti-2010-final.pdf
32. Slaughter J, Meinzen-Derr J, Rose SR, Leslie N, Chandrasekar R, Linard S, et al. The Effects of Gestational Age and Birth Weight on Newborn-Screening. Pediatrics. 2010;126(5):910-6. ]]>
33. Kaye CI. Newborn Screening Fact Sheets. Pediatrics. 2006;118(3):934-63.
34. Van der Kamp H, Oudshoorn CG, Elvers BH, van Baarle M, Otten BJ, Wit J, et al. Cutoff levels of 17-hydroxyprogesterone in neonatal screening for congenital adrenal hyperplasia should be based on gestational age rather than on birth weight. J Clin Endocrinol Metab. 2005;90:3904-7.
35. Hung Llamos S. Endocrinología de la gestación. En: Hung Llamos S. Endocrinología en ginecología. Tomo I. La Habana: Editorial Ciencias Médicas; 2006. p. 52-80.
36. Porto AS, González MB, Santurio AM, Domínguez F. Recién nacido de alto riesgo. En: Colectivo de autores. Pediatría. Tomo 1. La Habana: Editorial Ciencias Médicas; 2006. p. 348-59.
37. Ersch J, Beinder E, Stallmach T, Bucher HU, Torresani T. 17-Hydroxyprogesterone in premature infants as a marker of intrauterine stress. J Perinat Med. 2008;36(2):157-60. ]]>
38. Matthews SG. Desarrollo del eje hipotálamo-hipofiso-adrenal. En: Pombo M. Tratado de endocrinología pediátrica. 3ra ed. Madrid: McGraw-Hill Interamericana; 2002. p. 186-95.
39. Al Saedi S, Dean HJ, Dent W, Cronin C. Reference ranges for serum cortisol and 17-hydroxyprogesterone levels in preterm infants. J Pediatr. 1995;126:985-7.
40. Linder N, Davidovitch N, Kogan A, Barzilai A, Kuint J, Mazkeret R, et al. Longitudinal measurements of 17 alpha-hydroxyprogesterone in premature infants during the first three months of life. Arch Dis Child Fetal Neonatal. 1999;81(3):175-8.
41. Soardi FC, Lemos-Marini SH, Borchers Coeli F, Gonçalves Maturana V, Duarte Barbosa da Silva M, Darin Bernardi R, et al. Heterozygosis for CYP21A2 mutation considered as 21-hydroxylase deficiency in neonatal screening. Arq Bras Endocrinol Metab. 2008;52(8):1388-92.
42. Fingerhut R. False positive rate in newborn screening for congenital adrenal hyperplasia (CAH)-ether extraction reveals two distinct reasons for elevated 17alpha-hydroxyprogesterone (17OHP) values. Steroids. 2009;74(8):662-5. ]]>
43. Gruñieiro-Papendieck L, Chiesa A, Méndez V, Prieto L. Neonatal screening for congenital adrenal hyperplasia: experience and results in Argentina. J Pediatr Endocrinol Metab. 2008;21(1):73-8.
Recibido: 31 de agosto de 2011.
Aprobado: 30 de noviembre de 2011.
Tania Mayvel Espinosa Reyes. Instituto Nacional de Endocrinología. Calle Zapata y D, Vedado, municipio Plaza de la Revolución. La Habana. Cuba. Correos electrónicos: tania.espinosa@infomed.sld.cu taniaesp@gmail.com ]]>