Validación de métodos alternativos para análisis microbiológico de alimentos y aguas
Validation of alternative methods for the microbiological analysis of food products and water
Lic. Meylín Ortega González, Dr. C. Claudio Rodríguez Martínez, Dra. C. Raisa Zhurbenko
Centro Nacional de Biopreparados (BioCen). La Habana, Cuba.
]]>
El empleo de métodos microbiológicos alternativos para la detección de microorganismos es una herramienta importante para garantizar la inocuidad de alimentos y aguas. Numerosos y diversos métodos alternativos para microbiología se comercializan actualmente gracias a avances recientes, sobre todo en el campo de la biotecnología. Para que un nuevo método microbiológico sea aceptado, su fabricante debe demostrar su adecuación. En una primera revisión, se realizó el análisis de los principales parámetros determinados en la validación de los métodos microbiológicos cualitativos. El objetivo de esta segunda parte consiste en abordar los indicadores más importantes a considerar para los métodos microbiológicos cuantitativos.
Palabras clave: validación, métodos cualitativos, métodos alternativos, microbiología, estudios colaborativos.
INTRODUCCIÓN
En la actualidad, como resultado de avances vertiginosos en el campo de la biotecnología, la automatización y la microelectrónica son propuestos, por varios fabricantes, numerosos y diversos métodos alternativos implementados a su vez en muchas instituciones para la investigación microbiológica.1,2 Un número de tecnologías nuevas y heterogéneas han sido desarrolladas y ofrecen nuevos enfoques alternativos a la enumeración y detección de microorganismos en los alimentos.
Es fundamental el uso de métodos validados en cualquier sistema de calidad.3 En particular, la validación de los métodos microbiológicos es de vital importancia por la propia naturaleza de los organismos vivientes, los cuales muestran una considerable capacidad de variaciones genéticas y mutaciones.2 Es por tanto indispensable la validación de los métodos microbiológicos alternativos.4,5 La norma ISO 16140:20036 ha sido diseñada para cubrir esta necesidad tanto para los métodos cualitativos como cuantitativos.
El laboratorio debe asegurarse de escoger correctamente el método para el análisis, ajustándose al propósito en cuestión, en especial con los procedimientos de recuentos de microorganismos, y de esta manera obtener resultados efectivos.7
Se escoge la palabra "alternativo" con el propósito de indicar que los métodos estandarizados de referencia, como aquellos publicados por la Organización Internacional de Estandarización (ISO), mantendrán su relevancia en el comercio internacional. Los métodos de referencia son a menudo laboriosos, caros y consumidores de tiempo. En consecuencia, se prefieren para el uso rutinario métodos más económicos, rápidos y convenientes.
En la primera parte de esta serie de trabajos, se realizó una recopilación sobre los temas esenciales relacionados con la validación de los métodos alternativos, enfatizando en el análisis de los métodos cualitativos según ISO 161406 aplicados al análisis microbiológico de aguas y alimentos. En este caso, se dirigirá la atención hacia los métodos cuantitativos, también basándose, fundamentalmente, en el mismo estándar.
]]>
VALIDACIÓN DE UN MÉTODO MICROBIOLÓGICO CUANTITATIVO ALTERNATIVO
Un método cuantitativo es definido por ISO6 como un método de análisis, cuya respuesta es la cantidad del mesurando, medido directamente (ej. enumeración en una masa o en un volumen) o indirectamente (ej. absorbancia del color, impedancia, etc.) en una cantidad determinada de muestra. En el control de calidad de aguas y alimentos, su aplicación es esencial, pues permite detectar si el nivel de uno o más microorganismos se encuentra dentro de los rangos permisibles para la declaración de su inocuidad.
La validación en términos cuantitativos se expresa en forma de recuentos y son agrupados otros datos tales como: el peso de la muestra, las diluciones seriadas empleadas, el volumen de inóculo, así como los recuentos obtenidos en cada dilución.
Para el análisis de los resultados, se tienen en cuenta los recuentos de aquellas placas que tengan 300 unidades formadoras de colonias (UFC) o menos, y se aplica posteriormente el recálculo teniendo en cuenta el factor de dilución para obtener los valores finales. Según las recomendaciones de las guías de validación de organizaciones, como Internacional Organization for Standarization (ISO),6 Nordic System for Validation of Alternative Microbiological Methods (NordVal),8 Association of Official Analytical Chemists (AOAC),9 y el estándar internacional ISO 17994,10 específico para análisis de aguas, los resultados se transforman a logaritmos (log10) para obtener una función lo más cercana a la distribución normal. Este artificio matemático ha sido empleado por varios especialistas en el análisis estadístico de estudios colaboraborativos desarrollados aproximadamente a partir de la década de los años 80.
PARÁMETROS ESTABLECIDOS
Según ISO 16140:20036 se deben determinar los siguientes parámetros en la etapa intra-laboratorial:
Para lograr un óptimo diseño de análisis de regresión, se debe escoger un rango relevante y apropiado de concentraciones de analito. Los resultados repetitivos pueden ser eliminados, o no tener en cuenta las muestras con recuentos similares. En el caso específico de matrices líquidas, el rango puede ser obtenido por dilución.Para la confección del gráfico se utiliza el eje (vertical) para el método alternativo, y el eje X (horizontal) para el método de referencia. Los puntos a cada nivel deben formar una agrupación discreta. Posteriormente se analiza de manera visual el gráfico para detectar puntos aberrantes (obviamente fuera del cúmulo), descartando temporalmente los resultados y examinando cuidadosamente los puntos. Sin embargo, se conoce que los datos no siempre muestran una distribución normal (sino Gausiana), así que el rechazo de resultados resulta controversial teniendo en cuenta si refleja realmente la realidad de la posible variabilidad del método, además que reduce el número de valores para el análisis estadístico.11 El estándar ISO 16140 introduce un análisis estadístico robusto que tiene la ventaja a ser menos sensible a valores extremos. A. J. Hedges y B. Jarvis,15 en el año 2006, describieron técnicas para la aplicación de métodos robustos en el análisis de estudios colaborativos, utilizando datos cuantitativos, y convirtiendo sus datos artificialmente generados de igual manera.
LÍMITES DE DETECCIÓN Y CUANTIFICACIÓN
Nivel crítico: cantidad menor que puede ser detectada (no nula), pero no cuantificable como nivel exacto. Por debajo de este valor no podemos estar seguros de que el verdadero valor no es nulo.
El límite de detección (LOD) es mayor que el nivel crítico porque involucra, en términos estadísticos, el poder 1- b, la probabilidad de detectar significativamente un valor mayor que el nivel crítico (NC). Por otra parte, el límite de cuantificación (LOQ) puede definirse como la menor cantidad de analito (número de microorganismos), que puede ser medida y cuantificada con precisión y exactitud bajo condiciones experimentales por el método bajo validación. Para los métodos cuantitativos, LOQ=10 SO según AOAC.9
SENSIBILIDAD RELATIVA Y DETERMINACIÓN DE MUESTRAS DESCONOCIDAS ]]>
La sensibilidad relativa para los métodos cuantitativos se define como la habilidad del método para detectar el analito cuando es detectado por el método de referencia en una determinada matriz, a un determinado valor promedio o superior por todo el rango de medición, y que representa la mínima cantidad de variación (aumento de la concentración de analito X), la cual representa una variación significativa de la señal medida (respuesta y).
La sensibilidad es calculada para cada valor en el rango de medición, por lo que difiere del límite de detección. Este análisis se emplea, como un estimado de la sensibilidad, con el objetivo de cerciorarse de que los valores proporcionados por el método alternativo no difieren marcadamente de los del método de referencia (menos del 30 % en la diferencia). El protocolo de medición a emplear es el mismo a utilizar para la determinación de la linealidad.
Zhurbenko y otros,16 en el año 2006, mostraron los valores de la especificidad relativa alcanzados para las cepas de Salmonella en alimentos en los medios CromoCen AGN y agar entérico de Hektoen, agar verde brillante, agar sulfito bismuto y agar XLD, todos superiores el 94 %.
ESPECIFICIDAD, INCLUSIVIDAD Y EXCLUSIVIDAD
La especificidad es la habilidad del método de medir exactamente un analito determinado o su cantidad, dentro de la muestra y sin interferencia de componentes no diana como el efecto de la matriz o el ruido de fondo.
]]> Por otra parte, la selectividad es una medida del grado de no interferencia en presencia del microorganismo diana. Un método es selectivo si puede ser empleado para detectar el analito en estudio y puede garantizar que la señal detectada puede ser solo producto del microorganismo diana.ISO 161406 plantea que, en microbiología, para los métodos cuantitativos (excepto en los casos del recuento total en placa), la inclusividad y exclusividad se establecen por el análisis de al menos 30 cepas puras positivas (del microorganismo en estudio) y al menos 20 cepas puras negativas (otros microorganismos que causan interferencia) respectivamente.
Para el desarrollo del estudio se deben analizar y seleccionar, luego de un análisis, las cepas puras negativas y positivas que contaminan regularmente cada producto. En el caso de ser empleadas cepas que no provengan de una colección, es necesario llevar a efecto una identificación completa, y es obligatorio registrar el origen real de la cepa proveniente de los alimentos.
Puede ser analizado como diana o analito, un grupo indefinido de microorganismos (coliformes, levaduras), una familia (Enterobacterias), género (Staphylococcus, Klebsiella, Listeria), especies (Enterococcus avium, Proteus vulgaris), o una cepa específicamente (Salmonella enterica subsp. enterica ser. Typhi). En el caso de los microorganismos que no son de interés, tendrán prioridad para su selección aquellos que puedan ocasionar interferencia en la respuesta, como por ejemplo, en un medio de cultivo diseñado para la detección de Escherichia coli basado en su respuesta por actividad enzimática de b-galactosidasa y b-glucuronidasa, que no exista confusión con la respuesta de otro coliforme presente en la muestra.
El nivel de inoculación para cada una de las cepas puras es 100 veces mayor que el límite de detección y el ensayo se realiza por duplicado. Los resultados se expresan, de manera descriptiva, en lo relativo al límite de detección del microorganismo diana; no se necesitan cálculos. Si al analizar los parámetros inclusividad y exclusividad, encontramos alteraciones teniendo en cuenta los resultados pronosticados, esto afecta directamente la especificidad del método y se evalúa si el método alternativo cumple con las especificaciones del fabricante y con los requerimientos específicos para su uso confiable. Contrastando con este criterio de plasmar los resultados de este ensayo, algunos autores lo expresan en porcentajes.17,18.
ETAPA INTERLABORATORIAL
El estudio colaborativo tiene como objetivo determinar comparativamente las características del desempeño (exactitud y precisión) del método alternativo contra el método de referencia. El laboratorio organizador debe tener en cuenta aspectos específicos para la preparación y el transporte de las muestras, así como organizativos, para el desarrollo del estudio colaborativo.
]]> PREPARACIÓN Y TRANSPORTE DE LAS MUESTRAS DE ALIMENTOS
ORGANIZACIÓN DEL ESTUDIO COLABORATIVO
Antes de comenzar el ensayo, el laboratorio organizador debe proveer al resto de los laboratorios de procedimientos estándar de operación para que estos se familiaricen con los documentos y emitan sus comentarios, luego de ser especialmente instruidos, mediante un método estándar, en el recuento de las bacterias en la muestra designada. Además, todos los técnicos que participan en el estudio colaborativo, deben estar familiarizados con ambos métodos, el alternativo y el de referencia.
Otros factores, tales como calidad y composición de los medios de cultivo y reactivos empleados, control de las temperaturas y tiempo de incubación, recuentos de colonias, variabilidad entre analistas, entre otros, pueden tener un efecto significativo en los resultados y su interpretación. Es por esto que todos esos factores deben ser identificados y minimizados, y cualquier incidencia debe ser registrada para decisiones posteriores de inclusión o no en el análisis de los resultados. El laboratorio organizador debe proveer un cuestionario para que sean registrados todos los detalles posibles.
En el estudio colaborativo se determinan la exactitud, la precisión y los valores extremos. La exactitud se define como la relación entre los resultados de la prueba y los valores de referencia aceptados. La precisión es la cercanía de acuerdo entre valores independientes obtenidos bajo las condiciones estipuladas de repetibilidad y reproducibilidad.
Para la determinación de estos parámetros, el estudio interlaboratorio abarca, como mínimo, 8 laboratorios que den resultados sin valores extremos. La exactitud y precisión estimadas se calculan a partir de un amplio número de pruebas duplicadas, y dará un mínimo de 96 resultados (8 laboratorios x 2 métodos x 3 niveles de contaminación con el microorganismo diana x duplicado) para la matriz de alimento escogida, además de incluir un control negativo. Las muestras pueden ser contaminadas artificialmente. Para poder comparar ambos métodos (alternativo y de referencia), deben ser analizados con la misma muestra. El redondeo de los resultados se realiza por el laboratorio organizador (experto). Después de agrupar los resultados de cada laboratorio los datos para cada analito a cada nivel j, se presentan en forma de tabla.
Tal y como se había mencionado, en microbiología los datos no siempre muestran una distribución estadística normal,19 que puede ser, por ejemplo, una distribución gausiana). Es por esto que muy a menudo, con el objetivo de obtener una distribución más simétrica, los puntos esparcidos son mejor transformados a logaritmos, pues es difícil calcular estimados confiables (promedio, desviación estándar, etc.) con pequeños sesgos y presencia de puntos extremos.
]]>LÍMITE DE DETECCIÓN Y CUANTIFICACIÓN PARA RECUENTOS
LÍMITE DE DETECCIÓN
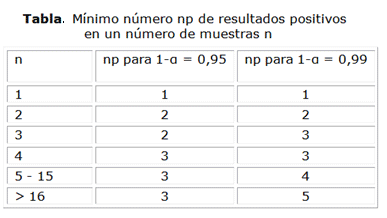
Teniendo en cuenta la incertidumbre de los métodos microbiológicos, así como el bajo nivel de inoculación con el que se lleva a efecto este tipo de ensayo, no es posible asumir la presencia del mesurando solo por observar una UFC en el medio de cultivo. Considerando que el control negativo teórico no arroja ningún resultado sobre la presencia del analito, el límite de detección para una contaminación baja (poissoniana) es alcanzado por al menos np presencias, en un número determinado de muestras. Por ejemplo, para un número de muestras n= 4, es necesario detectar positividad en 3 muestras con con 1-a = 0,95 (tabla).
]]>
Por otra parte, es importante analizar si el tamaño de la muestra n es muy pequeño, para evitar otro tipo de error estadístico: la falta de poder. Por ejemplo, según ISO, luego de analizar matemáticamente varios ejemplos, la probabilidad mínima p de contaminación disminuye cuando n aumenta; y si se desea detectar la probabilidad de contaminación p = 10 % (al 95 %), se deben tomar más de 30 muestras para el análisis satisfactorio de este parámetro. Deberá ser expresado como un número de UFC en una cantidad de muestra dada (por ejemplo, 30 UFC/g).
El límite de cuantificación puede expresarse como el menor número de microorganismos en una muestra que puede ser cuantitativamente determinado con adecuada exactitud y precisión. Una técnica cuantitativa de PCR puede mostrar valores entre 103-104 UFC/g o mL,20 teniendo en cuenta que detecta tanto microorganismos viables como muertos.
EXACTITUD RELATIVA, REPETIBILIDAD Y REPRODUCIBILIDAD
ISO 1614020 refiere que acepta como valores de referencia a aquellas respuestas obtenidas por el método estándar en muestras idénticas. Por consiguiente, la desviación de las mediciones obtenidas por el método alternativo, respecto al método de referencia, corresponden a la exactitud relativa. La relación entre la exactitud relativa y los niveles puede ser modelada y se tiene en cuenta que si los valores de sesgos son muy elevados para el propósito del método, o si las diferencias estadísticas entre ambos son significativas, se considera diferente el método alternativo del método de referencia.
Se define como repetibilidad, la cercanía de resultados independientes obtenidos por el mismo método, con material de prueba idéntico, bajo las mismas condiciones (equipo, operador, laboratorio y a cortos intervalos de tiempo, lo cual se considera condiciones de repetibilidad). El límite de repetibilidad (r) es el valor menor o igual, en el cual la diferencia absoluta, obtenida bajo condiciones de repetibilidad, se espera que tenga una probabilidad del 95 %. Si la diferencia entre los dos resultados excede a (r), los resultados deben ser considerados como sospechosos. La desviación estándar de repetibilidad sr, obtenida a partir de ambos métodos, permite obtener una F (Fisher) calculada, que al compararla con el valor tabulado (F crítico) nos orienta sobre la posible diferencia de ambos métodos a un nivel de analito determinado.
La reproducibilidad, por su parte, es la cercanía de la concordancia entre resultados individuales en un material de prueba idéntico, usando el mismo método y obtenido por operadores en diferentes equipos, (o sea, condiciones de reproducibilidad). El límite de reproducibilidad (R) precisa el valor menor o igual, en el cual la diferencia absoluta entre los resultados obtenidos bajo condiciones de reproducibilidad se espera que tenga una probabilidad del 95 %. Si la diferencia entre dos resultados de diferentes laboratorios exceden a R, los resultados son considerados sospechosos.
]]>
El valor de R es calculado a partir de la desviación estándar de repetibilidad sr y la desviación estándar sb inter- laboratorios para cada método y cada nivel de analito. Las reproducibilidades de los métodos alternativos y de referencia son comparadas con una distribución F y en dependencia de los resultados podrán tener, o no, diferentes reproducibilidades, para un nivel dado.
Cuando los resultados muestren que los métodos no son equivalentes, se deben analizar con profundidad cada detalle del ensayo, asegurando que todas las instrucciones fueron bien comprendidas, la habilidad de los técnicos responsables de la realización práctica, entre otros. El rechazo de valores extremos,21,22 se realiza siempre teniendo en cuenta que existe una elevada variabilidad asociada al recuento microbiano.
La incertidumbre en las mediciones es una indicación cuantitativa de la variabilidad analítica de los resultados. Consensos internacionales apoyan el uso de los datos de reproducibilidad y repetibilidad en la evaluación de la incertidumbre en la microbiología de los alimentos.22
CONSIDERACIONES FINALES
Las validaciones de métodos microbiológicos son, luego de analizar el elevado número de muestras, medios materiales empleados, número de laboratorios involucrados, entre otros factores, muy costosas y con grandes volúmenes de datos generados para ser analizados. No obstante, se mantienen como una necesidad imperiosa a la hora de incorporar nuevas metodologías ya sea para sustituir los métodos tradicionales, que son por lo general más caros y consumidores de tiempo, como para incorporar procedimientos más innovadores en cuanto a la tecnología y el avance de la ciencia se refiere.
]]>
REFERENCIAS BIBLIOGRÁFICAS
1. MicroVal secretariat. MicroVal: a European approach to the certification of new microbiological methods. Int J Food Microbiol. 1998;45(1):17-24.
2. Scotter S, Wood R. Validation and acceptance of modern methods for the microbiological analysis of foods in the UK. Food Control. 1996;7(1):47-51.
3. International Commission on Microbiological Specifications for Foods (ICMSF), Bruce Tompkin R. Micro-organisms in Foods Pt 7. Microbiological Testing in Food Safety Management. New York: Springer; 2002.
4. Entidad Nacional de Acreditación. Análisis microbiológicos. Documento aclaratorio sobre la validación de métodos. NT-32 Rev. 1. Madrid: ENAC; 2007.
5. Freitas EI, Lemos AA, Marin VA. Validação de métodos alternativos qualitativos na detecção de patógenos alimentares. Ciência & Saúde Coletiva. 2006;11(4):1073-83.
6. ISO 16140. Microbiology of food and animal feeding stuffs - Protocol for the validation of alternative methods. Geneva: ISO; 2003.
7. ISO 17025. General requirements for the competence of testing and calibration laboratories. Geneva: ISO; 1999 (revised 2005).
8. ordVal Validation NV-DOC. D-2002-10-22. Protocol for Validation of alternative microbiological methods. Denmark: NordVal Validation; 2002.
9. Feldsine P, Abeyta C, Andrews WH. AOAC International Methods Comité Guidelines for Validation of Qualitative and Quantitative Food Microbiological Oficial Methods of Analysis. J AOAC Int 2002;85(5):1187-200.
10. ISO/CD 17994. Water Quality - Criteria for the establishment of equivalence, between microbiological methods. Geneva: ISO; 2001.
11. Scotter SL, Langton S, Lombard B, Lahellec C, Schulten S, Nagelkerke N, et al. Validation of ISO method 11290 Part 2. Enumeration of Listeria monocytogenes in foods. Int J Food Microbiol. 2001;70(1-2):121-9.
12. Buyser ML, Lombard B, Schulten SM, In't Veld PH, Scotter SL, Rollier P, et al. Validation of EN ISO standard methods 6888, Part 1 and Part 2: 1999-Enumeration of coagulase-positive staphylococci in foods. Int J Food Microbiol. 2003;83(2):185-94.
13. Schulten SM, Benschop E, Nagelkerke NJD, Mooijman KA. Validation of microbiological methods. Enumeration of Clostridium perfringens according to ISO 7937. 2nd.ed, Report 286555002. Netherlands: Research for Man and Environment; 1997.
14. Rosenquist H, Bengtsson A, Hansen TB. A collaborative study on a Nordic standard protocol for detection and enumeration of thermotolerant Campylobacter in food (NMKL 119, 2007). Int J Food Microbiol. 2007;118(2):201-13.
15. Hedges AJ, Jarvis B. Application of 'robust' methods to the analysis of collaborative trial data using bacterial colony counts. J Microbiol Methods 2006;66(3):504-11.
16. Zhurbenko R, Quesada Muñiz VJ, Rodríguez Martínez C, Lobaina Rodríguez T. Detección de Salmonella en alimentos con el empleo de un nuevo medio cromogénico. Rev Ind aliment Méx. 2007;29(4):28-32.
17. Malorny B, Hoorfar J, Hugas M, Heuvelink A, Fach P, Ellerbroek L, et al. Interlaboratory diagnostic accuracy of a Salmonella specific PCR-based method. Int J Food Microbiol. 2003;89(2-3):241-9.
18. Malorny B, Bunge C, Hoorfar J, Helmuth R. Multicenter validation of the analytical accuracy of Salmonella PCR: towards an international standard. Appl Environ Microbiol. 2003;69(1):290-6.
19. Corry JEL, Jarvis B, Passmore S, Hedges A. A critical review of measurement of uncertainty in the enumeration of food microorganisms. Food Microbiol. 2007;24(3):230-53.
20. Rantsiou K, Alessandria V, Urso R, Dolcia P, Cocolin L. Detection, quantification and vitality of Listeria monocytogenes in food as determined by quantitative PCR. Int J Food Microbiol. 2008;121(1):99-105.
21. Jarvis B, Hedges AJ, Corry JEL. Assessment of measurement uncertainty for quantitative methods of analysis: Comparative assessment of the precision (uncertainty) of bacterial colony counts. Int J Food Microbiol. 2007;116(1):44-51.
22. Lombard B. Estimation of measurement uncertainty in food microbiology: the ISO approach. Acred Qual Assur. 2006;11(1-2):94-100.
Recibido: 2 de junio de 2010. ]]> Aprobado: 20 de noviembre de 2012.
Lic. Meylín Ortega González. Departamento de Investigaciones de Medios de Cultivo. Centro Nacional de Biopreparados (BioCen). Apartado 6048, Habana 6, CP 32600. La Habana, Cuba. Correo electrónico: mortega@biocen.cu
]]>