Respuesta inmune para la vacuna heberbiovac-hb y factores de riesgo Consolación del Sur, año 2004
Immnune response to the Heberbiovac-HB and risk factors, Consolación del Sur 2004
Emilia Rosa Rieumont1, José Fco. Martínez Gutiérrez 2, Tania Cruz Gónzalez3, María Gloria Lugo Rosa 4.
]]>
1 MSc. Profesora Consultante. Facultad de Ciencias Médicas. "Dr. Ernesto Che Guevara de la Serna". Pinar del Río.
2 Dr. Profesor Consultante. Facultad de Ciencias Médicas. "Dr. Ernesto Che Guevara de la Serna". Pinar del Río.
3 Lic. Profesora Instructora. Facultad de Ciencias Médicas. "Dr. Ernesto Che Guevara de la Serna". Pinar del Río.
4 Dra. Epidemióloga Escuela Nacional de Salud Pública.
RESUMEN
Uno de los pilares fundamentales para el control, eliminación de la hepatitis tipo B es la utilización de la vacunas que se aplica en Cuba, desde el año 1992. (Heberbiovac -HB). La inmunogenicidad, indicador que se obtiene mediante la cuantificación de Títulos de Anticuerpos (Anti-HBs) contra el antígeno de superficie (HBsAg) post vacunación permite conocer la eficacia y calidad de la vacuna. En este estudio se utilizó el método inmunoenzimático (ELISA) tipo sandwich, llevado a cabo por el Departamento de Hepatitis B. del Laboratorio de Inmunología del Centro Nacional de Genética Médica, Ciudad Habana, considerándose protegidos los individuos cuyos resultados estaban entre ³10 UI/L y < 100 Ul/L, Hiperrespondedores ³ 100 UI/L y No Seroprotegidos cuando los títulos eran < 10 UI/L; en 498 niños de 10 años que fueron vacunados en la infancia con esquema de (0-1-6 meses) hijos de madres negativas para el HBsAg, pertenecientes al Municipio Consolación del Sur en la Provincia de Pinar del Río, resultando que el género masculino, las Hipersensibilidades Tipo I y los niños y niñas que mantuvieron tratamientos con drogas inmunosupresoras fueron los factores de riesgos que evidenciaron asociación con la no seroprotección; así como en los individuos que mostraron cifras de Títulos de Ac. < 10 UI/L; se aplicó un búster de la vacuna y pasados 15 días se obtuvo que el 100% de ellos alcanzaron valores de seroprotección, calculándose la media geométrica para 35.1 UI/L antes el refuerzo de la vacuna y después 109.5 UI/L.
Palabras clave: Programa de Inmunización, Vacunas Contra la Hepatitis B/ Inmunología, Antígeno de Superficie de la Hepatitis B/ Anti-Hbs, Análisis .
ABSTRACT
One of the mainstays to control and eliminate hepatitis-B is the use of the vaccines (Herberbiovac-HB) applied in Cuba since 1992. The immunogenicity, an indicator obtained through the quantification of the Antibodies Titers (Anti-HBs) against the surface antigens (HbsAg) post-vaccination, allowing knowing the effectiveness and quality of the vaccine. The immunoenzymatic method was used in this study kind of sandwich (ELISA), carried out by the Department for the study of Hepatitis B of the Immunology Laboratory in the National Center of Medical Genetics, Havana City. The individuals which results were between =10 UI/L and < 100 UI/L, Hyperresponsers = 100 UI/L are considered protected and sero-unprotected when the titers were < 10 UI/L; in 498 children of 10 years old that were vaccinated in the early childhood having the schedule (0-16 months) of negative mothers for HBsAg, belonging to Consolacion del Sur in Pinar del Rio province. Results showed that male sex, Hypersensibilities Type I and the boys and girls maintaining treatments with immunosupresor drugs were the risk factors that provided the association with the serum-unprotection; as for in the individuals having Titers of Ac < 10 UI/L; a buster of the vaccine was applied and after 15 days the 100% of them achieved the values of serum-protection, calculating the geometric media to 35.1 UI/L before the reinforcement of the vaccine and after it 109.5 UI/L.
Key words: Immunization Program; Hepatitis B Vaccines; Immunology; Surface Antigens/hepatitis B; Anti-HBs; analysis.
INTRODUCCIÓN
En el año 2000 la Organización Panamericana de la Salud (OPS) reportó que la tercera parte de la población mundial tenía evidencias serológicas como portadores de la infección por el virus de la hepatitis B, que 367 millones estaban infectados y que un millón de personas mueren a causa de las complicaciones como: cirrosis hepática y carcinoma hepatocelular.1,2
El control de la enfermedad es posible con el uso apropiado de las vacunas contra la hepatitis B, pero desafortunadamente la mayoría de las infecciones que hoy día se reportan son en adultos que escapan a los programas tradicionales instituidos en los países que cuentan con la vacuna, como es el caso de los EE.UU.3 ]]>
En Cuba se han dado pasos para el control y eliminación de la hepatitis viral tipo B; uno de los aspectos desarrollados ha sido la producción de una vacuna contra el virus, cuya aplicación evita las complicaciones antes mencionadas. La vacuna recombinante cubana expresa el fenotipo adw2 del AgsHB, utiliza como célula hospedera la levadura Pichia pastoris. Esta vacuna ha sido aplicada en el Programa Nacional de Inmunización (PNI), registrada y comercializada en otros países del mundo, después de los trabajos realizados por grupos de investigadores cubanos en los cuatro continentes mayores.4Entre los aspectos que se toman en cuenta para evaluar la eficacia de la vacuna están la durabilidad de la respuesta inmune post vacunal mediante la persistencia de títulos de anticuerpos (Ac); así como la presencia o ausencia de marcadores del virus de la hepatitis B (VHB).5 Mediante este trabajo se quiso conocer si la vacunación con Heberbiovac-HB (antihepatitis B) aplicada a niños de 10 años, instituida en Cuba desde el año1992, lograba niveles de protección y persistencia de títulos de Ac a 10 años de aplicada y cuáles factores de riesgos influyeron en la respuesta inmune; además, obtener incremento de Anti-HBs con refuerzo vacunal en los individuos que resultaran con valores < 10 UI/L, interviniendo a través de una estrategia comunitaria.
MÉTODO
Se realizó un estudio descriptivo, retrospectivo y prospectivo de corte longitudinal y de intervención. La muestra estuvo representada por el 50% del Universo (1001) 498 niños con 10 años de vacunados con Heberbiovac-HB en la infancia con esquema de (0-1-6 meses), pertenecientes al Municipio Consolación del Sur, en la Provincia de Pinar del Río.
Se utilizaron variables como: color de la piel y el género, que se asociaron con la respuesta inmune para la vacuna antihepatitis B. Para conocer los antecedentes patológicos personales (APP) se aplicó una encuesta a padres, madres o tutores, y los resultados obtenidos se asociaron con la respuesta inmune de los pesquisados.
Se utilizó el método inmunoenzimático (ELISA) tipo sándwich,6 considerándose protegidos los individuos cuyos resultados estaban entre ³ 10 UI/L y < 100 Ul/L, hiperrespondedores ³ 100 UI/L y no seroprotegidos cuando los títulos eran < 10 UI/L. Para los que resultaron no seroprotegidos se les aplicó un refuerzo vacunal de 10 ìg de la vacuna Heberbiovac-HB (dosis pediátrica) por vía IM y validación de niveles de títulos de Ac pasados 15 días, estrategia de intervención que proporcionó la medición del Impacto de la investigación.
Para el procesamiento estadístico se empleó la prueba de X2 de McNemar,7 para comparar frecuencias en muestras dependientes, o la prueba no paramétrica del signo, y variables cuantitativas en muestras dependientes. Se utilizó el cálculo del OR8 como medida de asociación y su intervalo de confianza, así como la fortaleza de asociación mediante la prueba de X2.
RESULTADOS
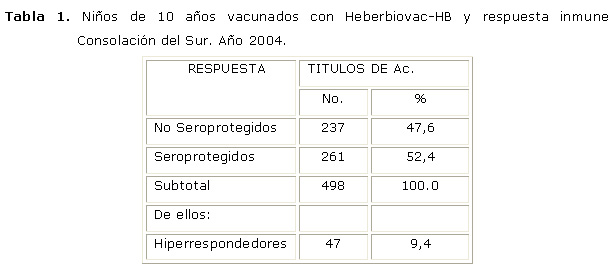
La respuesta inmune de los niños estudiados antes del refuerzo vacunal se puede observar que en la primera intervención diagnóstica, no se encontraban protegidos el 47,6 %, cifra casi similar a la de niños seroprotegidos 52,4 %, y menos del 10 % eran hiperrespondedores.
(Ver tabla 1). ]]>
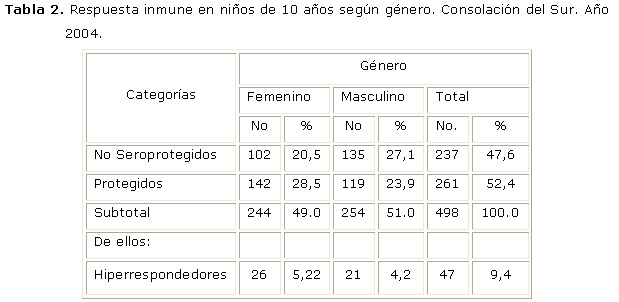
En la tabla 2 observamos la respuesta inmune según el género de los 498 escolares. De ellos 47,6 % fueron no seroprotegidos con un incremento en el género masculino de 6,6 % con relación al femenino, en la categoría de seroprotegidos se aprecia un 52,4 % en los dos géneros con ligera diferencia a favor de las féminas. En el caso de los hiperrespondedores (9,4%) la diferencia fue mínima. Sí bien había un ligero incremento de varones no seroprotegidos, las cifras se invertían en cuanto a los protegidos; lo que resultó en diferencias entre géneros, (X2 = 6.42; gdl = 1; p = 0.01).

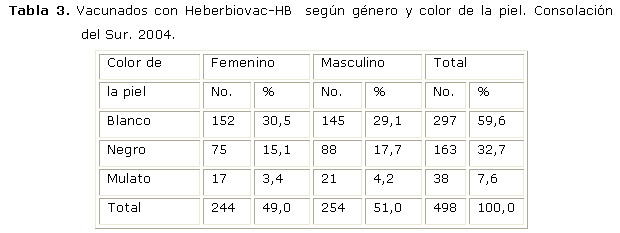
La muestra se comportó de manera uniforme en cuanto a género, 51.0% para el masculino y 49.0 % para el femenino. De igual manera al observar la tabla 3 las características del color de la piel fueron similares: 59,6 % para el color blanco, 32,7 % para el negro y 7,6 % para el mulato. No se detectaron diferencias entre géneros según el color de la piel. (X2 = 1.42; gdl = 2; p = 0.49).
Por otra parte, se comparó la distribución por género con la esperada en la población de Consolación del Sur para esa edad (según datos de población estimada para ese año de la Dirección Nacional de Estadísticas del MINSAP, y tampoco se detectaron diferencias (X2 = 0.04; gdl = 1; p = 0.84).
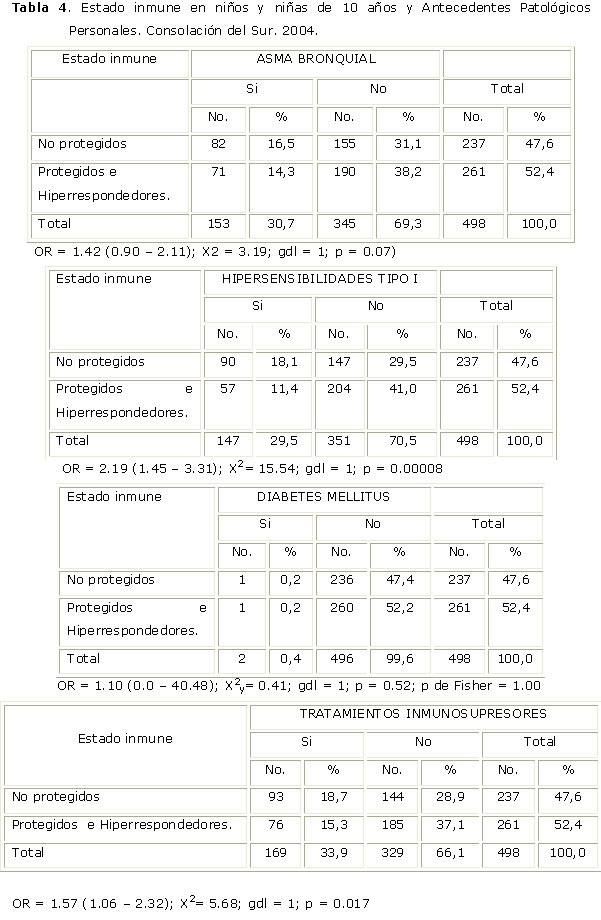
Se encontró asociación significativa entre las hipersensibilidades Tipo I y el estado de protección vacunal por HBsAg, y aquellos niños que habían recibido tratamientos inmunosupresores. Había incremento de niños protegidos o hiperrespondendores en aquellos escolares que eran asmáticos y se encontraban de igual forma más niños protegidos o hiperrespondendores en aquellos escolares que no habían recibido tratamientos inmunosupresores. (Ver tabla 4).
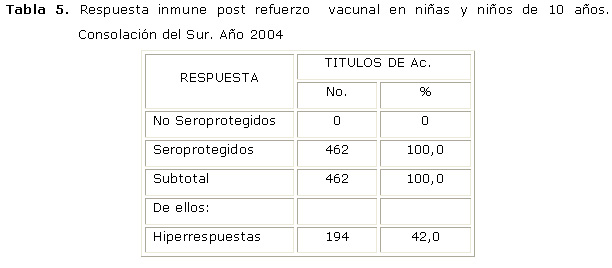
La (tabla 5) nos muestra que no habían niños y niñas no seroprotegidos, todos eran protegidos (100.0 %) y de ellos hiperrespondendores (42.0 %). Después del refuerzo vacunal. La comparación de frecuencias según el estadígrafo de McNemar dio resultados altamente significativos (X2A/D = 71.78; gdl = 1; p = 2.4 x 10-17; X2 B/C = 259.00; gdl = 1; p = 2.8 x 10-58).
 ]]>
]]>
En cuanto a los títulos de Ac antes y después hay que resaltar que antes había 192 con título = 0, y después solamente 23. Esos resultados no se tuvieron en cuenta para calcular la media geométrica, pero sí para calcular la media aritmética. En los resultados las diferencias de títulos de Ac resultaron ostensibles. Antes de la intervención la media fue de 35.1 UI/L y después era de 109.5 UI /L (Se utilizó la prueba de los signos para examinar la Ho de no diferencias). Se comprobó que v < V = 98.1; Z = 13,8; p < 0,0001.
DISCUSIÓN
En el estudio se obtuvo que un elevado porciento de la muestra estuvo representado por los no seroprotegidos y en la categoría de hiperrespondedores una pequeña proporción, ajustándose a lo esperado de acuerdo con el comportamiento predictivo de la caída de los anti-HBs, que describen una curva exponencial, con un tiempo de semivida de 3 años; donde la reducción de la concentración de anti-AgsHB en 3 semiperiodos ocurriría en el tiempo transcurrido desde que recibieron el esquema completo de vacunación, lo cual sería la estimación calculada en cuanto al tiempo para esta investigación.
En Cuba, año 2000, Almeida y Col evaluaron la inmunogenicidad de la vacuna cubana Heberbiovac HB en niños hasta 5 años de edad distribuidos por años de vida, todos habían recibido el esquema de (0-1-6 meses) reportando que los niveles de seroprotección e hiperrespuesta post vacunal fueron superiores a 93 y 76% respectivamente y la media aritmética por encima de 181 UI/L.9
En el año 2005, Shatat y Col reportan que en una cohorte de niños de 10 años que habían recibido esquema completo de vacunación en la infancia; se les realizó evaluación de anti-HBs y anti-HBc, utilizando la técnica de ELISA (3era generación), encontrando que sólo un 37.9% de los vacunados estaban protegidos e indicando la caída de anti-HBs con el tiempo.10
En este estudio las diferencias entre género fueron significativamente mayor para la no seroprotección en los varones con relación a las hembras.
Resultados que coinciden con reportes de otros estudios realizados por Zuckerman y Col, en el año 2006, donde comprobaron en una evaluación a diferentes grupos de individuos que la respuesta de anti-HBs, en cuanto a género no fue igual dentro de los diferentes grupos; ellos plantean que en el género femenino es mayor la respuesta de títulos de anti-HBs y también tiene más calidad con respecto al masculino.11
Otros estudios longitudinales indican que la vacuna de la hepatitis B hasta 10 años no es necesario el búster; pero con la aparición de la actividad sexual en los adolescentes debe evaluarse esta posibilidad a pesar de la eficacia de la vacuna, pues esta acción permitiría actuar consecuentemente para evitar enfermedades que se transmiten por vía sexual. Por lo que se recomienda analizar la necesidad de un búster en este periodo de la vida.11,10
En cuanto a las características socio - demográficas se estudiaron los factores de riesgos que pudieron influenciar en la respuesta inmune para la vacuna cubana Heberbiovac-HB, resultando que el género y el color de la piel no presentaron diferencias significativas, la distribución para ambas variables fue uniforme y similar a los caracteres en la población de Consolación del Sur para este grupo poblacional. ]]>
Al observar los resultados de protección para el virus de la hepatitis B en los niños evaluados con antecedentes patológicos personales y su asociación con la respuesta inmune. Se obtuvo significación estadística dado por la presencia de individuos no seroprotegidos, mayoritariamente en los que padecían de hipersensibilidades Tipo I y habían recibido tratamientos con inmunosupresores. Mientras que los resultados en los niños que padecían de Asma Bronquial mostraron incremento de seroprotección e hiperrespuesta, no existiendo asociación con la no seroprotección para esta afección en la investigación. Contrariamente a los resultados reportados en la investigación, Alerm y otros, en Cuba en el año 2000, estudiaron tres grupos de niños, asmáticos y no asmáticos, vacunados con la vacuna cubana Heberbiovac - HB (antihepatitis B). Cuando se compararon las variables entre los niños con historia de asma bronquial y otros sin este antecedente, en los tres grupos las concentraciones de Títulos de Ac fueron mucho más elevadas en los no asmáticos.12De los resultados alcanzados en la investigación es evidente que todos los niños quedaron seroprotegidos; lo cual habla a favor de la eficacia de las intervenciones realizadas. De igual forma se incrementó la categoría de hiperrespondedores. Estos resultados ponen en dudas la categorización de seroprotección por la detección de Títulos Ac en sangre, de manera aislada, y si pone de manifiesto la utilidad del estudio funcional frente al refuerzo vacunal que tuvieron los niños.
Un grupo de investigadores cubanos en el año 2001 evaluaron en todo el país la seguridad de la vacuna cubana recombinante Heberbiovac - HB (antihepatitis B), su inmunogenicidad y eficacia en las condiciones habituales de las prácticas de inmunización establecidas en Cuba, donde reportan que los vacunados se mantienen protegidos 5 años después de la última dosis. La media geométrica de los títulos de anticuerpos (MGT) fue de 193,39 UI/L, cifra casi 20 veces por encima del nivel mínimo protector (10 UI/L).4
Concluimos que los niveles de anti-HBs, post vacunación mantuvieron un comportamiento de semivida según lo esperado para el periodo analizado. El género femenino aportó el mayor número de Seroprotegidos contra el virus de la hepatitis B; mientras que el color de la piel no mostró asociación para la respuesta inmune contra la hepatitis B. Las hipersensibilidades tipo I y tratamientos con inmunosupresores evidenciaron asociación con la respuesta inmune en los niños y niñas pesquisados. Se constató en el estudio la no presencia de marcadores de infección del virus de la hepatitis B. La memoria inmunológica de respuesta secundaria post refuerzo vacunal en el total de niños y niñas fue excelente, por lo que los resultados obtenidos nos permite plantear que la investigación puede constituir una herramienta de trabajo para el Ministerio de Salud Pública en Cuba, en el control y prevención de la hepatitis B; además se consideró que la vacuna Heberbiovac- HB de producción cubana pasado 10 años ha mostrado ser efectiva y con una alta calidad.
REFERENCIAS BIBLIOGRÁFICAS
1- Ochoa Azze, Rolando F. Inmunoepidemiología y estrategias de vacunación.Finlay Ediciones. Cuba. 2006; 65-75.
2- Ministerio de Salud Pública. Proyecciones de la Salud Pública de Cuba para el año 2015[Serie en Internet] Abril del 2006. Disponible en: http://salud2015.sld.cu/
3- Yu AS, Cheung RC, Keeffe EB. Hepatitis B vaccines.Infect Dis Clin North Am. USA 2006 Mar; 20(1):27-45.
4- Muzio V, Cinza Z, Ortega A, Véliz G, Delgado MA, Delgado G, Díaz M Rodríguez L, Bravo J, Plácido P, et al.* Estudios postlicenciamiento de la vacuna cubana contra la hepatitis B, Heberbiovac-HB Biotecnología Aplicada April 2001; Vol18 (2):103-104.
5-Ramírez V, González A, Alerm A, Vega I, Penton E, González M. Seguridad e inmunogenicidad de la vacuna cubana Heberbiovac-HB en poblaciones de América, Europa, África y Asia. Rev Cubana Invest Biomed. 2000; 19(1):26-32.
6- Ramírez Albajés V. González Griego A, Método inmunoenzimático para la cuantificación de anticuerpos anti-HBs. Biotecnología Aplicada. 1993; 10:102.
7- Villanueva M, y Col. Laboratorio de Estadística Matemática I. Primera Parte. Editorial Félix Varela. (EFV). 2004; 240-247.
8- González E, Ochoa R, Armas P. Las Mediciones en Epidemiología. Instituto "Pedro Kourí" La Habana. Cuba. 2006; 50-63.
9- Almeida A, González G, González M, Ramírez V. Durabilidad de la respuesta inmune contra el VHB en niños de un círculo infantil en Cuba. Rev Cubana Invest Biomed. 2000; 19(1):68-7
10- Shatat H, Kotkat A, Farghaly A, Omar S,Zayton A. study of hepatitis B vaccine efficacy 10 years aftercompulsory vaccinationin Egypt. Jegypt Public Heath Assoc. 2005; 80(5-6):495-508.
11- Zuckerman JN. Protective efficacy, immunotherapeutic potential, and safety of hepatitis B vaccines. Med Virol. 2006 Feb; 78(2):169-77.
12- Alerm A, González A, Ramírez V, Martínez M, Sosa S, Dacourt A. Respuesta pos- vacunal y persistencia de anticuerpos contra el virus de la hepatitis B en niños asmáticos y no asmáticos vacunados con Heberbiovac -HB. Rev Cubana Invest Biomed. 2000; 19(1):72-81.
]]>
Recibido: 20 de Abril de 2009.
Aprobado: 2 de Junio de 2009.
MSc. Emilia Rosa Rieumont. Profesora Consultante. Facultad de Ciencias Médicas. "Dr. Ernesto Che Guevara de la Serna" Dirección: Km. 89 carret. Central, Pinar del Río. E-mail: emilia.rosa@fcm.pri.sld.cu. ]]>