ARTÍCULO ORIGINAL
Tratamiento de residuos provenientes de biomasa empleada en la producción de electricidad
Treatment of wastes from biomass used in electricity production
]]>
Ángel Guillemes Peira
Universidad del Pacífico, Facultad del Mar y Medio Ambiente, Guayaquil, Ecuador.
RESUMEN
El objetivo es encontrar una ruta de aproximación al tratamiento de los condensados de residuos tóxicos, obtenidos durante los procesos de generación eléctrica a partir de biomasa, que permita transformarlos en aguas residuales. Se han llevado a cabo dos desarrollos experimentales mediante la utilización de un reactor. Durante el primero se aplicaron potenciales sin seguir una ruta definida, para de manera eléctrica ir calibrando el sistema mediante observación de respuestas. En el segundo, en base a las observaciones eléctricas realizadas durante el primero, se fueron aplicando potenciales. La ruta de aproximación ha resultado ser apta para el tratamiento de los condensados, si bien dada la agresividad del residuo, es necesario emplear un reactor que permita alcanzar y mantener los potenciales de electro-oxidación necesarios y combinarlo con un reactor de electrocoagulación.
]]> Palabras claves: biomasa, electrolito, reactor, residuo, tratamiento.
ABSTRACT
The main objective of this study is to find an approach for the treatment of toxic waste condensates obtained during the generation of electricity from biomass that would transform them into wastewater. Two experimental conditions have been performed using a reactor. During the first condition, potentials were applied without following a defined path to electrically calibrate the system by observing responses. In the second experimental condition and based on these previous electrical observations, the potentials were applied. This technical approach has proven suitable for condensate treatment. However, given the aggressiveness of the residue, it is necessary to use a reactor which allows reaching and maintaining the necessary electro-oxidation potential and to combine it with an electrocoagulation reactor.
Keywords: biomass, electrolyte, reactor, waste, treatment.
INTRODUCCIÓN
La excesiva dependencia de los combustibles fósiles para la generación eléctrica, ha originado la búsqueda de alternativas más sostenibles a través del desarrollo de energías renovables, como la combustión de biomasa. Dependiendo del tipo de biomasa y del proceso y tecnología utilizada en la recuperación de la energía contenida en la misma, se obtienen residuos tóxicos y productos contaminantes, en menor o mayor proporción, constituyendo un serio problema para el medio ambiente, por lo que se hace necesario aplicar tratamientos para la inactivación de su peligrosidad. ]]>
En relación con la caracterización del residuo proveniente de la biomasa, hay que mencionar que el principal problema del electrolito a tratar son los elevados niveles que presenta con respecto a la demanda química del oxígeno (DQO), los compuestos fenólicos, la conductividad y los compuestos amoniacales.Tanto los fenoles como los compuestos amoniacales han sido, y son, motivo de numerosas investigaciones encaminadas a conseguir un método eficiente para eliminarlos de los residuos industriales (Abdelwahab et al. 2009), (Li et al. 2009). Estos compuestos son sustancias altamente corrosivas, tóxicas y debido a la estabilidad y a la solubilidad que presentan en el agua su degradación es difícil, por lo que se hace necesario el uso de técnicas que permitan lograr su oxidación. Una de las empleadas actualmente para su tratamiento es la electroquímica, en el que algunos electrodos son modificados para llevar a cabo su eliminación.
El tratamiento electroquímico, es decir, la oxidación sobre la superficie de un electrodo, presenta algunas ventajas como la de no requerir de reactivos extras ya que la reacción se da directamente sobre el electrodo, no se producen lodos que implicarían tratamientos posteriores y se obtienen altas eficiencias de corriente, o lo que es lo mismo, se minimizan reacciones competitivas. El procedimiento implica trabajar en soluciones alcalinas concentradas y usando como electrodos mezclas de óxidos de RuO2 + TiO2 (Scialdone et al. 2010). Por otra parte, es posible aumentar la conductividad de la solución añadiendo NaCl, permitiendo un mecanismo indirecto de oxidación por la acción del Cl2 formado, lo que a su vez colabora en laeliminación de ciertas sustancias como el amoníaco y el nitrito, pero puede llegar a disminuir la eficiencia de la eliminación de los nitratos (Mook et al. 2012). Como resultado del tratamiento se producen sustancias que son menos tóxicas que las iniciales.
La aplicación de corriente eléctrica (2-20 A) entre dos electrodos adecuados en agua produce reacciones químicas primarias, con generación de radicales hidroxilo, que oxidan luego la materia orgánica, fórmulas (1) y (2).
![]()
![]()
La oxidación electroquímica es útil no solamente en el tratamiento de los compuestos fenólicos, sino también para amplios rangos de DQO, desde 500-200000 mg O2/L (Abdelwahab et al. 2009) y en la eliminación, entre otros, de los compuestos amoniacales (Mooket al. 2012), (Li et al.2009).
Con el presente trabajo, se pretende encontrar una ruta de aproximación al tratamiento de los condensados de residuos tóxicos, que se han obtenido durante los procesos de generación eléctrica a partir de biomasa, que permita transformarlos en aguas residuales.
METODOLOGÍA
Los dos desarrollos experimentales realizados se han llevado a cabo introduciendo un reactor en un vaso de precipitados con un volumen de 5 litros. Por el incremento de nivel en el vaso, producido al introducir al reactor el volumen final, se ajustó a 4,75 litros para evitar reboses. ]]>
La duración de los mismos se fijó en 3 horas y 20 minutos, con registro de datos cada 20 minutos. Para el tiempo 0 min, las medidas corresponden a las iniciales del condensado en bruto. El tiempo cero 0* min corresponde al mismo condensado tras una adición de 71,25 miligramos de sal (NaCl), lo que equivale a una concentración de 15 mg/L en el volumen marcado de 4,75 litros. Durante el primer desarrollo experimental, se fueron aplicando potenciales sin seguir una ruta definida para de manera eléctrica ir calibrando el sistema mediante observación de respuestas. En base a las observaciones eléctricas realizadas durante ese primer desarrollo experimental y a las experiencias previas con otros electrolitos, se fueron aplicando los potenciales durante el segundo desarrollo experimental.La electrocoagulación resulta por lo tanto una técnica necesaria para el diseño de un tratamiento del condensado. Esta técnica requiere del uso de ánodos de sacrificio de hierro y aluminio fundamentalmente, que se disolverán formando hidróxidos de hierro y aluminio como coagulantes. Posteriormente los coágulos deberán ser eliminados por flotación, filtración, o decantación (Wenhuaand Shen 2012).
En la hidrólisis se generan grupos hidroxilos (OH-). Los grupos OH- en presencia de materia orgánica tienden a reaccionar oxidándola.
En el agua, la demanda química del oxígeno (DQO) es un parámetro directamente relacionado con la materia orgánica presente e inversamente relacionado con el oxígeno disuelto disponible.
El proceso de oxidación directa consiste en llevar a cabo la oxidación directa de amonio a gas nitrógeno en dos pasos según las siguientes fórmulas (3) y (4) (Scialdone et al. 2010).
![]()
![]()
El segundo paso descrito puede lograrse por oxidación directa al paso por el reactor electroquímico, o mediante la generación de especies muy oxidantes, como por ejemplo los radicales hidroxilos que completen la oxidación del amoniaco (Li et al.2009).
El principal problema de esta vía es que a priori es necesario disponer de electrodos con una elevada capacidad de oxidación, así como de medición diferencial con el medio. Por este motivo, aparte de utilizar electrodos convencionales de m. m. o. (mixed metal oxides) con base de titanio, se emplearon electrodos de m. m. o. con base de iridio y recubrimiento de diamante. Mientras que el titanio tiene una electronegatividad de 1,5, el iridio tiene una electronegatividad de 2,2 y el carbono (diamante) de 2,5 (Mook et al. 2012).
Aunque son electrodos de fabricación más costosa, permiten una mayor acción oxidante y un mayor rango de medición diferencial con el medio, que permite valorar la eficacia de la oxidación en tiempo real. ]]>
Hay que comprobar que la capacidad oxidante y la capacidad de dirigir específicamente esas oxidaciones son suficientes para contrarrestar la tendencia reductora del agua. En el ciclo natural del nitrógeno, se da una fase oxidativa y otra reductora (Feng et al. 2010), fórmulas (5) y (6).![]()
![]()
Al generarse un medio altamente oxidante, la desnitrificación se puede invertir oxidándose los nitritos (NO2-) a nitratos (NO3-). Los nitratos quedan siempre en esa forma, puesto que el nitrógeno en esa sal ya se encuentra en su mayor estado de oxidación, por lo que no podrá perder más electrones. Por otra parte, si la oxidación directa del amoniaco a gas nitrógeno no tuviese una eficacia del 100%, parte del nitrógeno amoniacal podría oxidarse a nitratos. Si ese hipotético porcentaje fuese elevado, podría darse un fenómeno de acumulación de nitratos que en zonas sensibles podría ser limitante para el nuevo producto.
Otra de las vías de la oxidación del amonio es la generación y destrucción de cloraminas. Se procede a generar electroquímicamente concentraciones muy elevadas de cloro libre, de tal manera que se produzca la formación de las cloraminas y su inmediata destrucción para mantener constantemente el break point de las mismas.
Esto consiste en el desplazamiento del siguiente equilibrio a amoniaco mediante hidrólisis, fórmula (7), (Ratnayaka et al. 2009).
![]()
También se empieza a formar cloro libre a partir de los cloruros presentes en el agua para formar, en combinación con oxígeno y agua, ácido hipocloroso, fórmulas (8), (9) y (10), (Bougeard et al. 2010).
![]()
![]() ]]>
]]>
Por otra parte, en un depósito se procede a formar ácido hipocloroso de la misma manera descrita anteriormente, pero en concentraciones muy elevadas potenciadas por la recirculación del agua a través de un reactor.
Debido a esas concentraciones se consigue formar y destruir cloraminas liberando a la atmósfera gas nitrógeno, fórmulas (11) y (12), (Goslan et al. 2009), (Bougeard et al. 2010):
![]()
![]()
A pesar de que en un tratamiento terciario el agua ya ha sido depurada en su mayor parte, lo habitual es encontrarse aún con un agua no desinfectada y con cierta presencia de materia orgánica, lo que se traduce en un agua con tendencia reductora.
En la dinámica de la formación de cloraminas, representada en la figura 1, la materia orgánica y las bacterias (reductores) van a competir con el amonio en el consumo de cloro, pudiendo generar un desplazamiento del break point por aumentar la dosis de cloro requerida. Para prevenir esto es posible que sea necesario aplicar, en el primer punto de tratamiento, electro-oxidación de materia orgánica y desinfección (Chakrabarti et al.2011).
]]>
RESULTADOS Y DISCUSIÓNDurante el primer desarrollo experimental, se aplicaron potenciales sin seguir una ruta definida para de manera eléctrica ir calibrando el sistema mediante observación de respuestas, por lo que los resultados experimentales no presentan ninguna lógica clara.
A base de las observaciones eléctricas realizadas durante ese primer desarrollo experimental y a las experiencias previas con otros electrolitos, se fueron aplicando los potenciales durante el segundo desarrollo experimental.
Los resultados obtenidos siguieron la lógica esperada. Los resultados experimentales para el primer y segundo desarrollo, se muestran en las tablas 1 y 2 respectivamente.
El estudio de la evolución de los valores frente al tiempo mediante gráficas, permite extraer las conclusiones. Estas interpretaciones se llevan a cabo con los análisis del segundo desarrollo experimental.
Como ya se ha comentado anteriormente, el tiempo0* min, tanto en la tabla 1 como en la tabla 2, corresponden al mismo condensado tras una adición de 71,25 miligramos de sal (NaCl), lo que equivale a una concentración de 15 mg/L.
En la figura 2, se puede observar como durante las dos primeras horas el pH disminuye debido a que los grupos hidroxilo se están consumiendo en la reacción con la materia orgánica. Sin embargo, a partir de las dos horas se observa cómo el pH comienza a aumentar, lo que indica que los grupos hidroxilo ya no están reaccionando y quedan en el agua incrementando el pH de la misma.
En relación con lo interpretado con el pH, se puede corroborar la deducción lógica al observar los datos registrados en la tabla 2, para el oxígeno disuelto (en porcentaje de saturación y en mg/L) y para el potencial de electrodo.
En la figura 3 se puede observar cómo el oxígeno disuelto va aumentando de manera exponencial hasta pasados los 100 minutos, momento en el cual comienza a estabilizarse sin dejar de aumentar. ]]>
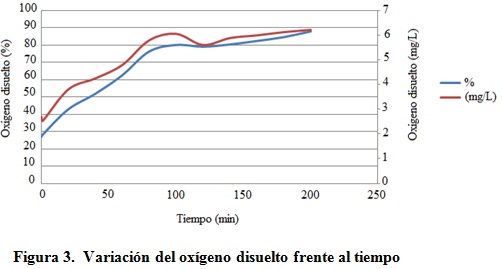
Al observar la variación del potencial de electrodo en la figura 4, se comprueba que el ambiente es muy reductor. Se aprecia también que el tratamiento de oxidación provoca una tendencia de incremento del mismo, con un ascenso más moderado que en el caso del oxígeno disuelto, pero más constante.
El incremento del pH, por falta de reacción de los grupos hidroxilo y la disminución de la tasa del oxigeno disuelto, mantuvo que el potencial de electrodo continuara siendo muy reductor.
En una observación visual se constató que el tratamiento produjo un aumento de la turbidez en el agua y un oscurecimiento de la muestra, que pasó de un color amarillo de tonalidad clara a un amarillo de tonalidad muy oscura. En una observación olorimétrica se constató una clara reducción del olor en la muestra.
El proceso oxidativo provocó la oxidación de los anillos aromáticos y de las cadenas largas de la materia orgánica presente, dando como resultado la generación de compuestos carbonados de cadena más corta. Llegado a este punto el proceso de oxidación no se detiene, pero se ralentiza mucho por lo que es necesario complementarlo con un proceso de electrocoagulación, para continuar manteniendo una tasa elevada de remoción de DQO. En la figura 5, se puede observar la evolución de la DQO en el tratamiento de aguas residuales.
Durante el desarrollo experimental no se pudo llevar a cabo la electrocoagulación, puesto que el reactor empleado no se encuentra equipado con ánodos de sacrificio de hierro y aluminio.
A continuación se pasa a interpretar los resultados relativos al cloro libre y conductividad, que en el caso de este condensado están estrechamente relacionados con la presencia de compuestos amoniacales y su tratamiento. Para esta fase del tratamiento no se esperaba poder observar grandes resultados, puesto que la técnica de eliminación de compuestos amoniacales en cortos periodos de tiempo requiere de la aplicación de potenciales elevados, que con el reactor empleado no se pudieron alcanzar por su sobrecalentamiento.
El cloro libre no se detectó en el electrolito hasta después de una hora de tratamiento. Esto era lo esperado y se debe a que tras la formación inicial de cloro libre y antes de que este reaccione, se provoca la formación de ácido hipocloroso para posteriormente formar cloraminas, cuya destrucción se provoca liberando gas nitrógeno y cloro libre. ]]>
En este momento, el cloro libre es detectable. El cloro libre no comenzó a formarse hasta pasada una hora del tratamiento, tal y como se aprecia en la figura 6.La explicación de esto es que durante los primeros momentos del tratamiento, es necesario reducir el amonio a amoniaco y en el momento que empieza a haber mayor disponibilidad de oxígeno disuelto, empieza a formarse el ácido hipocloroso que junto al amoniaco comienza a formar cloraminas. A partir de la hora de tratamiento, empiezan a destruirse las cloraminas generando cloro libre y nitrógeno molecular.
Se observó un incremento inicial de la conductividad debido a la adición de sal (NaCl). A partir de ahí, la conductividad comienza a descender rápidamente, como se observa en la figura 7, por dos razones que son la reducción de NH4+ a NH3 y la transformación de los cloruros a hipocloroso.
Como se ha comentado anteriormente, el reactor utilizado está limitado para esta aplicación, porque para una gestión eficaz de la misma es necesario aplicar potenciales elevados, lo que no es posible por limitaciones de sobrecalentamiento. El consumo máximo de este reactor fue de 25,89 W, momento a partir del cual empieza a disminuir por autoprotección.
En la figura 8, que combina el consumo del reactor con la temperatura del condensado, se puede observar como el consumo y la temperatura va aumentando simultáneamente, hasta alcanzar su valor máximo sobre las dos horas de tratamiento.
Como se puede apreciar, después de producirse el valor máximo de consumo del reactor, empieza a descender situándose sobre las dos horas y por lo tanto, coincidiendo con el momento en el que los efectos del tratamiento comienzan a estabilizarse.
]]>
CONCLUSIONES
· A pesar del incremento del pH, por la falta de reacción de los grupos hidroxilo y la estabilización o disminución de la tasa de aumento del oxigeno disuelto, el potencial de electrodo continuó siendo muy reductor, por lo tanto, la tasa de oxidación de la materia orgánica se vio disminuida aunque su presencia en el agua siguió siendo abundante.
· El proceso oxidativo provocó la oxidación de la materia orgánica presente en el condensado, pero se hace necesario complementar el proceso con electrocoagulación que permita continuar manteniendo una elevada tasa de remoción de la demanda química de oxígeno.
· La ruta de aproximación empleada a lo largo de la investigación ha resultado ser apta para el tratamiento de los condensados, si bien dada la agresividad que presenta el residuo, es necesario emplear un reactor que permita alcanzar y mantener los potenciales de electrodo que son necesarios, combinándolo con un reactor de electrocoagulación estándar, lo que permitirá transformar estos residuos tóxicos en aguas residuales.
]]>
REFERENCIAS1. Abdelwahab O., Amin N. and El-Ashtoukhy E. «Electrochemical removal of phenol from oil refinery wastewater». Journal of Hazardous Materials, (2009), volume 163, pages 711-716, Elsevier, Netherlands.
2. Bougeard C., Goslan E., Jefferson B. and Parsons S. «Comparison of the disinfection by product formation potential of treated waters exposed to chlorine and monochloramine», Journal of Water Research, (2010), volume 44, issue 3, pp. 729-740, Elsevier, Netherlands.
3. Chakrabarti M., Saleem M., Irfan M., Raza S., Hasan D. and Daud W. «Applicationof waste derived activated carbon felt electrodes in minimizing NaCl use for electrochemical disinfection of water», International Journal of Electrochemical Science, (2011), volume 6, pages 4470-4480, ESG.Serbia.
4. Feng C., Zhang Z., Yang S. and Sugiura N. «Treatment of nitrate contaminated water using an electrochemical method». Journal Bioresource Technology, (2010), volume 101, pages 6553-6557, Elsevier, Netherlands.
5. Goslan E., Krasner S., Bower M., Rocks S., Holmes P., Levy L. and Parsons S. «A comparison of disinfection by-products found in chlorinated and chloraminated drinking waters in Scotland», Journal Water Research, (2009), volume 43, issue 18, pages 4698-4706, Elsevier, Netherlands.
6. Li M., Feng C., Zhang Z., Zhao R., Lei X., Chen R. and Sugiura N. «Application of an electrochemical-ion exchange reactor for ammonia removal», Electrochimica Acta, (2009), volume 55, pages 159-164, Elsevier, Netherlands.
7. Mook W., Chakrabarti M., Aroua M., Khan G., Ali B., Islam M. and Abu Hassan M. «Removal of total ammonia nitrogen (TAN), nitrate and total organic carbon (TOC) from aquaculture wastewater using electrochemical technology: A review». Journal of Desalination, (2012), volume 285, pages 113, Elsevier, Netherlands.
8. Ratnayaka D., Brandt M. and Johnson K. «Twort's water supply». 6th edition, pages 439-442, Elsevier, Netherlands, (2009).
9. Scialdone O., Galia A., Gurreri L. and Randazzo S. «Electrochemical abatement in water: reduction, oxidation and combined processes». Journal of Electrochemical Acta, (2010), volume 55, issue 3, pages 701-708, Elsevier, Netherlands.
10. Wenhua Z. and Shen T.«Study of degradation of wastewater biomass after coagulation and adsorption», Journal of Capital Normal University, (2012), volume 23, pages 64-78, Natural Science Edition, China.
Recibido: 13 de noviembre de 2014.
Aprobado: 21 de enero de 2015.
]]>
Ángel Guillemes Peira, Universidad del Pacífico, Facultad del Mar y Medio Ambiente, Guayaquil, Ecuador, email: angel.guillemes@upacifico.edu.ec, angel_guillemes@hotmail.com ]]>