Gliomas malignos: biología molecular y detalles oncogenéticos
Wicked gliomas: molecular biology and oncogenetics detail
Dr. Enrique Marcos Sierra Benítez, Dra. Mairianny Quianella León Pérez, Dr. Lenier Laud Rodríguez, Dr. Alberto Lázaro Carrillo Comas, Dra. Letier Pérez Ortiz, Dra. Eglys Rodríguez Ramos
Hospital Universitario Comandante Faustino Pérez. Matanzas, Cuba.
RESUMEN
La biología de los gliomas malignos se asocia con el balance de la expresión de las proteínas que controlan de manera positiva o negativa el ciclo celular, la proliferación, la motilidad, la neoformación vascular y el reconocimiento del sistema inmune. La frecuencia de las alteraciones genéticas que están presentes en GBM2 y GBM1 son diferentes así como la edad de los pacientes en la que se presentan. Mientras que los GBM1 suelen aparecer en edades más tardías, alrededor de los 60-70 años, los GBM2 suelen presentarse en edades más tempranas, 40-50 años. En la génesis del glioblastoma existen alteraciones moleculares a nivel de genes supresores de tumores, oncogenes y genes reparadores de ADN.
Palabras clave: gliomas malignos, biología molecular, oncogenes.
ABSTRACT
The glioblastoma it is the primary wicked tumor of the central nervous system more common in adults and it invariably associates to a bad presage. The biology of the wicked gliomas associates with the balance of the expression of the proteins that they control of positive way or negative the cellular cycle, the proliferation, the motility, the vascular neoformation and the recognition of the immune system. The frequency of the genetic alterations that they are present in GBM2 and GBM1 is different. While the GBM1 usually appears in later ages, around the 60-70 years, the GBM2 usually presents in earlier ages, 40-50 years. In the genesis of the glioblastoma exist molecular alterations at level of suppressive genes of tumors (GST), oncogenes and reparative genes of DNA.
Key words: wicked gliomas, molecular biology, oncogenes.
]]> INTRODUCCIÓN
La incidencia de los tumores cerebrales a nivel mundial es de 3,5 casos por cada 100.000 habitantes con una mortalidad de 2,6 casos por cada 100.000 habitantes,1,2 la incidencia de los tumores cerebrales oscila entre 10 y 17 casos por cada 100.000 habitantes al año según estadísticas de los Estados Unidos de América (EUA), además se relaciona el aumento de su prevalencia con la edad en forma constante hasta los 75-84 años,2 y representa la tercera causa de mortalidad por cáncer.3
Los gliomas malignos son los tumores primarios más frecuentes del sistema nervioso (SN) representan del 64 al 70% de los casos y la mayoría son astrocitomas.
En Estados Unidos, la incidencia de cáncer del cerebro se ha incrementado 1.2% por año desde 1973 y la mortalidad se ha incrementado 0.7% por año. Esto ha sido más evidente en los pacientes mayores de 60 años, en que la incidencia se incrementa 2.5% por año desde 1980. En este mismo grupo de pacientes se observa una mayor frecuencia de tumores agresivos de origen glial, en particular el glioblastoma multiforme y el astrocitoma anaplásico.4 Varios autores consideran que este incremento es artificial y arguyen que la incidencia se ha incrementado debido al considerable avance en la técnica de neuroimagen ocurrido desde la década del 70, que permite un diagnóstico preciso y evita los diagnósticos erróneos, así como a un incremento en la densidad de población. Antes de la tomografía (TC) muchos de esos pacientes eran catalogados erróneamente como portadores de enfermedades neurodegenerativas o cerebrovasculares.2,5
El glioblastoma (GB) es el tumor maligno primario del sistema nervioso central (SNC) más común en adultos (supone más del 50%) y se asocia invariablemente a un mal pronóstico. Solo el 33% de los pacientes sobrevive al año y el 5% de los pacientes llegan a vivir más de 5 años tras el diagnóstico.6,7 La Organización Mundial de la Salud (OMS) clasifica los gliomas fundamentalmente por criterios histopatológicos en: astrocitomas, oligodendrogliomas, oligoastrocitomas y ependimomas. Además, establece una gradación relacionada con el pronóstico de la enfermedad que identifica a los de alto grado como astrocitomas de grado III (astrocitoma anaplásico) y grado IV (GB).2,8
Las primeras teorías que intentaron explicar la génesis de los tumores cerebrales en 1878, plantea que los tumores nacían sobre el terreno de gérmenes diseminados, es decir que para el desarrollo de un tumor debería existir una rápida diferenciación de las capas germinales, así como emigración de células, lo cual provocaría que se quedasen células embrionarias mal situadas y se iniciara la formación de neoplasias. Años más tarde, se postuló que los tumores se producían por irritaciones exógenas de naturaleza química o radioactiva.9
Han sido numerosas las teorías publicadas por diferentes autores. Primero se pensó que con posterioridad a un proceso de regeneración de los gérmenes podían diseminarse por la profundidad de los tejidos y ello explicaría la génesis de los tumores cerebrales después de un traumatismo craneal.9
En los últimos años el desarrollo de la genética ha permitido una explosión en el conocimiento de los numerosos eventos que se producen en la formación de un tumor cerebral.
MATERIALES Y MÉTODOS
]]> Se realizó una revisión sistemática de los principales artículos publicados en inglés y español durante el período comprendido desde el año 2012 hasta el 2016, acerca de los principales avances en el estudio de la biología molecular de los glioblastomas.En esta revisión se trató datos epidemiológicos acerca de estos tumores malignos cerebrales, así como las distintas alteraciones genéticas que conducen hacia la malignización de las células gliales enfatizando en la malignización glioblástica y en las perspectivas actuales de tratamiento génico de la misma. Las referencias de los artículos recuperados por la búsqueda electrónica fueron investigadas en otros artículos potencialmente elegibles.
DISCUSIÓN
La biología de los gliomas malignos se asocia con el balance de la expresión de las proteínas que controlan de manera positiva o negativa el ciclo celular, la proliferación, la motilidad, la neoformación vascular y el reconocimiento del sistema inmune. Estos fenómenos son el resultado de cambios en el nivel de expresión de un gen normal o de involucrar la pérdida de su expresión. La señal para que la célula normal prolifere comúnmente se inicia en la superficie celular, donde los factores de crecimiento liberados por la matriz extracelular o por el propio tumor interactúan con los receptores específicos en la membrana, desencadenando diversos mecanismos de señalización intracelular que afectan a la expresión génica para promover la división celular. Pueden existir alteraciones y mutaciones en cada una de estas vías que en conjunto o de forma independiente pueden dar lugar a la pérdida de regulación del ciclo celular, la angiogénesis, la proliferación y/o favorecer la invasión.8-10
La frecuencia de las alteraciones genéticas que están presentes en GBM2 y GBM1 es diferente así como la edad de los pacientes en la que se presentan. Mientras que los GBM1 suelen aparecer en edades más tardías, alrededor de los 60-70 años, los GBM2 suelen presentarse en edades más tempranas, 40-50 años. En la génesis del glioblastoma existen alteraciones moleculares a nivel de genes supresores de tumores (GST), oncogenes y genes reparadores de ADN.11,12
Alteraciones génicas en la patogenia de los glioblastomas
Alteraciones de genes localizados en el cromosoma 10.
]]>
La alteración más frecuente identificada en glioblastomas es la pérdida de heterocigocidad (LOH) en 10q. La frecuencia de LOH en 10q es similar en GBM1 (70%) y en GBM2 (63%) aunque en GBM1 se ha observado que la pérdida es del cromosoma 10 completo en la mayoría de los casos, mientras que en GBM2 se observa generalmente pérdida de 10q pero no de 10p. En el cromosoma 10 se han identificado varios GST: PTEN (homólogo de la tensina y fosfatasa) en 10q23.3, DMBT1 (supresor de tumores cerebrales malignos) localizado en 10q25.3-q26.1, FGFR2 (receptor del factor del crecimiento fibroblástico) en la región 10q26 y un gen reparador de ADN, la O6-metilguanina-DNAmetiltransferasa (MGMT), se localiza en 10q26. Estos GST intervienen en el control del ciclo celular y reparación de ADN. La inactivación de un GST ha de producirse en homocigosis, para que el gen pierda completamente su funcionalidad. En glioblastomas una copia de PTEN, DMBT1, FGFR2 y/o MGMT se pierde normalmente por LOH 10q y la otra copia del gen está sujeta a mutaciones o a procesos epigenéticos que lo inactivan.12-14 En glioblastomas se han observado alteraciones epigenéticas, que se definen como aquéllas que influyen en la actividad del gen pero no implican cambios en la secuencia del ADN. La principal modificación epigenética en humanos es la metilación de la citosina localizada en los dinucleótidos CpG. Existen lugares donde son más abundantes, denominándose islas CpG que normalmente no están metiladas en las células no tumorales. La metilación aberrante de las islas CpG produce una parada de la transcripción del gen originando su inactivación. Existen muchos GST y genes reparadores del ADN que pierden la expresión mediante este mecanismo en tumores de estirpe glial, así como también en otros tipos de cáncer.15,16
Las mutaciones de PTEN son más frecuentes en GBM1 (25%) pero no exclusivas, ya que algunos autores han identificado mutaciones de PTEN en GBM2 (4%). Se han identificado alrededor de 78 mutaciones diferentes de PTEN en glioblastomas, de las cuales el 12,8% son mutaciones silenciosas, el 32,1% son deleciones o inserciones distribuidas por todos los exones y el 33% son mutaciones con cambio de aminoácido; estas mutaciones se han localizado preferentemente en los exones 1-6 de PTEN, región que presenta homología con ciertos dominios de las fosfatasas. PTEN, como fosfatasa que es, puede retirar el fosfato del fosfatidil inositol 3 fosfato (PIP3), deteniéndose la señal de crecimiento celular y provocando generalmente una disminución de la actividad celular. Dado que la deleción en homocigosis de PTEN es bastante rara, otro mecanismo que se postula para su inactivación es la metilación de su promotor. Las mutaciones de PTEN son más frecuentes en glioblastomas que en astrocitomas anaplásicos. Estos datos sugieren que dichas mutaciones constituyen una alteración importante en el desarrollo de gliomas, pudiendo representar un paso molecular necesario en la transformación de gliomas de bajo a alto grado de malignidad.17-19
Las mutaciones de DMBT1 son bastante escasas en glioblastomas, por lo que la pérdida de función del gen se debe principalmente a una deleción en homocigosis; esta alteración ya se observa en astrocitomas de bajo grado. La pérdida de función de DMBT1 se postula que podría estar sujeta a la metilación en su promotor pero todavía no existen suficientes trabajos que lo permitan afirmar de forma concluyente. También se postula que FGFR2 podría funcionar como GST, ya que se pierde su expresión en estos tipos de tumores, pero todavía no se conoce muy bien su función en la génesis de los gliomas.20,21
El gen MGMT, cuya pérdida de expresión suele estar vinculada a hipermetilación, codifica para una proteína reparadora de ADN que actúa eliminando los radicales mutagénicos y citotóxicos en posición O6 guanina del ADN. Para ello, transfiere estos radicales a una cisterna interna en una reacción que inactiva a una molécula de MGMT por cada lesión reparada. De este modo, la capacidad de reparación de lesiones en el ADN de una célula, depende del número de moléculas de MGMT y por tanto de la tasa de síntesis de novo de la misma.22 La acumulación de mutaciones en gliomas subsecuente a la inactivación de MGMT no parece ser aleatoria ya que si bien esta inactivación produce acumulación de mutaciones en el oncosupresor TP53, dichas alteraciones son prácticamente inexistentes en otro gen, TP73, estrechamente relacionado con TP53.23 Esteller y colaboradores,24 demostraron que la metilación aberrante de MGMT producía una mejor respuesta a tratamientos con temozolomida en gliomas. Por lo tanto la ausencia de la proteína o la inactivación del gen es un factor de mal pronóstico debido a que los pacientes que poseen metilación en este gen acumulan más mutaciones, pero a la vez también podría representar un factor predictivo de respuesta a la quimioterapia en este tipo de tumores.
Alteraciones de la vía TP53/MDM2/P14arf
La vía genética TP53/MDM2/P14arf también está sujeta a alteraciones en glioblastomas y astrocitomas.25,26 Es una vía implicada en respuesta a estrés celular que va a provocar la activación de genes relacionados con el control del ciclo celular, reparación de ADN y apoptosis.4 TP53 es un gen que codifica para la proteína p53 que actúa como factor de transcripción (FT) uniéndose a los promotores de genes implicados en la reparación de ADN. En condiciones normales p53 está secuestrado por su represor MDM2 por lo que la proteína no es funcional; cuando la célula entra en división (fase G1-S), MDM2 libera a p53. Este FT va a promover la trascripción de otros genes implicados en reparación de ADN y/o apoptosis. En las células que no presentan alteraciones en esta vía y que poseen su material genético dañado, p53 se une a los promotores que van a activar a genes implicados en la reparación del ADN; sin embargo, si el material genético no puede ser reparado la célula entra en apoptosis antes de dividirse. Por contra, si la célula posee mutaciones en p53 los daños producidos en el ADN no podrán ser reparados provocando un aumento de la división celular y una disminución en la apoptosis y en las reparaciones del material genético. En esta vía también interviene p14arf, esta proteína es un represor de MDM2 cuando no está unida a p53. En caso de que p14arf no ejerza su correcta función, va a desencadenar un exceso de MDM2 libre, como consecuencia MDM2 secuestrará en unos niveles mayores a los normales a p53 y como resultado se producirá una mayor acumulación de daños en el ADN. Esta suma de alteraciones conduce a la célula a desencadenar un proceso tumoral. Alrededor del 65% de GBM2 presentan mutaciones en TP53, esta alteración molecular también está presente en astrocitomas anaplásicos y astrocitomas de bajo grado de malignidad por lo que se postula que sea un evento temprano en la transformación neoplásica.23,27 Las mutaciones en TP53 frecuentemente encontradas en GBM2 son las transiciones G:C → A:T. Alrededor del 57% de estas transiciones han sido identificadas en los codones 248 y 273 del gen, representando puntos calientes y van a estar sujetos a una mayor tasa de mutación que el resto de los exones. Por el contrario, las mutaciones de TP53 en GBM1 son menos abundantes, no sobrepasando el 28%. Las mutaciones de este gen en los GBM1 están distribuidas por todos los exones sin existir puntos preferenciales a sufrir mutación, y en la mayoría de los casos constituyen eventos secundarios debido a la inestabilidad genómica durante la progresión del tumor.27
Por otra parte, se ha observado que alrededor del 10% de GBM1 sufren amplificación de MDM2, cuando TP53 no se encuentra alterado, evento bastante infrecuente en GBM2. Se han identificado deleciones en homozigosis de p14 en GBM1 y se ha comprobado que alrededor de 1/3 de los astrocitomas de bajo grado presentan metilación en el promotor de p14. Así pues, la inactivación de p14 suele ser por deleción en homocigosis en GBM1 y por metilación en GBM2.26,27
Mutaciones en TP53, amplificaciones de MDM2 y/o deleciones y metilaciones de p14arf son alteraciones moleculares que dan lugar a un acúmulo de otras mutaciones en el ADN, pudiendo originar una muerte celular o una trasformación neoplásica.7
En un principio se creyó que las mutaciones de TP53 eran exclusivas de GBM2 por lo que mediante un análisis mutacional de este gen, seríamos capaces de distinguir entre un GBM1 y un GBM2. En la actualidad varios grupos de investigación también han encontrado mutaciones en GBM1 por lo que esta teoría se ha descartado. Se formula que la presencia de mutaciones en TP53 es un factor pronóstico de supervivencia debido a que las mutaciones de este gen ya se encuentran en gliomas de bajo grado, que comportan un mejor pronóstico. Sin embargo, dado que ahora se admite que las mutaciones de TP53 también están presentes en GBM1, la capacidad predictiva de estas alteraciones debería ser revisada.12,13
Alteraciones de la vía p16ink4/RB1/CDK4 ]]>
Otra de las vía afectadas en glioblastomas es p16ink4/ RB1/CDK4. RB1 (gen del retinoblastoma) se localiza en 13q14.2, su proteína es la que controla la transición G1-S en el ciclo celular. Cuando rb1 no está fosforilado secuestra a E2F, un factor de trascripción que activa genes implicados en la transición G1-S del ciclo celular cuando no está unido a rb1. La fosforilación de rb1 es producida por CDK4 (ciclina dependiente de la quinasa 4) y la proteína encargada de inhibir a esta ciclina es p16ink4 (inhibidor de la ciclina dependiente de la quinasa 4). La pérdida en homozigosis de p16ink4, y/o la amplificación de CDK4 provoca que rb1 esté continuamente fosforilada y no pueda unirse a E2F; como resultado se produce una división celular incontrolada. Estas dos alteraciones se encuentran presentes en glioblastomas,15 así como también la metilación del promotor de RB1, aunque esta metilación es más frecuente en GBM2 que en GBM1. En astrocitomas de bajo grado, hasta el momento no existen suficientes datos que nos demuestren que existe metilación del promotor de RB1. En astrocitomas anaplásicos es bastante infrecuente a metilación de dicho promotor, por lo que se cree que esta alteración sería un evento tardío en la progresión del astrocitoma a GBM2.25
Alteraciones en el gen EGFR
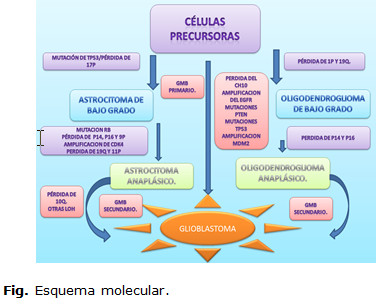
Otra de las alteraciones genéticas presentes en glioblastomas es la amplificación del gen codificador del receptor del factor de crecimiento epidérmico (EGFR). EGFR se localiza en 7p12 y su sobrexpresión génica puede deberse, entre otras alteraciones, a una amplificación en tándem que da lugar a diferentes variantes de la proteína; la más común es la variante EGFRvIII.13 Esta alteración estructural se debe preferentemente a una deleción de 801 pares de bases (p.b.), que abarca desde los exones 2 hasta el 7 y una posterior fusión del resto de los exones, dando lugar a una amplificación en tándem del gen. Ello provoca la síntesis de la proteína con el receptor truncado y constitutivamente activado independientemente del ligando; como resultado la célula comienza a dividirse de forma incontrolada.10 La detección de EGFRvIII por inmunohistoquímica no parece estar relacionada con la supervivencia en los GBM pero sí con los astrocitomas anaplásicos, lo cual sugiere que la detección de EGFRvIII puede ser utilizada para identificar y/o confirmar la identidad de un astrocitoma que se comportaría como un GBM1. La habilidad de las células tumorales para generar estas formas mutantes funcionales de EGFR puede contribuir a la capacidad de los gliomas para evadir la quimioterapia, así como las mutaciones presentes en el gen también pueden influir en el pronóstico o el tratamiento a utilizar.15,26 Otro de los mecanismos por los que puede existir una sobredosis del gen sería la polisomía del cromosoma 7 que frecuentemente se observa en este tipo de tumores. Por último, la amplificación de EGFR ocurre en el 40% de GBM1 siendo abundante en GBM2.11,19 Inicialmente se pensó que esta alteración era exclusiva de GBM1 con respecto a GBM2 pero con el tiempo otros trabajos han demostrado que en GBM2 también puede existir amplificación de EGFR. Existen diferentes mecanismos por los cuales se alteran desde el punto de vista molecular el material genético que originan los glioblastomas. La figura muestra el esquema de los diferentes mecanismos y alteraciones moleculares más frecuentes implicadas en la génesis de un glioblastoma.
Verhaak,25 (TCGA) analizaron perfiles de expresión génica en 200 Glioblastomas (GB) e identificaron 840 genes que les permitieron establecer cuatro subtipos moleculares de GB, que posteriormente fueron confirmados mediante diferentes estudios con cultivos celulares, modelos animales y muestras tumorales humanas: proneural, neural, clásico y mesenquimal.
Proneural: es el subtipo que más se asemeja a un oligodendrocito y es dominado por la activación de la vía de PDGR. Presenta, además, mutaciones en IDH1 y en TP53. Afecta a pacientes más jóvenes, presenta una mejor supervivencia y se asocia a GB secundarios. Neural: es el que más se asemeja a una neurona madura y no tiene una vía dominante en su biología. Tiene marcadores neuronales como NEFL, GABRA1, SYT1 y SLC12A5, y algunos sugieren que no es un subgrupo propio sino una mezcla de alguno y de tejido cerebral normal. Clásico: este subtipo y el mesenquimal son los que más se asemejan a los astrocitos y está dominado por amplificación y activación de la mutación activadora de EGFR. Además, presenta alteraciones típicas de los GB como ganancia del cromosoma 7, amplificación y/o mutación de EGFR, pérdida del cromosoma 10, deleción de CDKN2A y ausencia del resto de alteraciones (ej. TP53, IDH1, etc.). Mesenquimal: es dominado por perdida de NF1. Además, presenta sobreexpresión de marcadores de células mesenquimales, CHI3L1 y MET, y por deleción de NF1.23-25
Recientemente Brennan,7 (TCGA) realizaron un análisis genómico, epigenómico, transcriptómico y proteómico en más de 500 casos de GB, e identificaron distintas firmas de expresión de oncogenes y mutaciones que impactan en la sobrevida de los pacientes y pueden predecir respuesta a terapias blanco: encontraron que el 40% de los tumores tuvieron, al menos, una mutacion no- sinónima entre los genes modificadores de cromatina. La mayoría de GB tuvieron rearreglos estructurales y se encontró una alta frecuencia de las variantes estruturales en el brazo q del cromosoma 12 (región que contiene los genes MDM2 y CDK4). Encontraron, ademas, que el pronóstico favorable del subtipo proneural está asociado al fenotipo G- CIMP, y que la metilación del promotor MGMT se asocia con un pronóstico favorable solo en el sutipo clásico. El análisis proteómico encuentra que la expresión de estas no se correlaciona linearmente con la expresión de genes.7
]]>
Así mismo Sturm,et al26 evaluaron más de 130 muestras de GB a través de análisis basado en epigenética, número de copias y expresión de genes. Ellos encuentran seis subgrupos epigenéticos de GB de acuerdo al patrón de metilación de DNA global que albergan distintos puntos calientes de mutaciones, alteraciones en el número de copias de DNA y patrones transcriptómicos. Dos de estos subgrupos presentan mutaciones recurrentes de H3F3A que afectan a aminoácidos críticos (K27 y G34) de la histona H3.3. Cada una de estas mutaciones define un subgrupo de GB con predilección por compartimientos anatómicos separados, con un patrón de metilación global distinto, y con capacidad de regular en forma específica los factores de transcripción OLIG1, OLIG2 y FOXG1. Un tercer subgrupo presenta mutaciones IDH1 y ausencia de las mutaciones previamente mencionadas (H3F3A). Las tres mutaciones previamente descritas se presentaron en población pediátrica. Identifica también tres subgrupos epigenéticos adicionales en adultos con GB.26
Noushmehr,27 et al (TCGA) evaluaron las alteraciones en metilación de DNA promotor en 272 tumores GB y encontraron que un subgrupo específico de muestras presentaban hipermetilación en un número mayor de focos, y lo denominaron fenotipo metilador de islas CpG en gliomas (G-CIMP). Los tumores G-CIMP pertenecen al subgrupo proneural, son más prevalentes entre los gliomas de bajo grado, tienen distintas alteraciones en el número de copias, y están asociados con mutaciones somáticas de IDH1. Los pacientes con tumores G-CIMP son más jóvenes y tienen una mayor sobrevida.
Perspectivas actuales de diagnóstico y tratamiento
Un equipo de investigadores del Centro de Biología Molecular Severo Ochoa en el que se integra un equipo de la Universidad Autónoma de Madrid, el Ciberned y el CSIC, ha identificado una proteína del esqueleto celular como responsable de la progresión de tumores de cerebro de tipo glioma. El trabajo, publicado en la revista ‘Cell Reports’, describe que los niveles altos de esta proteína, denominada WIP, favorecen el crecimiento de los gliomas humanos y esto produce una baja tasa de supervivencia en quienes presentan esta variante de tumores. Según explican los directores del estudio, Inés Antón y Francisco “hemos observado que la proteína WIP mantiene una población de células madre tumorales con una alta capacidad de dividirse y de migrar, facilitando así la progresión tumoral”.
Para los investigadores, este hallazgo transciende a la investigación básica, ya que la descripción de este nuevo mecanismo permite proponer nuevas dianas terapéuticas para el tratamiento de tumores altamente invasivos como los gliomas.
“La eliminación o bloqueo de WIP sería un nueva diana terapéutica potencial para un grupo de tumores como los gliomas, muy agresivos y con pocas alternativas terapéuticas en estos momentos”, recalcaron.
El funcionamiento de cualquier tipo celular dentro de un organismo depende, en gran parte, de la capacidad de modificar su forma y dentro de cualquier célula existe un grupo de proteínas que mantienen un esqueleto responsable de hacer esto que es esencial para que una célula, tumoral o no, se divida, se adhiera o se mueva. Dicho esqueleto o andamiaje celular es esencial para la forma concreta de una célula, para que se divida, para que se adhiera, o para que se mueva. Y así ocurre tanto para las células normales como para las células tumorales, donde algunas de estas propiedades están muy exageradas o descontroladas, dicen los investigadores. Dentro de un tumor existe una población de células que mantiene un alto nivel de división, así como características de células madre que, se sospecha, son las responsables de mantener el crecimiento del tumor. Debido a su alta capacidad de migrar, dan además opciones para generar metástasis en otras regiones del cuerpo.27-29
]]> Por este motivo, el estudio sobre cómo se regula el esqueleto celular tiene implicación tanto en el desarrollo de todos los organismos multicelulares como en los desarrollos tumorales, donde dichos procesos (proliferación, adhesión y migración) están muy desregulados.
CONCLUSIONES
A modo de conclusión planteamos que el estudio sobre cómo se regula el esqueleto celular tiene implicación tanto en el desarrollo de todos los organismos multicelulares como en los desarrollos tumorales, donde dichos procesos (proliferación, adhesión y migración) están muy desregulados.
REFERENCIAS BIBLIOGRÁFICAS
1- Castañeda CA, Casavilca S, Orrego E, et al. Glioblastoma: análisis molecular y sus implicancias clínicas. Rev Peru Med Exp Salud Publica [Internet]. 2015 [citado 4 Abr 2017];32(2):316-25. Disponible en: http://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1726-46342015000200017
2- CBTRUS. CBTRUS Statistical report: Primary Brain and Central Nervous System Tumors Diagnosed in the Unites States in 2004-2007 [Internet]. USA: CBTRUS; 2011 [citado 4 Abr 2017]. Disponible en: http://www.cbtrus.org/2011-NPCR-SEER/WEB-0407-Report-3-3-2011.pdf
3- Liu W, Zhang S, Zhang L, et al. A prognostic analysis of pediatrics central nervous system small cell tumors: evaluation of EGFR family gene amplification and overexpression. Diagn Pathol. 2014 Jul 1;9:132. Citado en PubMed; PMID: 24986561.
4- Hardell L, Carlberg M, Hansson Mild K. Use of mobile phones and cordless phones is associated with increased risk for glioma and acoustic neuroma. Pathophysiology. 2013 Apr;20(2):85-110. Citado en PubMed; PMID: 23261330.
5- The Cancer Genome Atlas. Genomic Understanding of Glioblastoma Expanded [Internet]. USA: The Cancer Genome Atlas; 2013 [citado 4 Abr 2017]. Disponible en: http://cancergenome.nih.gov/newsevents/newsannouncements/GBM_Expanded_news_release_2013
6- Ohno M, Narita Y, Miyakita Y, et al. Secondary glioblastomas with IDH1/2 mutations have longer glioma history from preceding lower-grade gliomas. Brain Tumor Pathol [Internet]. 2013 Oct [citado 4 Abr 2017];30(4):224-32. Disponible en: https://link.springer.com/article/10.1007/s10014-013-0140-6
7- Dunn GP, Andronesi OC, Cahill DP. From genomics to the clinic: biological and translational insights of mutant IDH1/2 in glioma. Neurosurg Focus. 2013 Feb;34(2):E2. Citado en PubMed; PMID: 23373447.
8- Brennan CW, Verhaak RG, McKenna A, et al. The somatic genomic landscape of glioblastoma. Cell. 2013 Oct 10;155(2):462-77. Citado en PubMed; PMID: 24120142.
]]>
9- Popova SN, Bergqvist M, Dimberg A, et al. Subtyping of gliomas of various WHO grades by the application of immunohistochemistry. Histopathology. 2014 Feb;64(3):365-79. Citado en PubMed; PMID: 24410805.
10- Chinot OL, Wick W, Mason W, et al. Bevacizumab plus radiotherapy-temozolomide for newly diagnosed glioblastoma. N Engl J Med. 2014 Feb 20;370(8):709-22. Citado en PubMed; PMID: 24552318.
11- Gilbert MR, Dignam JJ, Armstrong TS, et al. A randomized trial of bevacizumab for newly diagnosed glioblastoma. N Engl J Med [Internet]. 2014 Feb 20 [citado 4 Abr 2017];370(8):699-708. Disponible en: https://www.nejm.org/doi/full/10.1056/nejmoa1308573
12- Hofland KF, Hansen S, Sorensen M, et al. Neoadjuvant bevacizumab and irinotecan versus bevacizumab and temozolomide followed by concomitant chemoradiotherapy in newly diagnosed glioblastoma multiforme: A randomized phase II study. Acta Oncol. 2014 Jul;53(7):939-44. Citado en PubMed; PMID: 24456504.
13- Pérez Ortiz L , Zaldivar-Vaillant T, Tamayo-Suárez JD. Gliomas malignos. Apuntes oncogenéticos. Rev Española de Neurología. 2000,31(1):49-52. Citado en PubMed; PMID: 12497279.
]]>14- Holdhoff M, Chamberlain MC. Controversies in the treatment of elderly patients with newly diagnosed glioblastoma. J Natl Compr Canc Netw. 2013;11(9):1165-73. Citado en PUBMed; PMID: 24029128.
15- Popova S, Bergqvist M, Dimberg A, et al. Subtyping of gliomas of various WHO grades by the application of immunohistochemistry. Histopathology. 2014;64(3):365–79. Citado en PUBMed; PMID: 24410805.
16- Hundsberger T, Brugge D, Putora P, et al. Re-irradiation with and without bevacizumab as salvage therapy for recurrent or progressive high-grade gliomas. J Neurooncol. 2013;112(1):133–39. Citado en PUBMed; PMID: 23314822.
17- Yana K , Yanga K, RichiJ. The evolving landscape of glioblastoma stem cells. Curr Opin Neurol. 2013;26:701–707. Citado en PUBMed; PMID: 24152818.
18- Franco-Hernández V, Martínez-Glez JA. Unidad de Investigación. Fundación para la Investigación Biomédica del Hospital Universitario La Paz. Madrid. Biología molecular de los glioblastomas. Neurocirugía [Internet]. 2007 [citado 4 Abr 2017];18(5):373-82. Disponible en: http://scielo.isciii.es/pdf/neuro/v18n5/investigacion1.pdf
19- Gargini R, Escoll M, García E, et al. WIP Drives Tumor Progression through YAP/TAZ-Dependent Autonomous Cell Growth. Cell Rep. 2016;17(8):1962-77. Citado en PubMed; PMID: 27851961.
20- Møller HG.A Systematic Review of MicroRNA in Glioblastoma Multiforme: Micro-modulators in the Mesenchymal Mode of Migration and Invasion. Mol Neurobiol. 2013;47(1):131-44. Citado en PubMed; PMID: 23054677.
21- Heroux M S. Comprehensive characterization of glioblastoma tumor tissues for biomarker identification using mass spectrometry-based label-free quantitative proteomics. Physiol Genomics. 2014 Jul 1;46(13):467-81. Citado en PubMed; PMID:24803679.
22- Bady P, Sciuscio D, Diserens AC, et al. MGMT methylation analysis of glioblastoma on the Infinium methylation BeadChip identifies two distinct CpG regions associated with gene silencing and outcome, yielding a prediction model for comparisons across datasets, tumor grades, and CIMP-status. Acta Neuropathol. 2012;124(4):547-60. Citado en PubMed; PMID: PMID: 22810491.
23- Solomón MT, Selva JC, Figueredo J, et al. Radiotherapy plus nimotuzumab or placebo in the treatment of high grade glioma patients: results from a randomized, double blind trial. BMC Cancer. 2013 Jun 19;13:299. Citado en PubMed; PMID: 23782513.
24- Brennan CW, Verhaak RG, McKenna A, et al. The somatic genomic landscape of glioblastoma. Cell. 2013 Oct 10;155(2):462-77. Citado en PubMed: PMID: 24120142.
25- Hofland KF, Hansen S, Sorensen M, et al. Neoadjuvant bevacizumab and irinotecan versus bevacizumab and temozolomide followed by concomitant chemoradiotherapy in newly diagnosed glioblastoma multiforme: A randomized phase II study. Acta Oncol. 2014 Jul;53(7):939-44. Citado en PubMed; PMID: 24456504.
26- Huse JT, Holland E, De Angelis LM. Glioblastoma: molecular analysis and clinical implications. Annu Rev Med. 2013;64:59-70. Citado en PubMed; PMID: 23043492.
27- Hegi ME, Janzer RC, Lambiv WL,et al. Presence of an oligodendroglioma-like component in newly diagnosed glioblastoma identifies a pathogenetically heterogeneous subgroup and lacks prognostic value: central pathology review of the EORTC_26981/NCIC_CE.3 trial. Acta Neuropathol. 2012 Jun;123(6):841-52. Citado en PubMed; PMID: 22249618.
28- Olson RA, Brastianos PK, Palma DA. Prognostic and predictive value of epigenetic silencing of MGMT in patients with high grade gliomas: a systematic review and meta-analysis. J Neurooncol. 2011 Nov;105(2):325-35. Citado en PubMed; PMID: 21523485.
29- Ramos TC, Figueredo J, Catala M, et al. Treatment of high-grade glioma patients with the humanized anti-epidermal growth factor receptor (EGFR) antibody h-R3: report from a phase I/II trial. Cancer Biol Ther. 2006 Apr;5(4):375-9. Citado en PubMed; PMID: 16575203.
]]>
Recibido: 10/10/17
Aprobado: 2/7/18
Enrique Marcos Sierra Benítez. Hospital Universitario Comandante Faustino Pérez. Matanzas. Correo electrónico: enriquem.mtz@infomed.sld.cu
]]>