Sistema para la inclusión de pacientes en ensayos clínicos en tiempo real
System for the real time inclusion of patients in clinical trials
Aliuska Frías Blanco,I Mabel Álvarez Cardona,II Yanela Santiesteban González,III Yuliannis Santiesteban Gonzáles,IV Carmen Viada González,V Yisel Sánchez Gallarado,VI Patricial Lorenzo-Luaces Alvarez,VII Tania Puente CollejoVIII
IGerente de datos. Técnico Innovador nivel II. Centro de Inmunología Molecular, 216 & 15, Atabey, Playa, Cuba. E-mail: aliuska@cim.sld.cu
IIGerente de datos. Centro de Inmunología Molecular, 216 & 15, Atabey, Playa, Cuba. E-mail: mabel@cim.sld.cu ]]>
El Centro de Inmunología Molecular ha venido desarrollando una serie de biomoléculas para el tratamiento del cáncer. El pronóstico anual de inclusión de pacientes al ensayo clínico es de 3000. El objetivo de este trabajo fue encontrar una forma de controlar este proceso. El grupo de manejo de datos, en conjunto con el Centro Nacional Coordinador de Ensayos Clínicos, comenzó la inclusión de pacientes en ensayos clínicos por vía telefónica y a través de correo electrónico. A partir del 2010 se creó el sitio de Inclusión de Ensayos Clínicos (http://cimensayossp/clinica/default.aspx), el cual es una potente herramienta que permite controlar la situación de la inclusión de los pacientes. El mismo permitió reportar el número de inclusión y conocer el ritmo de inclusión real en cada ensayo para poder tomar acciones y mejorar así la inclusión planificada. Además se garantiza que no existan retrasos en la entrega del producto de investigación. ]]>
Palabras clave: ensayos clínicos, inclusión de pacientes, velocidad de reclutamiento.The Molecular Immunology Center has developed a series of biomolecules for cancer treatment. With a forecast for the inclusion of 3000 patients per year in clinical trials, the aim of this study was to find a way to control that process. The data management group, in conjunction with the National Coordinating Center for Clinical Trials, began enrolling patients in clinical trials by phone and through email. In 2010 the web site (http://cimensayossp/clinica/default.aspx) was created to Include Clinical Trials, which is a powerful tool to control the status of patient inclusion. It allowed reporting the number of inclusions and to know the actual inclusion rate in each trial to take action and improve the planned inclusion. In addition, it ensures no delays in the delivery of the investigational product.
Key words: clinical trials, patient inclusion, speed of recruitment.
INTRODUCCIÓN
El Centro de Inmunología Molecular (CIM) se inauguró en 1994. Desde sus inicios, esta entidad cubana ha venido desarrollando, una serie de biomoléculas para el tratamiento del cáncer. Esto trae aparejado el incremento del número de pacientes a estudiar.1 En estos momentos se despliega una gama de más de 50 ensayos clínicos, algunos de ellos multinacionales, con un pronóstico de inclusión de 3000 pacientes por año; además se mantiene el tratamiento a más de 350 pacientes incluidos en años anteriores. En este proceso están involucrados más de 30 hospitales, en todo el país.
En la década del 90, el Grupo de manejo de datos de la Dirección de investigaciones clínicas, en conjunto con el Centro Nacional Coordinador de Ensayos Clínicos (CENCEC), comenzó la inclusión de pacientes en ensayos clínicos por vía telefónica y a través de correo electrónico. En fecha más reciente, se crearon bases de datos en el sistema estadístico profesional SPSS Versión 11.5, independientes por cada ensayo clínico y una base de datos en Microsoft Office Excel 2007, centralizada, donde se recogían los totales de incluidos por ensayo clínico y por mes del año en curso.2
Como cada base de datos se completaba por diferentes grupos de trabajo, no siempre reportaban igual cantidad de pacientes incluidos. Por esto se consideró importante controlar el proceso de inclusión en ensayos clínicos para poder administrar mejor los recursos necesarios para llevar a cabo las investigaciones, garantizando cumplir las buenas prácticas clínicas requeridas según los estándares de calidad internacionales.3
El Grupo de manejo de datos de la Dirección de investigaciones clínicas del centro identificó la necesidad de resolver este problema, para lo cual nos trazamos los siguientes objetivos: ]]>
- Proponer una forma de controlar la inclusión de pacientes en ensayos clínicos del Centro de Inmunología Molecular.- Identificar las variables necesarias para controlar el proceso de inclusión de pacientes en ensayos clínicos.
- Definir los tipos de informes, instancias y periodicidad que se requerían.4
MATERIAL Y MÉTODOS
Para identificar la información necesaria para la inclusión de pacientes en los ensayos clínicos se realizaron varios encuentros con el equipo multidisciplinario de investigación: promotores de investigación, monitores, distribuidores de producto, manejadores de datos y estadísticos. Se planificó crear una base de datos centralizada la cual debe ser actualizada por un responsable del CIM y otro por parte del CENCEC.
El tipo de investigación fue clasificada como longitudinal prospectiva. A través de esta investigación se identificaron los problemas que existen en el control de los pacientes incluidos en ensayo clínico, este proceso generaba diferencias en el número de incluidos reportados por el CENCEC y por el CIM, para cada ensayo clínico.
El método utilizado en esta investigación, fue el método teórico de generalización. Este método permitió caracterizar la inclusión por sitio de investigación y/o provincia, por ensayo clínico y por enfermedad a lo largo de todo el país. A partir de los resultados de esta investigación se tomaron medidas de apoyo para mejorar la inclusión en cada sitio clínico.
Se consideró que el estudio estuvo dirigido al universo, ya que se seleccionaron la totalidad de los ensayos clínicos del CIM, que son 132, de ellos 47 terminados y 89 en curso, tanto nacional como multinacional.
Se diseñó una base de datos en formato SharePoint que permitió la inclusión desde el CIM y desde el CENCEC, cuyos formularios de captación fueron diseñados en Microsoft Office InfoPath 2007, el envío de correos automáticos con Designer y los informes de inclusión en Microsoft Office Excel 2007.5 Las variables que fueron seleccionadas para este formulario se muestran en la figura 1. ]]>
El proceso de inclusión, se puede ver afectado por varias razones, que pueden ser: problemas en la conectividad al servidor de Infomed, ya que el CENCEC se conecta al CIM por esta vía; o problemas de conexión en la Intranet del CIM. Ambos problemas implicarían que no llegue la solitud del producto de investigación en tiempo real, lo que conllevaría a que la vacuna no sea enviada a tiempo y puede existir un retraso en el tratamiento del paciente, siendo este el principal perjudicado.
RESULTADOS
Con la creación de este sitio se obtiene un mejoramiento de los datos de inclusión reportado por ambas instituciones (CIM y CENCEC), lo que nos permitió tener un mejor control de los recursos necesarios para llevar a cabo la compleja actividad de ensayos clínicos a lo largo de todo el país.
La información se recoge diariamente a medida que se van incluyendo pacientes en los diferentes ensayos clínicos abiertos. Esto permitió la creación de informes mensuales, trimestrales y anuales para diferentes instancias: hospitales y policlínicos, provinciales y nacionales. Para la creación de estos informes fueron aplicadas técnicas estadísticas descriptivas como tablas de frecuencia y gráficos de barra por sitio clínico, por ensayo, meses y por año, los cuales fueron procesados utilizando la aplicación de Microsoft Office Excel 2007. La información que nos brinda el sitio se resume en la lista siguiente:
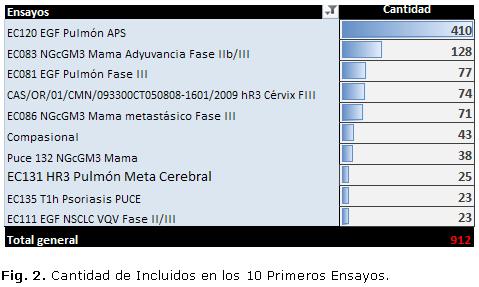
1. 10 Primeros Ensayos en Inclusión. Como se muestra en la figura 2.
2. 10 Primeros Sitios Clínicos en Inclusión. Similar a la figura 2 pero por sitio clínico, donde se muestran los 10 primeros hospitales que tienen más pacientes incluidos.
3. Comportamiento por Producto. Como se expone en la figura 3.
4. Control de Inclusiones Anuales. Como se revela en la figura 4. ]]>
5. Inclusiones Mensuales 2011. Similar a la figura 4 pero por meses, donde se muestran la cantidad de pacientes incluidos en cada uno de los meses del año en curso.6. Inclusiones por Provincia. Similar a la figura 2 pero por provincia, donde se muestran los 10 primeras provincias que tienen más pacientes incluidos.
Además se puede calcular el indicador de inclusión por meses el cual se considera el más importante de la Dirección de Investigaciones Clínicas para determinar el cumplimiento del plan de inclusión, como se observa en la figura 5.
Otra de las actividades que se ve beneficiada, con la creación del sitio de inclusión son las visitas gerenciales a las provincias, que se realizan por parte de la dirección del CIM, del CENCEC y el Grupo Nacional de Oncología, en las cuales se ofrecen los datos referentes a las cantidades de pacientes incluidos en la provincia por ensayos en curso, los pacientes incluidos en la base de datos de esos ensayos y de esas provincias, y la incidencia por indicación de cáncer reportada por el Registro nacional de cáncer de Cuba más vigente.
DISCUSIÓN
Según los resultados obtenidos se infiere que las provincias y sitios que más incluyen son: en La Habana el Instituto Nacional de Oncología y Radiología (INOR) y el Hospital Hermanos Ameijeiras (HHA), en Matanzas el José Ramón López Tabranes (JRLT) y en Villa Clara el Celestino Hernández Robau (CHR), porque son las provincias con más ensayos clínicos abiertos con varios productos e indicaciones. Los ensayos que más incluyeron fueron los Fase III o IV y los PUCE que son multicéntricos y tienen criterios de inclusión más flexibles que el resto de los ensayos lo que facilita el aumento del número de pacientes incluidos. El producto y la indicación que más incluyeron fueron el EGF en pulmón debido a la existencia de mayor cantidad de ensayos de ese producto en esa localización.6
Los ensayos clínicos para evaluar tratamientos del cáncer son una de las investigaciones más frecuentes. Sin embargo, aún hay muchas instituciones e investigadores que tienen poca experiencia en su desarrollo. Entre los años 2000 y el 2011 se han desarrollado más de 50 ensayos clínicos para el tratamiento del cáncer dirigidos por el CIM.7 Las experiencias prácticas que se sucedieron en su ejecución motivaron la propuesta de las variadas consideraciones que se deben tener en cuenta para futuros estudios de tratamientos para el cáncer en Cuba.
Para el cálculo y planificación del período de inclusión del estudio es indispensable tener los datos de cada una de las instituciones participantes. Estas características del sistema de información provocan dificultades para estimar adecuadamente el período de inclusión del ensayo. Esa información es de gran importancia para la planificación de los recursos del estudio y para establecer la estrategia del desarrollo clínico del producto en investigación.8 ]]>
En la planificación de todo ensayo clínico en Oncología es esencial tomar todas las medidas organizativas necesarias para la disminución del intervalo de tiempo entre el diagnóstico y el inicio del tratamiento.9 Para lograr ese objetivo es indispensable la coordinación entre todos los servicios involucrados en el tratamiento. Además, el suministro del medicamento en estudio y de los tratamientos controles debe ser rápido y tiene que quedar bien documentado.
CONCLUSIONES
Con la informatización del proceso de inclusión se evitan diferencias en la información reportada, ya que todo parte de una única base de datos. Además, esto garantiza que no existan retrasos en la entrega del producto de investigación ni en la actividad de monitoreo de cada ensayo clínico. Estos dos procesos se activan a partir de la inclusión de cada paciente en cada ensayo clínico.
El sitio de Inclusión de pacientes del CIM es una potente herramienta que permite controlar y monitorizar la situación de la inclusión de los pacientes en estudios clínicos dirigidos por el CIM.
Las tasas de reclutamiento son bajas con un elevado número de ensayos, lo que puede indicar una saturación de los centros.
El número de pacientes reclutados por sitio es bajo, probablemente causado por el elevado grado de complejidad de los ensayos clínicos pero también por una baja eficiencia de nuestros procesos.
El elevado porcentaje de ensayos con bajo reclutamiento hace necesario poner en marcha planes de contingencia específicos.
La velocidad de reclutamiento de pacientes por mes para todos los ensayos se comporta de una manera estable.
]]>
REFERENCIAS BIBLIOGRÁFICAS1. Laporte JR. El ensayo clínico controlado. En: Laporte J, ed. Principios básicos de la investigación clínica. 2da ed. Madrid: AstraZeneca; 2002. p. 27-54.
2. Hernández AR. Ensayos Clínicos. Sus pilares fundamentales. En: Pascual MA, Hernández AR, eds. Diseño y Conducción de Ensayos Clínicos. Lima: Instituto de Fitoterapia Americano; 2007. p. 12-26.
3. Farell GE, Egaña E, Fernández F. Investigación Científica y nuevas tecnologías. La Habana: Editorial Científico-Técnica; 2003. p. 35-74.
4. Hernández AR, Rodríguez BA, Parra JZ, Cachimaille YB. Metodología para la formación de recursos humanos del Sistema Nacional de Salud en ensayos clínicos. Educación Médica Superior. 2008;22(3). Disponible en: http://bvs.sld.cu/revistas/ems/vol22_3_08/ems09308.htm
5. PHP [sitio en Internet]. [Consultado, 23 de Marzo de 2011]. Disponible en: http://es.wikipedia.org/wiki/PHP
6. Martínez F. El reclutamiento de pacientes en los ensayos clínicos internacionales. [Citado el 17 May. 2012]. Disponible en: http://www.pmfarma.es/articulos/932-el-reclutamiento-de-pacientes-en-los-ensayos-clinicos-internacionales.html
7. Monreal M y Montenegro A. Consideraciones prácticas para los ensayos clínicos en el tratamiento del cáncer de ovario en Cuba. Rev Cubana Med 2002;41(4). Disponible en: http://bvs.sld.cu/revistas/med/vol41_4_02/med014202.htm
8. Álvarez C. Mejoras en el reclutamiento de pacientes en ensayo clínicos. IV Conferencia Anual de las Plataformas Tecnológicas de Investigación Biomédica. Madrid, 28 Febrero 2011. [Citado el 17 May. 2012]. Disponible en: http://www.medicamentos-innovadores.org/sites/default/files/medinnovadores/Espa%C3%B1ol/Eventos/2011/28_02_2011/Presentaciones/28defebrero/Paralela1 /CARMENALVAREZ.pdf
9. Esteban E. Indicadores en el Reclutamiento de Pacientes. IV Conferencia Anual de las Plataformas Tecnológicas de Investigación Biomédica. Madrid, 28 de febrero 2011. [Citado el 17 May. 2012]. Disponible en: http://www.medicamentos-innovadores.org/sites/default/files/medinnovadores/Espa%C3%B1ol/Eventos/2011/28_02_2011/Presentaciones/28defebrero/Paralela1 /ESTHERESTEBAN_RECLUTAMIENTO%209P_FINAL.pdf
Recibido: 17 de febrero de 2012.
Aprobado: 18 de mayo de 2012. ]]>