REVISIÓN BIBLIOGRÁFICA
Teoría celular de la coagulación: de las cascadas a las membranas celulares
Cell-based coagulation theory: from the waterfall sequence to cell membranes
Rafael Alejandro Gómez Baute , Tamara Guerra Alfonso , Liermis Dita Salabert , Julio Dámaso Fernández Águila , Maritza Cabrera Zamora
]]> Hospital General Universitario "Dr. Gustavo Aldereguía Lima", Cienfuegos, Cienfuegos, Cuba, CP: 55100
RESUMEN
El modelo clásico de la coagulación, propuesto hace más de 40 años, separa las fases celular y humoral de la coagulación. Considera que el proceso de hemostasia se consigue a través de la activación secuencial de enzimas efectoras en dos vías independientes: la extrínseca y la intrínseca. Una nueva teoría, conocida como modelo celular de la coagulación, reemplaza la tradicional hipótesis de las cascadas y enfatiza en las células como elementos esenciales capaces de dirigir el proceso hemostático, mediante la interacción de superficies celulares, factor tisular y factor VII, en tres fases simultáneas: iniciación, amplificación y propagación. En la presente revisión bibliográfica se abunda con detalle sobre la nueva teoría celular de la coagulación, para lo cual se consultaron 33 artículos, con el objetivo de describir los aspectos más importantes de la nueva teoría y sus ventajas respecto a la vieja.
Palabras clave: coagulación sanguínea, hemostasis.
ABSTRACT
The classical model of coagulation, proposed more than 40 years ago, separates humoral and cellular phases of coagulation. This model assumes that the hemostatic process is achieved through the sequential activation of effector enzymes in two independent ways: extrinsic and intrinsic. A new theory, known as the cell-based coagulation theory, has replaced the traditional hypothesis. In this new theory cells are emphasized as the essential elements capable of directing the hemostatic process, through the interaction of cell surfaces, tissue factor and factor VII in three simultaneous phases: initiation, amplification and propagation. The present literary review presents details on the new cell-based coagulation theory. In this sense, 33 articles were consulted in order to describe the most important aspects of the new theory and its advantages over the previous one.
Key words: blood coagulation, hemostasis.
]]>
INTRODUCCIÓN En situaciones fisiológicas la sangre se mantiene en estado líquido dentro de la vasculatura y al mismo tiempo es capaz de formar coágulos para sellar una herida. (1) El término hemostasia significa prevención de la pérdida de sangre. Siempre que se lesiona un vaso, la hemostasia se consigue por diversos mecanismos: espasmo vascular, formación de un tapón de plaquetas, formación de un coágulo sanguíneo y proliferación final de tejido fibroso para el completo cierre de la lesión. La coagulación de la sangre es un proceso delicadamente equilibrado que resulta de una serie ordenada de reacciones, en el cual existe participación e interacción entre células y proteínas con características bioquímicas especiales. (1) El modelo clásico de la coagulación fue descrito en 1964 por Davie y Ratnoff como dos secuencias de reacciones lineales e independientes entre sí, que culminaban en una vía final común con la activación del factor X. De acuerdo con este modelo, la activación de cualquiera de las dos vías resultaba en la producción de grandes cantidades de trombina y la subsecuente formación de fibrina. (2) El modelo fue muy útil al describir de forma organizada la interacción entre las proteínas con actividad pro-coagulante y probablemente siga encontrando utilidad al apoyar la evaluación de los tiempos globales de la coagulación. (2) Sin embargo, este modelo no es válido para explicar los mecanismos que llevan a la hemostasia in vivo; no le otorga importancia a cada uno de los complejos con actividad pro-coagulante; no considera la interacción del sistema con las células que participan en la coagulación; no considera las interacciones entre las dos vías de la coagulación y falla en explicar con detalle los aspectos fisiopatológicos del sistema hemostático. En otras palabras, el modelo no permite explicar los distintos grados de tendencia a la hemorragia que resultan de deficiencias de los diferentes componentes de las dos vías. (3)
En un intento por abordar el fenómeno de la hemostasia desde otra perspectiva, se han desarrollado modelos experimentales y conceptuales para probar las hipótesis en un modelo bioquímico ex vivo, y permitir un mejor entendimiento de cómo el sistema funciona in vivo.
El más logrado de éstos es el modelo celular de la coagulación desarrollado por Maureane Hoffman en el 2003 donde el aspecto más importante es considerar a las células como elementos esenciales en el proceso de formación del coágulo y demostrar que las superficies celulares poseen características especiales capaces de dirigir el proceso hemostático. La nueva teoría rompe así con el paradigma del modelo tradicional de Davie y Ratnoff en el cual el papel de la célula era únicamente el de ofrecer una superficie portadora de fosfatidilserina donde los complejos pro-coagulantes podrían ser armados. (4)
Todo lo anterior justifica y sustenta la importancia de esta revisión bibliográfica, debido a que la teoría tradicional de las cascadas de la coagulación conocida y empleada por decenas de años está siendo sustituida por un nuevo y complejo modelo celular que responde a todas las interrogantes que existían en relación con este tema.
Por todo lo anterior queda implícito el fundamento de esta revisión y la elección de esta temática, ya que representa una nueva ventana de exploración para poder describir y comprender efectivamente el mecanismo de la coagulación, proceso esencial para mantener la adecuada hemostasia del organismo. Por ello se pretende describir los aspectos más importantes de la nueva teoría celular de la coagulación y sus ventajas respecto a la vieja teoría, destacar los principales elementos de la teoría clásica de la coagulación así como las diferentes fases que conforman este nuevo modelo integrador de la hemostasia. Se comenta además sobre las perspectivas clínicas del modelo celular de la coagulación.
DESARROLLO
ASPECTOS IMPORTANTES DE LA COAGULACIÓN
La coagulación consiste en una serie de reacciones que se generan en la superficie celular y cuyo objetivo es la formación de trombina en sitios de lesión vascular. Es un proceso delicadamente equilibrado en el cual existe participación e interacciones entre células y proteínas con características bioquímicas especiales (también conocidas como factores de la coagulación), resaltando la importancia del complejo factor VII/factor tisular en la activación del sistema. (1)
Los factores de la coagulación dependientes de vitamina K, comparten características bioquímicas y estructurales especiales; la más importante de estas es la presencia de un dominio de ácido ?-carboxiglutámico en la región amino-terminal de la molécula. Este dominio contiene entre 8 y 12 residuos de glutamato (Gla) y tiene 3 funciones de gran importancia fisiológica: 1) permitir la activación de la proteína a través de la carboxilación de residuos de ácido glutámico; 2) favorecer la unión con iones de calcio y otros cofactores para catalizar las reacciones de proteólisis; 3) facilitar la interacción de los fosfolípidos de carga negativa para aumentar la actividad proteolítica. (1)
Además de la estructura, estos factores de la coagulación comparten características funcionales especiales; todos son sintetizados en el hígado y sufren cambios postranscripcionales consistentes en: eliminación del propéptido señal y la mencionada carboxilación de los residuos de ácido glutámico a través de la enzima glutamato-carboxilasa.
Estos factores circulan en forma de cimógenos o proenzimas que al activarse adquieren capacidad de proteasa de serina, la cual se ve potencializada por la presencia de cofactores específicos. (5)
De la misma manera, la asociación de estas enzimas con las cabezas con carga negativa de los fosfolípidos de membrana, especialmente la fosfatidilserina, incrementa la actividad de proteasa. (5)
FACTORES DE LA COAGULACIÓN
Factor II: la trombina es la enzima efectora central del sistema de coagulación al tener varias funciones importantes: a) la función principal y más conocida de la trombina es la escisión de los fibrinopéptidos A y B, los cuales se polimerizan para formar la fibrina; b) es un potente activador de plaquetas a través de receptores PAR-1 y PAR-4, así como de la glucoproteína Ib?; c) tiene efectos procoagulantes al participar en la retroalimentación positiva mediante la activación de los factores V, VIII, XI y XIII; d) activa a la enzima parecida a procarboxipeptidasa-B, también conocida como inhibidor de fibrinólisis activado por trombina (IFAT), la cual inhibe la degradación de fibrina mediada por plasmina; e) agregado a sus efectos pro-coagulantes la trombina se une a su cofactor celular, trombomodulina, presente en las células endoteliales de los lechos microvasculares, lo que permite la activación de la proteína; f) son también conocidas las actividades de factor de crecimiento y de citocina con un papel creciente en los procesos de aterosclerosis, reparación de heridas e inflamación. La protrombina es escindida por el complejo protrombinasa, que consiste en un complejo unido a fosfolípidos formado por la enzima factor Xa y su cofactor Va. El dominio efector (trombina) se separa del resto de la proteína. El principal inhibidor plasmático de la trombina es la antitrobina III. (5)
Factor VII/factor tisular: conocido como proconvertina, al factor VII actualmente se le considera la piedra angular de la activación de los procesos de hemostasia, junto con su cofactor, el factor tisular. La mayor parte del factor VII se encuentra en la sangre en forma de cimógeno y sólo un 1 % circula de manera activa. Su principal activador es el factor X.
El factor tisular es una proteína de membrana presente de manera abundante en las células que rodean el lecho vascular, sobre todo fibroblastos y músculo liso; es el único factor de la coagulación que normalmente no está presente en la sangre. Aunque algunos estudios señalan su presencia en las membranas de leucocitos y monocitos.
El factor VIIa y el factor tisular se ponen en contacto cuando existe lesión vascular, el complejo activa los factores IX y X y es inhibido principalmente por la vía del inhibidor del factor tisular (VIFT) y en menor medida por la antitrombina III. (6)
Factor IX/factor VIII: el factor IX es una enzima fundamental en los procesos de hemostasia y su ausencia congénita se traduce clínicamente en tendencia al sangrado (hemofilia B, deficiencia de Christmas). Tiene dos fuentes potenciales de activación: el complejo factor VIIa/FT y el factor XIa, existe también una glicoproteína plaquetaria con la capacidad de activar este factor.
Es activado por la trombina y por el factor Xa. Una vez activados, el factor IX se une con el factor VIII, que junto con Ca+ y en presencia de fosfolípidos constituyen el complejo Xasa. (5, 6)
Factor X/factor V: el factor de Stuart-Prower, como se le conocía anteriormente, es una proteasa de serina que, junto con el cofactor Va y fosfolípidos de membrana, forma el complejo protrombinasas que activa a la trombina. Representa el primer factor de la vía final común en el modelo antiguo de la hemostasia y tiene, de la misma manera, dos fuentes potenciales de activación: el complejo factor VIIa/FT y el complejo IXa/VIIIa.
El factor V es homólogo al factor VIII en su estructura génica, secuencia de aminoácidos y dominios moleculares. Circula en forma libre en el plasma, pero un 20 % se encuentra en los gránulos ? plaquetarios. Su principal activador es la trombina, pero puede también ser activado por el factor X. (7)
Fibrinógeno y factor XIII: el fibrinógeno es una glucoproteína perteneciente al grupo de las globulinas, presente en el plasma en grandes concentraciones (300-400 mg/dl), y en menor medida en los gránulos alfa de las plaquetas. Su síntesis corre a cargo del hepatocito y está influenciada por estímulos inflamatorios. Al ser escindido por la trombina, libera los fibrinopéptidos A y B, que forman la fibrina, las que al polimerizarse de forma espontánea forman una red que cubre y da resistencia al coágulo. (8)
El factor XIII es igualmente una glucoproteína formada por dos subunidades y cuya función es entrecruzar las cadenas ? y las ? de la fibrina para estabilizar el coágulo y protegerlo contra las acciones de la plasmina. (9)
ARN CON PAPEL SINGULAR EN LA HEMOSTASIA
Las proteínas son las moléculas biológicas por excelencia, ya que son los constituyentes característicos de las estructuras celulares y son también las especies que llevan a cabo las funciones celulares más importantes. Se encuentran codi?cadas en el ADN, pero desde el código genético hasta la correcta ejecución de una función celular realizada por una proteína median muchos pasos que son objeto de una estrecha regulación. (10)
El ARNm es el molde utilizado para la síntesis de proteínas, trasladando la información genética desde el ADN del núcleo a los ribosomas, donde se sintetizan las cadenas polipeptídicas que dan lugar a las proteínas.
En la última década se ha caracterizado una familia de ARN no codi?cantes relacionada con gran cantidad de procesos biológicos que, por su pequeño tamaño, ha recibido el nombre de microARN (miARN). Un miARN está formado por una cadena sencilla de ARN de unos 19-22 nucleótidos, capaz de controlar la expresión génica fundamentalmente a nivel postranscripcional (degradando el ARNm o inhibiendo su traducción, según el grado de complementariedad). (11)
Aunque resulta atractiva la hipótesis de que la amplia variabilidad observada en los niveles circulantes de los factores hemostáticos se encuentre regulada por miARN, hasta la fecha actual no hay evidencias que la sustenten. Por el contrario, sí existen trabajos publicados que describen el patrón de expresión de miARN en las diferentes líneas celulares sanguíneas tanto en el proceso de diferenciación, como en líneas maduras circulantes y en situaciones patológicas como linfomas, leucemias y la policitemia vera, entre otras. En particular en el proceso de hemostasia primaria se han publicado datos preliminares que apoyan la participación de los miARN en la activación plaquetaria. Así, aunque las plaquetas no poseen ADN genómico retienen cierta cantidad de ARNm procedente de los megacariocitos que puede ser sometida al control de los miARN. (12)
Recientemente se ha descrito que el daño tisular puede también liberar ARN a partir de las células lesionadas, que al alcanzar el torrente circulatorio puede exhibir una actividad pro-coagulante. (13)
SERPINAS HEMOSTÁTICAS
La hemostasia y la ?brinólisis son los sistemas que garantizan un correcto ?ujo sanguíneo, así como una adecuada respuesta pro-coagulante cuando es necesaria, mediante una red de procesos ?siológicos interconectados y una sucesión de reacciones proteolíticas. Las reacciones enzimáticas que promueven estas rutas son catalizadas por serinaproteasas, que necesariamente deben ser controladas por diferentes tipos de inhibidores. (14)
Gran parte de este control, trascendental para una correcta hemostasia, se realiza por un grupo de inhibidores conocidos como serpinas (acrónimo de las palabras "serine protease inhibitors") y sus cofactores. (15)
Las serpinas son una superfamilia de proteínas clasi?cadas dentro de 16 secciones (A-P). El genoma humano contiene aproximadamente 36 serpinas implicadas en la regulación de numerosos sistemas que incluyen la hemostasia y ?brinólisis, angiogénesis, la cascada del complemento y la in?amación. (15)
Todas ellas presentan un alto grado de homología estructural. Están típicamente compuestas por aproximadamente 400 aminoácidos que se organizan en 9 hélices ?(A-I) y tres hojas β (A-C).
Un esquema minimalista de la cinética de inhibición de las serpinas consta de dos pasos: 1) la formación de un complejo michaeliano, donde la secuencia del loop reactivo (RCL) es reconocida por la proteasa como un sustrato; y 2) la formación de un complejo covalente donde la proteasa es atrapada en un estado inactivo. (16)
Puesto que la especi?cidad de la serpina se determina ampliamente por la frecuencia de formación del complejo michaeliano, los cofactores que se unen a las serpinas (y a veces a la proteasa objeto) pueden alterar radicalmente la especi?cidad. El cofactor mejor entendido para las serpinas es la heparina y sustenta el potencial terapéutico anticoagulante de esta. La heparina se une a la mayoría de las serpinas implicadas en hemostasia y trombosis. (16)
Las serpinas con papel importante en la hemostasia son:
TEORÍA CLÁSICA DE LA COAGULACIÓN
La coagulación de la sangre se produce en tres pasos fundamentales:
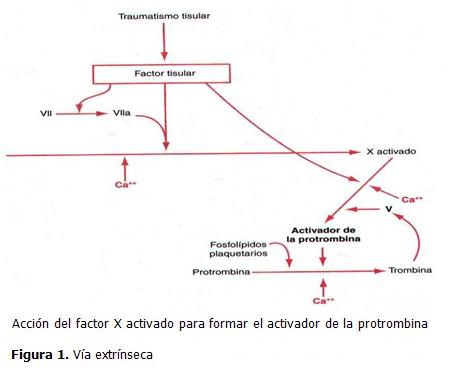
El mecanismo extrínseco para el inicio de la formación del activador de la protrombina comienza cuando la pared vascular o un tejido extravascular sufren un traumatismo y se produce mediante los tres pasos siguientes: (20, 21)

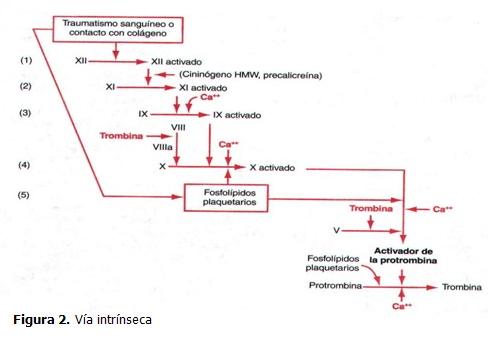
La primera fase de iniciación ocurre en las células portadoras de factor tisular (subendotelial); en la fase de amplificación el sistema se prepara para la producción a gran escala de trombina y finalmente la tercera fase, de propagación, ocurre en la superficie plaquetaria y resulta en la producción de grandes cantidades de trombina.(4,22)
Iniciación
El factor VIIa y el factor tisular son elementos esenciales en el inicio de los procesos de hemostasia. El factor VII circula en la sangre predominantemente como molécula inactiva y sus funciones a las concentraciones fisiológicas, son virtualmente nulas en ausencia de su cofactor. El factor tisular no está en contacto con elementos de la sangre; la célula que alberga este receptor (fibroblasto, miocito, célula mono nuclear, macrófago) se encuentra fuera del sistema vascular hasta que existe pérdida de la integridad del mismo. La interacción entre el factor tisular y el factor VIIa es el proceso fundamental en la iniciación de la coagulación; tal interacción incrementa la actividad del factor VII en 1 x 10(7). El complejo FVIIa/FT activa a los factores X y IX, y el factor Xa formado, es capaz de generar pequeñas cantidades de trombina de manera local.
Existe evidencia que sugiere que estas reacciones responsables de la iniciación de la coagulación ocurren de forma continua fuera de la vasculatura en individuos sanos.
El factor VII, X y la protrombina, son capaces de permear a través de espacios titulares fuera del sistema vascular y pueden ser detectados en linfa y tejidos perivasculares.
Sobre la base de estas observaciones se formuló la teoría de "mínima función", en la cual el sistema del factor tisular tiene actividad constante, generando constantemente pequeñas cantidades de trombina fuera del sistema vascular en individuos sanos. A pesar de que el paso inicial de la coagulación se produce de manera continua, esto no conduce a la formación de coágulos ya que las reacciones y sus productos se encuentran afuera de la vasculatura y de otros elementos esenciales del sistema; la interacción de unos con otros requiere de una pérdida de integridad de la pared de los vasos. (22) (Figura 3)


El tratamiento con el FVIIra en pacientes con hemofilia tuvo muy buenos resultados, mostrando mayor seguridad y eficacia que con tratamientos tradicionales. (26, 27)
Otras indicaciones:
Sangrado quirúrgico:
El daño por trauma es la principal causa de muerte entre los 5–44 años y el sangrado es la segunda causa de mortalidad en el daño del SNC. (28-30)
Ejemplos de otras situaciones hemorrágicas críticas son:
El uso del FVIIra tiene muy buenos resultados en todas estas afecciones debido al importante papel que juega en el mecanismo de coagulación, pero además tiene como ventaja que evita o disminuye el uso de las transfusiones masivas de glóbulos rojos, lo cual es una variable de riesgo para muchas complicaciones. (31, 32)
Todos estos avances del uso del FVIIra en el tratamiento de un amplio espectro de afecciones con compromiso hemostático se deben en gran parte al estallido de la nueva teoría celular de la coagulación, la cual sustituye un modelo que ha sido empleado tradicionalmente por varias decenas de años a nivel mundial, pero que no dejaba de estar inconcluso en muchos aspectos, dejando grandes interrogantes pendientes que son ahora abarcadas por este nuevo paradigma de la hemostasia. (33)
CONCLUSIONES
En los últimos años se desarrolló un nuevo modelo de la coagulación, el cual propone que esta se activa mediante la interacción de superficies celulares, factor tisular y factor VII en tres fases simultáneas: iniciación, amplificación y propagación, a diferencia del modelo tradicional el cual postula que la coagulación está regulada exclusivamente por una cascada de activación de factores solubles en dos vías independientes.
En este nuevo modelo, también conocido como teoría celular de la coagulación, se propone que las superficies celulares controlan y dirigen el proceso de la hemostasia. La nueva teoría permite un mejor entendimiento de los problemas clínicos observados en los trastornos de la coagulación.
Debido al importante rol que juega el factor VII en el nuevo modelo celular de la coagulación, sobre todo para darle inicio, se está comenzando a utilizar, con muy buenos resultados, para el tratamiento de varias enfermedades que provocan compromiso de la hemostasia.
REFERENCIAS BIBLIOGRÁFICAS
1. Griffin J. Control of Coagulation Reactions. En: Beutler E, Lichtman M, Coller B, editores. Williams. Hematology. 6th. ed. New York: McGraw-Hill; 2001: p. 1435-50
2. Davie E, Ratnoff O. Waterfall sequence for intrinsic blood clotting. Science. 1964;145:1310-12
3. Kjalke M, Ezban M, Monroe D, Hoffman M, Roberts RT, Hedner U. High-dose factor VIIa increases initial thrombin generation and mediates faster platelet activation in thrombocytopenia-like conditions in a cell-based model system. Br J Haematol. 2001;114(1):114-20
4. Hoffman M. A cell-based model of coagulation and the role of factor VIIa. Blood Rev. 2003;17(Supl 1):S1-S5
5. Dahlbäck B. Blood Coagulation. Lancet. 2000;355:1627-32
6. Grupo cooperativo español de citogenética hematológica. Simposios. En: LI Reunión Nacional de la AEHH y XXV Congreso Nacional de la SETH. Barcelona: GCECGH; 2009
7. Hoppe B, Tolou F, Radtke H, Kiesewetter H, Dörner T, Salama A. Marburg I polymorphism of factor VII-activating protease is associated with idiopathic venous thromboembolism. Blood. 2005;105(4):1549-51
8. Sidelmann JJ, Vitzthum F, Funding E, Münster AM, Gram J, Jespersen J. Factor VII-activating protease in patients with acute deep venous thrombosis. Thromb Res. 2008;122:848-53
9. Kanse SM, Parahuleva M, Muhl L, Kemkes-Matthes B, Sedding D, Preissner KT. Factor VII-activating protease (FS-AP): vascular functions and role in atherosclerosis. Thromb Haemost. 2008;99:286-9
10. Nakazawa F, Kannemeier C, Shibamiya A, Song Y, Tzima E, Schubert U, et al. Extracellular RNA is a natural cofactor for the (auto-)activation of Factor VIIactivating protease (FSAP). Biochem J. 2005;385:831-8
11. Yang B, Lu Y, Wang Z. Control of cardiac excitability by microRNAs. Cardiovasc Res. 2008;79:571-80
12. Hwang HW, Wentzel EA, Mendell JT. A hexanucleotide element directs microRNA nuclear import. Science. 2007;315:97-100
13. Vasudevan S, Tong Y, Steitz JA. Cell-cycle control of microRNA-mediated translation regulation. Cell Cycle. 2008;7:1545-9
14. Huntington JA. Shape-shifting serpins: advantages of a mobile mechanism. Trends Biochem Sci. 2006;31(8):427-35
15. Rau JC, Beaulieu LM, Huntington JA, Church FC. Serpins in thrombosis, hemostasis and fibrinolysis. J Thromb Haemost. 2007;5 Suppl 1:102-15
]]>16. Burghaus B, Langer C, Thedieck S, Nowak-Gottl U. Elevated alpha1-antitrypsin is a risk factor for arterial ischemic stroke in childhood. Acta Haematol. 2006;115(3-4):186-91
17. Antón AI, Teruel R, Corral J, Minano A, Martínez-Martínez I, Ordóñez A, et al. Functional consequences of the prothrombotic SERPINC1 rs2227589 polymorphism on antithrombin levels. Haematologica. 2009;4(4):589-92
18. Zhang W, Swanson R, Xiong Y, Richard B, Olson ST. Antiangiogenic antithrombin blocks the heparan sulfate-dependent binding of proangiogenic growth factors to their endothelial cell receptors: evidence for differential binding of antiangiogenic and anticoagulant forms of antithrombin to proangiogenic heparan sulfate domains. J Biol Chem. 2006;281(49):37302-10
19. Wayne C, Tomas V. Estimating the rate of thrombin and fibrin generation in vivo during cardiopulmonary bypass. Blood. 2003;101:4355-62
20. Furie B, Bouchard B, Furie B. Vitamin K-dependent biosynthesis of gammacarboxziglutamic acid. Blood. 2006;93:1798-808
21. Davidson C, Tuddenham E, Mcvey J. 450 million years of hemostasis. J Thromb Haemost. 2003;1:1487-94
22. Carrillo Esper R, Villaseñor Ovies P. Coagulopatía del paciente quirúrgico. El nuevo modelo celular de la coagulación y su aplicación en Anestesiología. Revista Mexicana de Anestesiología. 2004;27(4):219-30
23. Rott H, Trobisch H, Kretzschmar E. Use of recombinant factor VIIa, Novo Seven, in the management of acute hemorrhage. Curr Opin Anaesthesiol. 2007;17:159-69
24. Furie B, Bouchard B, Furie B. Vitamin K-dependent biosynthesis of gammacarboxziglutamic acid. Blood. 2006;93:1798-808
25. Schmaier AM, Rojkjaer R, Chiriat-Madar Z. Activation of the plasma kallikrein/kinin system on cells. A revised hypothesis. Thromb Haemost. 2009;82:226-33
26. Tankersley DL, Finlayson JS. Kinetics of activation and autoactivation of human factor XII. Biochemistry. 2006;23:273-9
27. Kaufmann J, Vischer U. Cellular mechanisms of the haemostatic effects of desmopressin (DDAVP). J Thromb Haemost. 2003;1:682-89
28. Armand R, Hess J. Treating Coagulopathy in Trauma Patients. Trans Med Rev. 2006;17:223-231
29. Popović N, Blagojević Z, Nikolić V, Arsenijević Lj, Karamarković A, Stefanović B, Kojić Z. Massive hemorrhage and mechanisms of coagulopathy in trauma. Acta Chir Yugosl. 2006;53(4):89-92
30. Tankersley DL, Finlayson JS. Kinetics of activation and autoactivation of human factor XII. Biochemistry. 2006;23:273-9
31. Ganter MT, Pittet JF. New insights into acute coagulopathy in trauma patients. Best Pract Res Clin Anaesthesiol. 2010;24(1):15-25
32. Tieu BH, Holcomb JB, Schreiber MA. Coagulopathy: its pathophysiology and treatment in the injured patient. World J Surg. 2007 May;31(5):1055-64
33. Hoffman M, Monroe D. The Action of High-Dose Factor VIIa (FVIIa) in a Cell-Based Model of Hemostasis. Dis Mon. 2003;49:14-21
]]> Recibido: 26 de abril de 2010.
Rafael Alejandro Gómez Baute. Especialista de I Grado en Medicina General Integral. Especialista de I Grado en Hematología. Profesor Asistente. Hospital General Universitario "Dr. Gustavo Aldereguía Lima". Cienfuegos. Correo electrónico: gomez@jagua.cfg.sld.cu
]]>