Centro Nacional de Genética Médica (CNGM), La Habana, Cuba
Factor reumatoideo, anticuerpos antipéptidos citrulinados y actividad de la enfermedad en pacientes con artritis reumatoidea
Rheumatoid factor, anticitrullinated peptides antibodies and disease activity in patients with rheumatoid arthritis
]]> Goitybell Martínez TéllezI, Jorge Alexis GómezII, Vicky Sánchez RodríguezIII, Cira Rodríguez PelierIV, Bárbara Torres RivesV, Ana María Torres LimaVI
I Máster en Ciencias, Investigador Auxiliar. Laboratorio de Inmunología. Centro Nacional de Genética Médica. e.mail: goity@infomed.sld.cu
II Especialista en Reumatología. Centro Nacional de Reumatología. e.mail: jalexys@infomed.sld.cu
III Laboratorio de Inmunología. Centro Nacional de Genética Médica. e.mail:vickysr@cngen.sld.cu
IV Laboratorio de Inmunología. Centro Nacional de Genética Médica. e.mail:cira@cngen.sld.cu
V Especialista en Inmunología. Máster en Ciencias. Profesor Auxiliar de la Universidad de Ciencias Médicas de La Habana. Investigador Agregado. Laboratorio de Inmunología. Centro Nacional de Genética Médica. e.mail: barbara@cngen.sld.cu
VI Especialista Segundo Grado en Inmunología. Máster en Ciencias. Profesor Auxiliar de la Universidad de Ciencias Médicas de La Habana. Jefa del Laboratorio de Inmunología. Centro Nacional de Reumatología. e.mail:amtl@infomed.sld.cu
RESUMEN
]]> Introducción: la artritis reumatoidea es una enfermedad inflamatoria crónica y multisistémica de causa autoinmune.Los anticuerpos antipéptidos citrulinados constituyen una herramienta importante para el diagnóstico de esta enfermedad.Palabras clave: artritis reumatoidea, autoanticuerpos, factor reumatoideo, antipéptidos citrulinados, enfermedad autoinmune, indicadores clínicos, indicadores serológicos.
ABSTRACT
Introduction: rheumatoid arthritis is a chronic inflammatory disease, multisystem and with autoimmune cause. Antibodies anti- citrullinated peptides are an important tool for the diagnosis of this disease.
Objective: to determine the relationship of rheumatoid factor, anti-mutated citrullinated vimentin and anti-citrullinated peptides of second and third generation antibodies, with clinical and serological indicators of disease activity in patients with established rheumatoid arthritis.
Material and methods: 88 patients with established rheumatoid arthritis participated in the study and C reactive protein, erythrocyte sedimentation rate, disease activity score based on the count of 28 joints (DAS 28) and autoantibodies were measured. Rheumatoid factor and anti-citrullinated peptides of second and third generation autoantibodies were quantified by enzyme-linked immunosorbent assay. ]]>
Results: association between C reactive protein and the presence of all autoantibodies was observed. Rheumatoid factor and anti-citrullinated peptides antibodies of second and third generation showed positive correlation with ESR and DAS 28. Only anti-citrullinated peptide antibodies were associated with a moderate or high disease activity.
Conclusions: anti-citrullinated peptide antibodies of second and third generation are of great value for identifying patients with more severe disease course in established rheumatoid arthritis.
Keys words: rheumatoid arthritis, autoantibodies, rheumatoid factor, anti- citrullinated peptides, autoimmune disease, clinical indicators, serological indicators.
INTRODUCCIÓN
Las enfermedades autoinmunes son la consecuencia de una respuesta inmunológica contra componentes del propio huésped. En todos los individuos se hallan presentes células del sistema inmune capaces de reconocer autoantígenos, pero normalmente son eliminadas por mecanismos físicos o funcionales. La alteración de cualquiera de los mecanismos de control imbricados en este proceso, puede dar origen a un estado de autoinmunidad patológica y a la generación de una enfermedad autoinmune. 1
La artritis reumatoidea (AR) es una enfermedad inflamatoria crónica y multisistémica de causa autoinmune, que afecta a las pequeñas articulaciones periféricas con una distribución simétrica, presentando una significativa morbilidad, mortalidad y discapacidad; con un considerable impacto en la vida de las familias y la sociedad. Se caracteriza por la capacidad de producir una inflamación sinovial con exudados inflamatorios, que provoca la destrucción del cartílago articular, erosiones óseas, deformidades articulares en fases posteriores y diversas manifestaciones extra articulares. La evolución de la AR puede ser muy variable, algunos pacientes pueden presentar solamente un proceso oligoarticular de breve duración y lesiones articulares mínimas, mientras que otros padecen una poliartritis progresiva que evoluciona hacia la aparición de deformidades articulares importantes y discapacidad en un período de 20 años. 1
El diagnóstico de la AR se basa en los criterios de la Asociación Americana de Reumatología (ARA) de 1988 con seis criterios clínicos y el FR como único criterio serológico, donde la positividad de cuatro o más de estos criterios establece el diagnóstico. 2
El FR es un biomarcador no específico para AR, debido a que se incrementa como consecuencia general de la activación de la respuesta inmune en el contexto de la formación de complejos inmunes. Además de estar presente en individuos sanos, puede hallarse en otras enfermedades autoinmunes. 1
En años recientes, el estudio de la citrulinación (conversión del residuo arginina a citrulina) de proteínas ha adquirido gran interés debido a su participación en diversos procesos, tanto fisiológicos como patológicos.
]]> Los anticuerpos antipéptidos citrulinados (anti-PC) fueron incluidos como criterios de clasificación para la AR en el nuevo Colegio Americano de Reumatología/Liga Europea contra el Reumatismo (ACR/EULAR). 2Durante la última década, varios estudios sugieren que los anticuerpos anti-PC de segunda generación (anti-CCP2), además de su alta especificidad, se presentan en etapas tempranas y discriminan entre AR y otras artropatías. 3
La tercera generación de ensayos anti-PC (anti-CCP3) se designó mediante ingeniería de péptidos, con similar sensibilidad y especificidad a los anticuerpos anti-CCP2. 4, 5
Diversos estudios demuestran que los anticuerpos anti-PC constituyen una herramienta diagnóstica útil para la AR. 4, 6, 7
Una vez establecido el diagnóstico de AR, es necesario identificar a los pacientes de peor pronóstico para implementar tempranamente tratamientos más agresivos.
OBJETIVO
El objetivo de este estudio fue determinar la relación de los anticuerpos FR, anti-CCP2 y anti-CCP3 con los indicadores clínicos y serológicos de actividad de la AR en pacientes con la enfermedad establecida.
MATERIAL Y METODOS
]]> Se realizó un estudio de corte transversal, donde participaron 88 pacientes con AR establecida (tiempo de diagnóstico mayor o igual a 1 año), provenientes del Centro Nacional de Reumatología en el período de noviembre 2013 abril 2014.Los pacientes fueron diagnosticados de acuerdo con los criterios establecidos por la ARA.3
Los datos se coleccionaron mediante entrevistas individuales realizadas por un especialista en reumatología. Se determinó el índice de actividad de la enfermedad basado en el conteo de 28 articulaciones (DAS 28).
Exámenes generales de laboratorio
Se determinó la velocidad de sedimentación globular (VSG) y la proteína C reactiva (PCR) mediante látex (DiagnosticAutomation/Cortez Diagnostics, EUA).
Determinación de autoanticuerpos: Se utilizaron ensayos tipo ELISA para determinar FR IgM (Orgentec Diagnostika, Germany), anti-CCP2 (IBL International, Germany) y anti-CCP3 (INNOVA Diagnostic INC, USA). Para el ensayo anti-CCP2 el valor de corte recomendado fue 30 U/mL y para los ensayos anti-CCP3 y FR IgM fue 20 U/mL.
Para el análisis estadístico de la información se utilizó el programa EPIDAT 3.1. Se calculó el tamaño de muestra. Las variables cualitativas se expresaron en tablas de frecuencias y las cuantitativas con media aritmética y desviación estándar. Se calculó el estadígrafo chi-cuadrado con un nivel de significación del 5% y se estimó el odd ratio (OR) como magnitud de asociación.
Para el desarrollo de la investigación se cumplieron los principios enunciados en la Declaración de Helsinki.8 El consentimiento informado de participación fue entregado a los pacientes en la consulta antes de las extracciones de sangre. La investigación fue aprobada por el Comité de Ética del Centro Nacional de Genética Médica (CNGM) y el Centro Nacional de Reumatología (CNR).
RESULTADOS
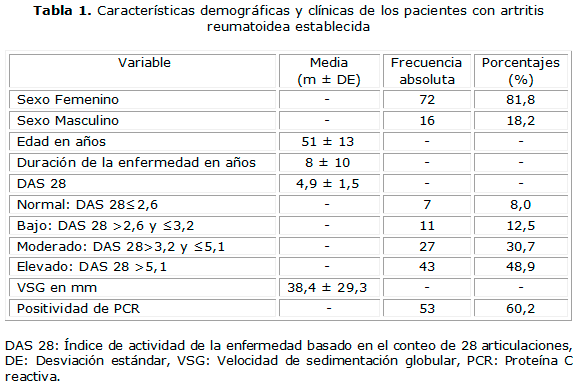
]]> Las características clínicas y demográficas de los pacientes se muestran en la Tabla 1. La mayor parte de los pacientes fueron del sexo femenino. La actividad de la enfermedad en el grupo de pacientes estudiados fue elevada. La media del DAS 28 fue mayor de 3,2 y la mayoría de los pacientes tuvo DAS 28 moderado o elevado. La VSG fue elevada y se observó una alta positividad de la PCR (Tabla 1).Las frecuencias de anticuerpos antipéptidos citrulinados fueron inferiores a aquella obtenida para el FR IgM. La positividad de anticuerpos anti-CCP2 fue superior a la de anticuerpos anti-CCP3. (Figura).
Los anticuerpos anti-CCP3 se detectan con mayor frecuencia que los anti-CCP2 en pacientes seronegativos de FR IgM. (Tabla 2).
Se observó asociación entre la positividad de PCR y la presencia de todos los autoanticuerpos estudiados. Solamente los anticuerpos anti-CCP2 y anti-CCP3 mostraron asociación con la presencia de un DAS 28 moderado o alto (Tabla 3).
]]> Todos los autoanticuerpos mostraron asociación positiva con la VSG y con el DAS 28 (Tabla 4).Estos coeficientes de correlación corresponden a la técnica de Spearman (rangos), las variables estudiadas no son estrictamente cuantitativas, por lo que no cumplen con la distribución normal, es por ello que se ha utilizado esta correlación no-paramética.
DISCUSIÓN
Varios estudios demuestran la evidencia y la utilidad diagnóstica de los anticuerpos anti-CCP2. 9, 10
En Latinoamérica, la positividad de anticuerpos anti-CCP2 varía desde 48 hasta 70%.8, 11, 12 La frecuencia de anticuerpos anti-CCP2 obtenida en este estudio se encuentra en los límites inferiores de este rango. Frecuentemente los valores varían en una misma población. Las diferencias pueden deberse a factores genéticos, medio ambientales, variaciones en el tiempo de diagnóstico de la población estudiada o en las características del inmunoensayo utilizado.11,12
Aunque en los casos estudiados, las frecuencias obtenidas de anticuerpos anti-CCP 2 y anti-CCP3 fueron inferiores a la de FR, el mayor valor de la determinación de los anticuerpos anti-PC está dado por su alta especificidad y su alto valor discriminativo entre pacientes con AR y pacientes con otras enfermedades antiinflamatorias. Para determinar el valor diagnóstico de estas determinaciones es necesario determinar la frecuencia de estos anticuerpos en individuos sanos y con otras enfermedades reumáticas y autoinmunes. Esto constituye una limitación de nuestro estudio.
Otra ventaja de los ensayos anti-PC es su valor para predecir el desencadenamiento de la enfermedad en pacientes con AR temprana, 11, 12 por lo cual es recomendable en estudios posteriores evaluar la presencia de estos anticuerpos en estudios longitudinales de cohorte con pacientes con menos de un año de diagnóstico.
Según los criterios del CAR/EULAR 4 en los pacientes con diagnóstico de AR se debe determinar al menos uno de las reactantes de fase aguda de la inflamación (PCR o VSG).
]]> En los pacientes con AR la VSG correlaciona con la actividad de la enfermedad. La PCR es comparable a la VSG para evaluar la respuesta inflamatoria y los cambios de su concentración en sangre son mucho más rápidos que los cambios de la VSG, por lo que pudiera ser un mejor predictor de la inflamación. Además la magnitud de la inflamación correlaciona directamente con la PCR.13 Esto concuerda con nuestro estudio donde se observó una buena correlación entre la PCR y el indicador clínico de actividad de la enfermedad DAS28.El FR IgM ha demostrado tener correlación significativa con los indicadores clínicos y serológicos de actividad y discapacidad funcional de la AR. 14 En nuestro estudio aunque el FR IgM se asoció a la positividad de PCR y mostró correlación con el DAS 28, no se asoció al DAS 28 moderado o alto, que constituye el mejor indicador clínico de la actividad de la AR.
Los anticuerpos anti-PC de segunda y tercera generación son los que mostraron mayor capacidad de definir el curso de la enfermedad por su asociación con la PCR, el DAS 28 moderado o alto, su correlación con el DAS 28. Otros autores han demostrado la correlación de los anticuerpos anti-CCP2 con la PCR.15
CONCLUSIONES
Los anticuerpos anti-CCP2 y anti-CCP3 tienen gran valor para la identificación de pacientes con un curso más severo de la enfermedad en la artritis reumatoidea establecida.
RECOMENDACIONES
Se recomienda en estudios posteriores la inclusión de individuos sanos para la determinación del valor diagnóstico de los ensayos de determinación de anticuerpos anti-PC.
]]> REFERENCIAS BIBLIOGRÁFICAS
1. Abbas AK, Lichtman A, Pillai S. Celular and Molecular Immunology. 7ma ed. Amsterdam: Elseiver; 2012.
2. Kochi Y SA, Yamada R, Yamamoto K. Ethnogenetic heterogeneity of rheumatoid arthritis—implications for pathogenesis. NR Rheum. 2010;6(1):290-95.
3. Arnett FC, Bloch DA. The American Rheumatism association 1987. Revised criteria for the classification of Rheumatoid Arthritis. Arthritis Rheum. 1988;31:315-23.
4. Aletaha D, Neogi T, Silman AJ, Funovits J, Felson DT, Bingham CO, col. Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum. 2010;62(9):2569-2581.
5. Burr M, Viatte S, Bukhari M, Plant D, Symmons D, Thomson W, col. Long-term stability of anti-cyclic citrullinated peptide antibody status in patients with early inflammatory polyarthritis. Arthritis Research & Therapy. 2012;14:109.
6. Levesque M, Zhou Z, Moreland L. Anti-cyclic citrullinated peptide testing for the diagnosis of rheumatoid arthritis and the quest for improved sensitivity and predictive value. Arthritis Rheum. 2009;60:2211-2215.
7. Swart A, Rufus W, Burlingame B, Gürtler I, Mahler M. Third generation anti-citrullinated peptide antibody assay is a sensitive marker in rheumatoid factor negative rheumatoid arthritis. Clin Chim Acta. 2012;414:266-272.
8. Díaz-Toscano ML, Olivas-Flores EM, Zavaleta-uñiz SA, Gámez-Nava JI, Cardona-Muñoz EG, Ponce-Guarneros M, col. Comparison of two assays to determine anti-citrullinated peptide antibodies in rheumatoid arthritis in relation to other chronic inflammatory rheumatic diseases: assaying anti-modified citrullinated vimentin antibodies adds value to second-generation anti-citrullinated cyclic peptides testing. Biomed Res Int. 2014.
9. Zahran W, Mahmoud M, Shalaby K, Abbas M. Unique Correlation Between Mutated Citrullinated Vimentine IgG Autoantibodies and Markers of Systemic Inammation in Rheumatoid Arthritis Patients. Ind J Clin Biochem. 2013,28(3):272-276.
10. World Medical Association Declaration of Helsinki. Ethical principles for mdical research involving human subjects. WMA: 2013.
11. Demoruelle M, Parish M, Derber L, Kolfenbach J, Hughes-Austin J, Weisman M y col. Anti-cyclic citrullinated peptide assays differ in subjects at elevated risk for rheumatoid arthritis and subjects with established disease. Arthritis Rheum. 2013;65(9):2243-2252.
12. Pruijn G, Wiik A, Venrooij JV. The use of citrullinated peptides and proteins for the diagnosis of rheumatoid arthritis. Arthritis Research & Therapy. 2010;12:203.
13. González-López L, Rocha-Muñoz AD, Ponce-Guarneros M, Flores-Chávez A, Salazar-Paramo M, Nava A, col. Anti-Cyclic Citrullinated Peptide (Anti-CCP) and Anti-Mutated Citrullinated Vimentin (Anti-MCV) Relation with Extra-Articular Manifestations in Rheumatoid Arthritis. J Immunol Res. 2014.
14. Henrique da Mota LM, Neto LL, Pereira IA, Burlingame R, Menard H, Laurindo IM. Autoantibodies in early rheumatoid arthritis-Brasília cohort- results of a three-year serial analysis. Rev Bras Reumatol. 2011;51(6):558-571.
15. Castro C, Gourley M. Diagnostic testing and interpretation of tests for autoimmunity. J Allergy Clin Immunol. 2010;125(2):238-47.
16. Kokuina H, Chico A, Carballar L, Gutiérrez A, Soto J, Estévez M, col. Factor reumoideo: Asociación erosión radiológica con la actividad de la artritis reumatoidea. Rev Cub Med. 2008;47(3).
17. Shidara K, Inoue E, Hoshi D, Sato E, Nakajima A, Momohara S, col. Anti-cyclic citrullinated peptide antibody predicts functional disability in patients with rheumatoid arthritis in a large prospective observational cohort in Japan. Rheumatol Int. 2012;32(2):361-366.
Recibido: 6 de febrero de 2015
Aprobado: 6 de julio de 201