Propuesta de nuevo método para la disección esqueletizada de la arteria mamaria interna: Fundamentos históricos y anátomo-fisiológicos
Proposal of a new method for the skeletonized internal mammary artery harvesting: Historical, anatomical and physiological fundaments
Yoandy López-De la Cruz, Yolepsis F. Quintero Fleites
Servicio de Cirugía Cardiovascular, Hospital Universitario Cardiocentro Ernesto Che Guevara. Santa Clara, Villa Clara, Cuba. Correo electrónico: yoandylc@infomed.sld.cu
]]>
RESUMEN
En los últimos 30 años se ha acrecentado el interés de los cirujanos cardiovasculares por la disección esqueletizada de la arteria mamaria interna, sobre todo estimulado por su empleo bilateral para lograr la revascularización arterial total en la mayor cantidad de pacientes; lo que, en teoría, se acompaña de una mayor incidencia de infecciones profundas de la herida esternal. Desde 1992, prácticamente no ha variado la técnica clásica de disección esqueletizada de la mamaria. Quizás los únicos cambios importantes han sido la introducción del cauterizador armónico alrededor del año 2000 y la tendencia de algunos escasos grupos de intentar conservar indemne el plexo venoso retroesternal. Después de un profundo análisis de los fundamentos históricos, anatómicos y fisiológicos sobre los que se sustenta este procedimiento, y basados en la práctica en más de 100 pacientes en un período de dos años, se presentan modificaciones a la técnica clásica de disección esqueletizada de la arteria mamaria interna que permiten la obtención de un hemoducto más saludable en menos tiempo, una mayor protección ante la infección y la isquemia del hueso y los órganos del mediastino, así como la conservación de la integridad de la vena mamaria interna.
Palabras clave: revascularización miocárdica, arteria mamaria interna, flujo sanguíneo, profilaxis antibiótica, espasmo, heparina.
ABSTRACT
In the last 30 years the interest of the cardiovascular surgeons for the skeletonized dissection of the internal mammary artery has increased, mainly stimulated by its bilateral use, to achieve the total arterial revascularization in the greater amount of patients; this, in theory, is accompanied by a higher incidence of deep infections of the sternal wound. Since 1992, the classical technique of the mammary skeletonized dissection has practically not changed. Perhaps, the only major changes have been the introduction of the harmonic cauterizer around the year 2000 and the tendency of a few groups to try to preserve intact the retrosternal venous plexus. After a thorough analysis of the historical, anatomical and physiological fundaments on which this procedure is based, and based on the practice in more than 100 patients over a period of two years, modifications are presented for the classical technique of the skeletonized dissection of the internal mammary artery that allow obtaining a healthier hemoduct in less time, greater protection against infection and ischemia of the bone and mediastinal organs, as well as the preservation of the integrity of the internal mammary vein.
Key words: myocardial revascularization, internal mammary artery, blood flow, antibiotic prophylaxis, spasm, heparin.
INTRODUCCIÓN ]]>
Desde 1987 se le ha acreditado a Samuel B. Keeley el mérito de haber sido el creador de la técnica de disección esqueletizada de la arteria mamaria interna (AMI) en la cirugía de revascularización miocárdica. Sin embargo, esta aseveración no parece ser históricamente cierta; el nacimiento de este procedimiento presuntamente ocurrió casi 40 años antes. Fue realmente el canadiense Arthur Martín Vineberg quien, el 28 de abril de 1950, protagonizó un hito en la historia de la medicina moderna, al implantar por primera vez una AMI esqueletizada en el miocardio del ventrículo izquierdo de un ser humano1, como una forma, extremadamente revolucionaria para la época, de crear una fuente sanguínea extracoronaria para ese músculo.Oclusión distal de la arteria mamaria al inicio de la disección
Todas las revisiones que se hagan de cualquiera de las técnicas empleadas para la disección de la AMI mostrarán siempre algunos elementos comunes: previa administración sistémica de heparina, una vez cortada la arteria al final de su disección, es ocluida su luz en su segmento distal (mediante una pinza [clamp] o la colocación de un clip metálico [grapa]) y permanecerá así, y envuelta en un paño embebido en una sustancia vasodilatadora, hasta el momento de comenzar la construcción del injerto. Durante este período de tiempo, de mayor o menor duración en dependencia de las habilidades de los cirujanos y de la modalidad quirúrgica que se decida emplear (con o sin circulación extracorpórea), la arteria latirá contra el obstáculo mecánico creado, lo que aumentará la presión hidrostática en su interior y forzará la dilatación circunferencial del hemoducto4, favorecida además por la producción endotelial de óxido nítrico5, mediada por un flujo hacia delante y hacia atrás, dentro del vaso distalmente ocluido.
Curiosamente, en la técnica propuesta por Keeley en 1987, la arteria es primero diseccionada en forma de un «generoso pedículo» que contiene vena, grasa, fascia y linfáticos; dividida distalmente y posteriormente esqueletizada con un electrocauterizador bipolar, mientras su extremo permanece ocluido con un clamp vascular6. En los meses que le siguieron a la publicación de esta experiencia, la técnica de esqueletización mamaria cambió radicalmente. El 1 de noviembre de 1988 comenzó la serie que Cunningham publicaba en el `923. La arteria empezará a esqueletizarse totalmente en su lecho, será pinzada y distalmente cortada después de ser completamente diseccionada. Al parecer, en los siguientes 25 años los cirujanos olvidaron por completo que la mamaria puede permanecer ocluida durante un tiempo considerable mientras es cuidadosamente preparada como hemoducto.
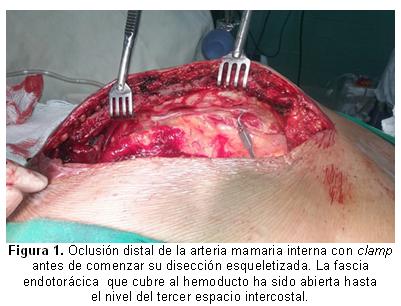
Por tanto, la primera modificación que se propone a la técnica clásica de esqueletización mamaria es la oclusión distal de la arteria con un clamp al inicio de su disección (Figura 1). Por razones que se explicarán más adelante, esta oclusión debe realizarse lo más proximal posible a la bifurcación de la mamaria en sus dos ramas terminales, pero sin comprometer la integridad de la comunicación entre las arterias musculofrénica y epigástrica superior7. Así, una vez visualizada la AMI y abierta la fascia endotorácica en toda la extensión o en la mayor parte posible del recorrido longitudinal del vaso, se procederá a identificarsu ramificación terminal.
En ocasiones se encuentran dificultades para precisar esta estructura. Una de las causas fundamentales de consumo innecesario de tiempo durante la preparación mamaria es la disección de la arteria más allá de su bifurcación. Algunos autores8,9, han expresado la necesidad de utilizar su segmento más distal, en cualquiera de las dos arterias, para poder alcanzar con seguridad el sitio ideal en la coronaria a anastomosar. Sin embargo, en el caso de la estrategia clásica de revascularización de la arteria descendente anterior con la AMI izquierda, y en muchas variantes en que se utiliza la AMI derecha10,11, pocas veces se requiere emplear el hemoducto más allá de su ramificación final (de hecho algunos estudios sugieren precaución en relación con el uso de ese segmento5,12); así, lo que se emplee en su preparación será, la mayor parte de las ocasiones, tiempo perdido. ]]>
Elementos anatómicos importantes para identificar adecuadamente la ramificación distal de la mamaria son la presencia de dos o tres ramas de mayor calibre13,14 en el segmento de la arteria que coincide con la unión del cuerpo del esternón con su proceso xifoideo. Debe recordarse que, en la mayoría de la población, la mamaria termina a nivel del 6º espacio intercostal (EIC) _aunque pocos autores sitúan la bifurcación entre el 5º y el 7º EIC14,15_, punto que coincide con la mencionada articulación. La disección que se realice alrededor del xifoides, generalmente involucrará a las arterias musculofrénica o epigástrica superior; que son vasos con características histológicas diferentes a la AMI, con una reactividad aumentada a estímulos vasoconstrictores, mayor contenido muscular y tendencia a la aterosclerosis12 y al espasmo5, lo que puede comprometer la salud de un injerto, si son empleados como tal.
Una vez identificada la bifurcación se coloca el clamp proximal a esta y se inicia la disección y control mediante clips del resto de las ramas. Algunas ventajas de la oclusión distal de la mamaria al inicio de su disección se muestran en el Anexo16-32.
Después de la realización de una extensa revisión de la literatura, no hemos encontrado ningún otro grupo quirúrgico en el mundo que aplique esta modificación en cualquier variante de técnicas de disección mamaria.
SEGUNDA MODIFICACIÓN
Control y división selectiva en dos tiempos de las ramas laterales de la arteria mamaria
Cuando se analizan las experiencias de diferentes grupos en la disección esqueletizada de la AMI, existen variaciones en relación con la dirección escogida para realizar el control de sus ramas laterales. La arteria puede prepararse en sentido cefálico (desde su bifurcación hacia el origen del vaso), caudal (desde la subclavia o primera costilla hacia el final de la arteria), o puede identificarse donde se visualice mejor (generalmente en su segmento medio) y realizarse una disección bidireccional. Generalmente, sea una u otra la opción escogida, se van ligando cada una de las ramas de la mamaria, independientemente de la dirección en la cual se originen.
La relación espacial que se establece entre el campo visual del cirujano y el recorrido de la AMI permite un fácil control de las ramas que se originan de su cara posterior (ramas pericárdicas), anterior (perforantes y esternales) y medial (tímicas, mediastinales)14. Casi siempre estas ramas son fácilmente identificadas por el cirujano y al hacer su recorrido generalmente alejadas de otros vasos pueden pinzarse y cortarse sin mucho riesgo de lesión y sangrado accidental. En cambio, las ramas que se originan en la cara lateral de la mamaria, se dirigen hacia el espacio intercostal, en forma de arterias intercostales anteriores, para conectarse con sus homónimas posteriores que provienen de la aorta torácica33. Son estas las ramas más difíciles de controlar, ya que, no solo «se alejan» del plano visual del cirujano, sino que para poder precisar su sitio de emergencia tendría que manipularse excesivamente la AMI. Además, estos vasos se acercan mucho al recorrido lateral de la vena mamaria y sus afluentes, lo cual constituye motivo frecuente de lesión accidental de estas estructuras, cuando el cirujano coloca el clip distal o corta una rama arterial sin tener un adecuado control visual de lo que subyace más allá de las partes visibles de la grapadora o la tijera. El control del sangrado venoso o de las ramas laterales de la mamaria (son las de mayor flujo al recibir irrigación de dos fuentes), es en ocasiones difícil, prolonga siempre el tiempo de disección y aumenta el riesgo de lesión de nervios y vasos sanguíneos y linfáticos, sobre todo si el cirujano decide hacerlo con el electrocauterizador15.
Nuestro grupo ha diseñado una metódica diferente para el control de las ramas de la mamaria, consistente en su división selectiva en dos tiempos, lo que ha permitido disminuir la duración de la disección y la incidencia de lesiones a estructuras periarteriales. Una vez que se ha colocado distalmente el clamp, se comienza, en dirección cefálica, la división de las ramas que emergen de las caras posterior y ántero-medial de la AMI hasta que se considere controlada la más proximal, justo antes de la salida de la arteria de la cavidad torácica. Como señaló Cunningham3 en su artículo, durante la disección esqueletizada: "un hallazgo relativamente constante es un gradual incremento en el diámetro de la AMI en la medida que son divididas las ramas proximales". Esta dilatación es potenciada, en nuestro caso, por los efectos físicos ya mencionados del clamp y por el rociamiento intermitente de la arteria, desprovista ya de la envoltura que le ofrece la fascia endotorácica, con una solución vasodilatadora.
Es importante durante esta primera fase de la disección, no perder tiempo en el control de ramas cortas que ofrezcan poco espacio para la colocación de los clips, en especial en mamarias con un trayecto muy adosado a las costillas, por la ausencia de tejido graso interpuesto. En este momento en que la dilatación de la mamaria aún es incipiente, el abordaje intempestivo de esas ramas que no han tenido tiempo de alongarse, puede provocar su desgarro, así como lesiones de la pared de la arteria. Es aconsejable, por tanto, realizar una disección cuidadosa en esta etapa, pero dividir totalmente solo aquellas ramas aisladas y con suficiente longitud para un control rápido y sin peligro de accidente. Puede ser conveniente, en ramas cortas, la colocación del clip proximal solamente, y terminar su control distal y división en la segunda fase (cefálico-caudal) de la extracción; es cierto que esta estrategia impedirá momentáneamente la total movilización de ese segmento, pero _según los mencionados preceptos de Cunningham_contribuirá a la dilatación arterial, lo que facilitará etapas posteriores de disección.
Generalmente, las ramas de mayor calibre de la AMI se encuentran diseminadas entre su origen y el 2º EIC. Es también ahí donde su disección se ve entorpecida por la interposición de su vena y por la insuflación de los segmentos superomediales del pulmón que afectan de manera importante la visión del cirujano3. Aquí, además, las ramas arteriales asumen una disposición anatómica diferente a las colaterales de otros espacios, a tono con una mamaria que ahora tiende a separarse de su lecho en la pared torácica, y alejarse oblicuamente de la zona operatoria de confort del cirujano. Alrededor del 2º EIC en ocasiones el recorrido de la arteria puede verse oscurecido (y hasta confundido) por una disposición cercana y medial de su vena o por la interposición de tejido graso, que cubre casi todo su segmento más proximal. En esta circunstancia se aconseja abandonar el sentido de la disección que se ha estado siguiendo, e intentar descubrir la arteria en una zona más proximal dentro del mencionado fascículo graso que la rodea, cuando nuevamente su curso se ha separado ligeramente de la vena. Se encontrarán en este segmento, habitualmente, ramas gruesas y largas, dispuestas en varias direcciones (hacia diversos puntos de la pared torácica, hacia los restos tímicos, pericardio, entre otros), de fácil control generalmente, y se concluirá de esta forma el primer tiempo de disección de las ramas (Figura 2A). ]]>
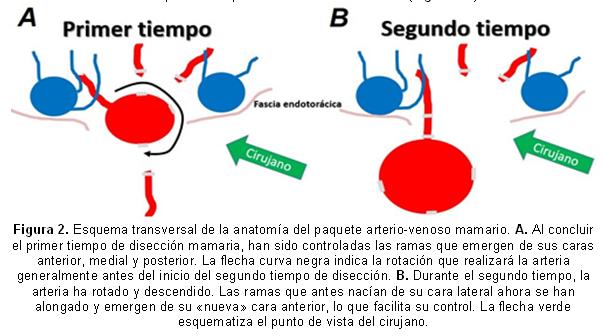
Una vez que el cirujano considera que ha divido todas o la mayor cantidad de las ramas que nacen de las caras posterior, medial y anterior de la mamaria, en especial las dispuestas en los primeros dos espacios intercostales, se inicia la disección y división en sentido céfalo-caudal del resto de las ramas que permanecen conectadas a la arteria. En este momento, una AMI que ha sido desprovista de la mayor parte de su desagüe (en especial, las ramas más proximales que son las de mayor flujo) y que ha permanecido generalmente más de 15 minutos pinzada, y rociada intermitentemente por una solución vasodilatadora, ha aumentado su diámetro, su volumen de sangre, y por tanto, su masa. Esta nueva situación provocará que la arteria lentamente se separe («caiga») por su propio peso de la pared torácica, a la cual solamente ha quedado anclada por las ramas _ahora también más dilatadas_ que antes se originaban de su cara lateral, pero ahora, por la rotación que ha sufrido el vaso, parece que emergen de su cara anterior (Figura 2B).
Esta nueva disposición anatómica que han adquirido las ramas laterales de la AMI, unido a la ptosis del vaso, permite ahora su pinzado y división de forma más fácil, sin peligro de lesionar el sitio en que se unen con los vasos procedentes de la aorta, elemento fundamental que justifica la esqueletización mamaria en aras de proteger la circulación colateral esternal34. Igualmente más fácil resulta el control de las ramas, ahora dilatadas y un poco más largas, que debieron haber sido totalmente controladas en la primera fase de la disección, pero por ser inicialmente demasiado cortas, se decidió pasarlas por alto o solo colocarles el clip proximal. Por su parte, las colaterales venosas han quedado en su posición habitual, adheridas a la pared torácica, por lo que se disminuye considerablemente el peligro de lesionarlas durante el control de las ramas arteriales.
Otra ventaja importante del control en dos tiempos de las ramas de la mamaria es que, durante la segunda fase sobre todo, facilita considerablemente la adecuada discriminación de las estructuras que deben ser pinzadas (tubulares, de mayor calibre) de otras adherencias no vasculares (grasa, tejido conjuntivo) que se han alongado, debilitado y muchas veces terminan por desgarrarse tan solo por el peso de la arteria. Esto evitará la innecesaria colocación de clips, con las consabidas ventajas prácticas que esto produce a la hora de manipular el hemoducto.
La introducción de esta modificación a la técnica clásica de disección esqueletizada de la AMI ha permitido acortar su duración y el sangrado durante el procedimiento, al disminuir considerablemente la incidencia de lesiones de estructuras vasculares.
TERCERA MODIFICACIÓN
Administración más precoz de la heparina
La casi totalidad de las descripciones que se analizan en relación con la disección de la AMI, en cualquiera de sus variantes, señala la conducta casi obligatoria de administración sistémica del anticoagulante entre 3 y 5 minutos antes de cortar el hemoducto7,35. Son pocos los que al realizar una rápida disección pediculada, solicitan la heparina al ejecutar aproximadamente la mitad del procedimiento36. Este lapso, suficiente para que se obtenga la cifra deseada de tiempo de coagulación activada, permitirá cortar el hemoducto (lesión del endotelio) sin riesgo de trombosis.
Resulta obvio que no es una condición obligatoria acometer la disección mamaria con el estado normal de coagulación del paciente. Por diversos motivos, los cirujanos cardiovasculares modernos tratan cada día a un mayor número de enfermos que llegan a la cirugía antiagregados o anticoagulados, pero existe el consenso casi unánime de que, en la medida de lo posible, debe evitarse la preparación mamaria en ese estado, para prevenir sangrados de gran cuantía, que entorpecerían el procedimiento, así como el elevado riesgo de lesión del hemoducto, lo que incluso puede provocarle su disecación haciéndolo inútil para la revascularización.
Se propone adelantar el momento de la administración de heparina al concluir el primer tiempo de división y control de las ramas. Si hasta ese momento se han cumplido los principios que se han expuesto, la disección de las ramas restantes, en dirección céfalo-caudal, se realizará de forma expedita con un riesgo mínimo de lesión de colaterales y sangrado, lo que no justifica demorar más la administración del anticoagulante. ]]>
Es opinión de los autores, si se logra evitar la lesión de los hemoductos, que su disección con el paciente anticoagulado ofrece más beneficios que desventajas; sin embargo, el abordaje más profundo de estos aspectos está más allá de los objetivos de este trabajo.
CUARTA MODIFICACIÓN
Maniobra para contribuir a conservar la vena mamaria
Al elemento alrededor de la disección de la AMI que quizás se le ha prestado menos atención, es al destino de su vena. Cuando Vineberg1 comenzó a implantar la arteria, solo necesitaba una fuente de sangre oxigenada; desafortunadamente en sus artículos disponibles no se hace mención a la vena mamaria. Por su parte Sewel2 la consideró un elemento importante en su técnica del pedículo, para actuar como retorno venoso y evitar hematomas en el miocardio, una teoría sin mucho sentido incluso en esa época, pues el canadiense no había encontrado esta complicación en ninguno de sus casos37. Tres décadas después Cunningham3 señalaba que: "puede ser necesario dividir la vena torácica interna para obtener exposición satisfactoria de las ramas proximales".
La extensa revisión de la literatura que se ha realizado para acometer esta investigación, permite asegurar que la mayoría de los grupos quirúrgicos que diseccionan la AMI de forma esqueletizada, no escatiman en dividir su vena, si se presenta la circunstancia comentada por Cunningham. Solo escasos artículos valoran la importancia de conservar, en la medida de lo posible, la integridad del retorno venoso retroesternal, al considerar su ruptura un posible factor de riesgo para el desarrollo de complicaciones en el sitio quirúrgico38.
Efectivamente, es durante el abordaje a los segmentos más proximales de la arteria que existe un mayor riesgo para la lesión de su vena acompañante. Según Schipper et al39, entre el 2º y 3º EIC, en dos de las cuatro variantes descritas por Schwabegger, esta asume un trayecto medial, por lo que se interpone entre la arteria y el cirujano; circunstancia que, sumada a otras particularidades anatómicas de esa zona, vuelve _en ocasiones_ muy compleja la disección arterial sin necesidad de prescindir de su vena.
Se propone, cuando el recorrido de la vena se adosa demasiado al hemoducto de interés y entorpece su extracción, una sencilla maniobra consistente en colocar un lazo a su alrededor y separarla de la vecindad de la arteria, ya sea mediante un punto anclado al borde de la piel, o con ayuda del peso de una pinza hemostática (Figura 3). Este sencillo procedimiento permitirá generalmente sustraer la vena del estrecho campo visual del cirujano (el procedimiento se hace habitualmente con lupas), lo que facilitará la disección arterial sin peligro de lesionar uno u otro vaso. Toda vez que haya concluido la preparación mamaria, la vena puede volver a su posición original, sin haber sufrido lesión alguna. Según lo mejor de nuestro conocimiento, ninguno de los escasos grupos que en sus artículos señalan conservar la vena mamaria en la realización de esta técnica, ha publicado experiencias con maniobras semejantes a la propuesta por nuestro equipo.
QUINTA MODIFICACIÓN
División distal del hemoducto antes de concluir su disección ]]>
Todas las técnicas clásicas de disección mamaria estipulan que la arteria se mantenga conectada y permeable por ambos extremos durante todo el procedimiento. Obviamente una vez que se haya realizado su oclusión distal, no se le pueden adjudicar grandes ventajas a la estrategia de mantenerla anclada a la pared torácica. Quizás el único beneficio será la necesidad de una menor manipulación del vaso mientras se disecciona.
Solo se ha encontrado un autor que, durante el inicio de su técnica de disección pediculada, divide distalmente la mamaria para fijarla con un punto que le permita su tracción hacia uno u otro lado durante la división de las ramas en dirección caudo-cefálica40. Mencionamos esta experiencia aislada como fundamento fisiológico de la modificación que a continuación se propondrá, pero no se considera que la referida estrategia sea aconsejable en una arteria que carece de pedículo.
Sin embargo, según el juicio del cirujano, puede resultar conveniente la división distal del hemoducto antes de haber concluido su disección. Sobre todo, esta táctica puede ser un complemento de la cuarta modificación, ya comentada, con el objetivo de evitar lesionar el drenaje venoso. En ocasiones, a pesar de haberse separado la vena, es aún deficiente la movilidad de la arteria, y cortarla distalmente _previa administración de heparina_ eleva las posibilidades de modificaciones posicionales del hemoducto que dispone el cirujano, lo que puede facilitar la división de ramas que aún puedan ser de difícil acceso. En otro escenario, la vena mamaria puede interponerse entre la arteria y la coronaria a revascularizar; el cirujano puede deslizar el hemoducto, después de cortado distalmente, «por detrás» de la vena, y tomar en este momento, de ser necesario, medidas que permitan prolongar su longitud, o asumir un trayecto más recto hacia la coronaria diana (Figura 4).
Antes de concluir, es importante recalcar que las tres primeras modificaciones presentadas son practicadas habitualmente en todas las AMI diseccionadas por los autores de este trabajo. La implementación de las últimas dos es opcional y dependerá obviamente, de las características anatómicas, sobre todo, de la vena mamaria.
COMENTARIO FINAL
La efectividad y ventajas de las modificaciones que se han expuesto han sido demostradas durante un período de dos años, pero en un pequeño número de pacientes, si se compara con las grandes series publicadas por grupos de centros con mayores volúmenes operatorios. Los autores recomiendan tácitamente a otros equipos quirúrgicos la introducción de estas modificaciones en sus técnicas de disección esqueletizada de la AMI, pero son conscientes de que se necesita experiencia en una mayor cantidad de pacientes para arribar a conclusiones más sólidas.
CONFLICTOS DE INTERESES
Los autores declaran que no existen conflictos de intereses. ]]>
ANEXO. Ventajas de la oclusión distal de la arteria mamaria interna
1. Inicio más precoz de las reconocidas ventajas de la oclusión distal de la mamaria: Estudios16 han demostrado que las mamarias tienen un flujo inicial bajo, el cual se duplica tras 15-20 minutos de aumento de la presión hidrostática, favorecido por los latidos contra el obstáculo que constituye el clamp. Adelantar en el tiempo la oclusión nos ha permitido en muchas ocasiones obtener hemoductos con un flujo cercano o superior a 2 ml por latido inmediatamente después de cortar la arteria (120 ml en un minuto a una frecuencia cardíaca de 60 latidos/minuto). El logro en un menor período de tiempo de un hemoducto con estas características, permitirá la construcción de puentes más saludables con la consiguiente disminución de espasmos, competencia de flujos y desarrollo del síndrome de hipoperfusión mamaria. Debe recordarse que estudios imagenológicos por fluorescencia han demostrado que el realce del torrente sanguíneo, durante la competencia de flujo, se inicia en la coronaria nativa y se disemina en forma retrógrada al injerto de mamaria, a través del sitio anastomótico17. Si a esto se le suma el conocimiento de que el incremento en las fuerzas de cizallamiento dentro del vaso (fuerzas tangenciales derivadas de la fricción de la sangre fluyendo sobre la superficie endotelial) aumentan la expresión de la sintetasa endotelial de óxido nítrico18 y, por consiguiente, el diámetro del hemoducto, se comprenderá entonces los enormes beneficios de la obtención de una AMI con el mayor nivel de flujo posible.
Estas se suman a otras indudables ventajas de elevados diámetros y flujos en estos hemoductos, en cualquier estrategia quirúrgica que se implemente; profundizar más en ellas mismas está más allá de los objetivos de este artículo.
2. El aumento en el diámetro y flujo de la AMI se beneficia también por los posibles factores locales presentes en su lecho. Durante años, diferentes grupos han estudiado la posible presencia de factores nerviosos o humorales en el vaso, en la pared torácica o en el tejido adiposo periarterial mamario, que disminuirían la posibilidad de espasmo y facilitarían la dilatación de la arteria con un consiguiente mayor flujo19. El análisis pormenorizado de estos estudios, igualmente supera los objetivos de este trabajo, pero la teórica presencia de estos factores ha llevado a algunos grupos, por ejemplo, a favorecer la disección pediculada de la AMI sobre la supuesta base de que su calibre será mayor si se beneficia de una sustancia anti-contráctil presente en la grasa periarterial. Existan o no estos factores20,21, lo cierto es que la dilatación del hemoducto se verá favorecida una vez que haya sido totalmente esqueletizada. En teoría, adelantar la colocación del clamp le permitirá a la mamaria, durante un mayor período de tiempo, sumar al aumento de la presión hidrostática los beneficios de los posibles factores vasorrelajantes presentes en su lecho; las técnicas actuales, al colocar el clamp una vez que la AMI ha sido separada de la pared, disminuyen la incidencia de los factores locales sobre el diámetro del vaso.
3. Favorece la visualización y control de ramas: En la medida que aumenta el diámetro y flujo de la AMI sucede lo mismo con los vasos que de ella nacen. Así, ramas con mayor flujo y calibre tienden también a elongarse lo que facilita su control, especialmente en la técnica «solo con clips y tijeras». Si el cirujano visualiza mejor las ramas le es más fácil su control, por lo que disminuye el tiempo de disección.
4. Aumento intencional de la irrigación a órganos en riesgo de isquemia o infección, mediante el redireccionamiento fisiológico del flujo sanguíneo de la AMI, durante su disección. Este quizás sea el más importante beneficio que se obtiene de la colocación distal del clamp. Durante muchos años se ha conocido el significativo potencial para la plasticidad que puede exhibir la AMI en presencia de una obstrucción al flujo anterógrado22. También es ampliamente reconocida la capacidad de las mamarias de aumentar sus diámetros y flujos de forma importante, para servir como vía colateral de irrigación a órganos distantes, en enfermedades que se acompañan de estenosis significativas de la aorta, como el síndrome de Leriche23,24 o la coartación de la aorta25. En este caso la oclusión del extremo distal de la arteria permitirá, durante el tiempo que dura su disección, una redistribución y aumento del flujo sanguíneo en otros órganos, de las siguientes formas:
- Al esternón y tejidos periesternales. Mientras existan ramas esternales o perforantes sin pinzar, el flujo de la AMI, al no contar _en esas circunstancias_ con su desagüe distal, se redireccionará en ese sentido. Una ventaja adicional de este nuevo aumento de flujo sanguíneo es que va acompañado del antibiótico administrado como profilaxis. Quizás el mayor inconveniente, aparentemente nunca estudiado, de permitir la integridad del flujo mamario durante su disección, es que una importante cantidad de la antibioprofilaxis se aleja irremediablemente del campo operatorio, lo cual es totalmente contraproducente pues la única función de esta dosis de antimicrobianos es precisamente evitar la infección del sitio quirúrgico. Un estudio26, al menos, ha señalado que el menor de los picos de concentración de la antibioprofilaxis se alcanza en el hemiesternón que está siendo diseccionado una hora después de la administración de 4 gramos de cefazolina (una dosis mayor a la usada en nuestro medio); a partir de ese minuto comienza una constante disminución de esa concentración. La precoz oclusión distal de la mamaria forzará al antibiótico que discurra por ella, a partir de ese momento, a impregnar al esternón y a otros tejidos mediastinales, que estarán luego sometidos a elevado riesgo de infección, en especial cuando se diseccionan ambas AMI27,28.
- Al corazón: La oclusión de la mamaria antes de su bifurcación favorece un aumento del flujo sanguíneo colateral no coronario al corazón, por dos vías:
• Anterógrada: Mediante la rama pericardiofrénica. Desde la década de 1930 se conoce que esta arteria es la principal fuente de irrigación extracardíaca del corazón29. Hasta 1959 varios cirujanos emplearon la ligadura distal de las arterias mamarias como una forma de aumentar la irrigación del corazón, sobre la base de que un estatus hipertensivo local produciría un incremento de la presión de perfusión dentro de canales, en especial la pericardiofrénica, que llegarían al miocardio22. Presumiblemente el desarrollo de la máquina de circulación extracorpórea y otras cuestiones éticas frenaron esta práctica, pero la teoría sobre la cual se sustenta sigue vigente, al punto de que recientemente ha vuelto a considerarse esta opción en situaciones donde otras variantes terapéuticas no pueden ser aplicadas30. ]]>
• Retrógrada: Mediante las conexiones de las arterias epigástrica inferior y superior, musculofrénica, frénica y pericardiofrénica al nivel del diafragma14. Es conocida la comunicación existente entre las arterias epigástrica superior e inferior31, que constituye la ya mencionada importante vía de colateralidad a los miembros inferiores. En sentido inverso, existe por tanto un flujo retrógrado proveniente de la arteria iliaca común, mediante ambas epigástricas hacia el sistema de la mamaria interna que puede aprovecharse en la realización de puentes a segmentos distales de la arteria descendente anterior32.
Al haberse colocado el clamp proximal a la bifurcación y conservarse, por tanto, íntegra la comunicación entre las ramas epigástrica superior y musculofrénica7, se garantiza _además de la acentuación del diámetro de ese extremo distal (al seguir los mismos principios del aumento de la presión hidrostática por vía retrógrada)_, un incremento de la irrigación del corazón mediante la ya mencionada anastomosis entre la arteria musculofrénica y pericardiofrénica a nivel del diafragma. En el lado derecho debe agregarse otra fuente de flujo sanguíneo retrógrado consistente en la anastomosis de ramas de la arteria hepática a través del ligamento falciforme con pequeñas ramas de la mamaria derecha14.
5. ¿Precondicionamiento isquémico del corazón? Esta posible ventaja necesita ser estudiada con más profundidad. Las extensas relaciones de colateralidad que se establecen alrededor de la AMI hacen poco probable el desarrollo de isquemia por la oclusión distal del vaso, pero si esta ocurriera a algún nivel, un mecanismo de precondicionamiento isquémico estaría favoreciendo al corazón de forma más temprana a como ocurre en el caso de la técnica clásica de esqueletización.
BIBLIOGRAFÍA
1. Vineberg A, Miller G. Internal mammary coronary anastomosis in the surgical treatment of coronary artery insufficiency. Can Med Assoc J. 1951;64(3):204-10.
2. Sewell WH. Results of 122 mammary pedicle implantations for angina pectoris. Ann Thorac Surg. 1966;2(1):17-30.
3. Cunningham JM, Gharavi MA, Fardin R, Meek RA. Considerations in the skeletonization technique of internal thoracic artery dissection. Ann Thorac Surg. 1992;54(5):947-50.
4. Gurevitch J, Kramer A, Locker C, Shapira I, Paz Y, Matsa M, et al. Technical aspects of double-skeletonized internal mammary artery grafting. Ann Thorac Surg. 2000;69(3):841-6.
5. He GW, Taggart DP. Spasm in arterial grafts in coronary artery bypass grafting surgery. Ann Thorac Surg. 2016;101(3):1222-9.
6. Keeley SB. The skeletonized internal mammary artery. Ann Thorac Surg. 1987;44(3):324-5.
7. Satdhabudha O, Noppawinyoowong N. A randomized comparison of flow characteristics of semiskeletonized and pedicled internal thoracic artery preparations in coronary artery bypass. J Cardiothorac Surg [Internet]. 2017 [citado 26 May 2018];12(1):28. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5434624 /pdf/13019_2017_Article_589.pdf
8. Ji Q, Xia L, Shi Y, Ma R, Shen J, Lai H, et al. In Situ Skeletonized Right Internal Mammary Artery Bypass Grafting to Left Anterior Descending Artery: Feasibility, Mid-Term Efficacy, and Risk Factors for Graft Failure. Int Heart J. 2018;59(1):35-42. ]]>
9. Gatti G, Dell'Angela L, Maschietto L, Luzzati R, Sinagra G, Pappalardo A. The impact of diabetes on early outcomes after routine bilateral internal thoracic artery grafting. Heart Lung Circ. 2016;25(8):862-9.
10. Robinson BM, Paterson HS, Naidoo R, Dhurandhar V, Denniss AR. Bilateral internal thoracic artery composite Y grafts: Analysis of 464 angiograms in 296 patients. Ann Thorac Surg. 2016;101(3):974-80.
11. Luzurier Q, Le Guillou V, Lottin M, Vermeulin T, Marini H, Petel T, et al. Is the risk of wound infection related to bilateral internal thoracic artery graft potentiated by age? Ann Thorac Surg. 2016;102(4):1239-44.
12. Sahar G, Shavit R, Yosibash Z, Novack L, Matsa M, Medalion B, et al. The physiologic and histologic properties of the distal internal thoracic artery and its subdivisions. J Thorac Cardiovasc Surg. 2015;149(4):1042-50.
13. Harky A, Mohammad HA, Garner M, Ali M, Alani MS. Anomalous right internal thoracic artery terminating in the right superior pulmonary vein. Ann Thorac Surg. 2017;104(4):e323-4. ]]>
14. Sajja LR, Mannam G. Internal thoracic artery: Anatomical and biological characteristics revisited. Asian Cardiovasc Thorac Ann. 2015;23(1):88-99.
15. Onan B, Yeniterzi M, Onan IS, Ersoy B, Gonca S, Gelenli E, et al. Effect of electrocautery on endothelial integrity of the internal thoracic artery: ultrastructural analysis with transmission electron microscopy. Tex Heart Inst J. 2014;41(5):484-90.
16. Martínez Comendador JM, Castaño M, Álvarez JR. Biología y resultados de la arteria mamaria interna. Cir Cardiov. 2011;18(4):269-75.
17. Honda K, Okamura Y, Nishimura Y, Uchita S, Yuzaki M, Kaneko M, et al. Graft flow assessment using a transit time flow meter in fractional flow reserve-guided coronary artery bypass surgery. J Thorac Cardiovasc Surg. 2015;149(6):1622-8.
18. Hwang HY, Koo BK, Yeom SY, Kim TK, Kim KB. Endothelial shear stress of the saphenous vein composite graft based on the internal thoracic artery. Ann Thorac Surg. 2018;105(2):564-71. ]]>
19. Saha KK. Graft spasm _ The Achilles heel of arterial grafts. Indian Heart J. 2017;69(5):571-2.
20. Kociszewska K, Malinowski M, Czekaj P, Deja MA. What is the source of anticontractile factor released by the pedicle of human internal thoracic artery? Interact Cardiovasc Thorac Surg. 2015;21(3):301-7.
21. Manenti A, Roncati L. Nervous network of skeletonized internal thoracic artery. Ann Thorac Surg. 2013;95(4):1511-2.
22. Picichè M. Noncoronary collateral myocardial blood flow: The human heart's forgotten blood supply. Open Cardiovasc Med J. 2015;9:105-13.
23. Al-Atassi T, Toeg HD, Chan V, Ruel M. Coronary Artery Bypass Grafting In: Sellke FW, del Nido PJ, Swanson SJ, eds. Sabiston & Spencer: Surgery of the chest. 9ª ed. Philadelphia: Elsevier; 2016. p. 1551-88. ]]>
24. Ahmed S, Raman SP, Fishman EK. CT angiography and 3D imaging in aortoiliac occlusive disease: Collateral pathways in Leriche syndrome. Abdom Radiol (NY). 2017;42(9):2346-57.
25. Hutchison SJ. Coarctation and Atresia of the Aorta. In: Hutchison SJ, Eagle KA, Diethrich EB, Peterson MD. Aortic Diseases Clinical Diagnostic Imaging Atlas. Philadelphia: Elsevier; 2009. p. 271-96.
26. Andreas M, Zeitlinger M, Hoeferl M, Jaeger W, Zimpfer D, Hiesmayr JM, et al. Internal mammary artery harvesting influences antibiotic penetration into presternal tissue. Ann Thorac Surg. 2013;95(4):1323-9.
27. Pasrija C, Ghoreishi M, Shah A, Rouse M, Gammie JS, Kon ZN, et al. Bilateral internal mammary artery use can be safely taught without increasing morbidity or mortality. Ann Thorac Surg. 2018;105(1):76-82.
28. Nakahara Y, Yoshida S, Kanemura T, Yamagishi S, Tochigi S, Osaka S. Bilateral internal thoracic artery grafts in hemodialysis: A single-center propensity score analysis. Ann Thorac Surg. 2018;105(1):153-9. ]]>
29. Hudson CL, Moritz AR, Wearn JT. The extracardiac anastomoses of the coronary arteries. J Exp Med. 1932;56(6):919-25.
30. Stoller M, Seiler C. Effect of permanent right internal mammary artery closure on coronary collateral function and myocardial ischemia. Circ Cardiovasc Interv [Internet]. 2017 [citado 20 Feb 2018];10(6):e004990. Disponible en: https://www.ahajournals.org/doi/pdf/10.1161/CIRCINTERVENTIONS.116.004990
31. Sever AJ, Patel C, Albeer Y, Darian VB. The technique and benefits of angiographic embolization of inferior epigastric arteries prior to pedicled TRAM flap breast reconstruction: Results from a single center. Cardiovasc Intervent Radiol. 2017;40(12):1845-50.
32. Nezic DG, Bojovic ZR, Milicic MD, Antonic ZD, Boricic MI, Micovic SV. Mid-term patency of the inverted left internal thoracic artery conduit. J Card Surg. 2014;29(6):790-3.
33. Schwabegger AH. Deformities of the anterior thoracic wall. In: Congenital Thoracic Wall Deformities Diagnosis, Therapy and Current Developments. New York: Springer-Verlag; 2011. p. 3-56.
34. Cheng K, Rehman SM, Taggart DP. A review of differing techniques of mammary artery harvesting on sternal perfusion: Time for a randomized study? Ann Thorac Surg. 2015;100(5):1942-53.
35. Ding WJ, Ji Q, Shi YQ, Ma RH, Wang CS. Incidence of deep sternal wound infection in diabetic patients undergoing off-pump skeletonized internal thoracic artery grafting. Cardiology. 2016;133(2):111-8.
36. Papaspyros S, Zamvar V. Operative Techniques: Coronary Artery Bypass Graft Surgery. In: Lanzer P, ed. PanVascular Medicine. Berlin: Springer-Verlag; 2015. p. 2351-8.
37. Vineberg AM, Becerra A, Chari RS. The influence of the Vineberg sponge operation upon the hydrostatics of the myocardial circulation in health and disease: Evidence of luminal ventricular circulation in the beating heart. Can Med Assoc J. 1961;85(20):1075-90.
38. Parissis H, Chughtai Z, Soo A. Two questions on bilateral internal mammary artery usage. Asian Cardiovasc Thorac Ann. 2013;21(6):751-5.
39. Schipper RJ, Lobbes MB, Dikmans RE, Beets-Tan RG, Smidt ML, Boetes C. Bilateral analysis of the cross-sectional area of the internal mammary arteries and veins in patients with and without breast cancer on breast magnetic resonance imaging. Insights Imaging. 2013;4(2):177-84.
40. Punjabi PP, Chan KMJ. Coronary artery bypass grafting. In: Punjabi PP, ed. Essentials of Operative Cardiac Surgery. Switzerland: Springer International Publishing; 2015. p. 67-79.
Recibido: 18 de abril de 2018
Aceptado: 24 de mayo de 2018
Yoandy López-De la Cruz. Servicio de Cirugía Cardiovascular, Hospital Universitario Cardiocentro Ernesto Che Guevara. Santa Clara, Villa Clara, Cuba. Correo electrónico: yoandylc@infomed.sld.cu
]]>