Estudio de la electropolimerización de polipirrol en presencia de un ácido quiral
Study of Polypyrrole Electropolymerization in the Presence of a Chiral Acid
MSc. Ana Isa Pérez-CordovesI; Dr. C. Abel Ibrahim Balbin-TamayoII; Dr. C. Pércio Augusto Mardini-FariasIII, Dr. C. Josino Costa-MoreiraIV
IInstituto Nacional de Controle de Qualidade em Saúde (INCQS)-Fiocruz, Rio de Janeiro, Brasil, anita116br@gmail.com ]]>
IIDepartamento de Química Analítica, Facultad de Química, Universidad de La Habana, Cuba
IIIDepartamento de Química, Pontifícia Universidad Católica de Rio de Janeiro, Brasil
IVCentro de Estudos da Saúde do Trabalhador e Ecologia Humana, Fundação, (ESTEH) Fiocruz, Rio de Janeiro, Brasil
RESUMEN
Se aborda el estudio de la modificación de electrodos con polipirrol e inductor quiral para su uso en reconocimiento de fármacos quirales que pueden traer la selectividad y sensibilidad requerida en el uso más simple de análisis en la detección de drogas quirales en muestras complejas, con límites de detección comparables con procedimientos muy elaborados, empleo de instrumentación compleja y altos costos de mantenimiento y adquisición, predominantes actualmente. Las técnicas utilizadas para la investigación fueron voltamperometría cíclica y cronocoulombimetría. El ácido Canforsulfónico (CSA) se utilizó como inductor quiral durante la electropolimerización. Los resultados mostraron que en el caso de la película obtenida en presencia de CSA muestra dos picos para el sistema Fe(CN)63-/4-, producto de la modificación en el sistema de polimerización. También se calculó el área electroactiva del electrodo determinándose que es mayor que el área geométrica, demostrándose así que la superficie modificada tiene una electroactividad superior.
Palabras clave: polímeros conductores, electrodos modificados, voltametría.
ABSTRACT
In this paper we address the study of the modification of electrodes with polypyrrole and a chiral inductor for use on the recognition of chiral drugs, that can bring the selectivity and sensitivity required for the use of simpler approaches of analysis for the detection of chiral drugs in complex samples with detection limits compared to the very elaborate procedures and complex instrumentation of employment and high maintenance costs and acquisition that predominate today. The techniques used for research were cyclic voltamperometry and crhonoculombimetry. Acid Canphorsulfonic (CSA) was used as chiral inductor. The results showed that in the case of pyrrol/CSA study system shows two peaks suggesting different electropolimerization form by the presence of CSA. Also electroactive area was calculated by determining the electrode is greater than the geometric area, thus demonstrating that the modified surface has a higher electroactivity.
]]> Keywords: conductive polymers, modified electrode, voltammetry.
INTRODUCCIÓN
Junto con el reto en los últimos años de la Química analítica para desarrollar metodologías rápidas, precisas y sensibles para la detección y determinación de fármacos quirales en diferentes tipos de muestras han surgido nuevos métodos basados en el uso de sensores electroquímicos que puede proporcionar selectividad y la sensibilidad necesaria para el uso de abordajes más simples de análisis para la detección de estos fármacos y sus metabolitos [1].
En contraste con los procedimientos muy elaborados y uso de instrumentación compleja de altos costos de manutención y de adquisición que predominan en la actualidad, la electroquímica resulta en una técnica bien simple y con similares límites de detección. L os electroquímicos, por su parte, continúan en su empeño por tratar de dominar la superficie de los electrodos con el objetivo de ser capaces de seleccionar y controlar la reacción redox deseada, incluso en la presencia de otras reacciones posibles [2-4].
Tanto es así que la demanda de estos dispositivos para aplicaciones específicas de las grandes empresas ha crecido de forma significativa en los últimos años. El desarrollo de elementos nuevos es uno de los requisitos básicos para el diseño de sensores químicos, incluyendo también la síntesis de nuevos receptores y biomoléculas de reconocimiento de iones con una mayor selectividad y estabilidad [1-3].
Como una alternativa a los métodos de separación cromatográficos quiral, la utilización de estos sensores electroquímicos enantioseletivos han sido muy importantes [5]. Ellos aportan la ventaja de ser capaces de analizar una mezcla racémica de una manera rápida y barata debido a la posibilidad de determinar un enantiómero en presencia del otra sin la necesidad de la separación previa, directamente en la matriz con procedimientos simples y baratos [6, 7]. Además, la mayoría de los sensores enantioselectivos se pueden utilizar como un detector en sistemas de flujo, encontrándose disponibles técnicas para el análisis enantioselectiva en línea con sensores electroquímicos para la detección de solo uno de los enantiómeros [8] o el análisis simultáneo de ambos [9].
Los primeros trabajos sobre sensores electroquímicos quirales fueron publicados en 1970 cuando fue descrita la construcción de un electrodo de membrana selectiva a iones para determinar la a-feniletilamonio empleando como ionoforos enantioselectivos éteres-corona macrocíclico quirales [6]. A partir de esto, los trabajos dirigidos a la construcción de estos sensores enantioselectivos se incrementaron y su número ha aumentado considerablemente [7]. Estos sensores pueden ser clasificados de acuerdo con el mecanismo de transducción de la señal analítica dividiéndose principalmente en sensores potenciométricos, amperométricos o voltamperométricos [8].
La estabilidad de los complejos es directamente proporcional a la pendiente de la curva de calibración del sensor. Por lo tanto, una gran diferencia entre las energías libre de Gibbs para las reacciones anteriores también podría proporcionar una gran diferencia entre las pendientes cuando se están analizando los enantiómeros R y S [8 ,10].
Hay tres formas diferentes para el desarrollo de estos sensores:
El uso de matrices a base de cloruro de polivinilo (PVC).
El uso de matrices basado en pasta de carbón.
El uso de polímeros de impresión molecular para la extracción selectiva.
Estos polímeros ayudan a aumentar la selectividad analítica pues son capaces de reconocer por mecanismos similares a los de reconocimiento de sistemas biológicos [11-14].
Algunos de los principales atractivos de los polímeros impresos molecularmente (MIP) son: a) se pueden fabricar a gran escala en forma simple, barata y con morfologías diferentes a partir de monómeros orgánicos; b) son química y físicamente estables, capaces de trabajar en condiciones extremas de pH, temperatura y en presencia de disolventes orgánicos sin cambiar su estructura y la afinidad para el analito [8, 15, 16]. Por consiguiente, los MIP son una alternativa al desarrollo de sensores electroquímicos generalmente destinados para identificar selectivamente enantiómeros.
]]> Polímeros electrodepositados sobre las superficies de los electrodos han sido, de igual manera, ampliamente utilizados en la construcción de sensores electroquímicos. Ellos son materiales eléctricamente conductores de naturaleza orgánica que pueden ser generados por polimerización química o electroquímica de los monómeros, como por ejemplo polipirrol (PPy), politiofeno (PTH) y la polianilina (PANI) (figura 1). Por su naturaleza orgánica y la capacidad de formarse como partículas, membranas o micro y nano fibras de estos polímeros se abren nuevos caminos para el diseño y desarrollo de sistemas específicos de reconocimiento molecular.Dentro de este grupo de polímeros, los basados en polipirrol (PPy) se encuentran entre los más utilizados. Se han aplicado, principalmente, para el reconocimiento enantioselectivo de aminoácidos tales como fenilalanina, ácido glutámico, ácido aspártico o triptófano. En estos enfoques, polipirrol quiral es eletrosintetizado en las superficies de los electrodos en presencia de L ácido canforsulfónico (CSA), glutamato y ácido aspártico [17] que actúan como agentes inductores quirales. Se ha postulado que la inclusión de un amino-ácido enantiómero en la cadena del polímero durante la síntesis del polímero hace que adopte una disposición helicoidal que depende de la lateralidad del anión incorporado.
En este contexto, dada la simplicidad de la síntesis de polipirrol con ácido quiral R o S canforsulfónico y en base a la emergente necesidad de dispositivos para el análisis de enantiómeros rápido y confiable, que resulten en características más favorables para los estudios de la disposición cinética de los medicamentos producidos incluso como mezcla racémica, se plantea como un objetivo de este trabajo la modificación de electrodos con polipirrol y un inductor quiral para su uso en el reconocimiento de fármacos quirales.
MATERIALES Y MÉTODOS
Reactivos
K3 [Fe (CN)6] y K4 [Fe (CN)6] se obtuvieron de Sigma (St. Louis, MO, EE.UU.) y se utilizó sin purificación previa. El KCl, H2SO4 y ácido R-canforsulfónico (R-CSA) se obtuvieron de Fluka (Buchs, Suiza). Todos los demás reactivos fueron utilizados tal como se obtiene comercialmente con la excepción de la polipirrol que se purificó previamente.
Todas las soluciones acuosas se prepararon con agua desionizada.
Equipos
]]> Los estudios se realizaron con un polarógrafo Analyser (EG & G PAR Modelo 384-B Princeton Applied Research, Princeton, Nueva Jersey, EE.UU.) equipado con una celda externa. El electrodo de trabajo utilizado fue un electrodo de oro (diámetro 3,0 mm de GCE, BAS Bioanalytical Systems, Inc., West Lafayette, Indiana 47906, EE.UU.); como electrodo de referencia se utilizó el de Ag/gCl y un electrodo de platino (Pt) se utilizó como electrodo auxiliar. Un agitador magnético con una barra de agitación en la celda (Nalgene Cat. No. 6600 a 0,01 mil, Rochester, NY) proporcionó transporte convectivo.Procedimientos
Antes de cada experimento el electrodo fue pulido por tratamientos sucesivos utilizando alúmina en polvo de 0,3 micrones.
Las películas fueron generadas electroquímicamente a través cronocoulometría (CC). En la celda con los electrodos se colocaron 150 µL de la solución 5.10-4 mol.L-1 e pirrol previamente destilado y 5 ml del ácido en estudio. El ácido R o S canforsulfónico (CSA) fue utilizado como inductor quiral y comparativamente se hizo la síntesis con H2SO4. Finalmente, las superficies de los electrodos se caracterizaron electroquímicamente y los dos filmes realizados en las mismas condiciones, se analizaron comparativamente.
Todas las mediciones fueron realizadas a temperatura ambiente (25 °C).
RESULTADOS Y DISCUSIÓN
Determinación del área efectiva
Cronocoulometría (CC) es una de las técnicas clásicas utilizadas en electroquímica, se basa en la medición de carga (coulombs) como una función del tiempo. Consiste en la aplicación de un pulso rápido-creciente de potencial al electrodo de trabajo y la carga eléctrica que pasa a través de este electrodo se mide como una función de tiempo /18/. El análisis de los datos cronocoulométrico se basa en la ecuación de Anson (ecuación 3) [19] que define la dependencia del tiempo de carga:
]]>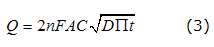
Aquí, Q representa la carga (coulombs) n y A representan el número de electrones transferidos en el área real de la superficie electródica (cm2), respectivamente.
F es la constante de Faraday (96,485coulombs/mol). La concentración del mediador es denotada por C. El coeficiente de difusión del mediador (cm2 s-1) y el tiempo (s) son indicados por D y T, respectivamente. Como se puede observar en la ecuación 3, existe una relación lineal entre la carga (Q) y la raíz cuadrada del tiempo (t1/2). De la pendiente de la recta obtenida al graficar Q vs. t1/2 se obtiene la ecuación 4:
Por lo tanto, el área electroactiva del electrodo de trabajo (A) puede ser calculada a partir de la pendiente mediante la ecuación 5, pues los otros cuatro parámetros (n, F, C y D) son conocidos
Además del número de electrones transferidos (n) y de la constante Faraday (F) ya bien conocidos, el coeficiente de difusión (D) del mediador fue para el ferrocianuro (7,6 x 10-6 cm2 s-1), y el coeficiente de difusión para el ferrocianuro (6,36 x 10-6 cm2 s-1) [19].
La figura 2 muestra los diagramas de Anson para a) pirrol / CSA y b) pirrol/H2SO4.
La fotografía de la superficie del electrodo modificado y sin modificar se muestra en la figura 3.
Los valores del área efectiva determinada por cronocoulometría y utilizando el diagrama de Anson se muestran en la tabla 1.
]]>
TABLA 1. ÁREA DE LOS ELECTRODOS
| Electrodos | Área (cm2) |
| Pirrol/H2SO4 | 0,151 +/-0,001 |
| Pirrol/ACS | 0,167 +/-0,002 |
| Oro sin modificar | ]]> 0,126+/- 0,004 |
| Área geométrica | 0,071 +/- 0,001 |
Como era de esperar, la superficie electroactiva del electrodo modificado es mayor que el área geométrica de la superficie del electrodo de oro sin modificación. El hecho puede explicarse por el factor de rugosidad (relación entre la superficie electroquímica y la superficie geométrica) que en el caso del electrodo modificado Pirrol /H2SO4 es de 2,1 y del electrodo modificado Pirrol/CSA es de 2,3. Este factor de rugosidad se puede atribuir a la morfología de la superficie modificada con polipirrol del electrodo de trabajo, formándose una capa polimérica conductora porosa. La presencia del inductor quiral CSA no afecta la rugosidad del sistema polimérico obtenido electroquímicamente.
Caracterización electroquímica de la superficie
La técnica utilizada para estudiar el mecanismo de reacción fue la voltametría cíclica, que es una de las técnicas más utilizadas para este estudio, pues proporciona información rápida sobre el comportamiento redox de las especies y las reacciones químicas involucradas (mecanismos de reacción, reacciones química acoplada) y la determinación de los parámetros termodinámicos. Además, permite electrolizar una especie e invertir el potencial para verificar la formación del par redox pudiéndose de esta forma dilucidar el mecanismo de reacción.
Realizando estudios de variaciones en la velocidad de barrido a diferentes concentraciones es posible conocer la cinética de las reacciones o la presencia de especies intermedias en el proceso redox. Por lo tanto, es posible hacer la relación entre las señales de corriente anódica y catódica a varias concentraciones a diferentes velocidades de barrido. Debe cumplirse que Ipa/Ipc = 1 para la electro-reducción y Ipc/Ipa = 1 para la electro-oxidación, situándose en el numerador del cociente la corriente debido a las especies que se genera en el electrodo.
El sistema utilizado como referencia para el estudio fue Fe(CN)63-/4-, pues la transferencia de carga de este sistema es dependiente del material del electrodo de trabajo y la forma de preparación del mismo [20].
Fueron registrados voltamogramas de los electrodos modificados en diferentes velocidades de barrido, a las dos concentraciones de solución equimolar de Fe(CN)63-/4-, para observar el efecto de polimerización del pirrol en la presencia del ácido sulfúrico y del inductor quiral CSA.
La figura 4 muestra las curvas de corriente / potencial para el sistema Fe(CN)63-/4- a diferentes velocidades de barrido.
]]>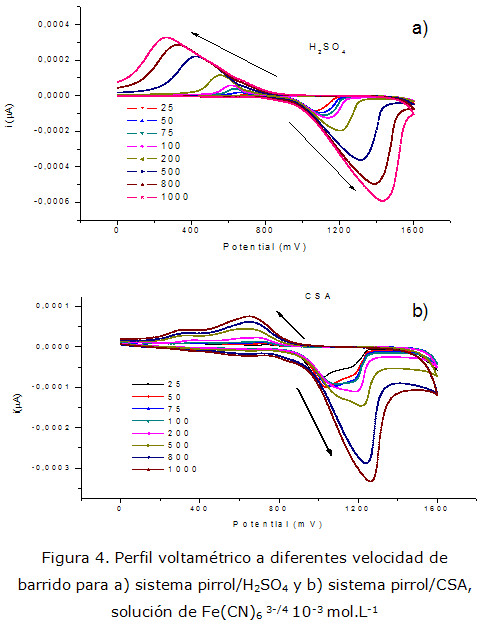
En el sistema pirrol/CSA se observan dos picos, tanto en el proceso de oxidación (304 mV, 649 mV) como en el de reducción (1036 mV, 1235 mV). Uno de ellos está en correspondencia con el pico de sistema Fe(CN)63-/4-, sintetizado en ácido sulfúrico. El segundo pico aparece a partir de la velocidad de barrido de 50 mV/seg. La presencia de este segundo pico justifica un posible proceso adsortivo de reactivos y productos causados por una interacción electrostática con una posible carga residual inducida por la presencia del CSA en la electropolimerización.
La ecuación RandlesSevcik (ecuación 6) que de manera simplificada queda representada por la ecuación 7, establece una proporcionalidad entre el perfil de corriente, con la concentración y la velocidad de barrido y la inclinación permite calcular el área efectiva del electrodo [21].
Para un sistema electroquímico, la dependencia del log ip = log k+ 0,5log v representa el perfil de una línea recta, cuando el mismo presenta un control difusional. La constante de Randles-Sevcik (k) permite extraer información analítica importante, como el número de electrones intercambiados y el valor del coeficiente de difusión de la especie electroactiva.
Cuanto más rápida la velocidad de barrido, mayor es la intensidad de la corriente de pico; pero si la especie electroactiva está adsorbiendo en el electrodo la intensidad de la corriente del pico será directamente proporcional a la velocidad de barrido en lugar de su raíz cuadrada. Las tablas 2 y 3 muestran los parámetros del ajuste lineal de la recta resultado del gráfico log v vs.log ip para los procesos catódicos y ánodicos.
TABLA 2. RESULTADO DE LA APLICACIÓN DE LA ECUACIÓN DE RANDLES-SEVCIK AL
ESTUDIO DE LA INFLUENCIA DE VELOCIDAD DE BARRIDO EN LA CORRIENTE
DE PICO CATODICO: (LOG ip = LOG K+ MLOG v)
|
| Pendiente (m) | Regresión (R) | |
| H2SO4 | 1,10-3 | 0,38±0,03 | 0,972 61 |
| 1,10-4 | 0,38±0,03 | ]]> 0,972 61 | |
| CSA (1036 mV) | 1,10-3 | 0,25±0,03 | 0,910 1 |
| 1,10-4 | 0,34±0,02 | 0,974 869 | |
| CSA ]]> (1235 mV) | 1,10-3 | 0,30±0,02 | 0,981 01 |
| 1,10-4 | 0,38±0,03 | 0,972 61 | |
TABLA 3. RESULTADO DE LA APLICACIÓN DE LA ECUACIÓN DE RANDLES-SEVCIK AL
ESTUDIO DE LA INFLUENCIA DE VELOCIDAD DE BARRIDO EN LA CORRIENTE
DE PICO CANODICO (LOG ip= LOG K + MLOG v)
|
| Pendiente (m) | Regresión (R) | |
| H2SO4 | 1,10-3 | 0,5±0,07 | 0,928 7 |
| 1,10-4 | 0,53±0,07 | ]]> 0,928 74 | |
| CSA (1036 mV) | 1,10-3 | 0,74±0,01 | 0,998 13 |
| 1,10-4 | 0,74±0,04 | 0,999 35 | |
| CSA ]]> (1235 mV) | 1,10-3 | 0,43±0,09 | 0,965 31 |
| 1,10-4 | 0,53±0,06 | 0,972 61 | |
Según los valores obtenidos, se aprecia una similitud entre las pendientes para cada sistema (pirrol/H2SO4 y pirrol/CSA) a las concentraciones estudiadas, no se evidencia influencia en el transporte de masa y la resistencia no compensada. Se puede apreciar también que el proceso anódico del sistema pirrol/H2SO4 y del sistema pirrol/CSA a las concentraciones estudiadas, presenta un control difusional. Se observa que la señal de 1 036mV del pirrol/CSA en ambas concentraciones muestra un proceso no difusional.
Para los procesos catódicos ambos sistemas en las concentraciones estudiadas mostraron comportamiento no regido por la difusión. Estos comportamientos alejados del control difusional sugieren posible adsorción de los productos y/o reaccionantes, causado por una modificación en el sistema de polimerización con el uso del inductor quiral.
Para ambos sistemas al aumentar la velocidad de barrido, aumenta la diferencia de potencial entre los picos catódicos y anódicos, que muestra un comportamiento cuasi-reversible (figura 5).
]]> Denotar que para el sistema pirrol/CSA tiene una menor diferencia de potencial entre los picos del Fe (CN)63-/4-, indicando una mayor facilidad termodinámica para la transferencia electrónica del proceso redox.Otro criterio para determinar el inicio de una reversibilidad del sistema consiste en realizar el cociente de las señales de corriente catódica y anódica de varias concentraciones o diferentes velocidades de barrido.
Además de esto, este cociente permite conocer el posible mecanismo asociado con la reacción en el electrodo. La figura 6 muestra el gráfico de Ipa/Ipc versus velocidad de barrido para el electrodo modificado pirrol/H2SO4 y la figura 7 para el electrodo modificado pirrol/CSA a las concentraciones I Fe 10-3 mol L-1 y II Fe 10-4 mol L-1.
Teniendo en cuenta el perfil de los cocientes de corriente catódica/ánodo obtenido, se observan dos comportamientos: uno a bajas velocidades de barrido donde el cociente de corriente aumenta con la velocidad de barrido y otro a altas velocidades donde el cociente se mantiene constante. Este comportamiento es más marcado a bajas concentraciones. Este aumento con la velocidad de barrido sugiere una transferencia de electrones reversible seguido de una reacción química irreversible. A altas velocidades de barrido el sistema tiene un comportamiento característico de una trasferencia electrónica sin reacciones químicas acopladas.
CONCLUSIONES
La voltamperometría cíclica utilizada en la caracterización del electrodo modificado mostró un aumento del área electroactiva tanto para la película de polipirrol electropolimerizado en presencia de H2SO4 y de CSA, estos sistemas mostraron que a bajas velocidades de barrido presenta una reacción química acoplada mientras que a altas velocidades de barrido solo se manifiesta una transferencia electrónica.
]]>Para la película de pirrol/ CSA se obtuvieron dos señales para el sistema redox Fe(CN)63-/4-, debido a una posible adsorción del mismo en el polímero, por cambio en el sistema de polimerización.
Los electrodos modificados obtenidos en este estudio mostraron características prometedoras para su uso en el reconocimiento de compuestos enantiómeros con interés biológico.
AGRADECIMIENTOS
REFERENCIAS BIBLIOGRÁFICAS
1. BRETT, C.M.A. "Fungaro, D. A.; Nafion-Coated Mercury Thin Film and Glassy Carbon Electrodes for Electroanalysis. Characterization by Electrochemical Impedance", Electroanalysis. 2001, 13, 212.
]]>2. JOSEPH Wang.; Electroanalytical Techniques in Clinical Chemistry and Laboratory Medicine; 1988. VCH, Inc.: New York.
3. BRANINA, Kh. Z. Stripping Voltammetry in Chemical Analysis, John Wiley & Sons, 1974.
4. SIBEL, A. O. "Analysis of pharmaceuticals and biological ?uids using modern electroanalytical techniques", Crit. Rev. Anal. Chem. 2003, 33, 155181.
5. MARKEK, Trojanowicz. "Enantioselective electrochemical sensor and biosensor: A Mini-review", Electrochemistry Communications. 2014, 38, 47-52.
6. STEFAN. Ranuca-Ioana. "Biosensor for the enantioselective analysis of S-Captopril", Sensor and Actuators. 2003, B92, 228-231.
]]>7. J.C.VIRE. "Trends in Electrochemistry in Drug Analysis Current Topics", Electrochemistry, 1994, 3, 493515
8. DENISE L. "Sensores electroquímicos: Considerações sobre mecanismos de espécies químicas em ambientes microscópicos", Quim. Nova. 2006, 29, 1318.
9. PARVIZ Norouzi . "Sotalol Nanolevel Detection at an Au Microelectrode in Flowing Solutions", Russian Journal of Electrochemistry. 2008, 44(9), pp. 10241030.
10. THOMA A. P. "Enantiomer-selective behavior in membranes of a chiral, electrically neutral ionophor", Chimia. 1975, 29, 344.
11. OZKAN S.A "Electroanalytical characteristics of amisulpride and voltammetric determination of the drug in pharmaceuticals and biological media", Electroanalysis. 2004. 16, 231237.
12. STEFAN, R. I., Aboul-Enein, H. Y. And Van Staden, J. F. "Enantioselective electrochemical sensors", Sensors Update. 2002, 10, p. 123.
13. ROSBACH, K. In Molecular and ionic recognition with imprinted polymers, American Chemical Society: Washing, DC, Cap 3, 1998.
14. EVANNS , G. P. In Advances in Electrochemical Science & Engineering ; Gerisher, H., Tobias, Ch., Eds.; VCH Publisher:Weinheim, FRG, 1990;
15. ZHOU, Y., Potentiometric sensing of chiral amino acids. Chemistry of Materials 2003, vol. 15, p. 2774.
16. LAHAV, M., Imprinting of chiral molecular recognition sites in thin TiO2 films associated with field-effect transistors: novel functionalized devices for chiroselective and chirospecific analyse. Chemistry A European Journal 2001, vol. 7, p. 3992.
17. VERA L., Os farmacos e a quiralidade: Uma breve abordagem. Quimica. Nova 1997, vol. 20, p. 6.
18. BRAD J. A., Electrochemical methods Fundamentals and Applications, 2nd. ed., John Wiley & Sons, Inc: New York, 2001.
19. VASILIKI Fragkou, et al. Determination of the Real Surface Area of a Screen-Printed Electrode by Chronocoulometry Int. J. Electrochem. Sci. 2012, vol. 7, p. 6214.
20. KIRYSHO, V. N., L. I. Electrochemical behavior of the system ferricyanide-ferrocyanide at a graphite-epoxy composite electrode. Journal of Analytical Chemistry, 2011, vol. 66(5), p. 510-514.
21. PINGARRON C. Química electroanalítica. Fundamentos y aplicaciones, España: Síntesis, 2003.
]]>
Recibido: 3/05/2016
Aceptado: 22/09/2016
MSc. Ana Isa Pérez-Cordoves, Instituto Nacional de Controle de Qualidade em Saúde (INCQS)-Fiocruz, Rio de Janeiro, Brasil, anita116br@gmail.com
]]>