
Estudio preliminar de la adsorción de níquel y cobalto utilizando carbón vegetal de conchas de coco
Preliminary Study of the Adsorption of Nickel and Cobalt using Charcoal From Foconut Shells
MSc. Dolores Salas-Tort, Ing. Norma Marzal-Blanco, Dra. Margarita Penedo-Medina
Facultad de Ingeniería Química, Universidad de Oriente, Santiago de Cuba, Cuba. dsalas@fiq.uo.edu.cu
]]>
Resumen
En el departamento se realiza el estudio de obtención de carbón activado a partir de biomasa de cascarón de coco y del carbón vegetal de conchas de coco, para luego poder ser utilizado en procesos de descontaminación ambiental. Este trabajo tiene como objetivo analizar el comportamiento de la adsorción de iones níquel y cobalto, utilizando carbón pirolizado de conchas de coco y soluciones de sulfato de ambos metales a diferentes condiciones de pH y concentración inicial. Entre los métodos empleados se planteó analizar la influencia del pH de las soluciones de sulfatos metálicos en la concentración de equilibrio. Los niveles de pH fijados fueron 1, 2; 3 y 5. Para cada pH se debían obtener entonces las concentraciones de equilibrio y la cantidad de metal adsorbido por unidad de masa de carbón, para las diferentes soluciones de partida. Los resultados del estudio demostraron que la concentración de equilibrio y la capacidad de adsorción del carbón se incrementan con el aumento de la concentración inicial de la solución. Se obtuvieron las Isotermas de adsorción para el níquel, el cobalto y su ajuste a los modelos de Langmuir y de Freundlich a los diferentes pH. Entre las conclusiones principales están, que los resultados experimentales demostraron que el carbón pirolizado de conchas de coco tiene amplias posibilidades de aplicación en la adsorción de iones níquel y cobalto de soluciones de sulfatos de estos metales, al obtenerse muy altos valores de por ciento de recuperación, y soluciones resultantes con muy bajas concentraciones de iones metálicos.
Palabras clave: carbón vegetal, adsorción, conchas de coco, níquel, cobalto.
Abstract
The department is conducting the study to obtain activated carbon from biomass and coconut shell charcoal from coconut shells to later be used in environmental remediation processes. This work aims to analyze the behavior of the adsorption of nickel and cobalt ions using pyrolyzed coal and coconut shell sulfate solutions of both metals to different conditions of pH and initial concentration. Among the methods used to analyze the influence raised the pH of the solutions of metal sulfates in the equilibrium concentration. Fixed pH levels were 1, 2, 3 and 5. For each pH should then obtain the equilibrium concentrations and the amount of metal adsorbed per unit mass of coal, for different starting solutions. The study results showed that the equilibrium concentration and adsorption capacity of coal increases with increasing initial concentration of the solution. We obtained the adsorption isotherms for nickel and cobalt and their adjustment to the models of Langmuir and Freundlich to different pH. Among the main conclusions are that the experimental results showed that coal pyrolysed coconut shell has broad potential application in the adsorption of nickel and cobalt ions from sulphate solutions of these metals, obtained very high values of % recovery, and resulting solutions with very low concentrations of metal ions.
Keywords: charcoal, adsorption, coconut shells, nickel, cobalt.
INTRODUCCION
]]> Actualmente, el mundo se está enfrentando a graves problemas de contaminación que están dando al traste con muchos fenómenos naturales, como la destrucción de la capa de ozono, el derretimiento de los glaciales, el cambio constante de las estaciones fuera de época, la contaminación de las aguas por el vertimiento de las industrias, todo esto se resume en peligro para la existencia de la vida en la tierra: de los animales, la vegetación y especialmente la vida del hombre. Una de las vías que se puede utilizar para contrarrestar este efecto es la utilización del carbón pirolizado [1].La contaminación en las fuentes de agua se establece por la presencia de compuestos que no estarían en forma normal sin la intervención del hombre o por un aumento o descenso en el contenido de las sustancias existentes por la acción humana. De manera que en el agua pueden existir componentes químicos potencialmente más tóxicos tales como metales pesados: entre estos se encuentran: Manganeso, Plomo, Zinc, Cadmio, Cromo, Cobre, Cobalto y Níquel entre otros [6].
De acuerdo con lo expresado anteriormente, se determinó que el objetivo general del trabajo es, analizar el comportamiento de la adsorción de iones níquel y cobalto utilizando carbón pirolizado de conchas de coco y soluciones de sulfato de ambos metales a diferentes condiciones de pH y concentración inicial.
FUNDAMENTACION TEORICA
El carbón vegetal es utilizado por su valor calórico como fuente de energía, pero que al ser un material poroso, si es tratado convenientemente se puede incrementar su capacidad de adsorción entre 500 y 1500 m2/g. [2]
Las reacciones de desvolatilización de la biomasa vegetal durante la pirolisis dan lugar a un residuo sólido, el cual es un substrato orgánico de carbono. El carbón vegetal esta caracterizado por contener grupos funcionales, que incluyen estructuras aromáticas y olefínicas. Su área superficial es elevada y tiene un alto grado de reactividad, lo cual depende de la extensión de las reacciones secundarias de pirolisis en fase sólida. [2]
El carbón vegetal puede ser considerado como un producto de calidad en dependencia de sus propiedades físicas y químicas, las cuales están altamente relacionadas con la materia prima y las condiciones operacionales de los procesos de pirólisis. Son muchos los parámetros que caracterizan el carbón, los más significativos según Emrich son (Emrich, 1985): rendimiento, contenido de volátiles, contenido de carbono fijo, contenido de cenizas y dureza. [2]
Se utiliza en determinadas aplicaciones que no requieren de una gran capacidad de adsorción. Entre sus usos están en la recuperación de metales preciosos, en la adsorción de sustancias radiactivas, en la potabilización del agua, purificación de aguas residuales, en el tratamiento de residuales textiles, en la biotecnología, en la adsorción de vapores orgánicos, en las máscaras antigases y en la purificación industrial de gases y vapores con vistas a la eliminación de sustancias contaminantes. [2]
Las ecuaciones de Langmuir y Freundlich adaptadas a sistemas de adsorción líquidosólido
]]> Las operaciones prácticas requieren las correlaciones de equilibrio de los datos de adsorción experimental para correlaciones empíricas, que pueden incluir modelos de Langmuir y Freundlich. La isoterma Langmuir se basa en la presunción de que todos los puntos de adsorción en un adsorbente estructuralmente homogéneo son idénticos y energéticamente equivalentes. La idea básica del modelo de Langmuir es la cobertura de la superficie con una capa mono molecular.Teóricamente, el adsorbente posee una capacidad finita para el adsorbido, por tanto, el valor de saturación es alcanzado cuando no tiene lugar otra adsorción. La capacidad del adsorbente en el equilibrio se denomina Qe. En el modelo de Langmuir se relacionan la capacidad del adsorbente y la concentración de la solución en el equilibrio por la ecuación siguiente:

donde:
Qm es una constante relacionada con el área ocupada por una capa uni-molecular de adsorbato y refleja la capacidad de adsorción (mg/g) del adsorbente y b es una medida directa de la intensidad de adsorción (L/g). Ci y Ce son las concentraciones de adsorbato en la solución inicial y en la solución final en el equilibrio. El término m es la masa de adsorbente y V el volumen de solución.
También se puede determinar la capacidad de adsorción del adsorbente a partir de la ecuación propuesta por (Deepatana y Valix, 2006) que plantea:

La forma lineal de la ecuación (1) es:
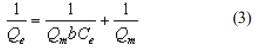
Un esquema de  produce una línea recta si los datos de la adsorción se adaptan al modelo Langmuir. Los valores de Qm y b están determinados por el desnivel y la intersección del esquema.
produce una línea recta si los datos de la adsorción se adaptan al modelo Langmuir. Los valores de Qm y b están determinados por el desnivel y la intersección del esquema.

La constante A es un indicador aproximado de la capacidad de adsorción (mg/g) y 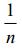 se relaciona con la intensidad de adsorción. La forma lineal de la ecuación (4) es:
se relaciona con la intensidad de adsorción. La forma lineal de la ecuación (4) es:
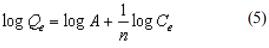
Una forma lineal de la ecuación Freundlich produce las constantes A y 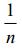 a partir de la intersección y el declive de logQe vs logCe.
a partir de la intersección y el declive de logQe vs logCe.
La magnitud de 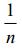 está directamente asociada a la eficiencia de la adsorción. Los valores desde
está directamente asociada a la eficiencia de la adsorción. Los valores desde 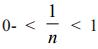 indican una adsorción favorable (Deepatana y Valix, 2006). [7]
indican una adsorción favorable (Deepatana y Valix, 2006). [7]
METODOS UTILIZADOS Y CONDICIONES EXPERIMENTALES
· Materia prima
En este trabajo la materia prima utilizada fue el carbón pirolizado a partir de conchas de coco. Este material fue suministrado para esta investigación por la fábrica de carbón activado UEB (Unidad Empresarial Básica) Carbón Activado ubicada en Baracoa. El carbón fue caracterizado determinándose el porcentaje de humedad, cenizas, materiales volátiles y carbono fijo.
]]> · Planificación de los experimentos de adsorciónPara el estudio del equilibrio de adsorción se decidió realizar los experimentos en reactores con agitación, poniendo en contacto una determinada masa de carbón con la solución cargada de iones metálicos. Las soluciones que se sometieron a estudio fueron soluciones de sulfato de níquel, y soluciones de sulfato de cobalto.
Los factores considerados fueron el pH y la concentración inicial de las soluciones de sulfatos de níquel y cobalto. Se mantuvieron fijas la temperatura y la velocidad de agitación.
Condiciones experimentales fijadas para los experimentos de adsorción
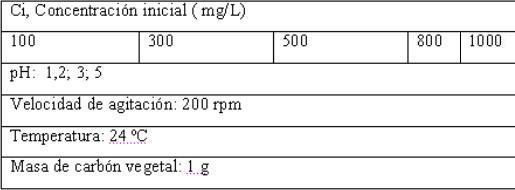
· Procedimiento para los experimentos sobre el equilibrio de adsorción
Para el estudio del equilibrio de adsorción de níquel y cobalto a partir de soluciones de sulfato, con carbón pirolizado a partir de conchas de coco, se planteó analizar la influencia del pH de las soluciones de sulfatos metálicos en la concentración de equilibrio. Los niveles de pH fijados fueron 1,2; 3 y 5.
Para cada pH se debían obtener entonces las concentraciones de equilibrio y la cantidad de metal adsorbido por unidad de masa de carbón, para las diferentes soluciones de partida. El procedimiento de los experimentos de adsorción fue el siguiente:
1. Se pesa 1 g de carbón y se deposita en el recipiente donde se realizará la adsorción (matraz o beaker).
2. Se miden 50 mL de solución de sulfato, a la cual previamente se le ha ajustado el pH con ácido sulfúrico. ]]>
3. Se deposita la solución de sulfato en el recipiente donde se colocó la masa de carbón, y se coloca en el agitador magnético, introduciendo previamente el magneto.
4. Se desarrolla el proceso de adsorción por agitación, durante 6 h.
5. Una vez concluida la agitación, se determina el pH de la solución.
6. Se filtra la solución utilizando papel de filtro.
7. El líquido filtrado se almacena en frascos y se guarda, igual que el sólido retenido en el papel de filtro.
8. Al experimento se le realiza una réplica.
RESULTADOS Y DISCUSION
A continuación se muestran los resultados experimentales obtenidos del estudio del equilibrio de la adsorción de níquel y cobalto en carbón vegetal. [4] y los modelos obtenidos a partir de los datos. Los resultados se muestran en las tablas 1 y 2.
Tabla 1 ]]> Parámetros de isotermas de adsorción para níquel adsorbidos en carbón vegetal

Tabla 2
Parámetros de isotermas de adsorción para cobalto adsorbidos en carbón vegetal

Para el modelo de Langmuir, se obtuvieron valores de Qm y b negativos (excepto para el cobalto a pH 1,2) los cuales no son lógicos desde el punto de vista físico, ya que el primer parámetro refleja la capacidad de adsorción (mg/g) del adsorbente y el segundo es una medida directa de la intensidad de adsorción (L/g).
Para el modelo de Freundlich se obtuvieron valores de A y 1/n positivos y aceptables desde el punto de vista físico, ya que A refleja la capacidad de adsorción (mg/g) del adsorbente y 1/n es una medida directa de la intensidad de adsorción (L/g). Sin embargo el valor de R2 para pH 5 es el menor (0,423 4), es decir que los datos prácticamente no se ajustan al modelo. Por eso se realizó otra prueba de ajuste para determinar el parámetro estadístico Durbin-Watson DW y llegar a conclusiones más exactas sobre esa anomalía, para eso se utilizó el programa Statgraphics Plus 5.1, a continuación se muestran los resultados:

Análisis:
La salida muestra los resultados del ajuste al modelo lineal para describir la relación entre Log Qe y Log Ce. La ecuación del modelo ajustado es
]]> logQe = 0,628867 + 0,999966 * logCeDado que el p-valor en la tabla ANOVA es mayor o igual a 0,01, no existe relación estadísticamente significativa entre Log Qe y Log Ce para un nivel de confianza del 90 % o superior. El estadístico R-cuadrado indica que el modelo explica un 42,336 % de la variabilidad en Log Qe. El coeficiente de correlación es igual a 0,650 661, indicando una relación moderadamente fuerte entre las variables.
El error estándar de la estimación muestra la desviación típica de los residuos que es 0,353 044. El error absoluto medio (MAE) de 0,218 262 es el valor medio de los residuos.
El estadístico Durbin-Watson (DW) examina los residuos para determinar si hay alguna correlación significativa basada en el orden en el que se han introducido los datos en el fichero. Dado que el p-valor es inferior a 0,05, hay indicio de una posible correlación serial.
En las figuras 1 a, b y c se muestran los valores de Qe experimentales obtenidos para el níquel y los calculados por el modelo de Freundlich a los diferentes pH planificados.
Fig. 1 Isotermas de adsorción para el níquel y su ajuste al modelo de Freundlich a los
diferentes pH; (a) pH 1,2, (b) pH 3 y (c) pH 5.
En las figuras 2 a, b y c se muestran los valores de Qe experimentales obtenidos para el cobalto y los calculados por el modelo de Langmuir y Freundlich (en el caso de la figura 2 a; a pH 1,2) y por Freundlich para los restantes pH (figura 2 b, figura 2 c).
]]> Fig. 2 Isotermas de adsorción para el cobalto y su ajuste a los modelos de Langmuir deResultados del porcentaje de recuperación en la adsorción de níquel y cobalto con carbón vegetal de conchas de coco
La expresión utilizada para la determinación del porcentaje de recuperación fue la siguiente:
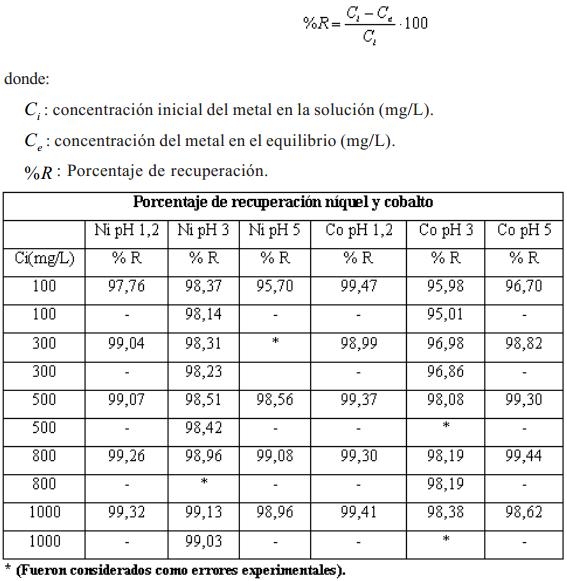
DISCUSION DE LOS RESULTADOS
Para el caso de la adsorción de níquel y cobalto se puede observar que la concentración de equilibrio y la capacidad de adsorción del carbón se incrementan con el aumento de la concentración inicial de la solución.
Para el modelo de Langmuir, se obtuvieron valores de Qm y b negativos los cuales no son lógicos desde el punto de vista físico ya que el primer parámetro refleja la capacidad de adsorción y el segundo es una medida directa de la intensidad de adsorción.
Para el modelo de Freundlich se obtuvieron valores de A y 1/n positivos y aceptables desde el punto de vista físico, ya que A refleja la capacidad de adsorción del adsorbente y 1/n es una medida directa de la intensidad de adsorción. Se evidencia que los resultados experimentales en la adsorción del níquel y el cobalto se ajustan mejor al modelo de Freundlich, aunque para el níquel todos los valores de 1/n son mayores que la unidad lo que indica que la adsorción no es tan favorable. Sin embargo para el cobalto a pH 1,2 y pH 5 indican una adsorción favorable.
]]> Evidentemente, la adsorción del níquel se adapta al modelo de Freundlich. Los valores R2 reportados para el modelo Freundlich en la tabla 1 confirman esta adecuación, pues los mismos oscilaron entre 0,939 4 y 0,902 6. Los valores de A, en la tabla 1, sugieren que el orden de la capacidad de adsorción del níquel es pH 3 > pH 5. Este orden es confirmado por los valores 1/n correspondientes ya que para pH 3 el valor de 1/n se acerca más a la unidad.Los valores de A, en la tabla 2, sugieren el orden de la capacidad de adsorción del cobalto es pH 5 > pH 3. Este orden es confirmado por los valores 1/n correspondientes ya que para pH 5 el valor de 1/n se acerca más a la unidad. Sin embargo el valor de R2 para pH 5 es muy pequeño indicando que el modelo no se ajusta, por eso se analizó el estadígrafo Durbin-Watson (DW) para determinar si los errores son independientes o están correlacionados.
Como conclusión del análisis estadístico anterior vemos que del ANOVA (Analysis of Variante, Análisis de Varianza) se puede observar que el P-valor es superior a 0,05 luego a este nivel de significación no existe correlación lineal entre Qe y Ce.
Además al analizar el P-valor del estadígrafo Durbin-Watson (DW) encontramos que es menor que 0,05 que es el nivel de significación normalmente utilizado. Esto indica que existen indicios de correlación entre los residuos, lo cual contradice una de las suposiciones principales del análisis de regresión lineal, que es la independencia de los residuos. Por tanto, no es posible aplicar esta técnica con este conjunto de datos, ya que el parámetro DW es igual a 1,148 26 o sea DW< 1,4 hay correlación entre los errores y por tanto se desecha el modelo.
En la adsorción del cobalto se observa que para pH 1,2 se adapta mejor el modelo de Langmuir, aunque la diferencia en la extensión de la adecuación entre los dos modelos no es significativa (0,037 8). Esto indica que la adsorción puede ocurrir tanto como adsorción multicapas o en monocapas.
CONCLUSIONES
1. Al determinar los parámetros característicos para el estudio del equilibrio en el sistema de adsorción de soluciones de sulfato de níquel y cobalto con carbón pirolizado de conchas de coco, se puede observar que la concentración de equilibrio y la capacidad de adsorción del carbón se incrementan con el aumento de la concentración inicial de la solución. También al analizar el efecto del pH sobre la capacidad de adsorción, los resultados sugieren que para pH 3 la capacidad de adsorción del níquel y cobalto fue la mejor.
2. La adsorción de los dos metales, bajo diferentes condiciones de pH, fue ajustada por el modelo de Freundlich. Esto sugiere que la recuperación ocurre por adsorción multicapas. En el caso del cobalto para pH 1,2 se adapta mejor el modelo de Langmuir, aunque la diferencia en la extensión de la adecuación entre los dos modelos no es significativa. Esto pudiera sugerir que la recuperación ocurre por adsorción multicapas y monocapas.
3. Los resultados experimentales demostraron que el carbón pirolizado de conchas de coco tiene amplias posibilidades de aplicación en la adsorción de iones níquel y cobalto de soluciones de sulfatos de estos metales, al obtenerse muy altos valores de % de recuperación, y soluciones resultantes con muy bajas concentraciones de iones metálicos.
]]>NOMENCLATURA
A: Indicador aproximado de la capacidad de adsorción (mg/g).
b: Intensidad de adsorción para el modelo de Langmuir (L/g).
Ce: Concentración del metal en el equilibrio (mg/L).
n:Constante empírica.
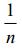 : Intensidad de adsorción para el modelo de Freundlich (L/g).
: Intensidad de adsorción para el modelo de Freundlich (L/g).
Qe:Capacidad de adsorción del adsorbente (mg/g).
Qm: Constante relacionada con el área ocupada por una capa uni-molecular de adsorbato (mg/g).
]]> BIBLIOGRAFIA
1. F. ALFONSO, E. BUGALLO. Memorias trabajos y resúmenes, jornada científica 40 aniversario del CIPIMM. 2007.
2. W. EMRICH. Handbook of Charcoal Making. 1985.
3. KAGANER. Evaluación comparativa del área superficial de materiales carbonosos. Colombia, 1993.
4. R. NICO. Estudio preliminar de adsorción de iones de níquel y cobalto utilizando carbón vegetal de conchas de coco. Trabajo de diploma. Universidad de Oriente. 2009.
5. MOLINA SABIO. Adsorbentes en la solución de algunos problemas ambientales. Ediciones CYTED, Alicante, 2004.
6. F. RODRIGUEZ REINOSO. Descontaminación ambiental mediante adsorbentes. Red Iberoamericana de adsorbentes para la protección ambiental, Ediciones CITECITED, Madrid, España. 2005.
7. DEEPATANA A., M. VALIX. "Recovery of nickel and cobalt from organic acid complexes: Adsorption mechanisms of metal-organic complexes onto aminophosphonate chelating resin". Journal of Hazardous Materials. Volume 137, Issue 2. 2006. Págs. 925-933.
Recibido: Abril 2012
Aprobado: Agosto 2012
]]>
MSc. Dolores Salas-Tort. Facultad de Ingeniería Química, Universidad de Oriente, Santiago de Cuba, Cuba. dsalas@fiq.uo.edu.cu
]]>