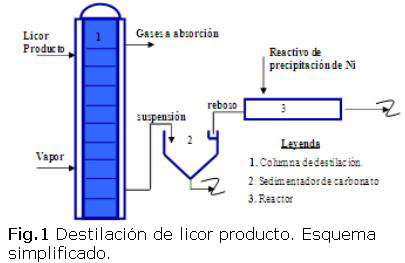
Rango de pH para destilar el licor de lixiviación carbonato amoniacal
PH range to distill the leaching liquor ammoniacal carbonate
Ing. María Elena Magaña-Haynes, MSc. Armando Rojas-Vargas
Centro de Investigaciones del Níquel, CEINNIQ, Moa, Holguín, Cuba. arojas@eros.moa.minbas.cu
]]>
RESUMEN
Se determinó el intervalo de pH para destilar el licor producto de la lixiviación carbonato amoniacal de mineral laterítico. El estudio se realizó en una torre de destilación industrial, operada mediante el Sistema de Supervisión y Control de Procesos Tecnológicos EROS. El rango de flujo de licor alimentado y de temperatura en el tope fue de 40 m3/h y 30 0C respectivamente. La concentración de amoníaco,dióxido de carbono, azufre y níquel en el licor alimentados fueron variables. Se determinó el pH de la suspensión para el cual disminuye el consumo de reactivo de precipitación de níquel y las pérdidas de amoníaco, recomendando un rango entre 8,10 < pH < 8,50 con un ahorro de 1,042 USD/(m3/h) y una pérdida propia del rango de 0,393 USD/(m3/h). Se demostró la posibilidad técnica de operar al rango de pH recomendado, al incrementando la distribución de los datos en norma de 28,9 % a 50 % en el período de estudio. A menor concentración de azufre en el licor, menor concentración de níquel y amoníaco disuelto, lo que reduce los gastos en la destilación.
Palabras clave: lixiviación carbonato amoniacal, destilación, pH, níquel.
ABSTRACT
The pH interval was determined to distill the product liquor coming from ammoniacal - ammonium carbonates leaching process of laterites mineral. An industrial distillation tower was used, operated by means of Supervisory Control and Data Acquisition EROS. The range of flow of fed liquor and of temperature at the top was of 40 m3/h and 30 0C respectively. The ammonia concentration was variable, as well as dioxide of carbon, sulfur and nickel of the fed liquor. The pH value of the suspension was determined for which diminishes the consumption of reagent of nickel precipitation and losses of ammonia, recommending a range among 8,10 < pH < 8,50, with a saving of 1,042 USD/(m3/h) and own loss of the range of 0,393 USD/(m3/h). The technical possibility of operating to the range of recommended pH was demonstrated, increasing the distribution of the data in norm from 28,9 % to 50 % in the period of study. To smaller concentration of sulfur in the liquor, smaller concentration of nickel and ammonia dissolve, reducing the expenses in the distillation.
Keywords: ammoniacal ammonium carbonate leaching, distillation, pH, nickel.
INTRODUCCIÓN
]]> Este trabajo posee campo de acción en el proceso de extracción de níquel y cobalto por la tecnología de lixiviación carbonato amoniacal (TCA) en el proceso de destilación. La operación sucede en las columnas de destilación (figura 1) al poner en contacto directo el vapor de agua con el licor producto procedente del proceso de lixiviación. Se obtienen producto, por el fondo, una suspensión carbonato de níquel-agua con níquel y amoníaco disueltos y por el tope, gases con contenido de amoníaco y dióxido de carbono, los cuales se recuperan por absorción. Posterior a la sedimentación de dicha suspensión, el níquel disuelto se precipita en un reactor tubular, mientras que el amoníaco disuelto se pierde en el agua residual.La forma de operar las columnas de destilación de licor producto es garantizando la norma de concentración de amoníaco en el anillo controlante de la columna debido a su elevada correlación con el amoniaco en la descarga. Dicha norma depende de la concentración de azufre disuelto, cuyas determinaciones analíticas para el control oportuno de la operación, encarecen el proceso; al modificar el número de anillos, se requiere evaluar la columna y determinar nuevamente su anillo controlante.
Estudios desarrollados en una minicolumna de destilación y en columnas industriales, reflejaron la relación entre el pH de la suspensión y la concentración de níquel y amoníaco disueltos, indicaron los valores en los que se produce una sobredestilación o redisolución de níquel, incrementando los costos por consumo de vapor y de reactivo de precipitación, o en caso contrario, subdestilación incrementando las pérdidas de amoníaco y también de níquel. Los autores recomiendan operar en un rango de pH entre 8,1 a 8,3 [1-3].
El licor destilado posee en disolución amoníaco, dióxido de carbono, azufre, de ahí su interacción con el pH. Al ponerse en contacto el amoníaco y el dióxido de azufre con el agua suceden las reacciones (1), (3) y (5), si el pH es inferior a 4, la formación de sulfito es baja. Para soluciones diluidas, a 25 0C, Kb = 1,74 10-5; Kc1= 1,45 10-2; Kc2= 7,08 10-8 [4-6]

El dióxido de azufre reacciona con el amoníaco por las reacciones (7 y 8), poseyendo valores de contante de equilibrio K1= 3,1 107; K2= 1,1 102 respectivamente [7].
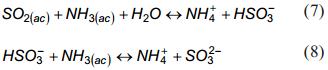
Cuando incrementa la concentración de azufre en el licor producto alimentado a la destilación, incrementa la concentración del níquel disuelto en la pulpa destilada. Se conoce la existencia de dos tipos básicos de carbonato de níquel 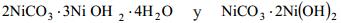 , pudiéndose explicar su redisolución, en dependencia del pH de la suspensión, por las ecuaciones (9 y 10) [8].
, pudiéndose explicar su redisolución, en dependencia del pH de la suspensión, por las ecuaciones (9 y 10) [8].
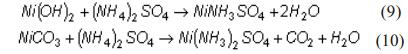
Para los flujos, composición iónica del licor y condiciones de la instalación industrial ¿Será posible lograr una operación estable en los rangos de pH recomendados entre 8,1 a 8,3?
El objetivo fundamental del trabajo fue evaluar el rango de pH para destilar el licor resultado de la lixiviación de carbonato amoniacal; también se plantearon como objetivos específicos: comparar las acciones correctivas derivadas del control por pH y por análisis de amoníaco en el anillo controlante, intercambiar con técnicos y operarios para conocer su apreciación sobre el comportamiento del sistema y realizar ajustes en el método propuesto.
MATERIALES Y MÉTODOS
El trabajó se realizó en una empresa productora de niquelífera del grupo empresarial CUBANÍQUEL, Holguín, Cuba, en cinco columnas de destilación, en dos períodos:
1 Muestreo y análisis de licores: Se tomaron muestras para caracterizar el licor de alimentación, en la descarga y el anillo controlante.
2 Operación conjunta de los técnicos del Centro de Investigaciones del Níquel, Holguín, Cuba y del área de destilación de la industria.
Las columnas poseen las siguientes especificaciones: altura total, 18,0 m; diámetro interior, 3,40 m; número de platos de copa de burbujeo 18; copas por anillos: 24.
Para el control de la operación se utiliza el sistema de supervisión y control (SCADA) de procesos tecnológicos EROS, el cual permite accionar sobre el proceso desde un panel de control.
]]> Durante el periodo de evaluación, se tomaron muestras en el licor de alimentación, la descarga y el anillo controlante para determinar las concentraciones de: amoníaco, dióxido de carbono, níquel, cobalto, azufre, sulfato, tiosulfato y además, se midió el pH de la suspensión a 25 0C, para un total de 195 muestras.En el análisis químico se empleó un equipo de Absorción Atómica SP-9, métodos volumétricos y gravimétricos, y para la medición del pH, un pHmetro de modelo Philips PW-9420.
El análisis de los datos y el cálculo de los gastos por consumo de reactivo de precipitación de níquel y pérdidas de amoníaco, se aplicaron los procedimientos descritos por Rojas, 2012 [3].
Se construyó una carta de operación a partir de datos previos como se refleja en la figura 2, se le explicó la esencia del control de la operación a los técnicos del área y las acciones correctivas necesarias.
Consiste en muestrear 100 ml de suspensión, enfriar hasta 25 0C, medir el pH y comparar el valor real con el normado (8,0 < pH < 8,4) y tomar acciones correctivas, como se indican en la figura 2.
Se midió el pH de la pulpa de descarga y determinó la concentración de amoníaco en el anillo controlante. Se analizaron los resultados según la figura 2 y la norma, y se compararon las acciones correctivas derivadas de ambos métodos.
RESULTADOS Y DISCUSIÓN
El licor producto alimentado a la destilación poseyó una relación r-NH3/CO2=1,68 +/- 0,1 y r-Ni/S=1,47 +/- 0,24 (promedio +/- desviación estándar). Las columnas de destilación industrial operaron en un rango de flujo de licor alimentado y de temperatura en el tope de 40 m3/h y 30 0C respectivamente. Estos datos se generaron del SCADA EROS.
]]> Se corroboraron los resultados obtenidos de interacción entre pH y concentración de Ni y NH3 en la descarga de las columnas de destilación, como se muestra en la figura 3. De esta forma el pH puede sustituir el método de control de la operación por determinación analítica de la concentración de amoníaco en el anillo controlante [1-3].
Se calculó el gasto para los nuevos datos analizados y se ilustran en la figura 4. En la tabla se muestran las especificaciones de los grupos de muestras estudiados.
Puede observarse en la figura 4, la incidencia que ejerce sobre el gasto, el incremento de la concentración de azufre en el licor. A menor concentración de azufre en el licor, menor la concentración de níquel y amoníaco disuelto, en acuerdo con lo expuesto por Rojas, 2012 [3].
Se propuso un nuevo rango de operación de pH entre 8,1 a 8,5, de acuerdo con la nueva composición iónica obtenida en el licor producto y se calcularon los gastos. Este rango de pH representa un ahorro de 1,042 USD/(m3/h) de licor producto procesado y un gasto propio del rango de 0,393 USD/(m3/h).
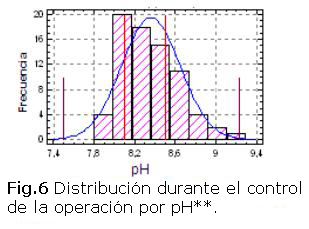
En las figuras 5 y 6 se muestra la comparación del pH de la suspensión antes de iniciar el control de la operación por pH y durante el período que se aplicó como criterio de decisión, conjuntamente con el análisis del amoníaco en el anillo controlante. Hasta la fecha de ejecución, se logró reducir la operación fuera de los límites recomendados de pH (8,1 < pH < 8,5) de un 71,1 % a un 49,8 %, incrementando la distribución de los datos en norma, lo que confirma la posibilidad de ajustar la operación al rango recomendado. Las acciones correctivas reflejadas en la figura 2 fueron las apropiadas en correspondencia con el análisis del amoníaco en el anillo controlante.
]]>
*71,06 % de la distribución ajustada se encuentra fuera de los límites de especificación.
**49,85 % de la distribución ajustada se encuentra fuera de los límites de especificación.
CONCLUSIONES
En la ejecución de este trabajo se verificó la factibilidad técnica económica del control de la operación de destilación por pH y se concluyó que:
1 El rango de pH propuesto para el control de la operación es entre 8,1 y 8,5 para disminuir los gastos de operación por pérdidas de amoníaco y consumo de reactivo de precipitación de níquel.
2 El control por pH permite un ahorro de 1,042 USD/(m3/h) de licor producto procesado.
3 Las acciones correctivas derivadas del control por pH fueron efectivas y se validaron con la determinación del amoníaco en el anillo controlante.
4 Se obtuvo que a menor concentración de azufre en el licor, menor la concentración de níquel y amoníaco disuelto, reduciendo los gastos en la destilación.
]]>BIBLIOGRAFÍA
1. ROJAS, V. A., TRUJILLO, M.E. "Medición del pH durante la destilación del licor producto del proceso de lixiviación amoniacal". Tecnología Química, vol. XXVII No. 1. Págs. 34-40. 2007.
2. ROJAS, V. A., TRUJILLO, M.E. "Medición del pH durante la destilación del licor producto del proceso de lixiviación amoniacal (II)". Tecnología Química. vol. XXVII, No. 3. Págs. 56-60. 2007.
3.ROJAS, V. A., TRUJILLO, M.E. "Medición del pH durante la destilación del licor producto del proceso CARON. PARTE (III)". Tecnología Química, vol. XXXII, No. 2. 2012.
4. XIA, J., RUMPF, B., MAURER, G. "Solubility of sulfur dioxide in aqueous solutions of acetic acid, sodium acetate, and ammonium acetate in the temperature range from 313 to 393 K at pressures up to 3 3 MPa: Experimental results and comparison with correlations/predictions". Industrial and Engineering Chemistry Research. vol. 38 No. 3. Págs. 1149-1158. 2009.
]]>5. GOLDBERG, R.N. Y PARKER, V.B.: "Thermodynamics of Solution of SO2 (g) in Water and Aqueous Sulfur Dioxide Solutions", J. Res. National Bureau of Standards vol. 90 No. 5. Pág. 341. 1985.
6. HIKITA, HARUO; ASAI, SATORU; TSUJI, TADASHI. "Absorption of Sulfur Dioxide into Aqueous Ammonia and Ammonium Sulfite Solutions". Engineering and natural sciences. vol. 26 No. 2. Págs. 89-97. 1978.
7. F. MANI, M. PERUZZINI, P. STOPPIONI. CO2 absorption by aqueous NH3 solutions: speciation of ammonium carbamate, bicarbonate and carbonate by a C NMR study. Green Chem. vol.8. Págs. 995-1000. 2006.
8. KAZUYOSHI SHIMAKAGE, MASAYOSHI HOSHI, TATSUHICO EJIMA. Kinetics and Mechanism of the Ammonia Pressure Leaching of Lateritic Ore Containig Nickel.
]]> Recibido: Mayo de 2013
Ing. María Elena Magaña-Haynes. Centro de Investigaciones del Níquel, CEINNIQ, Moa, Holguín, Cuba. arojas@eros.moa.minbas.cu
]]>