Adsorción de níquel y cobalto sobre carbón activado de cascarón de coco
Nickel and cobalt adsorption on activated coal of coconut shell
Dr. Margarita Penedo Medina, Msc. Enma Michel Manals Cutiño, Msc. Frank Vendrell Calzadilla, Msc. Dolores Salas Tort
Facultad de Ingeniería Química, Universidad de Oriente. mpenedom@gmail.com
]]>
RESUMEN
El presente estudio explora la capacidad del carbón activado de cáscara de coco para la extracción de níquel (II) y cobalto (II), bajo diferentes condiciones experimentales desde soluciones modeladas de sulfatos. Los experimentos se realizaron con el objetivo de obtener la capacidad de adsorción y el porcentaje de adsorción, aplicando un diseño factorial 23, considerando como efectos principales la concentración inicial de la solución, pH y dosis de adsorbente. La capacidad de adsorción de Co(II) alcanzó valores entre 0.70 y 9.94 mg/g; para Ni(II) alcanzó valores entre 2.62 y 98.21mg/g. La concentración inicial de la solución y dosis de adsorbente tuvieron influencia significativa en la capacidad de adsorción. El pH ejerció una influencia significativa en el porcentaje de adsorción. La capacidad de adsorción se favoreció en el nivel superior de concentración inicial y nivel inferior de dosis de adsorbente, a pH 5; siendo el porcentaje de adsorción elevado (99.6% de cobalto y 98.21% de níquel). Se obtuvieron las isotermas de adsorción a pH 1.2, 3 y 5; las isotermas de adsorción de Co(II) tuvieron un buen ajuste al modelo de Langmuir, siendo la capacidad máxima de adsorción de entre 33.33 y 71.43mg/g;la adsorción resultó muy favorable con alta afinidad adsorbato - adsorbente. Las isotermas de adsorción de Ni(II) tuvieron mejor ajuste al modelo de Freundlich, observándose una adsorciónfavorable, con capacidad de adsorción máxima de 15,86 y 17,60 mg/g a pH 3 y 5.
Palabras claves: adsorción, carbón activado, níquel, cobalto, isotermas de adsorción.
ABSTRACT
The present study explores the ability of activated carbon of coconut shell for the removal of nickel(II) and cobalt(II)under different experimental conditions from modeled sulfate solutions.Experiments were carried out in order to obtain the adsorption capacity and the adsorption rate. It was developed for 23 factorial design, considering as main effect initial concentration of solution, pH and dose of adsorbent. The adsorption capacity of Co (II) reached values between 0.70 and 9.94 mg/g; Ni (II) reached values between 2.62 and 98,21mg/g. The initial concentration of the solution and the dose of adsorbent had significant influence on the adsorption capacity. The pH exerted a significant influence in the percentage of adsorption.The adsorption capacity was favored at higher initial concentration level and lower level of dose of adsorbent, at pH 5; the adsorption percentage was high (99.6% cobalt and 98.21% nickel). Adsorption isotherms were obtained at pH 1.2, 3 and 5; adsorption isotherms of Co(II) had a good fit to the Langmuir model, the maximum adsorption capacity of between 33.33 and 71.43 mg/g; adsorption was very favorably with high affinity adsorbate - adsorbent. Adsorption isotherms of Ni(II) had better fit to the Freundlich model, showing a favorable adsorption, with maximum adsorption capacity of 15.86 and 17.60 mg/g at pH 3 and 5.
Keywords: adsorption, activated carbon, nickel, cobalt, adsorption isotherms.
INTRODUCCIÓN
]]> El tratamiento de residuales y la recuperación de sustancias a partir de efluentes son de mucho interés por los problemas ambientales y pérdida de sustancias valiosas que tienen lugar. En este contexto se enmarcan los residuales líquidos vertidos en suelos, mares y ríos, los cuales causan problemas de contaminación, ya sea por el contenido de metales pesados, hidrocarburos, ácidos, bases, sólidos en suspensión, microorganismos y otras sustancias presentes. Para eliminar o recuperar metales contenidos en residuales líquidos se aplican procesos de precipitación, coagulación/floculación, intercambio iónico, adsorción, extracción por solventes, cementación, procesos electroquímicos y biológicos, evaporación, filtración y procesos de membranas [3, 5, 18, 19].La adsorción y el intercambio iónico se desarrollan utilizando carbón activado, zeolitas y resinas de intercambio. Estos procesos tienen como desventaja el alto precio de algunos materiales adsorbentes y resinas, lo cual explica la diversidad de estudios relacionados con la evaluación de materiales naturales y sintéticos, que resulten baratos y efectivos para estos fines [2, 3, 5, 9, 12, 15, 17, 20, 21].En la metalurgia extractiva se ha intensificado la aplicación del carbón activado como adsorbente, empleándose en la purificación de electrólitos, recuperación de metales disueltos, como modificador del potencial REDOX, entre otros. Se puede citar su aplicación en la recuperación de oro y plata, cromo, níquel y cobalto, plomo, entre otros metales pesados [7, 25].
En Cuba, las industrias niquelíferas ubicadas en Moa y Nicaro generan residuales líquidos conteniendo metales pesados. Entre ellos se puede citar el licor de desecho de la Planta de Precipitación de Sulfuros de la Empresa niquelífera "Pedro Sotto Alba", de Moa, caracterizado por su alta acidez y la presencia de metales como aluminio, manganeso, cromo, hierro, níquel, cobalto, cobre, entre otros [18, 19]. El tratamiento de este residual líquido y otros provenientes de la industria niquelífera, aplicando adsorción con carbón activado se presenta como una alternativa, de acuerdo con los resultados reportados en diversas publicaciones científicas relativos a la adsorción de metales disueltos en líquidos.
El carbón activado es un adsorbente poroso, capaz de remover especies metálicas tóxicas; se caracteriza por parámetros físicos y químicos como área superficial, grupos funcionales, volumen de poro, capacidad de adsorción y pH [14].En Cuba se produce industrialmente carbón activado en la fábrica de Carbón Activado de Baracoa, provincia de Guantánamo, utilizando como materia prima la concha de coco o carbón vegetal obtenido por carbonización de diferentes especies forestales. El carbón activado elaborado a partir del coco es de muy buena calidad por su elevada porosidad y área superficial, bajo contenido de ceniza y el alto índice de yodo [11].Investigaciones recientes demuestran la aplicación de métodos químicos y físicos en procesos de activación para la obtención de carbones de muy alta calidad a partir de diversos materiales [6, 11, 13, 24].
El propósito principal de este trabajo fue determinar la capacidad de adsorción del carbón activado obtenido a partir de la concha de coco para separar níquel y cobalto, por contacto con soluciones modeladas de sulfatos metálicos; analizar la influencia de factores tales como pH y concentración de las soluciones de partida en la capacidad de adsorción y el porcentaje de adsorción; obtener las isotermas de adsorción y a partir de las mismas ajustaRLos modelos de Langmuir, Freundlich y Temkin.
MATERIALES Y MÉTODOS
Materiales
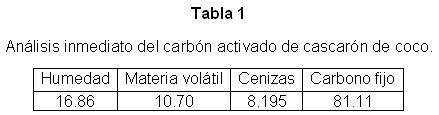
Carbón activado. El carbón activado granular (CAG) utilizado en el estudio de adsorción, fue suministrado por la Planta de Carbón Activado de Baracoa, provincia de Guantánamo. El mismo se produce por carbonización y activación posterior de cascarón de coco; los resultados del análisis inmediato del carbón activado se muestran en la tabla 1, y fue realizado de acuerdo con las normas ASTM. El diámetro promedio de partícula del CAG fue de 0.45 mm.
]]> Preparación de las soluciones de sulfato de níquel y de sulfato de cobaltoLas soluciones de sulfato de níquel y de sulfato de cobalto se prepararon disolviendo 0.05 g, 0.15 g, 0.25 g, 0.4 g y 0.5 g de NiSO4 o de CoSO4 en 500mL de agua destilada, obteniéndose soluciones con concentraciones iniciales de 100, 300, 500, 800 y 1000 mg/L (Ci).La concentración inicial de la solución de sulfato metálico se fijó teniendo en consideración la concentración del licor de desecho de la lixiviación ácida a presión (WL) [18,19].
Experimentos de adsorción batch. Diseño de experimentos
Para conocer el efecto de determinados factores en la capacidad del CAG como adsorbente de Ni (II) y Co(II), se desarrollaron los experimentos por un diseño factorial 23 con tres puntos centrales. Los factores considerados fueron: masa de carbón, concentración inicial de la solución y pH. Las variables respuesta fueron capacidad de adsorción y porcentaje de remoción de iones metálicos en la solución. Los experimentos se realizaron en reactores con agitación magnética, manteniendo fija la velocidad de agitación en 200 rpm. El tiempo de agitación fue de 6 horas, suficiente para alcanzar condiciones de equilibrio; la temperatura fue de21 ºC. El nivel de los factores considerados se muestra en la tabla 2.
La metodología experimental consistió en adicionar una masa determinada de CAG en un beaker de 250 mL y 50 mL de solución de sulfato metálico, denominándose la relación masa de CAG/volumen de solución dosis de adsorbente; a la solución de sulfato metálico se le ajustó el pH con soluciones de ácido sulfúrico y de hidróxido de amonio. Cada experimento se desarrolló con una solución de concentración inicial Ci. Al finalizar cada experimento se procedió a filtrar la suspensión. El líquido filtrado fue analizado utilizando un Espectrofotómetro de Absorción Atómica (EAA), Modelo CaRL Zeiss 5FL, obteniéndose el valor de la concentración de equilibrio, Ce. La capacidad de adsorción del ión metálico en disolución se determinó para cada valor de concentración inicial, con los datos experimentales de concentración de equilibrio y concentración inicial, utilizando la ecuación siguiente:
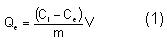
donde:
Qe es la capacidad de adsorción (mg/g);
Ci es la concentración inicial de soluto (adsorbato) en la solución (mg/L); ]]>
Ce es la concentración de soluto en el de equilibrio (mg/L); V el volumen de solución (L) y m la masa de adsorbente (g).
La eficiencia o porcentaje de absorción de ión metálico (Ra) se determinó por:
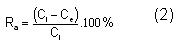
Isotermas de adsorción
La isoterma de adsorción es la relación de equilibrio entre las concentraciones que se alcanzan en la fase fluida y en las partículas de adsorbente, a una temperatura determinada. En la adsorción de un soluto (adsorbato) contenido en un líquido, la concentración del soluto en la fase líquida se expresa habitualmente en unidades de masa (partes por millón, mg de soluto/L) o en unidades molares (mmol/L). La concentración de soluto en el sólido se expresa como masa adsorbida de soluto por unidad de masa de adsorbente (mg de soluto/g de adsorbente) o moles adsorbidos por unidad de masa de adsorbente (mmol de soluto/g de adsorbente). Para obtener las isotermas de adsorción en este trabajo, se realizaron experimentos batch a concentraciones iniciales entre 100 y 1000 mg/L. Las condiciones experimentales fueron: velocidad de agitación 200 rpm, tiempo de contacto 6 horas y 21ºC de temperatura. La dosis de adsorbente en todos los casos fue de 1 g de adsorbente en 50 mL de solución (20 g de CAG/L).
Para evaluar las características del equilibrio de adsorción de Ni(II) y Co(II) los datos experimentales fueron ajustados a tres modelos de isotermas de adsorción: modelo de Langmuir, de Freundlich y Temkin [1, 16, 23].La evaluación de los parámetros de los modelos permite interpretar aspectos tales como mecanismo de adsorción, propiedades de la superficie y afinidad entre adsorbato y adsorbente.
Modelo de Langmuir
La isoterma de Langmuir se basa en la presunción de que todos los puntos de adsorción en un adsorbente estructuralmente homogéneo son idénticos y energéticamente equivalentes. La adsorción se realiza en una capa monomolecular sin interacciones laterales entre moléculas de adsorbato sobre una superficie energéticamente homogénea. El modelo de Langmuir está representando por la ecuación (3):
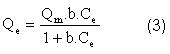
donde:
]]> b:constante de afinidad (L/mg),La forma lineal de la ecuación (3) es:
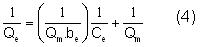
Gráficamente, 1/Qe vs 1/Ce da lugar a una línea recta si los datos de adsorción se adaptan al modelo Langmuir, siendo Qm y b la pendiente y el intercepto. La capacidad de adsorción máxima, Qm, es una constante relacionada con el área ocupada por una capa mono molecular de adsorbato. La constante de afinidad (b) es una medida directa de la intensidad de adsorción. Conocida la constante de afinidad se determina el parámetro de equilibrio o factor de separación, RL(ecuación 5) [2, 12]: ver ecuación
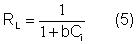
donde:
Ci es la mayor de las concentraciones iniciales del ión metálico de las consideradas en el estudio del equilibrio. El valor del parámetro de equilibrio indica el tipo de isoterma de adsorción, ya sea favorable (0 < RL < 1), lineal (RL=1), desfavorable (RL > 1) o irreversible (RL=0) [15, 21].
Modelo de Freundlich
Esta ecuación es empírica y se aplica en el equilibrio de adsorción de gases sobre sólidos y en la adsorción de sustancias en disolución sobre adsorbentes sólidos. La isoterma de Freundlich describe la adsorción sobre una superficie energéticamente heterogénea; en el modelo propuesto aparecen constantes que relacionan la capacidad de adsorción multicapas y la intensidad de la adsorción. Una de las expresiones más utilizadas para la ecuación de Freundlich es la siguiente:
]]>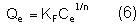
donde:
Kf y 1/n son constantes empíricas, parámetros de la isoterma de Freundlich. La constante Kf (mg/g),es un indicador aproximado de la capacidad de adsorción. La magnitud 1/n es una medida de la intensidad de adsorción, directamente asociada a la eficiencia de la adsorción, denominado también factor de heterogeneidad [2, 20]; valores de 0 < 1/n < 1 indican una adsorción favorable [16].
Modelo de Temkin
Este modelo contiene un factor que toma en cuenta de forma explícita las interacciones adsorbente - adsorbato. La isoterma de Temkin puede obtenerse en base a la isoterma de Langmuir, suponiendo que el calor de adsorción disminuye linealmente al aumentar la capacidad de adsorción [16, 22]. El resultado es:
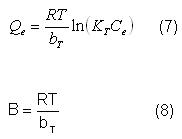
donde:
KT es la constante de la isoterma de Temkin (L/mg); bT, constante relacionada con el calor de adsorción; T, temperatura absoluta (K); R la constante universal de los gases (8,314 J/mol. K) y B la constante relacionada con el calor de adsorción (J/mol).
RESULTADOS Y DISCUSIÓN
]]> Influencia del pH, concentración inicial de la solución y masa de adsorbente, en la capacidad de adsorción y porcentaje de adsorción de Ni (II) y Co (II)En las tablas 3 y 4 se muestran los resultados de concentración en el equilibrio (Ce), capacidad de adsorción (Qe), calculada por la ecuación (1), y el porcentaje de adsorción o recuperación (Ra) calculado por la ecuación (2), obtenidos en los experimentos de adsorción batch (diseño experimental 23). Estos resultados fueron procesados estadísticamente, aplicando el Programa profesional STATGRAPHICS Plus 5.1. El nivel de confianza establecido fue de 95 %.
En los resultados de adsorción de cobalto (tabla 3) se puede apreciar que la concentración final alcanzada siempre fue mucho menor que la inicial, como resultado de la acción adsorbente del CAG. En las condiciones de los experimentos 6 y 8 (nivel superior de pH y de dosis de adsorbente) se alcanzaron las menores concentraciones de equilibrio y una alta recuperación de Co(II) (99.2% y 99.95 %), mientras que la capacidad de adsorción fue inferior a la obtenida en los experimentos 3 y 4, desarrollados en el nivel superior de concentración inicial y nivel inferior de dosis de adsorbente; en estos últimos se obtuvieron capacidades de adsorción de 9.77 y 9.94 mg de Co/g de CAG respectivamente, con elevado porcentaje de recuperación.
En los experimentos 3 y 4 el incremento de la concentración inicial dio lugar a una mayor capacidad de adsorción que en los experimentos 1 y 2 con la misma dosis de carbón. En los experimentos 7 y 8 también la capacidad de adsorción fue superior a los experimentos 5 y 6, debido al incremento de la concentración inicial.
Los resultados del análisis estadístico del diseño experimental correspondiente a la adsorción de cobalto se muestranen la figura 1 (diagramas de Pareto) para la capacidad de adsorción y porcentaje de adsorción. De igual forma fue obtenido el modelo de regresión para cada variable respuesta (ecuación 9-10).
En la variable respuesta capacidad de adsorción de Co (II)influyeron significativamente la concentración inicial, la dosis de adsorbente y la interacción de estos dos factores (fig.1a). El pH no tuvo efecto significativo. El incremento de la concentración inicial provocó un aumento de la capacidad de adsorción, mientras que el incremento de la dosis de adsorbente provocó una disminución de la capacidad de adsorción (ecuación 9); el modelo de regresión tuvo un coeficiente de correlación elevado (r2= 98.88 %). Las condiciones más favorables para esta variable respuesta fueron nivel superior de pH, nivel superior de concentración y nivel inferior de dosis de adsorbente.
QeCo= 3.24636 + 0.17625A + 2.90625B - 1.87875C + 0.10125AB+ 0.08125AC - 1.61875BC (9)
El pH tuvo una influencia significativa en el porcentaje de adsorción (fig.1b); el incremento del pH y de la concentración inicial provocaron un incremento de esta variable respuesta (ecuación 10), mientras que el incremento de la dosis de adsorbente provocó una disminución del porcentaje de adsorción, pero su influencia no fue significativa. Las condiciones más favorables para la mayor recuperación de Co (II) fueron nivel superior de pH y nivel superior de concentración. El modelo de regresión para el porcentaje de recuperación (ecuación 10) tuvo un r2 = 81.8279 %.
RaCo= 90.3564 + 9.9138A + 4.7663B - 2.0113C - 2.3538AB + 4.2238AC - 4.4338BC (10)
Los resultados correspondientes a la adsorción de Ni(II) (tabla 4) muestran que se logró reducir apreciablemente la concentración en la solución desde sus valores iniciales. La menor concentración de equilibrio (0.0001g/L) se alcanzó en las condiciones del experimento 6, a nivel superior de pH y dosis de carbón, y nivel inferior de concentración inicial. Los mayores porcentajes de adsorción se alcanzaron en los experimentos 6 y 8, siendo de 99.9 % y 98.92 %. En los experimentos 3 y 4 la capacidad de adsorción de Ni(II) fue elevada, de 97.91 y 98.21 mg de Ni(II)/g de CAG) respectivamente. La adsorción a partir de soluciones de sulfato de níquel permitió alcanzar capacidades de adsorción superiores a las obtenidas a partir de soluciones de sulfato de cobalto, por ser preparadas a concentraciones iniciales superiores. En la variable respuesta capacidad de adsorción de Ni (II) influyeron significativamente los factores concentración inicial y dosis de adsorbente así como la interacción de estos (figura 2). El pH no tuvo efecto significativo.
]]> De acuerdo al modelo estadístico para Qe (ecuación 11), el incremento de la concentración inicial provocó un aumento de la capacidad de adsorción, mientras que el incremento de la dosis de CAG provocó una disminución. El coeficiente de correlación para el modelo fue alto (r2=98.54%), muy cercano al valor de r2 (ajustado para g.l.) = 96.35%, mostrando un buen ajuste.QeNi = 33.2055 + 0.4613A + 29.8263B- 17.7162C - 0.2938AB- 0.1913AC- 14.9213BC (11)
En el porcentaje de recuperación de Ni(II)tuvieron un efecto muy significativo el pH y la concentración inicial, así como la interacción entre estos dos factores(fig. 2b).El incremento del pH y de la concentración inicial dio lugar al incremento del porcentaje de adsorción, el aumento de la dosis de CAG provocó también un aumento de esta variable respuesta pero su efecto no fue significativo. El modelo estadístico para porcentaje de adsorción (ecuación 12) tuvo un coeficiente de correlación r2=92.22%.
Ra Ni = 94.1045 + 5.7388A + 5.4038B + 0.9738C - 5.3863AB- 0.1113AC - 0.8213BC
Al comparar los resultados de los efectos de los factores en las variables respuesta, tanto para la adsorción de Ni(II) como de Co(II), se observó que el comportamiento fue muy similar, resultando significativas la influencia de los mismos factores. Las condiciones más favorables para alcanzar mayor capacidad de adsorción y porcentaje de adsorción, a las condiciones experimentales fijadas, resultaron el nivel superior de pH, nivel superior de concentración y nivel inferior de dosis de adsorbente.
La capacidad de adsorción del CAG de conchas de coco y el porcentaje de adsorción obtenidos en este trabajo, son comparables con resultados reportados en la literatura sobre adsorción de Ni(II) y Co(II) con carbón activado u otros materiales adsorbentes. Así, se pueden mencionar los resultados de adsorción de Ni(II) sobre carbón activado preparado a partir de cáscara de almendra, reportados por [8], donde la capacidad de adsorción tuvo valores entre 0.616 y 4.89 mg/g, y la remoción de níquel fue de hasta 97.8 %; se comprobó además que tenía lugar una disminución de la capacidad de adsorción con el aumento de la dosis de adsorbente y un pH óptimo de 5, al igual que en el presente trabajo, a las condiciones experimentales fijadas.
En la adsorción de iones de Ni (II) con carbón activado obtenido a partir de residuos de albaricoque reportado en se obtuvieron valores de capacidad de adsorción entre 17.04 y 101.01mg/L, a partir de soluciones con 10 mg Ni(II)/L como concentración inicial, siendo el pH óptimo de 5.
Por otra parte en [12] se reportan resultados de adsorción de Ni(II) sobre bagacillo, siendo las capacidades de adsorción de hasta 15.76 mg/g de adsorbente a pH óptimo también de 5.
Con relación a los resultados reportados sobre adsorción de Co(II), se tienen los resultados presentados en[4] para la adsorción con carbón activado obtenido a partir de cáscaras de avellana, con valores de capacidad de adsorción de hasta 6 mg/g de adsorbente y concentración de equilibrio de 200 mg/L, a pH 6 y 25 ºC. En la adsorción de Co(II) con carbón activado a partir de bagazo[10] informa valores de capacidad de adsorción entre 22.58 mg/g y 40.5 mg/g, desde soluciones a concentración inicial entre 50 y 100 mg/L, siendo la temperatura 30ºC y los pH más favorables entre 6 y 8. En [12] se reporta la aplicación directa de bagacillo como material adsorbente, en la adsorción de Co(II) con valores de capacidad de adsorción de hasta 12.41 mg/g de adsorbente a pH 4.3.
Isotermas de adsorción
]]> Como resultado de los experimentos de equilibrio de adsorción de Ni(II) y Co(II) con carbón activado de conchas de coco, fue obtenida la concentración en el equilibrio, Ce, correspondientes a cada concentración inicial Ci (figura 3); así como los valores de capacidad de adsorción en el equilibrio, Qe; a tres condiciones de pH: 1.2; 3 y 5. En la figura 4 se muestran las isotermas de adsorción de níquel y cobalto. Los valores menores de concentración en el equilibrio, tanto de níquel como de cobalto, se obtuvieron a pH 3 (figura 3), y en correspondencia con ello, a este mismo pH, se alcanzaron los mayores valores de capacidad de adsorción. En la fig.4 se observa que tanto para la adsorción de Ni(II) como de Co(II) la capacidad de adsorción se incrementó continuamente con el aumento de la concentración de equilibrio, sin llegar a formarse una meseta, por ello se puede plantear que no se alcanzó la saturación del sólido con los iones de metal adsorbidos.Con los resultados experimentales de equilibrio se determinaron los parámetros de los modelos de Langmuir, Freundlich y Temkin, aplicando el programa profesional EXCEL y las ecuaciones (3-7). En las tablas 5 y 7 se muestran los parámetros correspondientes a cada modelo y el coeficiente de correlación.
Los resultados de equilibrio en la adsorción de Co(II) muestran que se obtuvo buen ajuste con el modelo de Freundlich, con valores de r2 entre 0.9028 y 0.9124 (tabla 5). De acuerdo con este modelo, para el cobalto se alcanzaron valores de 0 < 1/n < 1, en los tres niveles de pH, indicando que la adsorción de Co(II) sobre CAG fue favorable. Aplicando el modelo de Langmuir, se obtuvieron coeficientes de correlación entre 0.925 y 0.973, superiores a los obtenidos por el modelo de Freundlich. Con el modelo de isoterma de Temkin se obtuvieron valores del coeficiente de correlación menores. Haciendo un análisis de estos resultados, se puede plantear que los datos de las isotermas de adsorción de Co(II) se describen mejor por el modelo de Langmuir en el rango de concentración estudiado. La forma de las isotermas obtenidas para la adsorción de Co(II) se compararon con las que aparecen reportadas para la adsorción en sistemas sólido-liquido [16]. Las mismas son cóncavas con respecto al eje de concentración a bajos valores de Ce, siendo los valores de b*Ce mucho mayores que uno (tabla 6).
La evaluación de la constante de afinidad del modelo de Langmuir (b) permitió determinar el parámetro de equilibrio de Langmuir o factor de separación (RL) por la ecuación 5. En la tabla 6 se muestran los resultados del cálculo de RL considerando como concentración inicial para el cálculo la mayor de todas las concentraciones con que se obtuvieron las isotermas de adsorción (1000 mg/L). Los valores obtenidos de RL se encuentran entre cero y uno, demostrando alta afinidad entre adsorbato-adsorbente. En el cálculo del factor de separación los valores mayores de b dieron lugar a factores de separación mucho menor de la unidad, lo cual favorece la adsorción. En la tabla 5 se observa que son altos los valores de capacidad de adsorción máxima monocapa (Qm) del modelo de la isoterma de Langmuir, y que siguen el orden:![]() . El resultado de mejor ajuste del modelo de Langmuir a los datos de equilibrio de adsorción de Co(II) indica que ocurre un proceso de adsorción física.
. El resultado de mejor ajuste del modelo de Langmuir a los datos de equilibrio de adsorción de Co(II) indica que ocurre un proceso de adsorción física.
Los parámetros resultantes de la evaluación de los modelos de Langmuir y Freundlich se compararon con los reportados para adsorción de Co(II) con otros tipos de carbón activado. Así, en [10] se reportan las constantes del modelo de Langmuir, en la adsorción con carbón activado a partir de bagacillo, siendo Qm = 153.85 mg/g, y b=0.0184, a pH 6, concentración inicial entre 50 y 1000 mg/L y 4 horas de contacto. Las constantes del modelo de Freundlich resultaron las siguientes: KF = 21.90mg/g y 1/n = 0.289.
En el caso de las isotermas obtenidas en la adsorción de Ni (II), los resultados del ajuste de los datos experimentales mostraron que para el modelo de Langmuir se obtuvieron valores negativos de la capacidad máxima de adsorción y de la constante de afinidad en los resultados correspondientes a pH 1.2 y 3, lo cual carece de significado físico; por lo que este modelo no se acepta (tabla 7). Para pH 5 se obtuvo muy poco ajuste con el modelo de Langmuir (r2 = 0.629). De acuerdo con los resultados del modelo de Freundlich, la intensidad de la adsorción se puede considerar favorable para pH 3 y pH 5, siendo los valores de 0 < 1/n < 1 (0.5718 y 0.435 respectivamente); la capacidad de adsorción dada por el coeficiente empírico KF fue de 15.86 y 17.60 mg/g, superiores al valor alcanzado a pH 1.2. Los valores de KF obtenidos para adsorción de Ni(II) son comparables con los reportados en [4] donde KF=7.073 mg de Ni(II)/g de carbón activado de cáscara de avellanas, a pH 5. En [8] se reporta KF = 4.20 mg de Ni(II)/g de carbón activado a partir de cáscara de almendras, y adsorción favorable (1/n = 0.467). Con el modelo de Temkin se obtuvo un mejor ajuste solo para pH 3, siendo los valores de las constantes semejantes a los reportados en otros trabajos de adsorción de Ni(II) en carbón activado[15].
]]> CONCLUSIONES
Los resultados experimentales obtenidos en este trabajo permitieron evaluar la capacidad de adsorción y el porcentaje de adsorción de Ni(II) y Co(II) contenidos en soluciones modeladas de sulfatos, utilizando carbón activado de conchas de coco. Como resultado del análisis estadístico se pudo comprobar que la capacidad de adsorción de Ni(II) y de Co(II) fue mayor en el nivel superior de concentración inicial del ión metálico y nivel inferior de dosis de adsorbente; esta última no ejerció una influencia significativa en el porcentaje de adsorción; tales condiciones pueden resultar ventajosas para lograr buena separación de los iones metálicos con economía en el consumo de adsorbente. El pH influyó significativamente en el porcentaje de adsorción. En las condiciones más favorables de adsorción (experimento 4) se alcanzó 98.1% de adsorción de níquel y 99.6% de adsorción de cobalto.
La evaluación de los modelos de Langmuir, Freundlich y Temkin, con los datos de isotermas de adsorción obtenidos experimentalmente a tres niveles de pH, permitió comprobar que las isotermas de equilibrio correspondientes a la adsorción de Co(II) tuvieron un buen ajuste al modelo de Langmuir, obteniéndose capacidades máximas de adsorción entre 33.33 y 71.43 mg de Co/g de CAG; siendo la adsorción muy favorable, con valores de RL mucho menores que la unidad (entre 0.00119 y 0.00573), lo cual indica que existe una alta afinidad adsorbato - adsorbente. Los resultados de equilibrio correspondientes a la adsorción de Ni(II) tuvieron un mejor ajuste al modelo de Freundlich. Los valores de KF obtenidos fueron 15.86 y 17.60 mg/g pH 3 y 5, siendo la adsorción favorable, con valores de 1/n entre cero y uno. El carbón activado de conchas de coco mostró efectividad como adsorbente de níquel y cobalto presentes en soluciones de sulfatos, siendo un método eficaz para el tratamiento de aguas residuales contaminadas con estos metales pesados.
NOMENCLATURA
b: constante de afinidad, L/mg.
B: constante relacionada con el calor de adsorción (J/mol)
bT: constante relacionada con el calor de adsorción, adimensional
Ce: concentración de soluto en el de equilibrio, mg/L
Ci: concentración inicial de soluto (adsorbato) en la solución, mg/L ]]>
KF: indicador aproximado de la capacidad de adsorción, mg/g
KT: constante de la isoterma de Temkin, L/mg
m: masa de adsorbente
n: factor de heterogeneidade (inverso)
Qe: capacidad de adsorción, mg/g de adsorbente
Qm: capacidad de adsorción máxima, mg de soluto/g de adsorbente, mg/g.
R: constante universal de los gases, 8,314 J/mol 0K
r2: coeficiente de correlación, %
Ra: porcentaje de absorción o recuperación
RL, denominada parámetro de equilibrio o factor de separación ]]>
T: temperatura absoluta, K
V: volumen de solución, L
BIBLIOGRAFÍA
1. M.L. Torem, et-al. "Evaluation of equilibrium, kinetic and thermodynamic parameters for biosorption of nickel(II) ions onto bacteria strain, Rhodococcusopacus". Minerals Engineering. 2009, 22, 15, 1318-1325.
2. Dada, A.O, et-al. "Langmuir, Freundlich, Temkin and Dubinin-Radushkevich isotherms studies of equilibrium sorption of Zn2+unto phosphoric acid modified rice husk". Journal of Applied Chemistry. 2012, 3, 1, 38-45.
3. Deepatana A., M. Valix. "Comparative adsorption isotherms and modeling of nickel and cobalt citrate complexes onto chelating resins". Desalination. 2008, 218, 334-342.
]]>4. Demirbas E.. Adsorption of Cobalt (II) Ions from Aqueous Solution onto Activated Carbon Prepared from Hazelnut Shells. Adsorption Science & Technology. 2003, 21, 10, 951-963.
5. Donia A.M., et-al. "Gold(III) recovery using synthetic chelating resins with amine, thio and amine/mercaptan functionalities". Separation and Purification Technology. 2005, 42, 111-116.
6. Fernández A., et-al. "Activación de carbones primarios para la obtención de tamices moleculares". INFOMIN. 2011, 3, 1, Pág.25-34.
7. Fleming C.A., et-al. "Factors influencing the rate of gold cyanide leaching and adsorption on activated carbon, and their impact on the design of CIL and CIP circuits". Minerals Engineering. 2011, 24, 484-494.
8. Hasar, H. "Adsorption of nickel(II) from aqueous solution onto activated carbon prepared from almond husk". 2003, 97, 1-3, 49-57.
]]>9. Heviánková S., et-al. "The application of wood ash as a reagent in acid mine drainage treatment". Minerals Engineering. 2014, 56, 109-111.
10. Krishnan K. A. ,T.S. Anirudhan. "Kinetic and equilibrium modelling of cobalt(II) adsorption onto bagasse pith based sulphurised activated carbon". Chemical Engineering Journal. 2008, 137, 257-264.
11. Labrada-Vázquez, B. Obtención de carbón activado de residuos lignocelulósicos por método de activación con etapa de lixiviación a escala de laboratorio. Facultad de Ingeniería Química. Universidad de Oriente. Cuba. 2005.
12. Parab H., et-al. "Determination of kinetic and equilibrium parameters of the batch adsorption of Co(II), Cr(III) and Ni(II) onto coir pith". Process Biochemistry. 2006, 41, 3, 609-615.
13. Rey-Mafull C. A., et-al. "Procedimiento tecnológico para la obtención de carbón activado calidad USP 30 para uso médico farmacéutico". Revista CENIC Ciencias Químicas. 2010, 41, 3, 167-175.
]]>14. S. Pércio, et-al. "Characterization of activated carbons from different sources and the simultaneous adsorption of Cu, Cr, and Zn from metallurgic effluent". Separation and Purification Technology. 2014, 122, 421-430.
15. Shah B.A., et-al. "Sequestration of Cu(II) and Ni(II) from wastewater by synthesized zeolitic materials: Equilibrium, kinetics and column dynamics". Chemical Engineering Journal. 2013, 220, 172-184.
16. Smith, J.M. Ingeniería de la Cinética Química. México. McGRAW-HILL BOOK COMPANY. 1991. 774 p. ISBN 968-26-0628-4.
17. Soco E., J. Kalembkiewicz. "Adsorption of nickel(II) and copper(II) ions from aqueous solution by coal fly ash". Journal of Environmental Chemical Engineering. 2013, 1, 581-588.
18. Sosa M. M., et-al. "Recuperación del cromo y aluminio del licor de desecho (wl) en forma de sales dobles". Minería y Geología. 2006, 22, 4, 1-12.
]]>19. Sosa, M.M., P.R. Bassas. Recuperación de metales del licor de desecho WL en forma de compuestos químicos. Minería y Geología. 2001, XVIII, 3-4, 107-112.
20. Srivastava V.C., et-al. "Equilibrium modelling of single and binary adsorption of cadmium and nickel onto bagasse fly ash". Chemical Engineering Journal. 2006, 117, 79-91.
21. Taffarel S.R., J.Rubio. "On the removal of Mn2+ ions by adsorption onto natural and activated Chilean zeolites". Minerals Engineering. 2009, 22, 336-343.
22. Tempkin M.I., V. Pyzhev. "Kinetics of ammonia synthesis on promoted iron catalyst". Acta Phys. Chim. 1940, 12, 327-356.
23. Wang, Q. , et-al. "Simultaneous adsorption of Cu(II) and SO42- ions by a novel silica gel functionalized with a ditopiczwitter ionic Schiff base ligand". Chemical Engineering Journal. 2014, 250, 55-65.
]]>24. Wang, X., et-al. "Optimization of Mesoporous activated carbon from coconut shells by chemical activation with phosphoric acid". BioResource. 2013, 8, 4, 6184-6195.
25. Yavuz R., et-al. "Factors Affecting the Adsorption of Chromium (VI) on Activated Carbon". Journal of Environmental Science and Health Part A. 2006, 41, 1967-1980.
Recibido: Diciembre 2013
Aprobado: Mayo 2014
]]> Margarita Penedo Medina. Facultad de Ingeniería Química, Universidad de Oriente. mpenedom@gmail.com ]]>