Obtención de hidróxido de níquel a escala de laboratorio
Obtaining of hydroxide of nickel to scale of laboratory
MSc. Deisy Cisneros-Sánchez, Ing. Elvira Leyva-Navarro, MSc. Neicis Capote-Flores
Centro de Investigaciones del Níquel (CEDINIQ), Cuba. dcisneros@cil.moa.minem.cu
]]>
RESUMEN
En el presente trabajo se brindan los resultados de la investigación realizada a escala de laboratorio para la obtención de hidróxido de níquel con características tales que puedan ser utilizados para la producción de baterías, catalizadores y pigmentos, entre otras aplicaciones. Se determinó la influencia de la temperatura, el pH y el tiempo de retención en la eficiencia de precipitación de níquel, cobalto y manganeso en forma de hidróxidos. Se establecieron las condiciones bajo las cuales se puede lograr una mayor precipitación de níquel a partir de una solución de sulfatos de níquel, cobalto y manganeso, en presencia de un ión donador de amonio.
Palabras clave: hidróxido, níquel, cobalto, manganeso.
ABSTRACT
The present work offers the results from the realized investigation to laboratory scale for the obtaining of nickel hydroxide with characteristic such that can be used for the production of batteries, catalysts and pigments, among other applications. It was determined the influence of the temperature, the pH and the time of retention in the efficiency of nickel precipitation, cobalt and manganese in form of hydroxides. The conditions under which you can achieve a bigger nickel precipitation starting from a solution of nickel sulfates, cobalt and manganese, in presence of an ion ammonium donor were established.
Keywords: hydroxide, nickel, cobalt, manganese.
INTRODUCCION
]]> A nivel mundial existe un incremento de la demanda de hidróxido de níquel para la producción de las baterías. Este es uno de los sectores en el cual se prevén aumentos para los próximos años, debido al auge que está tomando la producción de vehículos híbridos (combinan el uso de motores de combustión interna con motores eléctricos), los cuales reducen casi a la mitad las emanaciones de gases tóxicos al medio ambiente y el consumo de combustible [1]. En los países desarrollados adquiere gran importancia este vehículo dadas las fuertes restricciones medioambientales que existen.Este hidróxido, además se emplea en la producción de las baterías que se utilizan en los teléfonos inalámbricos y computadoras portátiles que también poseen una demanda creciente, y en su forma hidratada se utiliza comúnmente como material precursor en la producción de sales de níquel (principalmente el óxido de níquel). [1].
El cobalto también es utilizado con estos fines pero en menores cantidades, pues se emplea fundamentalmente como un aditivo que le confiere mayor estabilidad al material activo del electrodo positivo de las baterías y también suele ser utilizado como materia prima en la producción de carboxilatos y óxido de cobalto, pigmentos y catalizadores. [1].
El empleo de los hidróxidos de níquel y cobalto con los fines antes mencionados (baterías, catalizadores, pigmentos) demanda el cumplimiento de requisitos de calidad muy específicos en cuanto a diferentes parámetros (Ej: composición química, forma y tamaño de partículas, densidad, entre otros), siendo el sector de las baterías recargables uno de los más exigentes, por lo que su producción requiere que los especialistas estudien con profundidad las vías utilizadas para su obtención, de manera tal que puedan alcanzarse los indicadores de calidad exigidos, teniendo en cuenta las características particulares de las materias primas, materiales y entorno tecnológico.
El hidróxido de níquel, Ni(OH)2, es normalmente obtenido por la reacción de una sal de níquel con un hidróxido de metal alcalino [2]. Su composición química es variable y puede encontrarse en los siguientes rangos, en dependencia de la vía de obtención y grado de hidratación, etc.:
| Ni (%) | Co (%) | Na (%) | NH3 (%) | SO4 (%) |
|---|---|---|---|---|
| 55 -68 | <1% a varios %) | 0,3 | 0,05 | - |
Son diversas las vías empleadas para lograr la obtención de un hidróxido de níquel, mediante procesos que garanticen un producto estable y con los requisitos de calidad anteriormente mencionados.
Shin; Dong-Yup [3], refiere un método para preparar el hidróxido de níquel a partir del suministro continuo de una solución de sulfato de níquel y otra de hidróxido del amonio a un reactor para formar un complejo níquel-amonio, adicionando además a la mezcla ya formada, una solución del hidróxido de sodio, bajo condiciones específicas de temperatura, pH y tiempo de retención. También incluye en el proceso, la adición a la solución de sulfato de níquel de uno o más elementos seleccionados, que pueden ser Co, Zn y Cd en un rango de concentración de 0,05-0,3 mol/l. Con este procedimiento puede obtenerse un hidróxido de níquel de alta densidad útil para las baterías recargables alcalinas.
Wakao; Shinjiro [4], propone una invención mediante la cual se obtienen partículas de hidróxido de níquel proporcionando una solución acuosa de este metal, que contiene al mismo tiempo una solución acuosa de un aminoácido o sal, las cuales se adicionan a un reactor con suministro continuo de solución acuosa de un hidróxido de metal alcalino para mantener el pH de la mezcla en el reactor, en un valor constante. Refiere además, que para obtener un hidróxido de níquel de mayor actividad electroquímica, a la solución acuosa puede adicionarse por lo menos, una sal de otros metales tales como: cobalto, cadmio y zinc, en forma de sulfatos, nitratos y cloruros, en una cantidad, por ejemplo, de aproximadamente 1 a aproximadamente 5 % en peso, del contenido de níquel presente en la solución.
Ambos trabajos ofrecen alternativas relativamente sencillas para la obtención del hidróxido de níquel, las cuales pudieran ser implementadas para una producción comercial, sin embargo, no brindan información que permita establecer la influencia que tienen las variables principales del proceso sobre la eficiencia de recuperación del níquel y demás elementos adicionados a la solución, lo que constituye un aspecto que pudiera limitar la posibilidad de determinar la factibilidad técnico-económica para una producción a nivel industrial.
Teniendo en cuenta lo anterior, y sobre la base del procedimiento descrito en la invención [3], se realizó el presente trabajo, con el objetivo de determinar la influencia de diferentes variables en el proceso de precipitación del hidróxido de níquel, a partir de una solución de sulfato de este metal, que contiene además cobalto y manganeso.
]]>MATERIALES Y METODOS
Las corridas experimentales se desarrollaron a escala de laboratorio.
La instalación estuvo conformada por los siguientes equipos y accesorios:
Para determinar la composición química de las materias primas, materiales y productos sólidos y líquidos obtenidos en el proceso, se empleó la técnica de absorción atómica.
La materia prima utilizada fue la solución de sulfatos, obtenida a partir de la lixiviación del sulfuro de níquel, que contiene en menor cuantía cobalto y manganeso.
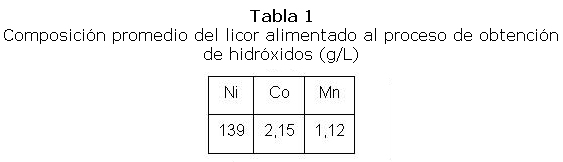
La composición promedio de la solución de sulfatos alimentada al proceso (en gramos por litro) fue la siguiente: Ver tabla 1.
Otros materiales empleados fueron los siguientes:
Se realizaron además, dos réplicas en el punto central, bajo las siguientes condiciones:
METODOLOGIA
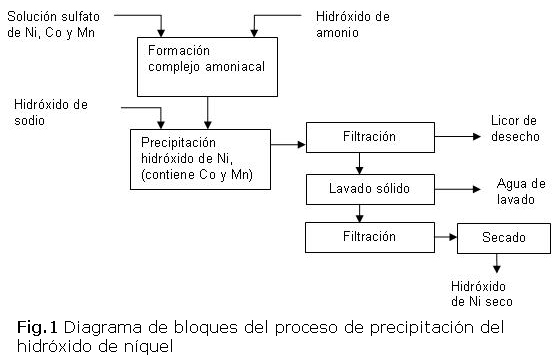
Los pasos seguidos para la ejecución del trabajo se ilustran en el diagrama de bloques que se muestra a continuación en la figura 1:
]]>
Al concluir las pruebas, se determinó la composición química del hidróxido de níquel obtenido, en por ciento, así como la concentración de la solución residual resultante del proceso. Se calculó la eficiencia de precipitación de níquel cobalto y manganeso, mediante la siguiente expresión:
Precp Mi = (%Mi sólido. Msól)/(Vlinic*Clinic)..............................(1)
Donde:
PrecpNi: Eficiencia de precipitación del metal, %
%Misólido: Contenido de metal "i" en el sólido, % (m/m)
Msólido: Masa de sólido seco obtenido, g
Vlinic: Volumen de licor inicial, L
Clinic: Concentración de metal "i" en el licor inicial, g/L
i : metal de interés, Ni, Co, Mn
Se determinó mediante la técnica de Difracción de rayos x, el tipo de compuesto obtenido, empleando un equipo Philips PW 1710. Estos análisis fueron realizados en el Centro de Investigaciones para la Industria Minero-Metalúrgica (CIPIMM).
RESULTADOS
Se determinó la composición química del hidróxido precipitado para metales involucrados en el proceso, bajo las condiciones que se indican en la tabla 3. Se evaluó la eficiencia de precipitación de Ni, Co, Mn, en %, (ver tabla 4). Se determinó la influencia de las variables: pH, temperatura y tiempo de retención (figuras 2a y b, 3a y b y 4a y b), se obtuvo la ecuación regresión ajustada, así como las condiciones óptimas para obtener la mayor eficiencia de precipitación de níquel en forma de hidróxido (tabla 5). Se caracterizó el compuesto mediante la utilización de la técnica de difracción de rayos X. figura 5 y 6).
]]>
DISCUSION DE LOS RESULTADOS
Influencia de las variables temperatura, pH, tiempo de reacción en la eficiencia de precipitación de los metales de interés
La precipitación de níquel se favorece con el incremento del pH y la temperatura y alcanzó valores entre 61,4 y 99,6%.
En la precipitación de cobalto tienen influencia significativa la interacción entre la temperatura, el tiempo de reacción y el pH. El incremento de este último afecta la precipitación del cobalto y alcanzó valores entre 63,8 y 100%.
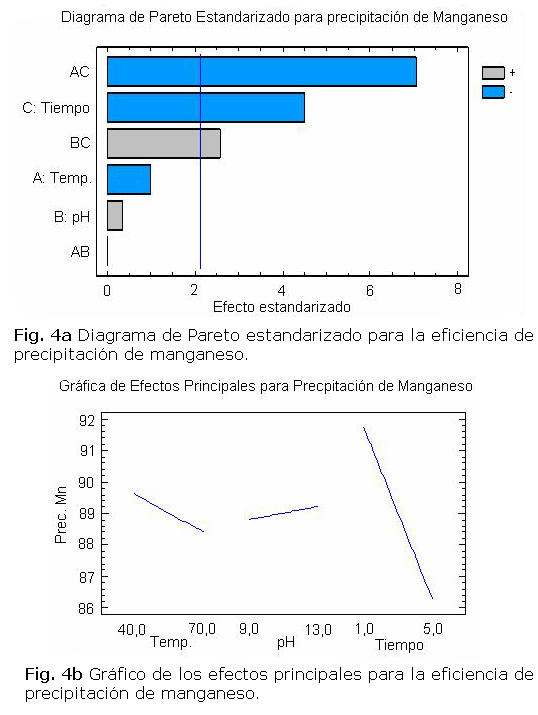
En la precipitación de manganeso, se obtuvieron eficiencias de precipitación del metal entre 78 y 98,6% influyen significativamente las mismas variables que en la precipitación de cobalto y también influye la interacción pH-tiempo de reacción. A diferencia del cobalto, el pH favorece la precipitación de este elemento, siendo un comportamiento no esperado que merece ser investigado con mayor profundidad.
| Temperatura | 70,0 | 0C |
| pH | 13,0 | unidades |
| Tiempo | 1,0 | hora |
Como resultado de la investigación realizada, se obtuvo el modelo ajustado para la precipitación níquel
PrecNi = -13,0062 + 0,219167*Temp + 7,36875*pH..............................(2)
El modelo explica el 98,8% de la variabilidad en PrecNi, dentro de los rangos especificados para cada una de las variables estudiadas.
Resultados de los análisis de Difracción de rayos X realizados a los productos obtenidos en las pruebas a nivel de laboratorio
Los análisis de Difracción de rayos x, fueron realizados en el Centro de Investigaciones para la Industria Minero-Metalúrgica (CIPIMM). Los difractogramas fueron obtenidos en el Equipo Phillips PW 1710. Los resultados numéricos de intensidades relativas y ángulos de difracción se convirtieron en difractogramas continuos con el empleo XPOWDER 12 el cual permite obtener las distancias interplanares correspondientes a los picos y la comparación de los difractogramas entre sí y obtención de todos los datos de intensidades de las difracciones. El análisis cualitativo de fases se realizó con la utilización de la base de datos PCPDFWIN; versión 1.30, JCPDS-ICDD / 2003, compatible con Windows 7 para Office 2010.
Las muestras analizadas presentan una composición cualitativa similar, pero con diferente grado de cristalinidad.
En las pruebas realizadas a pH igual a 9 se obtuvieron difractogramas de muestras con bajo grado de cristalinidad, que presentan picos anchos, alto fondo y de baja intensidad (figura 5). Estas muestras tienen los contenidos más bajos de níquel y mayor de cobalto y manganeso, mientras que las realizadas a pH igual a 13, muestran mejor cristalinidad, presentan picos menos anchos, menor fondo y mayor intensidad (figura 6). Estas muestras tienen mayores contenidos de níquel y menor de cobalto y manganeso.
Se encontró que los picos principales corresponden al hidróxido de níquel cristalizado en dos formas correspondientes a:
Ni(OH)2 REFERENCIA PCPDFWIN 01-1047: d (Å)= 2,70 - 2,33 - 4,67 - 1,56 ]]> Ni(OH)2 (Theoprasite Syn) REFERENCIA PCPDFWIN 74-2075: d (Å)= 2,33 - 4,63 - 2,71 -1,76 -1,56
Además contiene:
CoO(OH) Cobalt Hydroxide REFERENCIA PCPDFWIN 02-0214: d (Å)= 4,55 - 2,36 - 1,84 - 2,03 - 5,02 . 2,61
Estos hallazgos permiten confirmar que el producto obtenido es hidróxido de níquel, pero por si solos, no permiten definir si poseen las características apropiadas para ser empleados en la producción de baterías. En ese caso, sería conveniente, determinar además propiedades tales como: tamaño y forma de partícula, densidades aparente y de compactación y área superficial específica.
CONCLUSIONES
1. Se determinó la influencia de diferentes variables en el proceso de precipitación de un hidróxido de níquel que contiene cobalto y manganeso, resultando lo siguiente:
| Temperatura | 70,0 | 0C |
| pH | 13,0 | unidades |
| Tiempo | 1,0 | hora |
2. La composición química del hidróxido de níquel obtenido se encuentra en los siguientes rangos:
3. Se obtuvo el hidróxido de níquel cristalizado en dos formas correspondientes a:
Ni(OH)2 REFERENCIA PCPDFWIN 01-1047: d (Å)= 2,70 - 2,33 - 4,67 - 1,56 ]]> Ni(OH)2 (Theoprasite Syn) REFERENCIA PCPDFWIN 74-2075: d (Å)= 2,33 - 4,63 - 2,71 -1,76 -1,56
Además contiene:
CoO(OH) Cobalt Hydroxide REFERENCIA PCPDFWIN 02-0214: d (Å)= 4,55 - 2,36 - 1,84 - 2,03 - 5,02 . 2,61
BIBLIOGRAFIA
1. Heinz Pariser Alloy Metals and Steel Market Research. Nickel and Cobalt salts in Germany. Xanten, 2003. Págs 48-54.
2. Enciclopedia de Tecnología Química. México. 1962. Tomo XI, págs. 221-227.
3. Shin; Dong-Yup. "Método para preparar hidróxido de níquel de alta pureza para usar en baterías alcalinas recargables". Estados Unidos, 1996.
4. Wakao; Shinjiro. "Proceso para la producción de hidróxido de níquel". Estados Unidos. 1999.
5. Zelikman, A y col. "Teoría de los procesos hidrometalúrgicos". Editorial Metalurgia, Moscú, 1975. Págs 347-352.
6. Leyva E, Cisneros D, Capote N. "Pruebas exploratorias de obtención de hidróxidos de níquel y cobalto". Centro de Investigaciones del Níquel, Moa, 2002.
7. Leyva E, Castañeda D, Cisneros D. "Evaluación de las características y condiciones del hidróxido de níquel para su utilización en las baterías". Centro de Investigaciones del Níquel, Moa, 2002.
8. Cisneros D, Leyva E, Capote N. "Estudios experimentales a escala de laboratorio". Centro de Investigaciones del Níquel, Moa, 2013.
Recibido: Febrero de 2015
Aprobado: Junio de 2015
MSc. Deisy Cisneros-Sánchez. Centro de Investigaciones del Níquel (CEDINIQ), Cuba. dcisneros@cil.moa.minem.cu
]]>