
Sólido obtenido por electrocoagulación de la vinaza, nuevo inhibidor para la corrosión ácida del latón
Solid Obtained by Electrocoagulation of Vinasse, new Inhibitor for Acid Corrosion of Brass
Dra. C Elaine Ojeda-Armaignac, MSc. Romelia Hing-Cortón
Universidad de Oriente, Facultad de Ingeniería Química, Santiago de Cuba, Cuba. eoa@uo.edu.cu
]]>Resumen
Este trabajo se enmarca en las investigaciones relacionadas con la obtención de un inhibidor de la corrosión a partir de la vinaza, que tiene como ventajas básicas la posibilidad de utilizar un residuo industrial de las destilerías de alcohol etílico como materia prima en la obtención de un sólido inhibidor de la corrosión de producción nacional, mediante la electrocoagulación, lo cual implica sustitución de importaciones y reducción de los costos.La acción inhibidora de los sólidos obtenidos por electrocoagulación de la vinaza fue investigada por las técnicas de polarización potenciodinámica y espectroscopia de impedancia electroquímica. Se comprobó que las eficiencias de inhibición frente al latón en la solución electrolítica fueron muy buenas, comportándose como un eficiente inhibidor en medio ácido. La eficiencia de inhibición se incrementa con el incremento de la concentración. La máxima eficiencia de inhibición para la vinaza fue de 93,43 % para la concentración de 2 mg/L, Los parámetros termodinámicos fueron obtenidos a la temperatura de estudio. Se comprobó que la adsorción de las moléculas del inhibidor en la superficie del latón obedecen a la isoterma de Langmuir, y los valores de energía libre de adsorción de – 23,06 kJ mol-1 demuestran la espontaneidad de la adsorción e indican que el inhibidor es fuertemente adsorbido sobre la superficie del latón, El estudio de las curvas de polarización potenciodinámicas confirmó que es un inhibidor tipo mixto, con un predominio anódico y que existe un mecanismo predominante de adsorción física combinado con una quimiadsorción.
Palabras claves: inhibidor de la corrosión, latón, electrocoagulación, vinaza.
Abstract
This work is part of research related to obtaining a corrosion inhibitor from vinasse, whose basic advantages is the possibility of using an industrial waste from distilleries ethyl alcohol as raw material in the production of a solid corrosion inhibitor of national production by electrocoagulation, which implies import substitution and cost reductions. The inhibitory action of the solids obtained by electrocoagulation of vinasse was investigated by potentiodynamic polarization techniques and electrochemical impedance spectroscopy. It was found that the efficiencies of inhibition against the brass into the electrolyte solution were very good, behaving as an efficient inhibitor in acid medium. Inhibition efficiency increases with increasing concentration. The maximum inhibition efficiency was of 93,43 % for the concentration of 2 mg / L of vinasse. Thermodynamic parameters were obtained at the study temperature. It was found that the adsorption of inhibitor molecules on the surface of brass obey the Langmuir isotherm, and the values of adsorción free energy of - 23.06 kJ mol-1 show the spontaneity of adsorption and indicate that the inhibitor is strongly adsorbed on the surface of brass, study of potentiodynamic polarization curves confirmed that it is a mixed type inhibitor, with an anode predominance and there is a predominant mechanism of physical adsorption combined with a chemisorption.
Keywords: corrosion inhibitor, brass, electrocoagulation, vinasse.
INTRODUCCION
]]> La corrosión de los metales constituye un serio problema industrial a nivel mundial [14].resultando la prevención de este fenómeno uno de los retos más importantes que actualmente tiene la industria moderna. Metales valiosos como las aleaciones de cobre y cinc, son propensos a experimentar el proceso de corrosión cuando se exponen a medios agresivos tales como ácidos. De ahí la necesidad de proteger estos metales contra la corrosión [14].Uno de los métodos más utilizados para prevenir o atenuar la corrosión es el uso de inhibidores. Los inhibidores de corrosión más eficientes son los compuestos orgánicos que contienen grupos funcionales electronegativos y electrones π en sus triples enlaces o conjugados en los dobles enlaces [3]. La base de la acción inhibidora estriba en la adsorción de estas especies sobre la superficie metálica, bloqueando los sitios activos de corrosión. Cuatro tipos de adsorción pueden tener lugar por la moléculas orgánicas en la interface metal/solución: (1) atracción electrostática entre las moléculas cargadas y la carga del metal, (2) interacción de los pares de electrones no compartidos en la molécula del inhibidor con los orbitales incompletos del metal, (3) interacción de los π electrones con el metal y (4) combinación del mecanismo (1) y (3) [15].
En vistas de las desventajas de los compuestos de origen sintéticos tales como aspectos de costos, biodegradabilidad, toxicidad, disponibilidad y compatibilidad medioambiental, en la actualidad se ha producido un incremento repentino de compuestos de origen natural por su efecto inhibitorio de la corrosión, así como por aspectos ecológicos y económicos. [1, 3, 9-12].
La vinaza es un residual muy agresivo de la industria alcoholera, entre las características más relevantes se destaca el pH ácido, alta carga orgánica DQO (50000 – 100000 mg/L), DBO (45000 – 65000 mg/L), color marrón, alta temperatura y la presencia de compuestos nitrogenados entre los que se destacan: proteínas, aminoácidos y vitaminas [4-9]. La variada composición que posee este residual hace factible su valorización en diversos campos. Estudios realizados por Ojeda E. y Hing R. [13] permitieron evaluar los sólidos de la vinaza obtenidos por electrocoagulación, demostrando la efectividad de este producto como inhibidor de la corrosión del acero a diferentes valores de pH.
En el presente trabajo se investigaron las propiedades inhibidoras de la vinaza en H2SO4 frente al latón, mediante las técnicas de polarización potenciodinámica y de impedancia electroquímica. Los mecanismos de acción inhibidora, así como la cinética del proceso y los parámetros termodinámicos que gobiernan el proceso de adsorción también fueron calculados y discutidos.
METODO EXPERIMENTAL
Materiales y procedimiento para la electrocoagulación de la vinaza
Los ensayos experimentales se realizaron con muestras de vinaza, residual del proceso de destilación de alcohol a partir de las mieles finales de la caña de azúcar, que se lleva a cabo en la destilería perteneciente al complejo azucarero "Urbano Noris" de la provincia Holguín, Cuba.
En la electrocoagulación de la vinaza se utilizó una celda electroquímica a escala de laboratorio, constituida por un reactor intermitente de vidrio de geometría cilíndrica, 10 cm de diámetro y 20 cm de profundidad, para una capacidad útil de vinaza de 400 mL, equipada con dos electrodos planos de aluminio dispuestos verticalmente. Las dimensiones totales de los electrodos son de 6,8 cm de largo, 4 cm de ancho, y 0,1 cm de espesor, con un área total efectiva de 56,56 cm2, y espaciados 1,5 cm. Para el suministro de energía al sistema se utilizó una fuente de corriente directa, garantizando una correcta medición de las variables eléctricas a través de un amperímetro en serie, y un voltímetro en paralelo. Los electrodos fueron conectados en paralelo. El esquema de la instalación experimental se muestra en la figura 1.
]]> Preparación del electrodo de trabajoEl latón usado como electrodo de trabajo, posee una composición de: 70 % Cu - 30 % Zn. La muestra fue cortada de forma cilíndrica y recubierta por una resina de acrílico, el área superficial expuesta al medio corrosivo fue de: 0,79 cm2. Antes de cada experimento se realizó la preparación superficial del electrodo con la siguiente secuencia: primero se pulió con papel de lija de diferentes grados (600, 800 y 1200), luego se lavó con agua destilada, finalmente se desengrasó con acetona.Fig.1 Esquema de la instalación experimental de la electrocoagulación de la vinaza.
Experimentos electroquímicos
Los estudios de impedancia electroquímica y de polarización potenciodinámica se realizaron mediante el instrumento ACM Versión 5 modelo Gill AC. Los ensayos de corrosión fueron desarrollados en una celda electroquímica convencional de tres electrodos. El electrodo de trabajo fue el latón y como electrodos de referencia y auxiliar se utilizó un electrodo de calomel saturado y de platino, respectivamente. Los electrodos fueron sumergidos durante 30 min en la solución electrolítica para obtener el estado estable del potencial de circuito inicial.
Las curvas de polarización fueron obtenidas cambiando el potencial automáticamente desde -500 a 1 000 mV respecto al potencial de corrosión, con una velocidad de barrido de 0,5 mV/s. Los experimentos de espectroscopia de impedancia electroquímica se desarrollaron a un intervalo de frecuencia de 0,01 a 10 000 Hz y una amplitud de 10 mV usando una señal de corriente alterna al potencial de corrosión (Ecor). Los datos de los diagramas de impedancia se representaron en un diagrama de Nyquist. Los parámetros de impedancia y polarización tales como: capacitancia de la doble capa (Cdl), elemento de fase constante (CPEdl), resistencia a la transferencia de carga (Rtc), densidad de corriente de corrosión (icor), potencial de corrosión (Ecorr), pendientes de Tafel anódicas (ba) y pendientes de Tafel catódicas (bc) fueron calculados de las curvas de polarización y las curvas de Nyquist.[2, 9]. Las eficiencias del inhibidor fueron determinadas para las mediciones de la polarización potenciodinámica mediante la ecuación 1:

donde
icorr(0): densidad de corriente de corrosión sin inhibidor
icorr(1): densidad de corriente de corrosión con inhibidor.

donde
Rtc(0): resistencia a la transferencia de carga sin inhibidor
Rtc(i): resistencia a la transferencia de carga con inhibidor
RESULTADOS Y DISCUSION
Estudio de polarización potenciodinámica
El latón constituyó el material de electrodo estudiado mediante las técnicas de polarización potenciodinámica, en soluciones de pH 3 a diferentes concentraciones del sólido inhibidor, para determinar la cinética de las reacciones de corrosión anódica y catódica. Las curvas de polarización potenciodinámica se muestran en la figura 2. Los parámetros de corrosión electroquímicos obtenidos de las curvas de polarización, por el método de extrapolación de Tafel, así como los valores de eficiencia de inhibición correspondientes a las diferentes concentraciones del inhibidor se presentan en la tabla 1.
Como el latón es una aleación compuesta por 70 % de Cu y 30 % de Zn, ocurre una corrosión selectiva, siendo el cinc el metal que se disuelve preferentemente debido a que su potencial es menor que el del cobre y que el del hidrógeno. En la figura 2 para el latón a pH 3, se observa un desplazamiento marcado de las líneas de Tafel anódicas y ligeramente las catódicas con respecto al sistema sin inhibidor. Las icorr en presencia del sólido inhibidor, según tabla 1, son menores que en presencia de la solución ácida sola. Estos resultados demuestran que el inhibidor está actuando como un inhibidor tipo mixto con una acción predominantemente anódica. Para las ramas anódicas las líneas de Tafel se aplanan, lo que indica que el paso controlante del mecanismo cinético es la difusión de los iones Zn+2 de la superficie metálica hacia el seno de la solución. En las ramas catódicas al ser el ión hidronio el medio oxidante, debido al valor de pH en que se encuentra el material, se observa siempre un ascenso de las líneas de Tafel característico de la transferencia electrónica como paso controlante.
]]>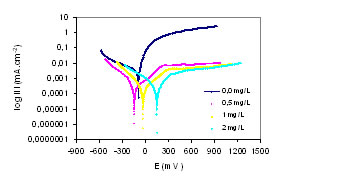
Fig. 2 Curvas de polarización para el latón en medio ácido a pH 3,
en presencia de varias concentraciones del inhibidor.
Tabla 1
Parámetros característicos del inhibidor frente al latón en medio ácido por polarización
potenciodinámica temperatura ambiente
| pH | C | Ecorr ]]> (mV) | icorr | ba | bc | θ | ξ |
| ]]>
3 | 0,0 | -92,52 | 0,029 57 | 1 034,9 | 484,04 ]]>
142,02 | - | - |
La tabla 1 muestra que los valores de la icorr disminuyen con el aumento de la concentración del inhibidor. Los valores de la eficiencia de inhibición, para todas las concentraciones del inhibidor, demuestran una alta efectividad de este inhibidor para el latón a pH 3, con una gran capacidad para incrementar la inhibición con el aumento de la concentración, alcanzándose la concentración óptima para 1 mg/L (90,43 %), ya que un aumento de concentración por encima de este valor produce poco cambio en la eficiencia de inhibición (93,43 %).
Los elevados valores de superficie cubierta, vinculados a elevadas eficiencias, indican que las moléculas del inhibidor son adsorbidas en la superficie del metal. Esto sugiere que el inhibidor actúa por adsorción sobre la superficie del latón bloqueando los sitios activos provocando una disminución de la oxidación del metal y por tanto se reduce la difusión de los iones Zn+2 y a su vez retarda la reacción de reducción de los iones H+.
Las moléculas del inhibidor, que es una sustancia superficialmente activa, presentan un dipolo, uno de estos polos, en este caso el positivo se adsorbe sobre la superficie del metal a través de la carga negativa de los aniones ácidos (SO 2- 4 ), quedando el polo negativo hacia afuera. Estas moléculas se pueden alinear formando una doble capa, la cual obstaculiza la difusión de los iones del metal de la superficie hacia el seno de la solución. Los Ecorr varían de forma irregular, para la menor concentración del inhibidor se desplazan hacia valores más negativos y para las concentraciones mayores hacia valores positivos con respecto al Ecorr del sistema sin inhibidor.
Las pendientes de Tafel anódicas, se incrementan con el aumento de la concentración del inhibidor, estos cambios se deben a la adsorción de las moléculas del inhibidor en la superficie metálica. Estos resultados demuestran que a medida que aumenta la concentración del inhibidor la reacción anódica o disolución del metal disminuye, lo que reduce a su vez la velocidad de corrosión. Sin embargo el proceso catódico se afecta menos con la presencia del inhibidor, lo que indica que el mismo, aunque actúa sobre las dos ramas su efecto es más marcado sobre el proceso anódico. Comparando estas tendencias de los valores de las pendientes de Tafel anódico y catódico con la fracción de la superficie cubierta y por lo tanto con la eficiencia, se observa que al valor de pH igual a 3 la reacción catódica se refiere a la reducción de los iones hidronio, y este medio ácido favorece la orientación de las moléculas del inhibidor, las cuales se adsorben sobre la superficie del metal, se incrementa la fracción de superficie cubierta y por tanto se incrementa la eficiencia.
Estudio de impedanciaLa representación de Nyquist, a partir de la técnica de espectroscopia de impedancia electroquímica, para el latón en soluciones de H2SO4 sin y con adición del inhibidor a diferentes concentraciones y a temperatura ambiente, se presenta en la figura 3 a), en la que se observa una mayor impedancia para los experimentos realizados con las diferentes concentraciones del inhibidor en comparación con la superficie del electrodo que no contiene inhibidor. Con la adición del inhibidor se observa en el diagrama de Bode (figura 4) un cambio característico del ángulo de fase, que indican tres tiempos constantes que pueden ser explicados debido a que bajo ciertas condiciones el sistema necesita más tiempo para alcanzar el equilibrio de adsorción. Sin embrago al ajustar los datos de los EIS por el programa ZSimpWin el estudio sugiere que al adicionar los inhibidores el sistema se puede separar en dos grandes grupos.
Fig. 3 (a) Curvas de impedancia para el acero al carbono a pH 3 en presencia de varias concentraciones
del inhibidor, (b) circuito eléctrico equivalente
Tabla 2
Parámetros característicos del inhibidor frente al latón en medio ácido por el método de impedancia
electroquímica a temperatura ambiente.
| pH | C | Rtc | ]]>
CPEdl (μF sn cm-2) | Ra | CPEa | σw | ξ |
| ]]> 3 | 0,0 | 4,6. 103 | 396,2 ]]>
235,5 | 3,4. 103 | 264,3 | 0,2814 | - |
En el circuito eléctrico de la figura 3 (b) el tiempo constante para la región de menor frecuencia se relaciona a los procesos interfaciales de las áreas expuestas a la adsorción de los inhibidores. El segundo tiempo constante aparece en la medida que aumenta la concentración del inhibidor, se encuentra en una región de mayor frecuencia y puede ser explicado porque bajo estas condiciones el sistema necesita más tiempo para alcanzar el equilibrio de adsorción debido a la acumulación de aniones y a una estructura más complicada de la doble capa en presencia de moléculas grandes adsorbidas en la superficie metálica. El modelo estructural ajustado por el programa presenta un elemento de fase constante (CPE) en lugar de un capacitor puro.
]]> En el circuito Rs es la resistencia de la solución electrolítica entre el electrodo de trabajo y el de referencia, y no está influenciada por los procesos de electrodos, su valor depende de la conductividad del medio y de la geometría de la celda. El par Ra/CPEa corresponde a los datos obtenidos a la mayor frecuencia, el cual está asociado a la resistencia y capacitancia de adsorción. El par Rtc/CPEdl representa el proceso de transferencia de carga y la capacitancia de la doble capa de la interface eléctrica. La difusión de los iones Zn2+ crea una impedancia llamada impedancia de Warburg, que se representa en el circuito por W. En la tabla 2 se presentan los parámetros de impedancia electroquímica de los ajustes de las curvas obtenidas para el latón a pH 3 a diferentes concentraciones del inhibidor.Isoterma de adsorción
En el presente trabajo, la isoterma de adsorción de Langmuir se determinó como satisfactoria para los experimentos desarrollados, descrita por la ecuación:

Los valores de la superficie cubierta (θ) por el inhibidor fueron determinados por el método de polarización potenciodinámica (según ecuación 4) para las diferentes concentraciones en la soluciones electrolítica de pH 3 a temperatura ambiente.

En la figura 5 se muestra la curva de C/θ contra concentración del inhibidor C para el latón a pH 3, observándose que existe una buena relación lineal. En la tabla 3 se presentan los parámetros de las isotermas de Langmuir para el acero al carbono, así como los valores de las energías libre de de adsorción ΔGads a presión y temperatura constantes.
El valor de la pendiente de la curva que representa la isoterma fue mayor que la unidad, lo cual corrobora que la adsorción del sólido inhibidor sigue la isoterma de Langmuir para el valor de pH 3 y a la temperatura ambiente. En la tabla 3 se muestra el coeficiente de correlación, cuyo valor es de 0,9999, resultado que también corroboran que la adsorción del inhibidor en la superficie del metal obedece a la isoterma de adsorción de Langmuir y confirman la validez de la ecuación estudiada.
Fig. 5 Isoterma de Langmuir a pH 3 para el inhibidor estudiado usando la superficie cubierta obtenida ]]> por la polarización electroquímica del latón a 300C
Tabla 3
Parámetros de la isoterma de adsorción de Langmuir para el latón a pH 3 y a temperatura ambiente, en presencia del inhibidor estudiado
| pH | R2 | Pendiente | Kads | ΔGads |
| 3 | ]]> 0,999 9 | 1,51 | 9,451 8 | -23,06 |
Mecanismo de adsorción del inhibidor frente al acero al carbono
Para explicar el mecanismo de adsorción del inhibidor en medio ácido (pH 3) frente al latón se tuvieron en cuenta que las moléculas del inhibidor estudiado existen como moléculas neutrales o en forma de especies protonadas (cationes), los valores de ΔGads (tabla 3), las elevadas ζ alcanzadas por el inhibidor frente al latón (tabla 2) y el complejo proceso de inhibición de la corrosión y la variada y compleja composición del inhibidor estudiado. Bajo estas consideraciones el sólido inhibidor puede adsorberse en la interface metal/solución ácida por los mecanismos siguientes:
1. Interacción electrostática entre la superficie cargada negativamente, la cual es proporcionada por los aniones SO2-4 adsorbidos específicamente en la superficie del metal, y la carga positiva de los grupos aminos presentes en los aminoácidos del inhibidor y que han sido protonados en medio ácido. La forma protonada con la parte cargada positivamente de la molécula es orientada hacia la superficie cargada negativamente
2. El inhibidor se adsorbe a través del donor (inhibidor) – aceptor (metal), interacción entre los electrones π y los pares de electrones no compartidos de los heteroátomos del inhibidor con los orbitales d incompletos de la superficie del metal.
La presencia de los iones sulfatos en la solución ácida, los cuales tienen cargas negativas excesivas cercanas a la interfaz, favorecen la adsorción de las moléculas inhibidoras cargadas positivamente. El grupo amino protonado se adsorbe a través de la interacción electrostática entre las moléculas cargadas positivamente y la superficie del latón el cual tiene ahora iones sulfatos cargados negativamente. Esto corresponde al mecanismo 1, que caracteriza al proceso de adsorción física que se lleva a cabo y que provoca una disminución de la disolución anódica del Zn que es el que se disuelve por ser el metal más electronegativo, y por tanto se reduce la difusión de los iones Zn+2.
Los elevados valores del grado de superficie cubierta, vinculados a las elevadas eficiencias que se encuentran por encima del 90 % (tabla 2), indican que las moléculas del inhibidor también se pueden adsorber por un proceso de adsorción química. La presencia de los dobles y triple enlaces, los heteroátomos de N y los grupos aminos pueden justificar el mecanismo 2 característico de una adsorción química, el cual se lleva a cabo en menor cuantía que la fisiadsorción. Las moléculas del inhibidor pueden adsorberse en la superficie del latón a través de las interacciones donor – aceptor de los electrones π de los triple enlaces y los pares de electrones no compartidos de los heteroátomos con los orbitales d incompletos del metal.
]]>CONCLUSIONES
1. Las eficiencias de inhibición para el sólido inhibidor estudiado se incrementan con el incremento de la concentración. La mayor eficiencia alcanzada para el latón fue de 93% para la concentración de 2 mg/L, comportándose como un eficiente inhibidor de la corrosión en medio ácido.
2. La adsorción de las moléculas del inhibidor en la superficie del latón obedecen a la isoterma de Langmuir. Los valores de ΔGads son negativos, los cuales muestran la espontaneidad de la adsorción y sugieren que el inhibidor es fuertemente adsorbido sobre la superficie del acero al carbono y el latón, mediante un proceso predominante de adsorción física combinado con una adsorción química.
3. El estudio de las curvas de polarización potenciodinámicas confirmó que el inhibidor altera las pendientes de Tafel anódicas y catódicas, funcionando como un inhibidor tipo mixto, con un predominio anódico para el latón.
4. Los resultados de la Espectroscopía de Impedancia Electroquímica (EIS) permitieron ajustar un circuito eléctrico equivalente que incluye dos tiempos constantes que describen los procesos de corrosión en presencia del inhibidor. La doble capa y la capacitancia de adsorción son modelados por el elemento CPE, y también se presentan procesos difusivos modelados por una impedancia Warburg.
BIBLIOGRAFIA
1. ABDEL-GABER A.M., ABD-EL-NABEY B.A., KHAMIS E., ABD-EL-KHALEK D.E., "A natural extract as scale and corrosion inhibitor for steel surface in brine solution". Desalination, vol. 278, 2011, p. 337-342.
]]>2. AGUILAR M., "Determinación de algunas vitaminas del complejo B en Mostos de Destilerías". Tesis en obtención al título de Licenciado en Química. Universidad de Oriente, 1989. p. 3-4.
3. AL-OTAIBI M.S., AL-MAYOUF A.M., KHAN M., MOUSA A.A., AL-MAZROA S.A., ALKHATHLAN H.Z., "Corrosion inhibitory action of some plant extracts on the corrosion of mild steel in acidic media". Arabian Journal of Chemistry, Volume 7, Issue 3, 2014, p. 340-346.
4. CAMEJO J.J., "Métodos químicos tecnológicos de protección contra la corrosión". Diplomado de Corrosión y Protección Anticorrosivo, Facultad de Ingeniería Química, Instituto Superior Politécnico José Antonio Echeverría, La Habana, Cuba, 2010.
5. CAÑIZARES P., JIMÉNEZ C., MARTÍNEZ F., RODRIGO M.A., SÁEZ C., "The pH as a key parameter in the choice between coagulation and electrocoagulation for the treatment of wastewaters", Journal of Hazardous Materials 163, 2009, p. 158-164.
6. CHEN Y., LEI H., WEIQING H., WANG L., XIUYUN S., JIANSHENG L., "Treatment of high explosive production wastewater containing RDX by combined electrocatalytic reaction and anoxic-oxic biodegradation".Chemical Engineering Journal , vol. 168, 2011, p. 1256-1262.
]]>7. BERMÚDEZ SAVÓN R.C. et al. "Características de la vinaza de destilería (mosto). Realizado por el grupo de tratamiento y aprovechamiento de residuales de la Facultad de Ciencias Naturales". Universidad de Oriente. 2004.
8. DOMÍNGUEZ J., CASTRO D., MATOS R., HING R., "Introducción a la Corrosión y Protección de Metales". Ediciones ENPES, La Habana, Cuba, 1987.
9. DÖNER A., SOLMAZ R., ÖZCAN M., KARDAS G., "Experimental and theoretical studies of thiazoles as corrosion inhibitors for mild steel in sulphuric acid". Corrosion Science, vol 53, 2011, p. 2902-2913.
10. GALVELE. G, DUFFO G.S. Degradación de Materiales II. Corrosión. Instituto de Tecnología, UNSAM-CNEA, Buenos Aires, Argentina, 2003.
11. GUANNAN M., XUEMING L., GUANGHENG L., "Synergistic inhibition between tween 60 and NaCl on the corrosion of cold rolled steel in 0.5M sulfuric acid", Corrosion Science, vol 47, 2005, p. 1932-1952.
]]>12. MIGAHED M.A., ABDUL-RAHEIM A.M., ATTA A.M., BROSTOW W., "Synthesis and evaluation of a new water soluble corrosion inhibitor from recycled poly(ethylene terphethalate)". Materials Chemistry and Physics vol 121, 2010, p. 208-214.
13. OJEDA E., HING R., "Estudio de inhibidores ecológicos y naturales". Tecnología Química, vol.26, Nº 3, 2006.
14. PIERRE R.R., "Handbook of Corrosion Engineering". McGraw-Hill, New York, 1999.
15. SINGH K.A., SHUKLA K.S., QURAISHI M.A., EBENSO E.E., "Investigation of adsorption characteristics of N,N′-[(methylimino)dimethylidyne]di-2,4-xylidine as corrosion inhibitor at mild steel/sulphuric acid interface", Journal of the Taiwan Institute of Chemical Engineers, vol. 43, p. 463-472, 2012.
]]> Recibido: Mayo 2016
Dra. C Elaine Ojeda-Armaignac. Universidad de Oriente, Facultad de Ingeniería Química, Santiago de Cuba, Cuba. eoa@uo.edu.cu
]]>