Bioadsorción de níquel en residuales de Empresa Minera por biomasa de Phyllanthus Orbicularis
Bioadsorption of nickel Mining Company by residual biomass Phyllanthus Orbicularis
Lic. Ariel Díaz-PuigI, Lic. Asel Guilarte-GainzaI, Lic. Alina Chaviano-BeitraII, Dra.C. Rosa M Pérez-SilvaIII
I: Empresa Comandante Ernesto Che Guevara, Moa, Holguín, Cuba
II: Centro de Estudios de Medio Ambiente. Instituto Superior Minero-Metalúrgico de Moa, Holguín, Cuba ]]>
III: Centro de Estudios de Biotecnología Industrial (CEBI). Facultad de Ciencias Naturales y Exactas, Universidad de Oriente, Santiago de Cuba, Cuba. rperezs@uo.edu.cu
Resumen
Se estudiaron parámetros cinéticos para la adsorción de níquel en el residual de la Planta de calcinación de la Empresa Comandante Ernesto Che Guevara por biomasa de Phyllanthus orbicularis en soluciones sintéticas y del residual industrial de la Planta de Calcinación de la empresa. Los resultados mostraron que los factores de mayor influencia sobre la capacidad de adsorción de la biomasa se incrementan al aumentar el pH y la concentración inicial de níquel en el efluente y se reduce al incrementar la concentración de biomasa. Por su parte, la eficiencia de remoción de níquel del residual se incrementa al aumentar el pH y la concentración de biomasa y se reduce cuando se incrementa la concentración inicial de níquel en el efluente. La capacidad de adsorción de níquel de la biomasa de Phyllanthus orbicularis a partir de soluciones sintéticas y del residual industrial de la Planta de Calcinación de la Empresa del níquel "Comandante Ernesto Che Guevara" fue de 44,05 y 26,25 mg.g-1 respectivamente. El proceso de adsorción de níquel por la biomasa de Phyllanthus orbicularis sigue una cinética de pseudo-segundo orden y de acuerdo a los valores de energía libre de adsorción obtenidos a través del modelo de Dubinin-Radushkevichfue de 267,26 kJ/mol, esto demuestra que la naturaleza se corresponde con un proceso mediado por la adsorción química donde predomina la formación de enlaces estables entre los grupos funcionales presentes en la biomasa y los iones metálicos.
Palabras clave: bioadsorción, níquel, Phyllanthusorbicularis, parámetros cinéticos, metales pesados, residuales de la empresa minera.
Abstract
Kinetic parameters for the adsorption of nickel were studied in the waste CalcinationPlant Company Ernesto Che Guevara biomass Phyllanthus orbicularis synthetic and industrial waste Calcination Plant enterprise solutions. The results showed that the major factors influencing the adsorption capacity of the biomass increases with increasing pH and the initial concentration of nickel in the effluent and is reduced by increasing the biomass concentration. Meanwhile, the removal efficiency of residual nickel increases with increasing pH and concentration of biomass and reduced when the initial concentration of nickel in the effluent increases. The adsorption capacity nickel biomass Phyllanthus orbicularis from synthetic solutions and industrial waste Calcination Plant Company Nickel "Comandante Ernesto Che Guevara" was 44,05 and 26,25 mg/g respectively. The adsorption process nickel biomass Phyllanthus orbicularis follows kinetics pseudo-second order and according to the values Of free energy of adsorption obtained through model-RadushkevichDubinin was 267,26 kJ/mol, this nature demonstrates that corresponds to a process mediated by chemical adsorption where the formation of stable bonds between the functional groups present in the biomass and the metal ions predominates.
Keywords: bioadsorption, nickel, Phyllanthusorbiculari, kinetics parameters, heavy metals, residualof the miningcompany.
]]>
INTRODUCCION
La acumulación de metales pesados en el medio ambiente constituye un factor de riesgo para la salud humana y al equilibrio de los ecosistemas [1]. La gran mayoría de estos elementos (Ni, Cd, Co, Cr, Pb, Zn) son introducidos a la esfera de interacción de la biosfera a través de los desechos generados por la actividad humana, destacándose la actividad industrial como principal fuente de emisión, debido a la obsolescencia e incapacidad de muchas de las tecnologías en uso para impedir que éstos pasen al medio a través de los efluentes de procesos, constituyendo en ocasiones pérdidas adicionales para la industria.
Las limitaciones que poseen las tecnologías convencionales para el tratamiento de residuales, en la actualidad, conduce a un marcado interés en la utilización de sistemas biológicos para recuperar iones de metales pesados contenidos en las soluciones de desechos originadas en los procesos industriales [2]. Labiorremediación ha emergido como una tecnología alternativa con potencialidades para convertirse en vía de preferencia para este fin. Esto se debe a que además de las probadas capacidades adsortivas sobre iones metálicos que poseen los diferentes tipos de biomasa utilizados, es en ocasiones altamente selectiva, fácilmente manejable y de obtención relativamente barata [3].
En este sentido, las plantas hiperacumuladoras resultan potencialmente atractivas para el desarrollo de tecnologías para la biorremediación de residuales industriales, altamente eficientes, ambientalmente limpias y menos costosas que las tecnologías convencionales. Estas plantas que evolucionaron en suelos con altas concentraciones de metales pesados, tienen la habilidad de acumular elevadas concentraciones de estos en su biomasa por lo que existe un creciente interés en su estudio para el desarrollo de la fitominería [4].
Phyllanthusorbicularises es un ejemplo de planta hiperacumuladora de níquel y se encuentra formando parte de la flora autóctona de los charrascales de Yamanigüey, en el municipio de Moa. Por tanto, el objetivo de este trabajo fue evaluar la capacidad de la biomasa de Phyllanthus orbicularis para bioadsorber el níquel disuelto en el residual de la planta de Calcinación de la Empresa "Comandante Ernesto Che Guevara" a través de la determinación de parámetros cinéticos en el proceso de adsorción.
MATERIALES Y METODOS
Colecta y preparación de la biomasa de Phyllanthus orbicularis: Las ramas de Phyllanthus orbicularis, Phyllanthuscomosusy Dracena cubensis fueron colectadas en la localidad de Yamanigüey, municipio Moa, al noreste de la provincia Holguín. Se lavaron con abundante agua destilada para eliminar la suciedad de su superficie. Inmediatamente se secaron en una estufa marca "JP SELECTA", modelo "DIGITRONIC" a 60°C durante 24 h. Posteriormente molida en un molino de rodillo marca "GY-RO MILL y con la tamizadora marca "FRITSCH", modelo "analysette 3PRO" se obtuvo una fracción homogénea de granulometría 0,7 a 1,0 mm [5]. Estas fueron lavadas con HCl (0,1 M) durante 30 min, filtradas a través de un papel Whatman No. 42 y lavadas nuevamente con agua destilada hasta que se registró en la misma un pH neutro [6]. La biomasa fue sometida otra vez a un proceso de secado bajo las mismas condiciones iniciales (60 °C, 24 h) y almacenada en un frasco de cristal hermetizado hasta su uso.
Se determinó la humedad por el método gravimétrico. Para esto se pesó en balanza digital "Sartorius", modelo "CP224S con cápsula tarada una muestra de 5,0 g de biomasa y se mantuvo en la estufa a 100°C por 24 h, la cápsula se enfrió en una desecadora hasta la temperatura ambiente y se pesó nuevamente, procedimiento que fue repetido hasta obtener una pesada constante. Los valores de peso inicial y final de la biomasa fueron usados para determinar la humedad (1).
]]>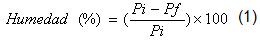
donde
Pi y Pf son el peso inicial y final de la biomasa.
Preparación de las soluciones sintéticas de níquel: Las soluciones sintéticas de níquel fueron preparadas disolviendo en un litro de agua bidestilada las cantidades de 1,000 6, 2,001 2, 3,001 8, 4,002 4 y 5,003 0 g de Ni(NO3)2•6H2O (Analar GR, BDH) para obtener concentraciones de 200, 400, 600, 800 y 1000mg/dm3 respectivamente; determinando a través de espectrometría de adsorción atómica (EAA) la concentración real de níquel para ser usada en el cálculo de la capacidad de carga de la biomasa en el equilibrio.
Estudios de adsorción en "batch" utilizando soluciones sintéticas de níquel: Para cada experimento de adsorción se tomaron 200 mL de solución de níquel en frascos ERLenmeyer de 500 mL y se pusieron en contacto con 0,5 g de biomasa en base seca durante 6 h en agitadores magnéticos termostatados (marca "Stuart Scientific", modelo "SM6"), a 120 rpm y 35°C de temperatura [7].
Las corridas se realizaron a 4 valores de pH (3; 4; 5,4 y 6,5 unidades) utilizando soluciones 0,1 M de HCl o NaOH, según se requirió. Para las soluciones sintéticas el pH se limitó al valor máximo de 6,5, teniendo en cuenta que según refiere la literatura por encima de valores cercanos a 7, el níquel comienza a precipitar interfiriendo con el proceso de adsorción, por lo que resulta difícil a nivel macroscópico separar el efecto de la bioadsorción del causado por la precipitación [7]. El pH y la temperatura de las soluciones fueron medidos utilizando un equipo marca "WTW", modelo "pH197i".
La biomasa de la mezcla fue separada por filtración a través de papel Whatman No. 42 y el filtrado clarificado se tomó para analizar la concentración de níquel residual a través de EAA. Todos los experimentos fueron realizados por duplicado tomando el valor promedio de concentración de níquel para expresar los resultados.
La eficiencia de remoción de níquel de la solución inicial y la capacidad de adsorción de níquel de la biomasa fueron calculadas a través de un balance de masas según se refiere en la literatura haciendo uso de las ecuaciones 2 y 3 [5, 7].
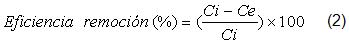
donde
]]> Ci y Ce son las concentraciones de níquel en la solución al inicio del experimento y al alcanzarse el equilibrio respectivamente.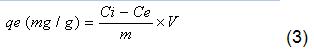
donde
qe es la capacidad de adsorción de la biomasa en el equilibrio expresada en (mg/g), m es la masa de bioadsorbente usado (biomasa, expresada en g) y V es el volumen de la solución en (L)
Estudios de adsorción en "batch" utilizando el residual industrial de la planta de Calcinación de la Empresa "Comandante Ernesto Che Guevara".
Para evaluar la capacidad efectiva de adsorción de la biomasa de Phyllanthus orbicularis bajo condiciones prácticas, se utilizaron muestras de residual proveniente del sedimentador de carbonato de la planta de Calcinación de la Empresa "Comandante Ernesto Che Guevara" al que se le determinó la concentración de níquel por EAA. Para cada experimento (por duplicado) se tomaron 200 mL muestra en frascos ERLenmeyer de 500 mL y se pusieron en contacto con diferentes concentraciones de biomasa en base seca (0,5; 2,5; 5,0; 10,0 y 20,0 g/dm3) durante 6 h, en agitadores magnéticos termostatados a 120 rpm y 35 °C de temperatura manteniendo el pH original del residual[7]. Posteriormente, la biomasa de la mezcla fue separada por filtración a través de papel Whatman No. 42 y el filtrado clarificado se tomó para analizar la concentración de níquel residual a través de EAA.
Todos los experimentos fueron realizados por duplicado tomando el valor promedio de concentración de níquel para expresar los resultados.
Evaluación de la cinética de la bioadsorción del níquel presente en el residual industrial en biomasa de Phyllanthus orbicularis: Para evaluar la cinética de adsorción de níquel bajo condiciones prácticas, se utilizaron muestras de residual provenientes del sedimentador de carbonato de la planta de Calcinación de la Empresa "Comandante Ernesto Che Guevara" al que se le determinó la concentración de níquel por EAA. Se tomaron 200 mL de residual en frascos ERLenmeyer de 500 mL y se pusieron en contacto con 1,0 g de biomasa durante diferentes intervalos de tiempo (10, 20, 30, 40, 50, 60, 7, 80, 90, 100 y 110 min) hasta alcanzar el equilibrio en agitadores magnéticos termostatados a 120 rpm y 35°C de temperatura manteniendo el pH original del residual [7]. A través de papel Whatman No. 42, se separa la biomasa y el filtrado clarificado se tomó para analizar la concentración de níquel residual a través de EAA.
Todos los experimentos fueron realizados por duplicado tomando el valor promedio de concentración de níquel para expresar los resultados.La eficiencia de remoción de níquel y la capacidad de adsorción de níquel de la biomasa fueron calculadas a través de las ecuaciones 1 y 2.
Con el objetivo de evaluar el mecanismo cinético del proceso de bioadsorción de níquel por la biomasa de Phyllanthus orbicularis, fueron aplicados a los datos experimentales los modelos para reacciones de pseudo-primer y pseudo-segundo orden. Para el modelo de pseudo-primer orden fue utilizada la ecuación dada por (Langergren, 1898 tomada de Sao y col. 2014):
]]>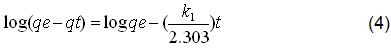
donde
qe y qt representan la cantidad de níquel adsorbido por la biomasa en el equilibrio y al tiempo t respectivamente, k1 (1/min) es la constante de la razón de adsorción de pseudo-primer orden y se calculó a partir de la pendiente de la recta de mejor ajuste a los datos experimentales, los que fueron representados en un gráfico de log(qe-qt) contra t.
La ecuación de pseudo-segundo orden para las condiciones límites cuando t y qt tienden a 0, ha sido presentada por (Ho y McKay, 1999) y puede representarse como:
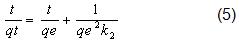
donde
k2 (g/mg•s) es la constante de la razón de adsorción de pseudo-segundo orden que se calculó a partir del intercepto de la recta de mejor ajuste a los datos experimentales, los que fueron representados en un gráfico de t/qt contra t.
RESULTADOS
Evaluación de la capacidad de adsorción de níquel de la biomasa de Phyllanthus Orbicularis
]]> Los resultados experimentales obtenidos en los ensayos de adsorción con soluciones sintéticas, fueron utilizados para obtener los modelos de isotermas de adsorción que permiten describir el comportamiento de la biomasa de Phyllanthus orbicularis como adsorbente del níquel a pH 6,5. La tabla 1 muestra los resultados luego de la aplicación de los modelos de Langmuir, Freundlich y Dubinin-Radushkevich que permiten describir el proceso de adsorción de níquel por Phyllanthus orbicularis.Tabla 1
Parámetros de los modelos de adsorción de níquel por
Phyllanthus orbicularis con soluciones sintéticas
| Modelo | Parámetros | Valores |
| Langmuir | qm (mg/g) | 44,05 |
| ]]> KL (L/mg) | 0,002 | |
| R2 | 0,981 3 | |
| Factor de separación (RL) | 0,488 | |
| Freundlich | N | 1,675 |
| Kf | ]]> 0,553 0 | |
| R2 | 0,980 2 | |
| Dubinin-Radushkevich | qs (mg/g) | 26,22 |
| Kd (mol2/KJ2) | 0,000 31 | |
| E (kJ/mol) | 40,16 | |
| ]]> R2 | 0,817 6 |
En la literatura aparecen reportados un gran número de qm obtenidos para diferentes tipos de materiales adsorbentes, entre los que destacan, Allyssumdiscolor con 34,70mg/g. Residuos de fábrica de té con 18,42mg/g, Ascophyllumnodosssum con 64,0, Sargassummuticum con 70 mg/g,Ceralite R-120 (pH 5) con 28,57, AmbeRLite-IRC86 y AmbeRLite200C con 37,93 y 43,11, respectivamente [10-16]. En el estudio evaluado se alcanza una qm de 26,25 y 44,05 por Phyllanthusorbicularis en la adsorción de niquel en agua residual y solución sintética, respectivamente.
Las isotermas obtenidas a través de los tres modelos aplicados y los datos experimentales son presentados en la figura 1.
Fig. 1 Isotermas predichas por los tres modelos aplicados.
Características: Solución de Ni(NO3)2·6(H2O); C0 (Ni): 200-1000 mg/L; pH: 6,5; 120 rpm; Tiempo de contacto: 6 horas; biomasa: 0,5 g; Temperatura: 35 °C
Efecto del pH en la adsorción de níquel por Phyllanthus orbicularis en soluciones sintéticas
Para conocer el efecto del pH en la adsorción de níquel por la biomasa de Phyllanthus orbicularis, se realizó una serie de experimentos a tres valores de pH adicionales (3; 4 y 5,4).Las isotermas de adsorción obtenidas para cada uno de estos valores de pH se muestran comparativamente en la figura 2 y los parámetros obtenidos de la aplicación del modelo de Langmuir a estos resultados experimentales se presentan en la tabla 2.
Basado en el modelo de Langmuir, puede calcularse una constante adimensional definida por Webber y Chakkravorti, [3] denominado factor de separación (RL) el cual está relacionado con la constante KL obtenida del modelo. Esta constante indica que la naturaleza de la adsorción puede ser desfavorable si RL>1, lineal si RL=1, favorable si 0<RL<1 e irreversibles en caso de que RL=0. Este valor de factor de separación obtenido para la biomasa de Phyllanthusorbicularis para cada uno de los valores de pH experimentados se muestra comparativamente en la tabla 2.
]]>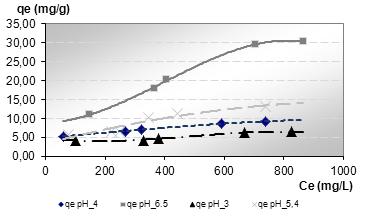
Fig. 2 Isotermas de adsorción de níquel a diferentes valores de pH.
Características: Solución de Ni(NO3)2·6(H2O); C0(N)i: 200-1000 mg/L; 120 rpm; Tiempo de contacto: 6 h; biomasa: 0,5 g; Temperatura: 35°C.
Tabla 2
Parámetros del modelo de Langmuir ajustado a la adsorción de níquel
obtenidos para Phyllanthus orbicularis con soluciones sintéticas
| Parámetros | pH 6,5 | pH 5,4 | pH 4 | ]]> pH 3 |
| qm (mg/g) | 44,05 | 10,42 | 8,55 | 6,55 |
| KL(L/mg) | 0,002 2 | 0,013 7 | 0,026 2 | ]]> 0,009 3 |
| R2 | 0,981 3 | 0,701 7 | 0,979 6 | 0,963 4 |
| Factor de separación (RL) | 0,49 | 0,35 | 0,20 | ]]> 0,33 |
Características: Solución de Ni(NO3)2·6(H2O); C0(Ni): 200-1000 mg/L; 120 rpm; Tiempo de contacto: 6 h; biomasa: 0,5 g; Temperatura: 35°C
Evaluación de la capacidad de adsorción de níquel de la biomasa de Phyllanthus orbicularis utilizando un residual industrial
Generalmente las isotermas de adsorción para el níquel son obtenidas a partir de soluciones con pH inferior a 7, pues por encima de este valor, el níquel comienza a precipitar interfiriendo con el proceso de adsorción, por lo que resulta difícil a nivel macroscópico separar el efecto de la bioadsorción del causado por la precipitación [7]. Es por esto que al evaluar la capacidad efectiva de adsorción de la biomasa de Phyllanthus orbicularis bajo condiciones prácticas, se utilizó una muestra de residual proveniente del sedimentador de carbonato de la planta de Calcinación de la Empresa "Comandante Ernesto Che Guevara". A los resultados experimentales obtenidos les fueron aplicados los tres modelos de isotermas de adsorción, utilizados para el caso de soluciones sintéticas con el objetivo de relacionar de una manera satisfactoria la concentración del níquel en la solución con el níquel adsorbido en la biomasa. Un resumen de los parámetros de los modelos utilizados para describir este proceso de adsorción por Phyllanthus orbicularis se presenta en la tabla 3. Cabe destacar que para los tres modelos fue usada la misma serie de datos experimentales.
Tabla 3
Parámetros de los modelos de adsorción de níquel
por Phyllanthusorbicularis en residual industrial
| Modelo | Parámetros | Valores |
| ]]> Langmuir | qm (mg/g) | 26,25 |
| KL (L/mg) | 0,044 | |
| RL | 0,188 | |
| R2 | 0,990 6 | |
| Freundlich | ]]> N | 2,15 |
| Kf | 2,67 | |
| R2 | 0,898 5 | |
| Dubinin-Radushkevich | qs (mg/g) | 16,42 |
| Kd (mol2/KJ2) | ]]> 0,000 007 | |
| E (kJ/mol) | 267, 26 | |
| R2 | 0, 922 1 |
Características: (C0(Ni): 99,14 mg/L; pH: 8,4; 120 rpm; t de contacto: 6 h; T: 35°C)
En la figura 3 se presentan las isotermas obtenidas a través de los tres modelos aplicados y los datos experimentales para las condiciones fijadas.
Fig. 3 Datos experimentales e isotermas predichas por los tres modelos aplicados en solución residual.
]]> Características: C0(Ni):99,14 mg/L; pH: 8,4; 20 rpm; Tiempo de contacto: 6 h; Temperatura: 35 °C.Evaluación cinética de la bioadsorción del níquel presente en el residual industrial en biomasa de Phyllanthus orbicularis
La relación entre la adsorción de níquel en la biomasa de Phyllanthus orbicularis y el tiempo de reacción se representa en la figura 4. Los resultados experimentales muestran que el 60 % del níquel es adsorbido en los primeros 20 min, transcurriendo el proceso más lentamente hasta alcanzar los 60 min aproximadamente. A partir de este tiempo el sistema no adsorbe más níquel alcanzando el equilibrio, evidenciándose que un tiempo de contacto de 1 h es suficiente para lograr la máxima adsorción de níquel posible por Phyllanthus orbicularis.
Fig. 4 Bioadsorción del níquel presente en el residual industrial por la biomasa de Phyllanthus orbicularis en relación al tiempo de reacción.
Características: C0(Ni): 99,14 mg/L; pH: 8,4; 120 rpm; Temperatura: 35 °C; biomasa: 0,962 8 g.
Para evaluar el mecanismo cinético del proceso de bioadsorción de níquel por la biomasa de Phyllanthus orbicularis, fueron aplicados a los datos experimentales los modelos para reacciones de pseudo-primer y pseudo-segundo orden [5, 22]. Los valores de los parámetros obtenidos para ambos modelos son presentados en la tabla 4.
Tabla 4
Parámetros de los modelos cinéticos aplicados
a la bioadsorción de níquel por Phyllanthus orbicularis
| ]]> Parámetros | Pseudo primer orden | Pseudo-segundo orden |
| qe (mg/g) | 52,991 0 | 23,041 0 |
| k1 (1/min) | 0,096 7 | - |
| k2 (g/mg·s) | ]]> - | 0,002 2 |
| R2 | 0,911 3 | 0,989 6 |
La figura 5, muestra los modelos lineales de las ecuaciones cinéticas aplicadas a los datos experimentales obtenidos del proceso de bioadsorción de níquel por Phyllanthus orbicularis.
La linealidad obtenida indica la aplicabilidad de los dos modelos; el coeficiente de regresión obtenido para el modelo de pseudo-segundo orden fue de R2=0,989 6 y la cantidad máxima de níquel adsorbido en el equilibrio (qe) estimada por el modelo fue de 23,04 mg/g, valor cercano al de qm obtenido por el modelo de Langmuir. El valor de la constante de la razón de adsorción de pseudo-segundo orden, k2, para estas mismas condiciones de adsorción se estimó en 0,002 2 g/mg·s.
ANALISIS DE LOS RESULTADOS
Evaluación de la capacidad de adsorción de níquel de la biomasa de Phyllanthus orbicularis
]]> A pesar de que los modelos de isoterma aplicados no brindan información alguna sobre el mecanismo seguido por el sistema de adsorción, los parámetros obtenidos son útiles para describir al adsorbente utilizado y como elementos de comparación para establecer similitudes y diferencias [7].El modelo de Langmuir es usado con frecuencia, debido a que contiene solo dos parámetros de fácil comprensión que reflejan dos importantes características de los sistemas de adsorción [3]. Sin embargo, debe tenerse en cuenta que este modelo originalmente fue desarrollado a partir de los trabajos realizados con carbón activado como adsorbente para especies moleculares, por tanto, la capa monomolecular considerada por el modelo implica una adsorción basada en la superficie, lo cual no se aplica completamente para los fenómenos de bioadsorción, donde la biomasa suele comportarse como un gel transparente para los iones metálicos en solución [7].
No obstante, varios autores [8, 9 y 3] reportan un buen ajuste de sus datos experimentales con la isoterma de Langmuir, coincidiendo este trabajo con los resultados reportados por ellos (figura. 1).
La tabla 1 muestra que con modelo de Langmuir se obtuvo el valor de máxima capacidad de adsorción para Phyllanthus orbicularis de 44,05 mg/g como qm, el cual constituye un importante parámetro de comparación entre los materiales adsorbentes (tabla 1) [7]. Aunque los mejores valores reportados para la adsorción de níquel, corresponden a los obtenidos con algas marinas como Sargassummuticum y Ascophyllumnodosssum [14, 7], la capacidad de adsorción de Phyllanthus orbicularis muestra valores apropiados que lo convierten en un bioadsorbente atractivo para la recuperación de níquel a partir de residuales de la industria del níquel en Cuba.
Por su parte, el valor relativamente elevado de la constante Kf de la isoterma de Freundlich (0,553 0), muestra la facilidad con que el níquel es adsorbido desde la solución en la biomasa. El valor de n calculado a partir del gráfico (1,675) refleja la intensidad de la adsorción y también significa que la superficie del adsorbente es de naturaleza heterogénea teniendo en cuenta que el recíproco de n se encuentra en valores entre 0 y 1 [17].
La aplicación del modelo de Dubinin-Radushkevich a los datos experimentales (R2=0,817 6) mostró un menor ajuste, sin embargo, permitió inferir un parámetro de utilidad en la evaluación del sistema de adsorción, la Energía libre media de adsorción (E) por mol de bioadsorbente, la que es transferida a la superficie del sólido desde una distancia infinita en el seno del fluido. Este parámetro es habitualmente usado para distinguir un proceso de adsorción física de uno de adsorción química [18, 19, 3]. Para valores de E menores de 8 kJ/mol, se infiere que el proceso de bioadsorción es de naturaleza física en la que intervienen las fuerzas de interacción débiles electrostáticas de Van der Vals; valores de E entre 8 y 16 kJ/mol, indican que en el proceso de bioadsorción predomina el intercambio de iones y para valores de E superiores a 16 kJ/mol, entonces se considera que la bioadsorción es de naturaleza química, predominando la formación de enlaces estables entre el adsorbente y los iones metálicos.
En la serie de resultados experimentales con soluciones deNi(NO3)2·6(H2O) a pH 6,5, el valor de E obtenido fue de 40,16 kJ/mol, lo que según el criterio derivado del modelo de Dubinin-Radushkevich, se corresponde con un proceso mediado por la adsorción química con la formación de enlaces estables entre los grupos funcionales presentes en la biomasa y los iones metálicos.
Esmaeili y Beni [3], reportan valores de E de 4,969 kJ/mol para biomasa de Sargassumglaucescens adsorbiendo níquel a partir de soluciones sintéticas, concluyendo que para este material predomina la adsorción de naturaleza física. Por su parte, Allaboun y Abu Al-Rub [20], refieren valores de E de 14,1 kJ/mol para biomasa de palmera adsorbiendo níquel, afirmando que para este bioadsorbente predominó el intercambio iónico, lo cual fue comprobado por los autores al determinar la liberación de iones de Ca2+, Mg2+ y K+, asociado a la adsorción de níquel. Estos resultados reportados en la literatura junto a los obtenidos en el presente estudio permiten afirmar que la naturaleza de la adsorción de níquel difiere para los distintos tipos de biomasa, siendo necesario el estudio detallado para cada una de ellas.
Efecto del pH en la adsorción de níquel por Phyllanthus orbicularis en soluciones sintéticas
La literatura reporta que el parámetro de mayor influencia en la adsorción de iones metálicos es el pH de la solución que entra en contacto con el bioadsorbente [7, 18, 6, 21, 3]. Los resultados experimentales obtenidos, confirma que la adsorción del níquel en la biomasa de Phyllanthus orbicularis es muy dependiente del pH. El mayor valor de adsorción de níquel por Phyllanthus orbicularis fue obtenido a pH 6,5 notándose un incremento de la capacidad de adsorción con el incremento del pH de la solución (44,05 mg/g). Este comportamiento ha sido señalado previamente por varios autores para otros bioadsorbentes con respecto a este mismo metal. [7, 20, 6, 21, 3]
]]> A valores de pH bajos la adsorción de níquel puede verse reducida debido a la competencia que se establece por los sitios activos entre los protones y los iones metálicos [7]. Adicionalmente, es conocido que a bajo pH, algunos de los grupos funcionales, tales como los grupos carboxílicos, pierden la capacidad de unirse a los iones metálicos presentes en la solución [20]. Al incrementarse el pH, las cargas negativas en la biomasa aumentan y el estado iónico de algunos ligandos como los carboxilos, favorecen el establecimiento de enlaces con los iones metálicos.Basado en el modelo de Langmuir, puede calcularse una constante adimensional definida por Webber y Chakkravorti, [3] denominado factor de separación (RL) el cual está relacionado con la constante KL obtenida del modelo. Esta constante indica que la naturaleza de la adsorción puede ser desfavorable si RL>1, lineal si RL=1, favorable si 0<RL<1 e irreversibles en caso de que RL=0.
Los resultados experimentales obtenidos, revelan que el Factor de separación se mantiene en valores favorables para el rango de concentraciones y pH estudiados, indicando la capacidad que tiene la biomasa de Phyllanthus orbicularis para adsorber níquel bajo diversas condiciones.
Evaluación de la capacidad de adsorción de níquel de la biomasa de Phyllanthus orbicularis utilizando un residual industrial
Generalmente las isotermas de adsorción para el níquel son obtenidas a partir de soluciones con pH inferior a 7, pues por encima de este valor, el níquel comienza a precipitar interfiriendo con el proceso de adsorción, por lo que resulta difícil a nivel macroscópico separar el efecto de la bioadsorción del causado por la precipitación [7]. Sin embargo, los residuales generados en el proceso Caron, poseen en su mayoría un pH que oscila entre 8,4 y 10. En estas condiciones el níquel permanece en solución debido a que se encuentra formando complejos con el amoniaco presente en el residual. Cualquier material que se pretenda utilizar para adsorber el níquel presente en el residual de esta industria, debe entonces, ser capaz de mantener sus capacidades de adsorción en las condiciones antes mencionadas.
Los ensayos en los que se utilizó efluente industrialmostraron data con buen ajuste al modelo de Langmuir (R2=0,990 2). Se obtuvo una máxima capacidad de adsorción para Phyllanthusorbicularisde 26,25 mg/g, valor que resultó inferior al obtenido anteriormente con soluciones sintéticas de Ni(NO3)2·6(H2O), lo que puede estar dado por la presencia en la solución de elementos que compiten con el níquel por los grupos funcionales responsables de la adsorción.
El valor del factor de separación obtenido en la serie de experimentos con residual industrial resultó ser de 0,188, confirmando que la bioadsorción del níquel por la biomasa de Phyllanthus orbicularis resulta un proceso favorable, semejante a lo previamente inferido en los experimentos con soluciones sintéticas de Ni(NO3)2·6(H2O).
Para las condiciones experimentales presentes durante el tratamiento del residual industrial con la biomasa de Phyllanthus orbicularis, la constante Kf de la isoterma de Freundlichfue de valor elevado (2,674), lo que confirma que la adsorción del níquel es un proceso que ocurre con facilidad, comprobado previamente en los experimentos con soluciones sintéticas a pH inferiores. El valor de n calculado a partir de la pendiente de la recta de mejor ajuste (2,15), conduce a un proceso intenso y coincide en indicar que la superficie del adsorbente es de naturaleza heterogénea teniendo en cuenta que el recíproco de n se mantiene en valores entre 0 y 1 [17].
El valor de E obtenido (267,26 kJ/mol), indica que para las condiciones ensayadas, también existen evidencias de un proceso mediado por la adsorción química donde predomina la formación de enlaces estables entre los grupos funcionales presentes en la biomasa y los iones metálicos, según el criterio derivado del modelo de Dubinin-Radushkevich(R2=0,922 1) con coeficiente mayor que el obtenido ensoluciones sintéticas de Ni(NO3)2·6(H2O) evidenciando un mejor ajuste.
Evaluación cinética de la bioadsorción del níquel presente en el residual industrial en biomasa de Phyllanthus orbicularis
]]> Los resultados muestran que el 60 % del níquel es adsorbido en los primeros 20 min, transcurriendo el proceso más lentamente hasta alcanzar los 60 min aproximadamente. A partir de este tiempo el sistema no adsorbe más níquel alcanzando el equilibrio, evidenciándose que un tiempo de contacto de 1 h es suficiente para lograr la máxima adsorción de níquel posible por Phyllanthus orbicularis (figura 4).Los valores de los parámetros obtenidos para los modelos de pseudo-primer y pseudo-segundo orden, evalúan el mecanismo cinético del proceso de bioadsorción de níquel por la biomasa de Phyllanthusorbicularis (tabla 4). El comportamiento lineal conduce a la aplicabilidad de los dos modelos. Sin embargo, el valor del coeficiente de regresión obtenido para el modelo de pseudo-segundo orden (R2=0,989 6) explica un mayor grado de ajuste de los datos experimentales a una cinética de pseudo-segundo orden, lo que también es una predicción de la prevalencia de un mecanismo de adsorción química, como es el paso limitante de la velocidad de reacción. El modelo estimó la cantidad máxima de níquel adsorbido en el equilibrio (qe) en 23,04 mg/g, cercano al valor de qm obtenido por el modelo de Langmuir. El valor de la constante de la razón de adsorción de pseudo-segundo orden, k2, para estas mismas condiciones de adsorción se estimó en 0,002 2 g/mg·s.
La bioadsorción de níquel sigue cinéticas distintas para diferentes materiales, de esta forma Allaboum y col.[20]reportan que la bioadsorción de níquel por hojas de palmeras siguen una cinética de pseudo-segundo orden con un valor de la constante k2 de 0,043 g/mg·s y qe= 20,4 mg/g, similar a lo reportado en el presente trabajo. Sin embargo, otros autores refieren que las nanopartículas de Sargassumglaucescens mostraron una cinética de pseudo-primer orden al adsorber níquel de soluciones artificiales a 33 °C estimando un valor de la constante k1 de 0,079 1/min y qe de 11,587 mg/g [3].
CONCLUSIONES
La capacidad de adsorción de níquel de la biomasa de Phyllanthus orbicularis se estableció a partir de soluciones sintéticas y del residual industrial de la planta de Calcinación de la Empresa del níquel "Comandante Ernesto Che Guevara", la cual fue de 44,05 y 26,25 mg/g respectivamente, la misma se incrementa al aumentar el pH y la concentración inicial de níquel en el efluente y se reduce al incrementar la concentración de biomasa. El proceso sigue una cinética de pseudo-segundo orden y de acuerdo a los valores de energía libre de adsorción obtenidos a través del modelo de Dubinin-Radushkevich (267,26 kJ/mol), la naturaleza de la misma se corresponde con un proceso mediado por la adsorción química donde predomina la formación de enlaces estables entre los grupos funcionales presentes en la biomasa y los iones metálicos.
BIBLIOGRAFIA
1. ABDEL-GHANI, NOUR T. and GHADIR A. El-CHAGHABY. "Biosorption for metal ions removal from aqueous solutions: a review of recent studies", International Journal of Latest Research in Science and Tech. 2014, Vol. 3, núm. 1, p. 24-42.
]]>2. MACEK, T. and MARTINA, Mackova. "Potential of Biosorption Technology". 2011.
3. ESMAEILI, A., AGHABABAI,Beni. "Biosorption of nickel and cobalt from plant effluent by Sargassumglaucescens nanoparticles at new membrane reactor". Int. J. Environ. Sci. Technol. 2015, Vol.12, p. 2055-2064.
4. KIDD, P.S. et al. "Aplicación de plantas hiperacumuladoras de níquel en la fitoextracción natural: el género AlyssumL". Ecosistemas. 2007, Vol.16, núm.2, p. 26-43.
5. SAO, Kaja, et al. "Biosorption of Ni(II) Ions from Electroplating Industrial Effluent using Tinosporacardifolia Biomass". Civil and Environ. Research. 2014, Vol. 6, núm.10, p. 91-100.
6. BAYRAMOGLU, G., ARICA, MY, ADIGUZEL, N. "Removal of Ni (II) and Co (II) ions using native and acid treated Ni-hyoeraccumulator plant Alyssum discolor from Turkish serpentine soil". Chemosphere. 2012, Vol. 89, núm.3, p. 302-309.
]]>7. HOLAN, Z R and VOLESKY, B., "Biosorption of Lead and Nickel by Biomass of Marine Algae". Biotechnol and Bioengineering. 1994, Vol.43, p. 1001-1009.
8. MALKOC, Emine and YASAR, Nuhoglu. "Investigations of nickel (II) removal from aqueous solutions using tea factory waste". J. of Hazardous Mat. 2005, Vol B127, p.120-128.
9. AHMADY-ASBCHIN, Salman, et al. "Potential of Azollafiliculoides in the removal of Ni and Cu from wastewaters". African J. of Biotech. 2012, Vol.11, núm. 95, p. 16158-16164.
10. RAO, M., PARWATE, A.V., and BHOLE, A.G. "Removal of Cr 6+ and Ni 2+ from aqueous solution using bagasse and fly ash". Waste Manage. 2002, Vol. 22, p. 821-830.
11. REHMAN, H., et al. "Sorption studies of Nickel ion On to Sawdust of Dalbergiasissoo". J. Chin. Chem. Soc. 2006, Vol. 53, p. 1045-1052.
]]>12. PATIL, S., RENUKDAS, S., and PATEL,N. "Kinetic and Thermodynamic study of removal of Ni (II) ions from aqueous solutions using low cost adsorbents". International J. of Enviromental Science. 2012, Vol. 3, núm.1.
13. KAPUR, M. and MONDAL, M. K. "Adsorption Kinetics and Isotherms for Cu(II) and Ni(II) Ions Removal from Electroplating Industrial Wastewater". International J. of Applied Eng. Research. 2014, vol 9, núm.1, p. 47-52.
14. GONZÁLEZ-BERMÚDEZ, et al. "Nickel biosorptionusingGracilaria caudata and Sargassummuticum". Chemical Engineering Journal. 2011, Vol. 166, núm. 1, p. 122-131.
15. SENTHIL-KUMAR, P., et al. "Removal of Nickel (II) frim aqueous solutions by Ceralite IR-120 cationic exchange resins". J. of Eng. Sci. and Tech. 2010, Vol. 5, núm.2, p. 232-243.
16. KARTHIKA, C. and SEKAR, M. "Comparison studies of Adsorption Properties on Ni (II) Removal by Strong and Weak acid Cation-exchange Resins". Research J. of Chem. Sci. 2013, Vol. 3, núm.3, p. 65-69.
]]>17. AIKPOKPODION, P.E, et al. "Biosorption of Nickel (II) from Aqueous Solution Using Waste Tea (Camellacinencis) Materials". American-Eurasian J. of Toxicological Sci. 2010, Vol. 2, núm. 2, p.72-82.
18. ITODO, A.U. and ITODO, H.U. "Sorption Energies Estimation Using Dubinin-Radushkevich and Temkin Adsorption Isotherms". Life Science Journal. 2010, Vol.7, núm.4, p. 31-39.
19. DADA, A.O., et al. "Langmuir, Freundlich, Temkin and Dubinin-Radushkevich Isotherms Studies of Equilibrium Sorption of Zn2+ Unto Phosphoric Acid Modified Rice Husk". IOSR J. of Applied Chem. 2012, núm.1, p. 38-45.
20. ALLABOUN, H. and ABUAL-RUB, F., "Dynamics, Mechanistics and Equilibrium Studies for the Biosorption of Nickel on Palm Tree Leaves". Jordan J. of Civil Eng. 2008, Vol. 2, núm.2, p. 124-138.
21. AHMADY-ASBCHIN, Salman, et al. "Study of nickel and copper biosorption on brown algae Sargassumangustifolium: application of response surface methodology (RSM)". Environ. Tech. 2013, Vol. 34, núm.16, p. 2423-2431.
]]>22. HO, Y.S. and MCKAY, G. "Pseudo-second order model for sorption processes". Proc. Biochem. 1999, Vol. 34, p. 451-465.
Recibido: Septiembre 2016
Aprobado: Diciembre 2016
Lic. Ariel Díaz-PuigI. Empresa Comandante Ernesto Che Guevara, Moa, Holguín, Cuba
]]>