
La corrosión en la unidad de reformación catalítica de nafta de una refinería de petróleo (I Parte)
Corrosion in the catalytic naphtha reforming unit of a petroleum refinery (Part I)
MSc. Katiuska Santos-CedeñoI, Dr. Jorge A. Domínguez-DomínguezII, Dr. Rigoberto Marrero-ÁguilaII, Ing. Yuselkys Cordero-ZamoraIII
I Universidad de Oriente, Santiago de Cuba, Cuba. katiuska@uo.edu.cu
II Universidad Tecnológica de la Habana, La Habana, Cuba ]]>
III Central Termoeléctrica "Máximo Gómez Báez", Mariel, Artemisa, Cuba
Resumen
Los problemas corrosivos presentes en el sistema de enfriamiento de la unidad de reformación catalítica de nafta de una refinería del occidente del país, traen consigo el intenso deterioro de intercambiadores de calor, y además ocasionan significativas pérdidas de producción con importantes afectaciones económicas. Estos deterioros se presentaron cuando comenzó a emplearse un nuevo catalizador Pt/Re en base alúmina en el reformador de lecho fijo, el cual requiere un mayor porcentaje de compuestos clorados durante su regeneración. En este trabajo se realizó un estudio a escala de laboratorio mediante ensayos gravimétricos y electroquímicos, que permitieron la obtención de las velocidades de corrosión para los distintos metales, empleados en la construcción del equipamiento, y expuestos al medio corrosivo existente en dicha unidad de reformación catalítica. Como resultado, se determinó que los gases que aportan la mayor acidez al medio son el HCl y el SO2, y en menor medida el CO2 y el H2S. Se comprobó que la adición de sosa es suficiente para neutralizar todos los gases ácidos generados durante el proceso de regeneración del catalizador. Sin embargo, se observó que los materiales metálicos presentes que conforman el equipamiento: acero al carbono, aluminio y latón son severamente afectados por corrosión debido a la acción corrosiva de estos gases.
Palabras clave: corrosión, reformación catalítica, refinería de petróleo.
Abstract
Corrosive problems showed up in the cooling system of the naphtha catalytic reforming unit of a petroleum refinery, not only implies intense deterioration of heat exchangers, but also significant operation losses and consequently significant economic affectations. These problems arose since the use of a new catalyst made with Pt/Re based on alumina in the fixed-bed reformer, which requires higher concentration of organic chlorine compounds during regeneration. In this work, a study was performed at a laboratory scale using gravimetric and electrochemical tests, which allowed obtaining corrosion rates for the various metals used in the construction of the equipment, exposed to existing corrosive medium of the aforementioned catalytic reforming unit. As a result of this study it was determined that the gases that contribute to the highest acidity of the medium are HCl and SO2, and in lesser extent CO2 and H2S. However, it was observed that the metallic materials which make up the equipment: carbon steel, aluminum and brass are severely affected by corrosion due to the corrosive action of these gases.
Keywords: corrosion, catalytic reforming, petroleum refinery.
]]>
INTRODUCCION
El desarrollo de la industria petrolera cubana evidencia un aumento en los últimos años. La explotación de este hidrocarburo reporta cuantiosas ganancias al país, así como la utilización de sus derivados entre los que se encuentra la gasolina. El componente principal de la gasolina es la denominada nafta reformada que se obtiene durante el proceso de reformado de la nafta pesada de destilación directa del crudo. El proceso de reformación catalítica cuenta con dos secciones: la sección de hidrofinación y la de reformación de la nafta. Esta última tiene como objetivo aumentar el octanaje de la gasolina y producir hidrógeno [ 1,2 ].
En la unidad de reformación de la refinería objeto de estudio, luego de un largo período de conservación de sus unidades se cargó, en el reformador de lecho fijo, un catalizador de última generación serie RG 682A de Pt/Re, en base alúmina. Al reactivarse el proceso, comenzaron a surgir fugas de productos en los equipos del sistema de enfriamiento, pertenecientes al circuito de reacción del reformador. Las incidencias se acrecientan en la etapa de regeneración del catalizador ya que este requiere de un contenido de cloro mayor que el catalizador concebido en el diseño y puesta en marcha de la refinería. Esto implica la utilización de una mayor concentración del compuesto orgánico clorado y como consecuencia la generación de mayores cantidades de cloruro de hidrógeno (HCl), el cual circula conjuntamente con otros gases y vapores por los intercambiadores del sistema de refrigeración. Para la neutralización de los ácidos formados, la tecnología original preveía la inyección de una solución de hidróxido de sodio (NaOH) al 2 % en peso, pero al elevarse la concentración de HCl, esta solución resultó insuficiente, aumentándose su concentración a cuatro. Para obtener una buena neutralización, la inyección de sosa se realiza a un flujo entre 25-35 % del caudal de diseño. A medida que se produce el agotamiento de la solución neutralizante se evidencia un descenso en el pH, produciéndose ataques de gran magnitud en los materiales metálicos de construcción del equipamiento. Los intervalos de concentración de los diferentes gases que componen la corriente de salida del reformador durante la cloración del catalizador se muestran en la tabla 1 [3].
Tabla 1
Intervalo de concentraciones de los componentes de la corriente de salida del reformador

La figura 1 muestra un esquema simplificado de la planta de reformación catalítica.
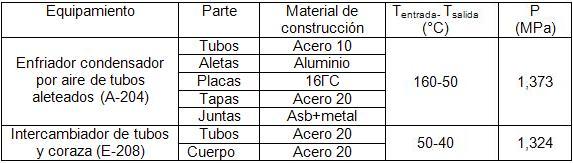
El problema de corrosión más crítico es el enérgico deterioro de los cabezales, tubos y placas de los intercambiadores (A-204) y (E-208), como se muestra en las figuras 2 y 3. Además, se han afectado las válvulas de succión de los compresores de gas de reciclo (C-202). Los materiales metálicos empleados en la construcción de los mismos y sus parámetros de operación se muestran en la tabla 2.
]]> La concentración máxima reportada (tabla 1) para los gases ácidos es de 200 mL/m3 , que provocan un ataque significativo a temperatura ambiente pudiendo ser mayor a 100 ºC o más. Si se tiene en cuenta que los procesos electroquímicos de corrosión, controlados por transferencia de carga, pueden duplicar su velocidad cada 10 ºC y que un aumento de temperatura de 50 ºC incrementa la velocidad de corrosión unas 15 veces cuando hay HCl en el medio, es de esperar un elevado ataque en este sistema.Tabla 2
Materiales metálicos de construcción y parámetros de operación de los equipos más afectados
Como es conocido, la velocidad de reacción entre un ácido y una base es enorme si ambos son electrolitos fuertes como el HCl y la sosa. Para el caso de la neutralización de ácidos débiles con bases fuertes el proceso es más lento y aun así las velocidades son altas. Sin embargo, se produce el ataque corrosivo en este sistema.
Este trabajo tiene como objetivo determinar las causas que provocan el deterioro corrosivo del equipamiento del sistema de enfriamiento de la unidad de reformación catalítica de la nafta.
MATERIALES Y METODOS
Con el objetivo de corroborar lo expuesto con anterioridad y en vías de ofrecer soluciones prácticas a los problemas corrosivos existentes, se planificaron los experimentos que se exponen a continuación.
Preparación de las disoluciones de trabajo
]]> Se preparó, a partir de reactivos puros para análisis y agua destilada, una disolución que simula el medio corrosivo, con la siguiente composición química: Na2S + Na2CO3 + Na2SO3 (0,1 N de cada sal). Con este fin, se preparó una disolución concentrada de sulfuro de sodio a partir de Na2S x nH2O, se valoró mediante el método yodométrico para calcular su concentración y por dilución intermedia, se preparó la disolución de Na2S 0,1 N. Los reactivos Na2CO3 y Na2SO3 se pesaron y se añadieron directamente [8].Ensayo Nº1. Dependencia del valor de pH de la disolución vs volumen de disolución de HCl
Para caracterizar la relación entre la acidez libre y la neutralizable en el agua condensada procedente del gas de regeneración, se determinó la dependencia del valor de pH de la disolución de trabajo con el volumen de disolución de HCl añadido, mediante el siguiente procedimiento: Se vertieron en un vaso de precipitado 100 mL de disolución salina agitándose suavemente en una plancha con agitador magnético. Posteriormente se introdujo con cuidado el electrodo de vidrio y se midió el pH inicial. Se llenó una bureta con disolución de HCl (5 mol/L) y se inició adición de 1 mL en forma paulatina, midiendo el pH después de cada adición, hasta que el mismo alcanzó un valor estable de 0,5.
Como resultado de este experimento se pudo obtener la curva de la figura 4, la cual muestra la dependencia del pH de la disolución vs volumen de HCl.
Ensayo Nº2. Determinación gravimétrica de la velocidad de corrosión del acero en la disolución de trabajo a diferentes pH
Este ensayo permite definir qué grado de neutralización es conveniente alcanzar para lograr el efecto anticorrosivo deseado. Para ello, partiendo de la disolución de trabajo, se ajustaron tres valores de pH 0,5, 4 y 7,5 mediante la adición de HCl (5 mol/L). En todos los ensayos gravimétricos se utilizaron probetas rectangulares, tubos de ensayo de 100 mL, gradillas para tubos gruesos, pié de rey y balanza analítica.
Las probetas de acero fueron tratadas inicialmente para preparar su superficie mediante decapado con ácido clorhídrico y luego lijadas con papel esmeril. Posteriormente fueron medidas, desengrasadas con cal de Viena, enjuagadas, secadas con papel de filtro y acetona y pesadas. Los ensayos se realizaron a temperatura ambiente y las probetas fueron expuestas al medio corrosivo durante 20 h. Al transcurrir el tiempo de ensayo se secaron y pesaron nuevamente. Se realizaron cinco réplicas en cada caso.
Ensayo Nº3. Determinación de la velocidad de corrosión del aluminio en medio ácido y alcalino
Este ensayo gravimétrico tiene como objetivo estimar el daño que pueden sufrir las aletas de aluminio de producirse una perforación en los tubos del enfriador por aire A-204. Se emplearon probetas de aluminio y como medios, la solución de trabajo a pH 0,5 ajustado con HCl y una disolución de NaOH al 4 % en peso. Para la preparación de la superficie de las probetas se empleó un procedimiento similar al del Ensayo N O2, solo que en esta ocasión las probetas no fueron decapadas. El tiempo de exposición para el medio ácido fue de 4 h y para el medio básico de 1 h.
Ensayo Nº4. Comportamiento de los latones y del par latón-acero en el sistema corrosivo estudiado
]]> Para este ensayo se empleó la disolución de trabajo a pH 0,5, ajustado con HCl y probetas de latón común. La gravimetría se efectuó como en los casos anteriores con un tiempo de ensayo de 20 h y de 168 h (7días) para evaluar la sensibilidad del latón al descincado.La corrosión galvánica del par metálico latón-acero se midió por el método galvanostático empleando una técnica operatoria conocida. Como electrodo auxiliar se empleó un electrodo de platino y como electrodo de referencia uno de Ag/AgCl. Los resultados de este ensayo permitieron determinar la conveniencia o no de colocar un mazo de tubos de latón en el intercambiador E-208 en lugar de uno de acero al carbono o cambiar la placa o espejo de latón por acero. Para evaluar la velocidad de corrosión por par galvánico se empleó el método de extrapolación o de las curvas completas de polarización [9].
Para el cálculo de la velocidad de corrosión se emplearon los índices: gravimétrico (DP) y de penetración o disminución de espesor (DE), mediante las siguientes expresiones matemáticas:

El factor 8,76 permite obtener DE en (mm/año) a partir de DP en (g/m2 h) y la densidad del material metálico ρ en (g/cm3 ). El valor de DE en (mm/año) también puede calcularse mediante la densidad de corriente de corrosión (ic), obtenida a partir de métodos electroquímicos, según:[9]

El cálculo del índice de penetración (DE) permite establecer la estabilidad de un metal en un medio agresivo dado. Los criterios de estabilidad se deben a Fontana y se muestran en la tabla 3 [10].
Tabla 3
Criterios de estabilidad para medir la resistencia a la corrosión

RESULTADOS Y DISCUSION
Primeramente es necesario conocer si todos los gases de reacción ácida son responsables del ataque inadmisible a los materiales metálicos presentes o sólo los más fuertes y si existe efecto sinérgico en la acción corrosiva en el caso de mezclas gaseosas.
Los valores de las constantes de disociación de los gases involucrados mostrados en la tabla 4, ofrecen información sobre la acidez que aporta cada uno a la corriente de salida del reformador. Como puede apreciarse, el HCl se encuentra totalmente disociado, y en menor medida el H2SO3 , casi 100 veces más débil. Ellos, y en especial el HCl deben ser los principales responsables del ataque observado. Además, se conoce que en otras etapas de la regeneración donde no se genera el HCl o este se forma en cantidades pequeñas, el ataque es mucho menor. No debe descartarse alguna posible oxidación del SO2 a SO3 en la zona caliente y en contacto con hierro que funge como catalizador de esta reacción, lo cual incrementaría el ataque por formación de ácido sulfúrico fuerte. Esta posibilidad no ha sido comprobada experimentalmente. El H2CO3 y el H2S, por su debilidad, prácticamente no disminuyen el valor de pH, sobre todo si se encuentran en presencia de ácidos más fuertes. Sin embargo, el H2S, se considera un activador anódico de la corrosión y de la hidrogenación del acero al adsorberse sobre el metal en forma de HS - y formar depósitos oscuros de sulfuro de hierro con deficientes propiedades protectoras, que frecuentemente funcionan como cátodo, acelerando la corrosión local del acero. No obstante, en presencia de cantidades apreciables de HCl los sulfuros de hierro apenas se depositan. Se desconoce cuál es el resultado de la acción conjunta de estos ácidos en el sistema considerado [ 4,5 ].
Tabla 4
Constantes de disociación de los gases ácidos involucrados en el sistema a 25 ºC

Además de los gases ácidos, el O2 constituye un agente oxidante fuerte, aunque su cinética es mucho más lenta que la corrosión por H + de los ácidos. En cualquier caso, refuerza la acción corrosiva de estos.
El vapor de agua que no es corrosivo para estos aceros, al condensar provoca la disolución de los gases ácidos y el proceso de corrosión electroquímica. En ausencia total de agua, la corrosión por los gases ácidos y el O2 a esas temperaturas intermedias sería despreciable. La humedad del gas se incrementa con el recorrido gracias a la evaporación del agua de la solución de sosa cáustica. De los gases presentes sólo el N2 inerte y el CO reductor no coadyuvan al ataque corrosivo. Los valores de saturación de estos gases en agua para diferentes temperaturas a 101,3 kPa se muestran en la Tabla 5. Se puede verificar que los gases más ácidos son los de mayor solubilidad, especialmente el HCl, el cual es capaz de formar soluciones de muy bajo pH. Si bien la solubilidad de los gases disminuye con el aumento de temperatura, cuyo máximo en este caso está entre 130-140 ºC, aumenta con su presión parcial y por ende con la presión total de los gases que es de 0,75-1,5 MPa, por lo que debe producirse un efecto positivo neto en su solubilidad.
Tabla 5 ]]> Solubilidad en agua de los gases ácidos a diferentes temperaturas y 101,3 kPa
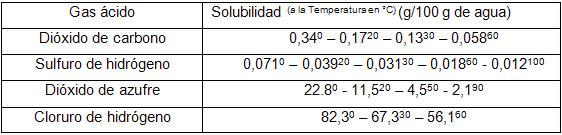
No obstante, la relativamente baja solubilidad del CO2 respecto a la del HCl, como su concentración y presión parcial son mucho mayores, podría competir con este en lo referente a la magnitud de la reacción de neutralización con la sosa. Sólo la medición analítica de la fase gaseosa o de la líquida en distintos puntos de su recorrido, puede describir el proceso de adsorción de los diferentes gases [4,5].
Para conocer el grado de neutralización que es conveniente alcanzar con el objetivo de disminuir la velocidad de corrosión del acero hasta lograr el efecto anticorrosivo deseado, se realizó el Ensayo N o 1 que aportó la curva de valoración mostrada en la figura 4. Se puede observar la contribución correspondiente a la liberación de protones H + por parte de los ácidos débiles presentes (H2CO3 y H2S) en la disolución, lo cual está relacionado con los valores de sus constantes de disociación (tabla 4). Esta curva permite preparar disoluciones de trabajo a diferentes valores de pH de interés.
El pH típico del agua condensada saturada con CO2 es cercano a cuatro o un poco más bajo. También se plantea que la saturación del agua a pH 7 con H2S a presión parcial igual a 100 kPa y temperatura ambiente disminuye su pH a 4, por tanto una disolución saturada de estos ácidos tendrá un pH ~ 4[5,11].
La dependencia de la velocidad de corrosión del hierro y los aceros con el pH se conoce. A valores de pH entre 4 y 9 la corrosión es prácticamente independiente del pH. A valores cercanos a cuatro comienza el desprendimiento de H2 gaseoso a partir de la solución debido a la presencia de los ácidos débiles, lo cual provoca ligeros aumentos en la velocidad de corrosión comparados con los obtenidos a valores de pH cercanos a la neutralidad y mayores. Pequeñas cantidades de ácido clorhídrico adicionadas al medio, por encontrarse este ácido completamente disociado debido a su fortaleza, desplazan el pH hacia valores menores a cuatro, aumentando aceleradamente el desprendimiento de H2 y la velocidad de corrosión.
Por lo anteriormente expuesto las disoluciones de trabajo escogidas para determinar la velocidad de corrosión de los metales empleados en este estudio se ajustaron a pH iguales a 0,5 (región francamente ácida con predominio de la presencia de HCl), 4 (región cercana a la neutralidad con predominio de la acción de los ácidos débiles presentes en el medio) y 7,5 (región neutral). El ajuste se realizó mediante la adición de diferentes volúmenes de HCl obtenidos a partir de la curva mostrada en la figura 4.
Como se planteó, el problema de corrosión consiste en el enérgico deterioro de tubos y placas de los intercambiadores A-204 y E-208, fundamentalmente durante la etapa de oxicloración del catalizador en el proceso de regeneración del mismo. Parece indicar que la velocidad de transferencia de masa desde la fase gaseosa a la fase líquida neutralizante no es lo suficientemente efectiva en las primeras etapas de contacto entre fases, por lo que los vapores condensan conjuntamente con la humedad de la corriente gaseosa sobre la superficie metálica de los intercambiadores sin haber sido neutralizados por la sosa. La primera zona favorable para la condensación del vapor de agua es la placa fría y el interior de los tubos de los enfriadores por aire A-204. Esto también se evidencia en la zona de entrada de los gases a los E-208.
Otro inconveniente es que el fluido heterogéneo (mezcla de gases y solución neutralizante) circula por dentro de los tubos, lo que minimiza el área de transferencia de masa entre las fases. Los gases apenas son neutralizados antes y al pasar por los A-204. Así en los conductos de entrada, la fase gaseosa ácida fluye por encima de la líquida básica, la cual no ebulle a 130 ºC debido a las elevadas presiones de operación y sólo alguna cantidad de agua es vaporizada teniendo en cuenta que el NaOH no es un compuesto volátil, por tanto, el contenido de gases ácidos es aún elevado al entrar a los A-204. Una vez dentro de las cajas distribuidoras de estos intercambiadores, la fase gaseosa ácida circulará por los tubos superiores y el líquido por los inferiores, no estando completamente en contacto las fases, por lo que la neutralización apenas tiene lugar. Esto provoca que las perforaciones deban producirse mayormente en los tubos superiores o medios, como puede observarse en la figura (2a).
]]> Como resultado de la falta de contacto interfacial los gases más ácidos, llegan a los E-208 sin haber sido neutralizados totalmente y crean problemas a la entrada (figura 3a). Como se aclaró anteriormente, en estos intercambiadores el fluido bifásico fluye ahora por la coraza y se pone en contacto con la cara exterior de los tubos de intercambio, la cual se moja con la solución alcalina y funciona como el relleno de una torre de adsorción al aportar un área de contacto entre fases y de transferencia de masa grande. Es por eso que, a la salida de estos equipos, o lo que es igual, en el tanque separador B-204, el pH de la sosa se acerca a la neutralidad. Los resultados obtenidos en el Ensayo NO2 corroboran lo antes expuesto. Los valores de DP y DE obtenidos mediante (1) y (2), para el acero al carbono, se reportan en la tabla 6. Se puede observar que la velocidad de corrosión del acero a pH 0,5 es un orden mayor que las obtenidas a pH 4 y 7,5, lo que evidencia un mayor deterioro del metal en disoluciones de menor pH. Empleando los criterios de estabilidad mostrados en la tabla 3, se observa que a pH 4 y 7,5 el acero al carbono presenta una resistencia buena comparada con la resistencia inaceptable obtenida para pH 0,5.Si la disolución formada por el agua condensada y los gases ácidos hubiera sido neutralizada antes de entrar a los A-204 y E-208, los efectos corrosivos no tuvieran tal magnitud. De los valores de velocidad de corrosión reportados en la Tabla 6, se observa claramente que el ataque corrosivo, aun con una mediana neutralización, no es de gran intensidad por lo que los daños serían menores a los ocasionados. Otra manera de evidenciar la no neutralización del HCl, se presenta en las aletas de aluminio de los tubos del intercambiador A-204, ya que una vez perforados los tubos de acero al carbono por corrosión ácida, los gases atacarán las mismas. De existir arrastre de solución alcalina por el gas, las aletas de aluminio estarían expuestas al ataque por esta disolución.
Tabla 6
Velocidades de corrosión promedio del acero al carbono a diferentes valores de pH

Tabla 7
Velocidades de corrosión promedio del aluminio en medio ácido y en disolución de NaOH

La tabla 7 muestra los valores promedios calculados mediante (1) y (2) de DP y DE para el aluminio técnico. Se observan los mayores valores para la disolución de NaOH al 4 %, infiriéndose por el deterioro presente que debe existir, en este caso, un exceso de solución neutralizante que es arrastrada por los gases ácidos.
]]> Los tubos y la placa de los E-208 eran de latón y en la actualidad son de acero 20. Se plantea por parte de los tecnólogos de la planta que los tubos de latón no resisten altas concentraciones de HCl en la etapa de regeneración. Este planteamiento no se justifica, a menos que afecte el desempeño del catalizador por la presencia de posibles sales de cobre y cinc, pues los latones estabilizados contra el descincado son de 10 a 100 veces más resistentes que los aceros frente al HCl a flujo, incluyendo a los aceros inoxidables. Sólo criterios económicos o de disponibilidad pueden justificar dicho cambio [4].Se realizó una evaluación de la velocidad de corrosión del latón para determinar la conveniencia o no de colocar un mazo de tubos de latón en el intercambiador E-208 en lugar del actual de acero al carbono o cambiar la placa o espejo de latón por acero. Los valores de DP y DE promedios, obtenidos mediante (1) y (2), para el latón en medio ácido se muestran en la tabla 8. Al comparar estos valores con los obtenidos para el acero al carbono (tabla 6) se puede observar que las velocidades, aunque inferiores, son del mismo orden de magnitud.
Empleando los criterios de resistencia mostrados en la tabla 3, el latón presenta una pobre resistencia ante este medio, sin embargo, la del acero al carbono es inaceptable. En este caso el ensayo se realizó con latón común por la no disponibilidad de latones estabilizados contra el descincado como es el caso de los latones de aluminio o latón admiralty.
Tabla 8
Velocidad de corrosión promedio del latón en medio ácido
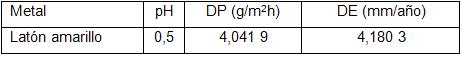
El latón común es susceptible al descincado durante largos períodos de exposición sobre todo en medios estancados, condiciones bajo las cuales se realizó este ensayo. Si se acepta la teoría acerca del mecanismo para el descincado que plantea la disolución del Cu y el Zn y la posterior redeposición del Cu [9], existe la presencia en el medio de iones Cu2+ . Estos iones constituyen un agente oxidante fuerte, se reducen para formar Cu+ , alcanzando grandes densidades de corriente de forma rápida y por tanto aumentando los valores de velocidad de corrosión. Para latones estabilizados o en sistemas a flujo, como es el caso, donde los iones Cu2+ sean arrastrados, la velocidad de corrosión debe ser menor que la mostrada en la tabla 8.
Bajo las condiciones descritas en el Ensayo No.4 se obtuvo, mediante técnicas electroquímicas, la curva característica de la corrosión galvánica del par metálico latón-acero (figura 5). El valor de la corriente galvánica medida fue de 1258,9 m A/cm2 . Mediante (3) se calculó la velocidad de corrosión del acero al carbono obteniéndose el valor de 1,16 mm/año, siendo su resistencia evaluada de regular a pobre.
Mediante los resultados experimentales obtenidos se puede constatar que logrando una neutralización parcial de los gases se evitaría el enérgico deterioro al que se ven expuestos los A-204 y E-208.
]]>CONCLUSIONES
- Se determinó que la causa del severo deterioro por corrosión de los materiales metálicos de construcción de los equipos del sistema de enfriamiento perteneciente al circuito de reacción del reformador (acero al carbono, aluminio y latón), es la acción corrosiva de los gases ácidos, que se generan durante la etapa de cloración del proceso de regeneración del catalizador, los cuales no han sido neutralizados.
- En los experimentos realizados se determinó la estabilidad de los metales presentes en el medio corrosivo a diferentes valores de pH, siendo el aluminio el más deteriorado, debido a su marcado carácter anfótero. En medios alcalinos el efecto fue mayor, lo que evidencia, por el deterioro corrosivo de las aletas de aluminio de los A-204, una pobre neutralización de los gases ácidos al pasar por los tubos, los cuales deterioran al acero y arrastran sosa cáustica consigo.
- Se observó que al alcanzar una neutralización media o superior (4= pH=7) de los gases se obtiene el efecto anticorrosivo deseado.
- Es necesario determinar, si la presencia en el sistema de los gases ácidos que provocan la corrosión se debe a que la cantidad de sosa añadida para su neutralización es insuficiente y en tal caso se necesita conocer la cantidad requerida para reducir el ataque a valores admisibles, si la velocidad de transferencia de masa entre la fase gaseosa ácida y la líquida básica es muy pequeña y por tanto no se logra una neutralización adecuada, o si son ambos factores los que se combinan para provocar una corrosión tan intensa.
- De acuerdo a lo planteado anteriormente, se hace necesario estudiar con más profundidad este sistema para proponer una solución racional al problema, desde el punto de vista técnico económico.
BIBLIOGRAFIA
1. LLUCH URPÍ, J. "Tecnología y Margen de refino". Instituto Superior de la Energía. Curso para CUPET. Ciudad de la Habana. 2009. 335 pp.
2. DELGADO, Alisbel. "Evaluación Energética de la Planta de Tratamiento de crudos de Boca de Jaruco". Tesis de diploma. Instituto Superior Politécnico José Antonio Echeverría, Ciudad de La Habana, 2007.
3. PÉREZ, Irenaldo. "Análisis del proceso de regeneración llevado a cabo en la unidad de reformación catalítica". Cienfuegos. 2010. 10 pp.
4. Groysman, Alec. Corrosion in Systems for Storage and Transportation of Petroleum Products and Biofuels. Identification, Monitoring and Solutions. New York: Springer Science, 2014. 291 pp.
5. RADKEVYCH, O., POKHMURS'KYI, V. I. "Influence of hydrogen sulfide on serviceability of materials of gas field equipment". Materials Science, 2011, vol. 37, núm. 2, pp. 319-332.
6. UHLIG, H.H. Corrosion and corrosion control. New Jersey. Editorial John Wiley and Sons, 2012.
7. KEENAN. J H. Steam Table. Edición Revolucionaria. 1998.
8. APHA, AWWA, WPCF. Métodos Normalizados para el análisis de aguas y residuales: Editorial Díaz de Santos S. A. 4-222 pp.
9. DOMINGUEZ, Jorge A., CASTRO, Dulce M. et al. Introducción a la corrosión y protección de metales. La Habana. Ministerio de Educación Superior. ENPES.1987. 485 p.
10. FONTANA, M. G. and GREENE, N. D. Corrosion Engineering. Editorial Mc Graw Hill, 1978.
11. Neic, S. "Key issues related to modelling of internal corrosion of oil and gas pipelines A review". Corrosion Science, 2010, vol. 49, pp. 43084338.
Recibido: Noviembre 2016
Aprobado: Marzo 2017
MSc. Katiuska Santos-CedeñoI. Universidad de Oriente, Santiago de Cuba, Cuba. katiuska@uo.edu.cu
]]>