Descriptores DeCS: QUITINA/química; ESTABILIDAD DE MEDICAMENTOS; ESPECTROFOTOMETRIA INFRARROJA/métodos. Los estudios de estabilidad por su importancia son considerados actualmente requisito indispensable para el registro y venta de medicamentos. De esta forma se garantiza la integridad de la formulación durante el lapso de tiempo donde ésta cumpla los fines para los cuales fue creada.1
La quitina es un polímero de origen natural que posee actividad como acelerador de la cicatrización y reconstructor hístico.2-4 Su efecto farmacológico, unido a su carácter biocompatible y atóxico, han propiciado su introducción con éxito en diferentes formas farmacéuticas.
Por esta razón, se hace necesario establecer una metodología para evaluar el comportamiento químico de este fármaco. Los métodos químicos de determinación cuantitativa reportados en la bibliografía,5-8 constituyen técnicas indirectas de limitada confiabilidad para su utilización en la estimación del contenido de quitina, ya que se basan en la determinación de sus productos de hidrólisis química o enzimática.
La extremada estabilidad química de la quitina ha sido evaluada en el polvo obtenido en Cuba a partir de los desechos de la industria pesquera.9 Se reporta un tiempo de vencimiento superior a los 5 a, según estudios cinéticos realizados a la hidrólisis ácida del polímero (Nieto OM. Quitina. Su estudio y utilización como fármaco acelerador de la cicatrización. Tesis presentada en opción al título de Doctor en Ciencias Farmacéuticas. Instituto de Farmacia y Alimentos. Universidad de La Habana, 1993).
En el presente trabajo nos proponemos evaluar la combinación de la gravimetría directa con la espectroscopia infrarroja (IR) en el seguimiento de la estabilidad química de la quitina en 3 formas farmacéuticas: suspensión, crema y supositorio.
Suspensión: se tomaron 5 mL, se añadió una mezcla de etanol-agua-NaOH 20 % (10:15:40) y se calentó a temperatura de 50 oC en baño termostatado con agitación.
Supositorios: se colocaron 3 suposi-torios en un balón de reflujo y se añadieron 100 mL de KOH/etanol 0,5 mol/L. Se introdujo el balón en un baño termostatado ajustado a 100 oC y se reflujó durante 30 min con agitación a intervalos.
Crema: se pesaron con exactitud 3 g, se añadió una mezcla de etanol-cloroformo (10:5) y se calentó a temperatura de 60 ± 5 oC en un baño termostatado con agitación constante.
| Forma farmacéutica | Características del lavado | Temperatura de secado |
| Suspensión | Dos fracciones de etanol-agua-NaOH 20 % | |
| Dos fracciones de etanol de 5 mL | ||
| Supositorio | Se arrastran las partículas de quitina con pequeñas porciones de agua destilada hasta completar 400 mL | |
| Cuatro fracciones de etanol de 20 mL | ||
| Crema | Dos fracciones de cloroformo de 5 mL | |
| Dos fracciones de etanol de 5 mL |
| Forma terminada | | Temperatura de almacenamiento |
| Suspensión | Frascos de vidrio ámbar por 120 mL (V) | Ambiente (A) |
| Supositorio | Tiras de aluminio | Ambiente (A) |
| termosellable por | Refrigeración 8-15 oC (R) | |
| 7 supositorios (T) | Climatización 20 oC ( C ) | |
| Crema | Frascos plásticos (P) | Ambiente (A) |
| Frascos de cristal ámbar por 200 g (CA) | Refrigeración 2-8 oC ( R) |
| Forma terminada | | | | |
| Suspensión | r = 0,9998 | texp = 0,921 | CV 80 % = 0,87 % | CV = 0,93 % |
| r2 = 0,9996 | tteo = 2,120 | CV 100 % = 0,63 % | ||
| texp = 1,804 | CV = 0,697 % | CV 120 % = 0,53 % | ||
| tteo = 2,160 | R = 98,56 % | |||
| p = 0,000003 | ||||
| Supositorio | r = 0,9994 | texp = 0,165 | CV 80 % = 1,2 % | CV = 1,0 % |
| r2 = 0,9988 | tteo = 2,160 | CV 100 % = 1,4 % | ||
| texp = 1,530 | CV = 2,0 % | |||
| teo = 2,120 | R = 97,09 % | CV 120 % = 0,5 % | ||
| p= 0,000001 | ||||
| Crema | r = 0,9999 | texp = 2,358 | CV 0 % = 1,21 % | CV = 0,99 % |
| r2 = 0,9998 | tteo = 2,360 | CV 00 % = 1,04 % | ||
| texp = 1,998 | CV = 0,2 % | CV 20 % = 0,89 % | ||
| tteo = 2,160 | R = 98,03 % | |||
| p = 0 | ||||
| Criterio de aceptación | r 3 ³ 0,99 | texp < tteo | CV £ 1,5 % | CV £ 3,0 % |
| r2 _³ 0,98 | CV £ 3,0 % | |||
| texp < tteo | R = 97-103 % | |||
| p << 0,5 |
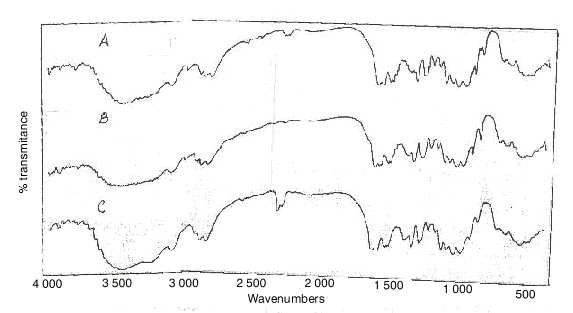
En la figura se muestran los espectros IR obtenidos para cada forma terminada transcurridos 12 meses del estudio, después de procesar las muestras almacenadas a temperatura ambiente por gravimetría.

Como se observa en la figura, existió total coincidencia entre todos los espectros, por lo que al cabo de 1 a, fue quitina y no otra la sustancia que se retuvo por los filtros Gooch. Se mantuvieron en localización e intensidad las bandas asignables a los grupos funcionales, lo cual evidencia que desde el punto de vista químico no ocurrió degradación del principio activo.
Al analizar los espectros IR obtenidos en todos los casos, podemos apreciar una banda ancha de mediana intensidad asig-nada al n O-H, que aparece entre 3 280 y 3 440 cm-1, seguidamente se observa una ban-da característica del n N-H a los 3 120 cm-1. En estado sólido las bandas N-H apare-cen entre 3 330 y 3 060 cm-1 como ban-das múltiples en dímeros cis y polí-meros trans, el OH puede salir hasta 3 200 cm-1. ]]>
En el rango de 1 880-2 960 cm-1 aparecen bandas de mediana intensidad caracterís-ticas del n C-H, simétrico y antisimétrico de grupos metílicos y metilénicos.A los 1 640, 1 555 y 1 320 cm-1 aparecen bandas asignadas a las vibraciones de amida III, II y I respectivamente. La primera correspondiente al n C=O, y las dos restantes pertenecientes al d N-H. Todas son bandas agudas de mediana intensidad. A continuación en el rango de 1 380-1 410 cm-1 aparecen bandas agudas de mediana intensidad, atribuidas a la deformación de doblajes simétricos y antisimétricos de grupos metílicos y metilénicos, características del d _C-H. Por último podemos observar bandas agudas débiles, pertenecientes al enlace b (1-4), que aparecen entre 900 y 895 cm-1.
Con el análisis cualitativo por espectroscopia IR se garantizó que los contenidos de principio activo reportados por gravimetría correspondieron únicamente al fármaco, sin manifestarse interferencias de sustancias auxiliares o productos de degradación.
La limitada sensibilidad de la gravimetría pudo ser contrarrestada ya que se trabajó con una elevada cantidad de muestra, de modo que pudo disminuir significativamente el error por pesada.
Finalmente, la tabla 4 brinda los resultados de la cuantificación de la quitina en el tiempo al aplicar la técnica gravi-métrica adaptada para cada forma far-macéutica. Los valores son la media de 3 determinaciones y provienen de un mismo lote.
| | ||||||
| | ||||||
| Forma farmacéutica | | ]]> Temperatura | | | | |
| Suspensión | | | | | | ]]> 96,01±0,38 |
| Crema | | | | | | |
| | | | ]]> 103,71±0,5 | | ||
| Crema | | | | | | |
| | | ]]> 104,46±0,9 | | | ||
| Supositorio | | | | | | |
| | ]]> 96,76±1,68 | | | | ||
| | | | | | ||
Cuando analizamos los resultados de la cuantificación de la quitina en el tiempo por gravimetría directa durante los 12 me-ses estudiados, pudo apreciarse que la variación del contenido de quitina fue muy pequeña y no se observaron diferencias con respecto a los diferentes envases y temperaturas de almacenamiento. Todos los valores se encontraron en el rango de 90-110 %, por lo que los productos se conservaron químicamente estables.
Se alcanzó en las 3 técnicas diseñadas, una elevada linealidad entre el 80-120 %, según mostraron los coeficientes de correlación (r) y de determinación (r2). Para los interceptos las pruebas de la t de Student experimentales fueron inferiores a las teóricas para el 95 % de confianza, por lo que no resultaron significativamente diferentes de cero. Por otra parte, las pendientes fueron significativas con t de Student muy altas y valores de probabilidad (p) para la hipótesis nula de la pendiente muy por debajo del 0,05 establecido como límite, por lo que el valor observado fue prácticamente igual al predicho.
La evaluación de la exactitud reflejó el error sistemático, que para este método a pesar de requerir un alto grado de manipulación, dio valores de coeficientes de variación (CV) y de recobrado medio (R) dentro del rango establecido y se alcanzó gran correlación lineal entre los miligramos recuperados y los añadidos de principio activo.
Para la precisión, al igual que en los parámetros anteriores, se cumplieron los criterios de aceptación reportados en la literatura para la repetibilidad y la reproducibilidad, por lo que los errores aleatorios no repercutieron apreciable-mente en el método propuesto.
A pesar de los resultados satisfac-torios obtenidos en la evaluación de la especificidad de esta técnica gravimétrica, es conocido que la gravimetría como método, carece de la especificidad y sensibilidad requerida para el seguimiento de la estabilidad de este principio activo. La quitina es un producto de elevada estabilidad química y térmica, que rinde por hidrólisis ácida o enzimática: quitosana, N-acetil glucosamina, D-glucosamina y ácido acético, cuando este proceso transcurre totalmente.
Las condiciones para que se realice una hidrólisis total son extremadamente drásticas. No obstante, de los productos obtenidos sólo la quitosana presenta limitada solubilidad, ya que el resto son compuestos altamente solubles que pueden ser eliminados con lavados que empleen soluciones hidroalcohólicas.
En cada una de las técnicas evaluadas pudiera interferir la quitosana en la pesada del residuo por su insolubilidad en las soluciones de lavado. Por esta razón, el seguimiento de la estabilidad por gravimetría se complementó con la espectroscopia IR. De este modo pudimos descartar la presencia de quitosana por comparación de las bandas características de los espectros obtenidos durante el estudio con los espectros de la materia prima y de los productos procesados por gravimetría cuando estaban recién elaborados.
Subject headings: CHITIN/chemistry; DRUG STABILITY; SPECTOPHOMETRY, INFRARED/methods.
M. Yania Suárez Pérez. Instituto de Farmacia y Alimentos. Universidad de La Habana. Ave 23 No. 21422 entre 214 y 222, La Coronela, municipio La Lisa, Ciudad de La Habana, Cuba.
1 Master en Tecnología y Control de Medicamentos. ]]>
2 Doctor en Ciencias Farmacéuticas. ]]>