Mirna Fernández Cervera,1 Tania Fernández Cárdenas,2 Beatriz García Verdecia,3 Jackeline Gutiérrez Leiva4 y Antonio Iraizoz Colarte5
Se realizó el estudio de estabilidad acelerada de tabletas de levodopa-carbidopa (250-25 mg) con el empleo de un método de cromatografía líquida de alta resolución y se comprobó su especificidad para estos fines. Se analizó la influencia de medios degradantes artificiales sobre los productos activos, además del efecto de la humedad sobre la estabilidad del producto, colocándolo en hidrostatos con humedades controladas. Este medicamento, producción nacional, cumplió con las especificaciones de calidad descritas en la USP 23 y mostró una alta estabilidad térmica.
DeCS: ESTABILIDAD DE MEDICAMENTOS; COMPRIMIDOS/normas; CROMATOGRAFIA LIQUIDA DE ALTA PRESION/métodos; LEVODOPA/ /uso terapéutico; CARBIDOPA/uso terapéutico; QUIMIOTERAPIA COMBINADA; TECNOLOGIA FARMACEUTICA; CALIDAD DE LOS MEDICAMENTOS.
La levodopa constituye la droga más importante en el tratamiento del parkinsonismo incapacitante, aunque también lo es para el resto de las formas de parkinsonismo.1 La carbidopa no posee acción terapéutica propia, pero se emplea para proteger a la levodopa, lo que contribuye a elevar sus niveles en el sistema nervioso central, y aumenta así su biodisponibilidad en el cerebro.2 En la actualidad se acepta la terapia combinada como el preparado de elección para dicha afección.
Las preparaciones que incluyen a la levodopa y carbidopa en formas sólidas, tabletas, presentan combinaciones de dosis 100-25 mg, 100-10 mg y 250-25 mg, respectivamente.3
La finalidad de los estudios de estabilidad es garantizar la integridad de la formulación durante un lapso de tiempo donde el medicamento y su materia prima deben cumplir con los fines para los cuales fueron creados. Para ello se necesita desarrollar métodos que determinen cuantitativamente el fármaco en presencia de sus productos de degradación, constituyendo la cromatografía el método de elección para estos fines, no sólo por su alta sensibilidad y exactitud, sino también por su característica de método separativo. ]]>
El objetivo del presente trabajo consiste en realizar el estudio de estabilidad acelerada de las tabletas de levodopa- -carbidopa (250-25 mg), comprobando previamente la especificidad de la técnica analítica empleada.
Métodos analíticos. Se empleó la cromatografía líquida de alta resolución (CLAR) según la técnica descrita en la USP 23.4 Para demostrar su especificidad se sometieron muestras de ambos principios activos a degradación artificial por hidrólisis ácida y alcalina, y oxidación, durante 30 d. Conjuntamente con el análisis por CLAR se desarrolló la técnica por cromatografía en capa delgada (CCD) con soporte de silicagel GF-254 y sistema de solventes constituido por la mezcla acetona: :cloroformo:n-butanol:ácido acético glacial:agua (60:40:40:40:35). Además, para determinar la no interferencia de las sustancias auxiliares empleadas en la elaboración de las tabletas, se trabajó con los placebos.
Estudio de estabilidad. Este estudio se realizó por el método5 de estabilidad acelerada (Asociación Española de Farmacéuticos de la Industria. Desarrollo de un estudio de estabilidad. Madrid, 1993), con muestras del lote 5001 que fueron elaboradas en el Departamento de Tecnología y Control de Medicamentos, Instituto de Farmacia y Alimentos (IFAL), a las que inicialmente se les realizó su valoración y el ensayo de disolución.4
Las tabletas se distribuyeron y almacenaron en hornos a 40, 50 60 y 70 °C, a las que se les realizaron valoraciones periódicas durante 120 d. Los valores obtenidos se procesaron con la ayuda de un programa de computación confeccio-nado por Leonard y Valdés para estudios cinéticos de estabilidad.
También otras muestras de tabletas fueron colocadas en hidrostatos con humedades controladas de 75, 84 y 92 % durante 90 d, para comprobar la incidencia de este factor sobre la degradación de los principios activos.
En la tabla 1 se reportan los resultados iniciales del análisis del lote estudiado, de acuerdo con las especificaciones de calidad establecidos para el producto terminado. ]]>
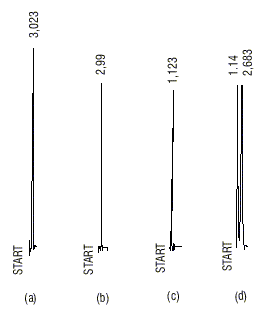
En la figura 1 se presentan los cromatogramas de las muestras de levodopa sometidas a las condiciones drásticas que permitieron su degradación. En medio ácido se aprecia un pico único con tiempo de retención (tr) de 2,99 min, correspondiente al principio activo.La hidrólisis en medio alcalino produjo la desaparición total del fármaco, y se confirmó la aparición de un producto de degradación con un tr = 1,1 min y otra señal pequeña a 3,4 min asociada con la levodopa. En medio oxidante se observan 2 señales con tr menores que no aparecen en el cromatograma de la muestra de referencia, y otra muy pequeña de levodopa.
Tabla 1. Resultados analíticos del lote estudiado
|
Ensayos | Levodopa | Carbidopa | Límites |
| Valoración (%) | ]]> 101,70 | 96,90 | 90,0-110,0 |
| Disolución*(%) | 101,38 |
99,68 | No menor del 80 % en
30 min |
| ]]>
Uniformidad de | |||
|
dosis**(%) | 101,15 | 95,32 | 85,0-115,0 |
| ]]> DER =1,9 % DER = 4,2 % | |||
* Valor promedio de 6 tabletas.
** Valor promedio de 10 tabletas.
DER: desviación estándar relativa.
Fig. 1. Cromatogramas de las muestras de levodopa sometidas a condiciones drásticas: a) muestra de referencia, b) muestra sometida a hidrólisis ácida, c) muestra sometida a hidrólisis básica y d) muestra sometida a medio oxidante.
En el caso de la carbidopa en medio ácido se detecta un pico ausente en el cromatograma de referencia con un tr menor. Al cabo de los 30 d desaparece en medio básico y oxidante (fig. 2).
Fig. 2. Cromatogramas de las muestras de carbidopa sometidas a condiciones drásticas: e) muestra de referencia, f) muestra sometida a hidrólisis ácida, g) muestra sometida a hidrólisis básica y h) muestra sometida a medio ambiente.
]]> Tabla 2. Resultados de la valoración periódica de las tabletas sometidas al estudio de estabilidad acelerada
|
Valoración periódica de levodopa-carbidopa (%) | ||||||||
| Tiempo(días) | 40 °C | 50 °C | 60 °C | 70 °C | ||||
| Lev | ]]> Carb | Lev | Carb | Lev | Carb | Lev | Carb | |
|
0 | 101,70 | ]]> 96,90 | 101,70 | 96,90 | 101,70 | 96,90 | 101,70 | 96,90 |
|
29 | 100,30 | ]]> 98,60 | 99,50 | 96,80 | 100,30 | 97,90 | 99,90 | 99,60 |
|
36 | 101,60 | ]]> 100,60 | 100,30 | 100,20 | 100,30 | 100,80 | 101,10 | 100,60 |
|
66 | 99,90 | ]]> 98,30 | 99,10 | 98,70 | 99,50 | 95,90 | 99,60 | 96,50 |
|
120 | 99,70 | ]]> 97,60 | 99,00 | 98,20 | 98,70 | 95,30 | 98,80 | 96,20 |
Lev: levodopa; Cab: carbidopa.
Al trabajar con los placebos no se detectó ninguna interferencia por parte de las sustancias auxiliares presentes en las tabletas y se comprobó la especificidad del método. ]]>
Los resultados de la valoración periódica de las tabletas sometidas al estudio de estabilidad acelerado se reportan en la tabla 2, mientras que los correspondientes al estudio de humedad se presentan en la tabla 3.Tabla 3. Resultados de la valoración periódica de las tabletas sometidas al estudio de humedad
|
Valoración periódica de levodopa-carbidopa (%) | ||||||
|
Tiempo (días) | 75 % HR | 84 % HR | 92 % HR | |||
| ]]> Lev | Carb | Lev | Carb | Lev | Carb | |
|
0 | 101,70 | 96,90 | ]]> 101,70 | 96,90 | 101,70 | 96,90 |
|
15 | 101,03 | 100,90 | 102,50 | 95,00 | ]]> 102,20 | 98,26 |
| 30 |
100,30 | 96,40 | 99,90 | 99,10 | 95,30 | 95,28 |
| ]]> 60 | 99,00 | 98,36 | 98,10 | 98,26 | 96,10 | 94,40 |
|
90 | 99,60 | ]]> 97,66 | 98,67 | 99,63 | 95,38 | 95,07 |
HR: humedad relativa; Lev: levodopa; Carb: carbidopa.
Como se observa en los resultados de la tabla 1, los parámetros de calidad del producto, recién elaborado, son satisfactorios.
Las condiciones drásticas ensayadas conllevaron a la degradación de la levodopa en medio básico y oxidante, lo que no ocurrió así en el ácido donde el principio activo mostró un pico único con un tiempo de retención similar al de la muestra de referencia; en el caso de la CCD el valor del factor de retardo (RF) fue el mismo que para el patrón.
El medio alcalino produjo la aparición de un producto de degradación en el punteo con una mancha de coloración fuerte, lo cual se confirmó por CLAR. En el caso del oxidante se obtuvo una mancha con cola atribuida a productos de degradación que por CLAR pudo resolverse con la detección de 2 señales, ausentes en la muestra de referencia.
]]> Sin embargo, la carbidopa sufrió afectación por todas las condiciones degradantes artificiales estudiadas. En medio ácido se obtuvo una cola en la mancha correspondiente al producto principal, que a pesar de no lograr su total resolución implicaba la existencia de algún producto de degradación con Rf similar al del patrón, comportamiento confirmado por CLAR en la que se detectó un pico con tr menor que al del patrón. Tanto en medio básico como en el oxidante se comprueba la desaparición del principio activo, resultados estos acordes con los obtenidos por CCD.Por lo tanto, el método cromatográfico resultó ser específico pues permitió cuantificar los principios activos en pre-sencia de sus productos de degradación.
La valoración periódica de las tabletas demostró su gran resistencia a la degradación térmica, ya que después de 120 d mantiene valores tanto para la levodopa como la carbidopa dentro de los rangos establecidos para este medicamento, con la misma actividad inicial. De igual forma los valores alcanzados para ambos principios activos en el estudio de humedad se encuentran dentro del límite establecido. En el caso del 92 % de humedad relativa se aprecia una disminución ligeramente mayor respecto al 75 y 84 %, pero siempre dentro del rango, resultados estos lógicos debido al efecto que se plantea en algunas literaturas1,3 de este parámetro en las formulaciones de levodopa-carbidopa.
Dado este comportamiento, no fue posible aplicar la ecuación de Arrhenius hasta tanto el nivel de degradación se encuentre en un valor entre 50 ó 60 %. En estos casos, usualmente se les concede a los medicamentos una fecha de vencimien-to tentativa de 3 años, lo cual debe ser corroborado por el estudio de vida útil.
An accelerated stability study of levodopa-carbidopa tablets (250-25 mg) was made using high-performance liquid chromatography which specificity for these purposes was proved. The influence of the artificial degrading media on the active products was analyzed and also the effect of humidity on the product´s satbility was examined after placing the tablets into hydrostats under controlled humidity levels. This domestically-made drug met the quality standards described in USP 23 and showed high heat stability.
Subject headings: DRUG STABILITY; TABLETS/standards; CHROMATOGRAPHY, HIGH PRESSURE LIQUID/methods; LEVODOPA/ therapeutic use; CARBIDOPA/therapeutic use; DRUG THERAPY, COMBINATION; TECHNOLOGY, PHARMACEUTICAL//methods; DRUG QUALITY.
Recibido: 11 de diciembre del 2000. Aprobado: 22 de enero del 2001.
M.Sc. Mirna Fernández Cervera. Instituto de Farmacia y Alimentos. Universidad de La Habana, Ave. 23 No. 21422 entre 214 y 222, La Coronela, municipio La Lisa, Ciudad de La Habana, Cuba.
1 Máster en Ciencias Farmacéuticas. Profesora Instructora.
2 Máster en Ciencias Farmacéuticas. Profesora Asistente. ]]>
3 Licenciada en Ciencias Farmacéuticas. Industria Médico farmacéutica (IMEFA).
4 Técnico Medio en Química. Centro de Investigaciones y Desarrollo de Medicamentos (CIDEM)
5 Doctor en Ciencias Farmacéuticas. Profesor Titular
]]>