Loipa Galán Martínez,1 Merly de Armas Ricard,2 Adriana Artiles Valor,3 Tania Ferrer Villada,4 Emilio Rolando,5 Margarita Suárez6 y Julio L. Álvarez González7
Se estudiaron las propiedades antagonistas del calcio de 2 nuevas 1,4- dihidropiridinas sintéticas (I y II). Ambos compuestos disminuyeron en gran medida las contracciones de anillos de aorta de conejo y con menor potencia inhibieron las contracciones de papilares de ventrículo derecho de rata, acortaron la duración del potencial de acción cardíaco a 0 mV y redujeron la corriente de calcio tipo L en cardiomiocitos ventriculares aislados de rata. La inhibición de la corriente de calcio tipo L fue dependiente del potencial, con un incremento de la potencia de acción en más de un orden de magnitud de concentración en células parcialmente despolarizadas (-50 mV). Estos resultados permiten concluir que las 1,4- dihidropiridinas I y II poseen acciones antagonistas del calcio vasoselectivas marcadas y este mecanismo está dado por el bloqueo de la corriente de calcio tipo L de manera dependiente del potencial.
Palabras clave: Antagonistas del calcio, dihidropiridinas, vasoselectividad, canales de calcio, corazón, patch-clamp.
Los antagonistas del calcio (AC) se introdujeron en clínica hace más de 30 años. Estos compuestos, en particular los más clásicos: la nifedipina (1,4- dihidropiridina), el verapamil (fenilalquilamina) y el diltiazem (benzotiazepina), se utilizan exitosamente en el tratamiento de numerosas enfermedades cardiovasculares como la hipertensión, la angina en sus diversas formas y en algunas arritmias cardíacas. Estos 3 fármacos pertenecen a una primera generación de AC y constituyen un grupo heterogéneo en cuanto a farmacología, terapéutica y estructura química.1-5 Los AC bloquean la entrada de calcio extracelular a través de los canales de calcio tipo L dependientes del voltaje, que son esenciales en el acoplamiento excitación-contracción del sistema cardiovascular (presentes tanto en el músculo liso vascular como en el músculo cardíaco). El mecanismo preciso del bloqueo y la selectividad hística varía entre estos 3 tipos de familia de fármacos.4-6 La principal diferencia entre estos compuestos es la dominante actividad vasodilatadora de las 1,4-dihidropiridinas (DHP), mientras que el verapamil y el diltiazem tienen propiedades vasodilatadoras y cardiodepresoras (efecto inotrópico negativo) en un mismo intervalo de concentración.3,6
Desde la introducción de la nifedipina en 1975, se han descrito una gran cantidad de nuevos derivados de DHP, conocidos como de segunda y tercera generación.4-6 El grado de selectividad vascular varía considerablemente entre las DHP, por lo que actualmente se sigue trabajando en la búsqueda de nuevas modificaciones estructurales, con el objetivo de encontrar una mayor vasoselectividad para así evitar los efectos colaterales sobre el miocardio durante la terapia antihipertensiva a largo plazo.7-9
A pesar de que la popularidad de las DHP había disminuido en la década de los 90, debido a algunos resultados de estudios observacionales que sugerían que estos AC no eran seguros ni eficaces.6,10,11 Existen otros estudios recientes que demuestran todo lo contrario y refieren una reducción de las complicaciones en hipertensos y en la insuficiencia cardíaca congestiva, con la misma efectividad que compuestos inhibidores de la enzima convertidora de angiotensina, por lo que aún se siguen prescribiendo exitosamente y sobre todo las DHP de larga duración.4,5,11-13 También se ha encontrado que las DHP tienen propiedades antiateroscleróticas y natriuréticas, además de ofrecer mayor seguridad en pacientes hipertensos que también son asmáticos, diabéticos, nefrópatas y ancianos.7,11,13
Atendiendo a los argumentos anteriores el presente trabajo tuvo como objetivo estudiar farmacológicamente 2 compuestos sintéticos nuevos del tipo DHP. Concretamente se verificaron sus acciones sobre la contracción de los músculos liso vascular y cardíaco, precisando para cada uno las propiedades antagonistas del calcio y el índice de vasoselectividad. Se caracterizaron las acciones de estos compuestos sobre la actividad eléctrica del músculo cardíaco y sus mecanismos de acción sobre la corriente de calcio tipo L con la técnica de patch-clamp en cardiomiocitos aislados enzimáticamente. Se precisaron las acciones dependientes del potencial de membrana y de la frecuencia de estimulación.
Se registró la fuerza de contracción de forma comparativa en músculo liso vascular (anillos de aorta abdominal de conejo) y en músculo ventricular (papilares de ventrículo derecho de rata), en este último se registró de manera simultánea a la contracción la actividad eléctrica cardíaca (potencial de acción).9
Los anillos de aorta abdominal fueron extraídos de conejos Nueva Zelandia machos con pesos corporales entre 2 000 y 3 000 g y los músculos papilares de ventrículo derecho se extrajeron de ratas Wistar machos con pesos corporales entre 150 y 180 g. Todos los animales fueron suministrados por el Centro Nacional para la Producción de Animales de Laboratorio (CENPALAB) y sometidos a condiciones ambientales y de manejo convencionales, alimentados con pienso estándar para ratas suministrado por CENPALAB y recibieron agua ad libitum.
]]> Los anillos y los papilares se fijaron por un lado a un transductor fuerza-desplazamiento TB-612T (Nihon Kohden) y por otro al fondo de una cámara de perfusión por la que fluía contínuamente (10 mL/min) una solución Tyrode de la siguiente composición (mmol/L): NaCl, 140; KCl, 4; CaCl2, 2; MgCl2, 0,5; hidroxietilpiperazina- N'- 2- ácido etanosulfónico (HEPES), 10 y glucosa, 5 (pH = 7,4, gaseada con O2 ). La contracción en los anillos de aorta fue inducida sustituyendo el NaCl por KCl (140 mmol/L) o adicionando noradrenalina (10 µmol/L) a la solución Tyrode, dejándose estabilizar de 8-10 min antes de la aplicación de los fármacos. Los papilares fueron estimulados eléctricamente mediante electrodos de campo de Ag/AgCl, con pulsos de 2 ms de duración y a una frecuencia de 1,25 Hz (ciclo básico de 800 ms) y de intensidad 2 veces el umbral diastólico; los pulsos fueron suministrados por un estimulador electrónico SEN 7103 (Nihon Kohden). Los experimentos se realizaron a una temperatura de 35 ºC.Se utilizó la técnica estándar de microelectrodos de vidrio para el registro de los potenciales de acción9 a través de un amplificador de microelectrodos MEZ-8201 (Nihon Kohden).
Para el estudio del efecto de los compuestos sobre la frecuencia cardíaca se utilizaron corazones extraídos de ratas adultas (Wistar, 150-180 g) y luego fueron montados en una columna de Langendorff. Los corazones fueron perfundidos a un flujo constante (10 mL/min) con solución Tyrode. El apex de los corazones se acopló al transductor fuerza-desplazamiento y se dejaron contraer espontáneamente bajo una carga constante de 1 g por al menos una hora antes de comenzar el experimento y se registró la fuerza contráctil. La cánula aórtica sirvió como electrodo de referencia y el electrodo activo se fijó por una aguja a la superficie del ventrículo izquierdo. El electrograma de superficie se registró con un amplificador biofísico AVB-10 (Nihon Kohden).9
Los registros de la corriente de calcio tipo L se realizaron en miocitos aislados de ventrículo derecho de ratas adultas (Wistar, 150-180 g). Las células ventriculares de rata adulta fueron aisladas enzimáticamente con colagenasa y tripsina por un método similar antes descrito.9 En los experimentos, alícuotas de células fueron depositadas en placas de Petri con solución Ringer y puestas en la platina de un microscopio invertido. Las células se perfundieron por gravedad a temperatura ambiente con una solución Ringer modificada (en mmol/L): NaCl 88,4, CaCl2 1,8, MgCl2 1,8, ácido N-2-hidroxietilpiperazin-N'-2-etanosulfónico (HEPES) 10,0, glucosa 10,0 y piruvato de sodio 5,0 a pH= 7,4. Además, estas soluciones contenían tetrodotoxina (TTX) 50 µmol/L y CsCl 20 mmol/L con el objetivo de inhibir las corrientes de sodio y potasio.
La corriente de calcio tipo L (ICaL) fue registrada mediante la técnica de patch-clamp convencional en la variante de célula entera,14 con la utilización de un amplificador RK-300 (Biologic, Francia) y micropipetas de vidrio (Drummond microcaps, USA; Broomall, PA, USA) con resistencias de 1-2 megaohmios, las cuales se llenaron con una solución (intracelular) de la composición (en mmol/L) siguiente: CsCl 120,0, ácido etilenglicol-bis-(b-aminoetil éter)-N,N,N',N'-2-etanosulfónico (EGTA) 10,0, MgCl2 4.0, creatínfosfato de sodio 5,0, Na 2 ATP 3,0, Na 2 GTP 0,4 y HEPES 10,0, ajustada a pH 7,2 con CsOH. Estos experimentos se realizaron a la temperatura del laboratorio (21-23 °C). Para las mediciones de I CaL se aplicó el pulso test a 0 mV (200 ms de duración) cada 8 s. La amplitud de la corriente se determinó como la diferencia entre el valor pico hacia adentro y el valor de corriente al final del pulso de 200 ms.
La generación de pulsos y la adquisición y procesamiento de datos (on line) se hicieron utilizando una computadora 80486DX2 (66MHz), con un conversor A/D (LabMaster DMA; 125 KHz, Scientific Solutions, Solon, OH, USA) y el programa de adquisición y procesamiento de datos ACQUIS1 (versión 2, Licencia CNRS, Francia). La frecuencia de muestreo fue de 20 kHz. Los cálculos de las constantes de tiempo de inactivación de las corrientes de calcio y de las corrientes capacitivas se hicieron con las funciones de ajuste intrínsecas del programa ACQUIS1.
Los resultados fueron analizados a través del ensayo-t de Student para muestras pareadas, se tomó como nivel de significación p < 0,05 y se expresan como medias y errores estándar de las medias.
Se estudiaron las acciones farmacológicas cardiovasculares de dos nuevas 1,4- dihidropiridinas (DHP-I y DHP-II) y se compararon con la clásica nifedipina (también es una DHP):
DHP-I: 3,5-dimetilcarboxi-2,6 dimetil-4(2-piridil)-1,4 dihidropiridina.
DHP-II: 3,5-dietilcarboxi-2,6 dimetil-4(2-piridil)-1,4 dihidropiridina. ]]>
Las DHP I y II se sintetizaron en el Laboratorio de Síntesis Orgánica de la Facultad de Química de la Universidad de La Habana.
Los resultados con las DHP I y II fueron muy alentadores pues ambos compuestos mostraron notables características de vasodilatadores vasoselectivos. La tabla resume los efectos de estas dos DHP y la nifedipina sobre las contracciones cardíaca (papilares de ventrículo derecho de rata) y vascular (anillos de aorta abdominal de conejo precontraídos con KCl 140 mmol/L).
Tabla. Efectos de las DHP I, II y nifedipina sobre las contracciones cardíaca y aórtica
| DHP | Corazón | Aorta | IVS | ||
| ]]> I | 90 | 60-120,00 | 0,95 | 0,43-1,47 | 95,00 |
| II | 40 | 30-50,00 | 0,185 | ]]> 0,14-0,23 | 216,00 |
| Nifedipina | 0,03 | 0,02-0,04 | 0,007 | 0,0029-0,0082 | 4,28 |
*Límite de confianza 95 %.
Los valores expresados son las IC50 obtenidas por el ajuste de las medias experimentales obtenidas (n= 7 para cada concentración entre 0,001 y 100 µmol/L) a la función de Hill Y= 100/[1 + (x/IC50)N], donde Y es el porcentaje de inhibición, x es la concentración del compuesto, N es el número de Hill e IC50 es la concentración que induce el 50 % de inhibición. ]]>
Tanto la DHP-I como la DHP-II inhibieron parcialmente la contracción aórtica evocada por noradrenalina (10 µmol/L). A la concentración de 100 µmol/L (la máxima estudiada), la DHP-I y la DHP-II inhibieron este tipo de contracción en el 20,7± 7,2 y 31,8 ± 1,02 %, respectivamente. La nifedipina, en t odo el intervalo de concentración estudiado, no afectó la contracción inducida por noradrenalina (n= 4).
En corazones de rata perfundidos con la técnica de Langendorff, la DHP-I (n= 6), la DHP-II (n= 5) y la nifedipina (n= 5), disminuyeron el ritmo espontáneo de manera dependiente de la concentración. A 10 µmol/L, el intervalo R-R aumentó por más de 150 ms con las tres DHP.
Dado que las DHP-I y II mostraron acciones vasoselectivas, se realizaron estudios más profundos sobre sus mecanismos básicos de acción, comparados con la nifedipina. En primera instancia se estudiaron los efectos sobre la actividad eléctrica ventricular, registrada en preparaciones multicelulares (músculos papilares de ventrículo derecho de rata) con la técnica de microelectrodos de vidrio.
Como era de esperar de una acción antagonista del calcio, ambas DHP redujeron significativamente (p < 0,05) la duración del potencial de acción cardíaco a 0 mV (D0), aunque la acción de la DHP-I fue menos potente que la de antagonistas clásicos de ese tipo como la nifedipina. A la concentración de 100 µmol/L, la DHP-I redujo D 0 en solamente el 25,5 ± 15,2 %, mientras que la DHP-II lo hizo en un 50,0 ± 10,2 % y la nifedipina en el 49,7 ± 3,2 %. Ninguna de estas DHP provocó cambios significativos (p < 0,05) sobre otras variables electrofisiológicas en el intervalo de concentraciones estudiado.
Tanto la DHP-I como la DHP-II provocaron una reducción en la corriente de calcio tipo L (I CaL ) en células ventriculares cardíacas aisladas de rata. En esta serie de experimentos la densidad de I CaL en condición control fue de 7,50 ± 3,5 pA/pF (Cm= 163,9 ± 37,5 pF; n=27), registrada a 0 mV desde un potencial basal de - 100 mV con 200 ms de duración. El tiempo al pico de I CaL fue de 6,7 ± 2,3 ms y el curso de la corriente se ajustó con dos exponenciales, cuyas constantes de tiempo de inactivación fueron 8,1 ± 3,0 ms ( t 1) y 36,7 ± 8,2 ms ( t 2). La concentración que inhibió el 50 % de I CaL (IC50) para la DHP-I, estimado en células con potenciales de reposo de -100 mV, fue de 32 µmol/L. Las constantes de tiempo de inactivación para I CaL fueron disminuídas significativamente (p < 0,05) por la DHP-I (10 µmol/L) de 8,1 ± 3,0 ms a 6,0 ± 2,2 ms y de 36,7 ± 8,2 ms a 28,9 ± 7,2 ms (n= 17).
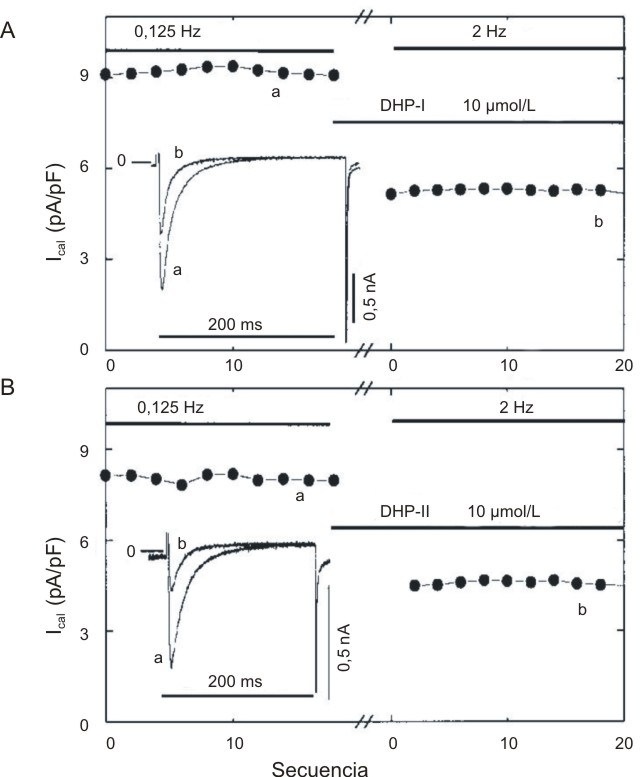
Para el estudio de los efectos dependientes de la frecuencia de las DHP, se aplicó el siguiente protocolo de imposición de voltaje. Bajo condiciones control se aplicó un tren de 10 pulsos a 0 mV, a una frecuencia de 0,125 Hz, desde un potencial basal de - 100 mV. Se detuvo la estimulación, y el potencial de membrana se mantuvo a - 100 mV por 3 min, durante los cuales las células fueron perfundidas con las soluciones control o con el fármaco en estudio. Entonces se reinició la estimulación a la misma o a más alta (2 Hz) frecuencia. El bloqueo tónico se estimó como la diferencia entre el pico de I CaL control y el pico de I CaL al primer pulso después de la perfusión del fármaco. El bloqueo dependiente del uso o la frecuencia se consideró como la diferencia entre el pico de I CaL del primer pulso y el pico de I CaL del pulso 20, después de la perfusión con el fármaco. Los cambios en I CaL dependientes de la frecuencia, bajo condiciones control, se tomaron en cuenta para el estimado de la acción dependiente del uso de los fármacos. Al igual que para la mayor parte de las DHP, esta reducción en I CaL por la DHP-I no fue dependiente de la frecuencia de estimulación y sí se evidencia un bloqueo tónico, aunque no muy marcado (fig. 1, A).
Fig. 1. Efectos tónicos de las dihidropirirdinas I (DHP-I) (A) y II (DHP-II (B) sobre la corriente de calcio tipo L (ICal) en cardiomiocitos de ratas. Las barras horizontales indican las frecuencias de estimulación y la aplicación de los compuestos. Los puntos representan las densidades de corriente pico en función del número de pulsos (secuencias). Nótese el fuerte bloqueo tónico de I Cal por ambos compuestos. Las estimulación se detuvo por tres minutos, tiempo durante el cual se añadió el fármaco en estudio.
]]> Las relaciones corriente/voltaje y las curvas de disponibilidad se determinaron por el protocolo estándar de doble pulso. Desde un potencial basal ( holding potential, HP) de -100 mV a una frecuencia de 0,125 Hz, se dio un prepulso de 200 ms a varios potenciales de membrana (de - 100 a +70 mV), y depués de un intervalo de 5 ms, se le dio un pulso test a 0 mV para I CaL a un potencial basal de - 100 mV. La inhibición de ICaL por la DHP-I fue, como era de esperar, dependiente del potencial. A la concentración de 10 µmol/L, la DHP-I desplazó la curva de disponibilidad de I CaL hacia potenciales más negativos, esta curva se ajustó desde - 100 a 0 mV con una función de distribución de Boltzman del tipo f=1/1+ exp[Vm-Vf)/k], donde Vm es el potencial de membrana, Vf es el potencial para la mitad de la inactivación y k es el factor pendiente. La DHP-I (10 µmol/L) provocó un corrimiento significativo en el Vf desde - 22,5 ± 1,1 mV a - 31,1 ± 0,5 mV (n= 8; p < 0,05) (fig. 2). Esta acción implica un incremento en la potencia de acción sobre I CaL en al menos un orden de magnitud de concentración, cuando las células están parcialmente despolarizadas (por ejemplo a potenciales de reposo de - 50 mV). Cuando las células se mantuvieron a un potencial basal de -50 mV, en presencia de La DHP-I (10 µmol/L) el Vf de la curva de disponibilidad cambió a - 37,1 ± 2,1 mV (n= 4) (fig. 2).Fig. 2. Efectos despendientes del voltaje de 10 µml/L de la dihidropiridina de I )DHP-I) sobre lCal) en cardiomiocitos de rata. Panel superior: Inhibición de la l Cal a 0 mV desde diferentes "holding potentials" (HP) o potenciales basales (-100 y -50 mV). Obsérvese como se potencia la inhibición de la corriente cuando la célula se encuentra a un potencialmás reducido (-50 mV). Panel intermedio: curvas de la relación corriente-voltaje desde los dos potenciales basales. Panel inferior: curvas de disponibilidad para lCal desde dos potenciales basales. Véase el corrimiento de ambas curvas hacia la izquierda en presencia de DHP-I.
En el caso de la DHP-II, el IC50 estimado para la inhibición de ICaL fue de 0,3 µmol/L. La DHP-II (10 µmol/L) también disminuyó significativamente (p < 0,05) la inactivación de ICaL , donde t 1 y t 2 fueron 10,2 ± 2,6 ms y 40,8 ± 7,7 ms en condición control (n = 21) y 7,3 ± 2.2 ms y 36,1 ± 8.6 ms, respectivamente en presencia de la DHP-II (n = 15). Esta acción fue esencialmente independiente de la frecuencia y se observó un ligero bloqueo tónico de ICaL (fig. 1B) y altamente dependiente del potencial (fig. 3), de manera que incrementó la potencia de acción de la DHP-II sobre ICaL en más de un orden de magnitud de concentración en células parcialmente despolarizadas (- 50 mV). Al potencial basal de - 100 mV la DHP-II (10 µmol/L) provocó un corrimiento significativo (p < 0,05) en el valor de Vf de la curva de disponibilidad de ICaL desde - 28,1 ± 1,1 mV en condición control a - 32,7 ± 0,7 mV en presencia de la DHP-II (n= 5) y al potencial basal de - 50 mV desde - 25,3 ± 2,1 mV a - 31,7 ± 1,7 mV (n=4) (fig. 3).
Fig. 3. Efectos dependiente del volyaje de 10 µmol/L de la dihidropiridina de II (DHP-II) sobre lCal en cardiomiocitos de ratas. Panel superior: Inhibición de la l Cal a 0 mV desde diferentes "holding potentials" (HP) o potenciales basales (-100 y - 50 mV). Obsérvese como se potencia la inhibición de la corriente cuando la célula se encuantra a un potencial más redicido (-50 mV). Panel intermedio: curvas de la relación corriente-voltaje desde los dos potenciales basales. Panel inferior: curvas de disponibilidad para l Cal desde los dos potenciales basales. Véase el corrimiento de ambas curvas hacia la izquierda en presencia de DHP-II.
El IC50 estimado para la inhibición de ICaL por nifedipina fue de 0,11 µmo/L (n= 6). La nifedipina esencialmente mostró un bloqueo tónico sobre ICaL (fig. 4, B). La inhibición de ICaL por nifedipina también fue dependiente del voltaje, es decir, cuando los pulsos de imposición de voltaje se aplicaron desde un potencial basal reducido de -50 mV, se observó un aumento en la inhibición (fig. 4, A). A este potencial basal la IC50 de ICaL disminuyó a 0,01 µmol/L para la nifedipina.
Fig. 4. A-Efectos despendiente del voltaje de 1µmol/L de la dihidropiridina nifedipina sobre lCal en cardiomicitos de rata. Inhibición de lCal a+ 10 mV desde diferentes "holding potentials" (HP) o potenciales basales (-80 y -50 mV). Nótese el aumento en la inhibición de lCal cuando el potencial basal fue -50 mV). B- Efectos dependientes del uso o la frecuencia de la nifedipina sobre l Cal. Las barras horizontales indican las frecuencias de estimulción y la aplicación de nifedipina. Los puntos representan las densidades de corriente pico en función del número de pulsos (secuencia). Nótese el fuerte bloqueo tónico de lCal por nifedipina. Encima de la figura se muestra un duagrama del protocolo de estimulación.
La DHP-I y la DHP-II poseen acciones antagonistas del calcio vasoselectivas marcadas, en particular la DHP-II. En ambos casos, el índice de vasoselectividad (IVS) fue considerablemente mayor que el reportado2,3,15 y el obtenido por este estudio para la nifedipina, y está en los órdenes de magnitud de los determinados para DHP de nuevas generaciones.1,3,5,6,9
]]> Se encontró que la DHP-I y la DHP-II, al igual que los antagonistas de canales de calcio clásicos, bloquean la contracción del músculo cardíaco y liso vascular y disminuyen la frecuencia espontánea del corazón aislado perfundido.1-2Como era de esperar para una acción antagonista del calcio, tanto la DHP-I como la DHP-II disminuyeron la duración del potencial de acción a 0 mV, existiendo una correlación entre el acortamiento de la duración del potencial de acción y la disminución de la fuerza contráctil en tejido cardíaco, lo cual se corresponde con que existe una relación directa entre las acciones sobre la duración del potencial de acción y la fuerza contráctil.16
Las acciones de las DHP I y II sobre el canal de calcio tipo L son clásicas de las DHP antagonistas del calcio.3,6 En particular, la acción dependiente del potencial constituye el mecansimo básico de su vasoselectividad: la potencia de inhibición sobre ICaL es mayor en células parcialmente despolarizadas (-50 mV), como por ejemplo en las células musculares lisas de los vasos sanguíneos. Esto también se demostró por el corrimiento del potencial para la mitad de la inactivación (Vf) en las curvas de diponibilidad de ICaL hacia potenciales más negativos (dirección hiperpolarizante) en presencia de ambos compuestos (DHP-I y DHP-II). Mientras más marcado sea este efecto dependiente del potencial, mayor será su vasoselectividad. Estas evidencias indican que como la mayoría de las DHP, las DHP I y II interactúan con los canales de calcio en su estado inactivado, dando las bases de la vasoselectividad de estos compuestos ya que en el músculo liso vascular los potenciales de reposo son menores que en el músculo cardíaco y el tiempo durante el cual los canales de calcio están en su estado inactivado es mayor que en el músculo cardíaco.17,18 Por todo esto, la interacción de estas DHP con los canales de calcio inactivados está favorecida en el músculo liso vascular.
Al igual que para la mayor parte de las DHP, el comportamiento dependiente del uso del bloqueo de ICaL por estos compuestos, incluida la nifedipina en nuestros resultados, fue esencialmente tónico y no dependiente de la frecuencia,3 lo cual indica en términos de la hipótesis del receptor modulado, que estos compuestos interactúan con el canal en estado de reposo o inactivado. Después de la interacción de estos compuestos con el canal, este entra en un estado absorbido inactivado con alta afinidad por los compuestos.
Las características estructurales de las DHP I y II (su liposolubilidad), hacen que tengan mayor afinidad por la forma inactivada del canal de cacio, la cual predomina en células parcialmente despolarizadas,6 como en el caso del músculo liso vascular. Los compuestos liposolubles que interactúan preferentemente con el estado inactivado del canal, tienen acceso a éste a través de la matriz lipídica de la membrana y por tanto, su acción es esencialmente dependiente del potencial.3 De hecho, se ha demostrado que un aumento en la liposolubilidad de las moléculas de diferentes antagonistas del calcio, incrementa la selectividad vascular de estas.3,6 De la misma manera, al aumentar la liposolubilidad de estos compuestos, disminuye su acción inotrópica negativa sobre el músculo cardíaco.3,6 Las moléculas de las DHP I y II son más liposolubles que la nifedipina, ya que la estructura química de estas tienen una mayor cantidad de grupos y cadenas apolares en comparación con la estructura de la nifedipina, lo cual coincide con nuestros resultados en que las DHPI y II son más vasoselectivas que la nifedipina. Coincidentemente también, la cadena lateral de la DHP II es más liposoluble que la cadena de la DHP I, y la DHP II nos dio un índice de vasoselectividad superior al de la DHP I.
Por todos estos resultados se puede concluir que las DHP I y II constituyen 2 nuevas DHP con propiedades antagonistas del calcio vasoselectivas, de un alto interés potencial para la Cardiología. Se recomienda continuar la investigación con la serie de las DHP, partiendo de la base de modificar las estructuras de las DHP I y II para lograr una mayor liposolubilidad y en consecuencia una mayor vasoselectividad.
The calcium antagonist properties of 2 new 1,4 synthetic dihydropyridines (I and II) were studied. Both compounds reduced in a great extent the contractions of rabbit's aorta rings, and they inhibited with less potency the papillary contractions of rat's right ventricle. They also shortened the duration of the heart action potential to 0 mV, and decreased the L calcium current in ventricular cardiomyocites isolated from rats. The inhibition of calcium L current depended on the potential, with an increase of the action potential in more than one order of concentration magnitude in partially depolarized cells (-50 mV). These results allow to conclude that 1,4 dihydropyridines I and II have marked vasoselective calcium antagonist actions, and that this mechanism is due to the blockade of the calcium L current depending on the potential..
Key words: Calcium antagonists, dihydropyridines, vasoselectivity, calcium channels, heart, patch-clamp.
1. Nayler WG. Calcium antagonists. London : Academic Press; 1988.
2. Godfraind T. Vasodilators and calcium antagonists. En: van Zwieten PA, Greenlee WJ (ed). Antihypertensive drugs. The Netherlands : Harwood Academic Publishers; 1997. p. 313-75.
3. Triggle DJ. The pharmacology of ion channles: with particular reference to voltage-gated Ca 2+ channels. Eur J Pharmacol. 1999;375:311-25.
4. Sica DA. Calcium channel blocker class heterogeneity: select aspects of pharmacokinetics and pharmacodynamics. J Clin Hypertens (Greenwich). 2005; 7(4 Suppl 1):21-6.
5. Grossman E, Messerli FH. Calcium antagonists. Prog Cardiovasc Dis. 2004; 47(1):34-57.
6. Clusin WT, Anderson ME. Calcium channel blockers: current controversies and basic mechanisms of action. Adv Pharmacol. 1999;46:253-96.
7. Brixius K, Gross T, Tossios P, Geissler HJ, Mehlhorn U, Schwinger RH, et al. Increased vascular selectivity and prolonged pharmacological efficacy of the L-type Ca 2+ channel antagonist lercanidipine in human cardiovascular tissue. Clin Exp Pharmacol Physiol. 2005;32(9):708-13.
8. Matsumura Y, Hayashi K. Vetanidipina hydrochloride: a new long-lasting antihypertensive agent. Expert Opin Investig Drugs. 2001;10(1):139-55.
9. Galán L, Talavera K, Vassort G, Alvarez JL. Characteristics of Ca 2+ channel blockade by oxodipine and elgodipine in rat cardiomyocytes. Eur J Pharmacol. 1998;357:93-105.
10. Furberg CD, Psaty BM, Meyer JV. Nifedipine: dose-related increase in mortality in patients with coronary heart disease. Circulation. 1995;92:1326-31.
11. Kizer JR, Kimmel SE. Epidemiologic Review of the Calcium Channel Blocker Drugs. Arch Intern Med. 2001;161:1145-58.
12. Motro M, Shemesh, Grossman E. Coronary benefits of calcium antagonist therapy for patients with hypertension. Curr Opin Cardiol. 2001;16:349-55.
13. Doggrell SA. Has the controversy over the use of calcium channel blockers in coronary artery disease been resolved? Expert Opin Pharmacother. 2005;6(5):831-4.
14. Hamill OP, Marty A, Neher E, Sakmann B, Sigworth FJ. Improved patch-clamp technics for high resolution current recording from cells and cell-free membrane patches. Pflügers Arch. 1981;391:85-100.
15. Godfraind T, Eglème C, Finet M, Jaumin P. The actions of nifedipine and nisoldipine on the contractile activity of human coronary arteries and human cardiac tissue in vitro. Pharmacol Toxicol. 1987;61:79-84.
16. Bers DM. Cardiac excitation-contraction coupling. Nature. 2002;415(10):198-205.
17. Bolton TB, Lim SP, Salmon DMW, Beech DJ. Calcium Channels and Calcium-Mediated Effects in Smooth Muscle Cells. J Cardiovasc Pharmacol. 1988;12:S96-9.
18. Thorneloe KS, Nelson MT. Ion channels in smooth muscle: regulators of intracellular calcium and contractility. Can J Physiol Pharmacol. 2005;83(3):215-42.
Recibido: 22 de diciembre de 2005. Aprobado: 30 de enero de 2006.
Dra. Loipa Galán Martínez . Instituto de Cardiología y Cirugía Cardiovascular. Calle 23 No. 654, Vedado, CP 10 400, Ciudad de La Habana. Correo electrónico: logama@infomed.sld.cu
1Doctora en Ciencias Farmacéuticas. Investigadora Agregada.
2Licenciada en Bioquímica. Aspirante a Investigadora. ]]>
3Doctora en Ciencias Biológicas. Aspirante a Investigadora.
4Maestro en Ciencias. Aspirante a Investigador.
5Maestro en Ciencias. Profesor Auxiliar. Facultad de Química. Universidad de La Habana.
6Doctora en Ciencias Químicas. Profesora Titular.
7Doctor en Ciencias. Investigador Titular.